Изобретение относится к области органической химии, а именно к новым индивидуальным соединениям класса 6-антипирил-9-ароил-8-гидрокси-2-имино-1,3-дифенил-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-дионов и способу их получения. Полученные соединения являются перспективными кандидатами для синтеза новых гетероциклических соединений.
Известен структурный аналог заявленных соединений [Пятичленные 2,3-диоксогетероциклы. LXXV. Взаимодействие 1-арил-4-ароил-5-метоксикарбонил-1Н-пиррол-2,3-дионов и 1,3-дифенилгуанидина. Кристаллическая и молекулярная структура 9-бензоил-8-гидрокси-2-имино-1,3-дифенил-6-(4-толил)-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-диона / Н.В. Бубнов, Е.С. Денисламова, З.Г. Алиев, А.Н. Масливец // ЖОрХ. - 2011. - Т. 47. - № 4. - С. 526-528], полученный по следующей схеме:
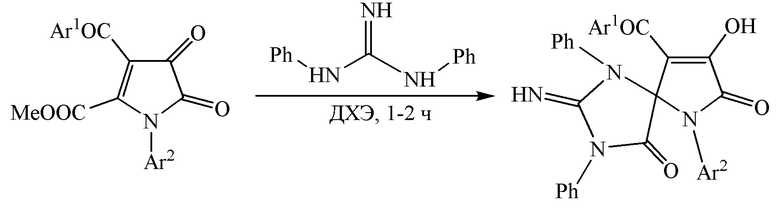 .
.
К недостаткам данного способа относится невозможность получения 6-антипирил-9-ароил-8-гидрокси-2-имино-1,3-дифенил-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-дионов.
Задачей изобретения является разработка простого способа синтеза неописанных в литературе 6-антипирил-9-ароил-8-гидрокси-2-имино-1,3-дифенил-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-дионов, которые могут быть использованы в качестве исходных реагентов для синтеза новых гетероциклических соединений.
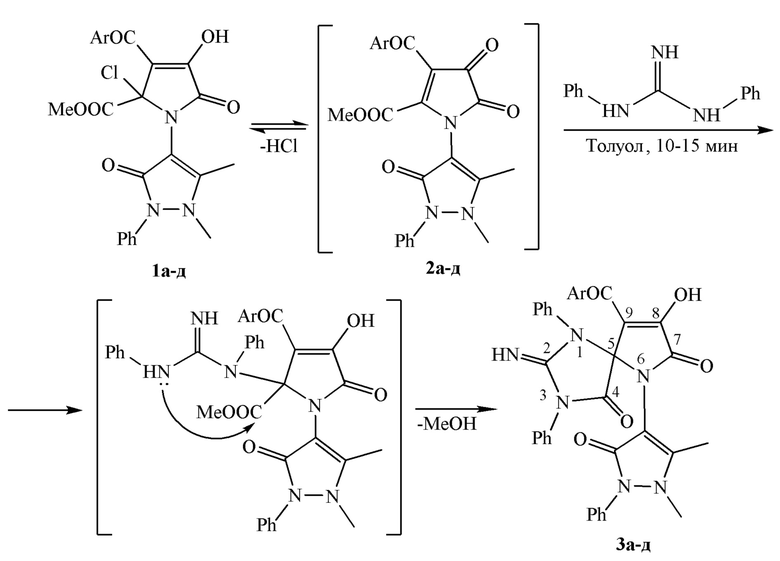
Поставленная задача решается путем взаимодействия 1-антипирил-4-ароил-5-метоксикарбонил-1Н-пиррол-2,3-дионов (1а-д) с 1,3-дифенилгуанидином, взятыми в соотношении 1:1, в течение 10-15 минут при кипячении в безводном толуоле по схеме:
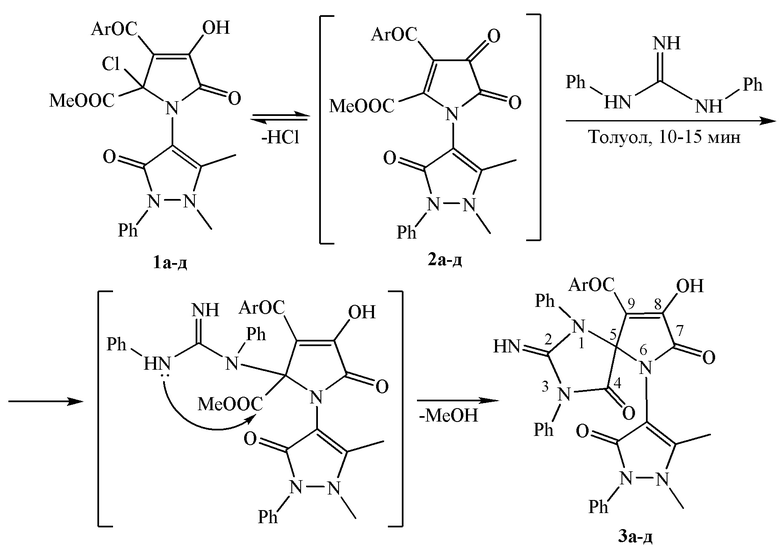
1, 2, 3: Ar = Ph(a), 4-ClC6H4(б), 4-BrC6H4(в), 4-MeC6H4(г), 4-MeOC6H4(д)
Из патентной и технической литературы не были выявлены способы получения 6-антипирил-9-ароил-8-гидрокси-2-имино-1,3-дифенил-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-дионов, имеющие сходные признаки с заявляемым способом, а именно не использовались исходные продукты, изменены условия проведения синтеза: в качестве растворителя использовался толуол, и сокращен интервал времени реакции.
На основании полученных данных можно сделать вывод о соответствии заявленного технического решения критериям «новизна» и «изобретательный уровень».
Изобретение иллюстрируется следующими примерами.
Пример 1. 6-Антипирил-9-бензоил-8-гидрокси-2-имино-1,3-дифенил-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-дион (3а)
Получение (3а): Навеску 1-антипирил-4-бензоил-3-гидрокси-5-метоксикарбонил-5-хлор-1Н-пиррол-2-она 1а массой 0.223 г (0.500 ммоль) растворили в 40 мл толуола и кипятили до появления интенсивно-бордовой окраски с последующей отгонкой растворителя и хлороводорода. В полученный раствор добавили 0.106 г (0.500 ммоль) 1,3-дифенилгуанидина, который предварительно растворили в 10 мл толуола. Кипятили в течение 10 минут, при охлаждении выпадал светло-коричневый осадок, который перекристаллизовывали в этаноле. Выход 0.159 г (51%), т.пл. 234-235°С.
Соединения (3а) - бесцветное кристаллическое вещество, легкорастворимое в ДМФА, ДМСО, ацетоне, ацетонитриле, труднорастворимое в хлороформе, толуоле, метаноле, этилацетате, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
ИК-спектр, ν, см-1: 3053-3069 ш (OH, NH), 1780 (C4O), 1735 (C7O), 1619 (CO ароил).
Спектр ЯМР 1Н соединения (3а) снят в растворе ДМСО-d6 при частоте 400 МГц, δ, м.д.: 2.16 с (3H, Me-С), 3.21 с (3H, Me-N), 7.21-7.96 гр.с (10H, 2Ph), 9.08, 9.42 уш.с (OH, NH).
Соединение (3а) C36H28N6O5. Найдено, %: С 69.75, Н 4.75, N 13,61. Вычислено, %: С 69.22, Н 4.52, N 13.45.
Пример 2. 6-Антипирил-8-гидрокси-2-имино-1,3-дифенил-9-(4-хлорбензоил)-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-дион (3б)
Получение (3б): Навеску 1-антипирил-3-гидрокси-5-метоксикарбонил-5-хлор-4-(4-хлорбензоил)-1Н-пиррол-2-она 1б массой 0.239 г (0.500 ммоль) растворили в 40 мл толуола и кипятили до появления интенсивно-бордовой окраски с последующей отгонкой растворителя и хлороводорода. В полученный раствор добавили 0.106 г (0.500 ммоль) 1,3-дифенилгуанидина, который предварительно растворили в 10 мл толуола. Кипятили в течение 15 минут, при охлаждении выпадал светло-коричневый осадок, который перекристаллизовывали в этаноле. Выход 0.161 г (49%), т.пл. 232-233°С.
Соединения (3б) - бесцветное кристаллическое вещество, легкорастворимое в ДМФА, ДМСО, ацетоне, ацетонитриле, труднорастворимое в хлороформе, толуоле, метаноле, этилацетате, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
ИК-спектр, ν, см-1: 3050-3070 ш (OH, NH), 1780 (C4O), 1730 (C7O), 1611 (CO ароил).
Спектр ЯМР 1Н соединения (3б) снят в растворе ДМСО-d6 при частоте 400 МГц, δ, м.д.: 2.16 с (3H, Me-С), 3.20 с (3H, Me-N), 7.07-7.96 гр.с (10H, 2Ph), 9.04, 9.31 уш.с (OH, NH).
Соединение (3б) C36H27ClN6O5. Найдено, %: C 65.34, H 4.16, N 12.77. Вычислено, %: С 65.60, Н 4.13, N 12.75.
Пример 3. 6-Антипирил-9-(4-бромбензоил)-8-гидрокси-2-имино-1,3-дифенил-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-дион (3в)
Получение (3в): Навеску 1-антипирил-4-(4-бромбензоил)-3-гидрокси-5-метоксикарбонил-5-хлор-1Н-пиррол-2-она 1в массой 0.262 г (0.500 ммоль) растворили в 40 мл толуола и кипятили до появления интенсивно-бордовой окраски с последующей отгонкой растворителя и хлороводорода. В полученный раствор добавили 0.106 г (0.500 ммоль) 1,3-дифенилгуанидина, который предварительно растворили в 10 мл толуола. Кипятили в течение 10 минут, при охлаждении выпадал светло-коричневый осадок, который перекристаллизовывали в этаноле. Выход 0.172 г (49%), т.пл. 238-239°С.
Соединения (3в) - бесцветное кристаллическое вещество, легкорастворимое в ДМФА, ДМСО, ацетоне, ацетонитриле, труднорастворимое в хлороформе, толуоле, метаноле, этилацетате, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
ИК-спектр, ν, см-1: 3049-3078 уш (OH, NH), 1781 (C7O), 1732 (C4O), 1630 (CO ароил).
Спектр ЯМР 1Н соединения (3в) снят в растворе ДМСО-d6 при частоте 400 МГц, δ, м.д.: 2.17 с (3H, Me-С), 3.21 с (3H, Me-N), 7.06-7.80 гр.с (10H, 2Ph), 9.03, 9.30 уш.с (OH, NH).
Соединение (3в) C36H27BrN6O5. Найдено, %: C 61.43, H 3.89, N 11.92. Вычислено, %: С 61.46, Н 3.87, N 11.95.
Пример 4. 6-Антипирил-8-гидрокси-2-имино-9-(4-метилбензоил)-1,3-дифенил-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-дион (3г)
Получение (3г): Навеску 1-антипирил-3-гидрокси-4-(4-метилбензоил)-5-метоксикарбонил-5-хлор-1Н-пиррол-2-она 1г массой 0.230 г (0.500 ммоль) растворили в 40 мл толуола и кипятили до появления интенсивно-бордовой окраски с последующей отгонкой растворителя и хлороводорода. В полученный раствор добавили 0.106 г (0.500 ммоль) 1,3-дифенилгуанидина, который предварительно растворили в 10 мл толуола. Кипятили в течение 15 минут, при охлаждении выпадал светло-коричневый осадок, который перекристаллизовывали в этаноле. Выход 0.165 г (52%), т.пл. 233-234°С.
Соединение (3г) - бесцветное кристаллическое вещество, легкорастворимое в ДМФА, ДМСО, ацетоне, ацетонитриле, труднорастворимое в хлороформе, толуоле, метаноле, этилацетате, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
ИК-спектр, ν, см-1: 3053-3071 уш (OH, NH), 1782 (C7O), 1733 (C4O), 1613 (CO ароил).
Спектр ЯМР 1Н соединения (3г) снят в растворе ДМСО-d6 при частоте 400 МГц, δ, м.д.: 2.17 с (3H, Me-С), 2.40 с (3H, Me-C6H4), 3.21 с (3H, Me-N), 7.11-7.74 гр.с (10H, 2Ph), 8.96, 9.23 уш.с (OH, NH).
Соединение (4г) C37H30N6O5. Найдено, %: C 69.53, H 4.96, N 13.38. C37H30N6O5. Вычислено, %: С 69.58, Н 4.73, N 13.16.
Пример 5. 6-Антипирил-8-гидрокси-2-имино-9-(4-метоксибензоил)-1,3-дифенил-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-дион (3д)
Получение (3д): Навеску 1-антипирил-3-гидрокси-4-(4-метоксибензоил)-5-метоксикарбонил-5-хлор-1Н-пиррол-2-она 1e массой 0.230 г (0.500 ммоль) растворили в 40 мл толуола и кипятили до появления интенсивно-бордовой окраски с последующей отгонкой растворителя и хлороводорода. В полученный раствор добавили 0.106 г (0.500 ммоль) 1,3-дифенилгуанидина, который предварительно растворили в 10 мл толуола. Кипятили в течение 15 минут, при охлаждении выпадал светло-коричневый осадок, который перекристаллизовывали в этаноле. Выход 0.167 г (51%), т.пл. 236-237°С.
ИК-спектр, ν, см-1: 3050-3070 уш (OH, NH), 178 (C7O), 1730 (C4O), 1611 (CO ароил).
Соединение (3д) - бесцветное кристаллическое вещество, легкорастворимое в ДМФА, ДМСО, ацетоне, ацетонитриле, труднорастворимое в хлороформе, толуоле, метаноле, этилацетате, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
Спектр ЯМР 1Н соединения (3д) снят в растворе ДМСО-d6 при частоте 400 МГц, δ, м.д.: 2.17 с (3H, Me-С), 2.40 с (3H, Me-C6H4), 3.21 с (3H, Me-N), 7.11-7.74 гр.с (10H, 2Ph), 8.96, 9.23 уш.с (OH, NH).
Соединение (3д) C37H30N6O5. Найдено, %: C 69.53, H 4.96, N 13.38. Вычислено, %: С 69.58, Н 4.73, N 13.16.
Предлагаемый способ прост в осуществлении и позволяет получить новые индивидуальные соединения класса 6-антипирил-9-ароил-8-гидрокси-2-имино-1,3-дифенил-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-дионов. Полученные соединения являются перспективными кандидатами для синтеза новых гетероциклических соединений.
Изобретение относится к способу получения 6-антипирил-9-ароил-8-гидрокси-2-имино-1,3-дифенил-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-дионов общей формулы (I), где Ar означает Ph(a), 4-ClC6H4(б), 4-BrC6H4(в), 4-MeC6H4(г) или 4-MeOC6H4(д). Способ включает взаимодействие 1-арил-4-ароил-5-метоксикарбонил-1Н-пиррол-2,3-дионов (1а-д), указанных в формуле изобретения, с 1,3-дифенилгуанидином, взятыми в соотношении 1:1, при температуре в течение 10-15 минут при кипячении в безводном толуоле по схеме, указанной в формуле изобретения. Технический результат – получение соединений класса 6-антипирил-9-ароил-8-гидрокси-2-имино-1,3-дифенил-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-дионов. 5 пр.
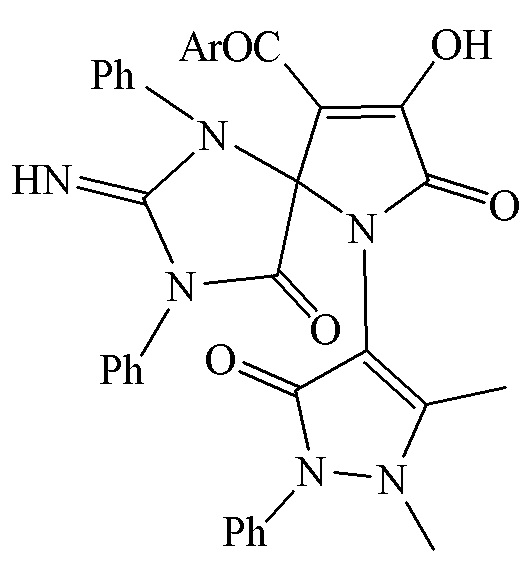 (I)
(I)
Способ получения 6-антипирил-9-ароил-8-гидрокси-2-имино-1,3-дифенил-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-дионов общей формулы:
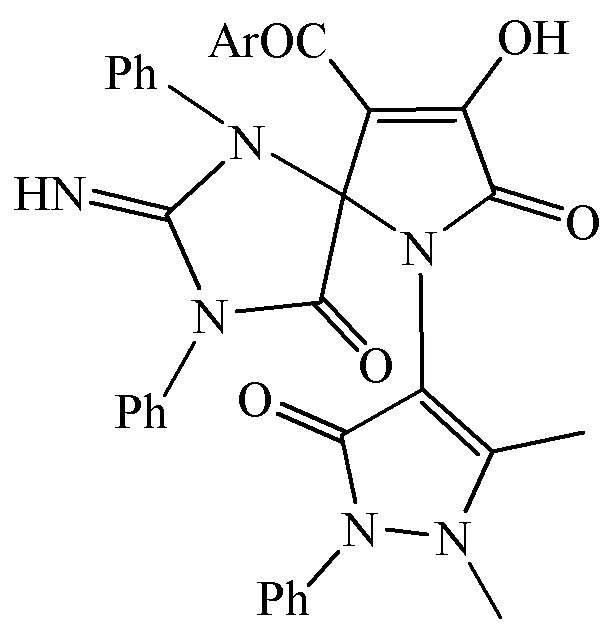
где Ar означает Ph(a), 4-ClC6H4(б), 4-BrC6H4(в), 4-MeC6H4(г), 4-MeOC6H4(д), заключающийся в том, что 1-арил-4-ароил-5-метоксикарбонил-1Н-пиррол-2,3-дионов (1а-д) подвергают взаимодействию с 1,3-дифенилгуанидином, взятыми в соотношении 1:1, при температуре в течение 10-15 минут при кипячении в безводном толуоле по схеме:
1, 2, 3: Ar = Ph(a), 4-ClC6H4(б), 4-BrC6H4(в), 4-MeC6H4(г), 4-MeOC6H4(д)
Авторы
Даты
2025-03-31—Публикация
2023-10-17—Подача