Изобретение относится к области органической химии, а именно к новым биологически активным 8-гидрокси-6-(2-гидроксифенил)-9-ароил-1-(фениламино)-2-тиоксо-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-дионам формулы:
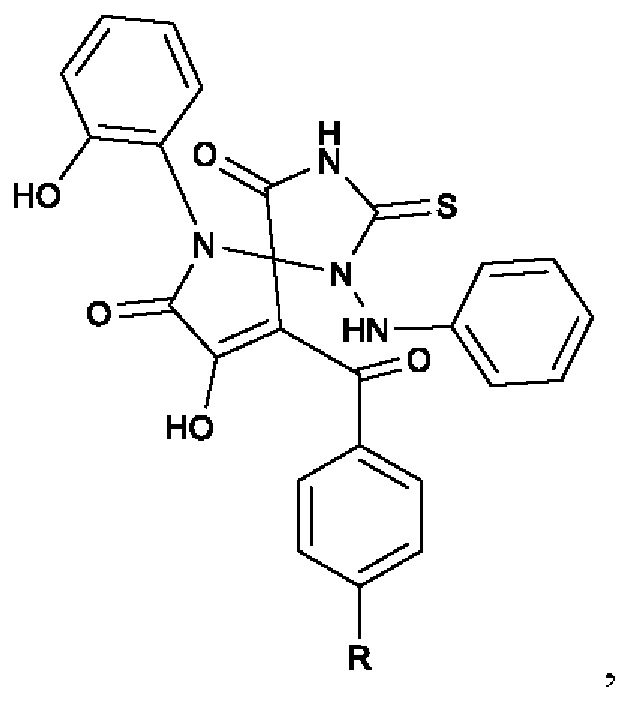
обладающим противомикробной активностью, что позволяет предположить их использование в фармакологии и в медицине в качестве лекарственных средств с противомикробным эффектом.
Известны структурные аналоги заявленных соединений - спиро-тиогидантоины ([4+2]-Cycloaddition to 5-methylidene-hydantoins and 5-methylidene-2-thiohydantoins in the synthesis of spiro-2-chalcogenimidazolones / D.E. Shybanov, M.E. Kukushkin, Y.S. Hrytseniuk et al. // Int. J. Mol. Sci. - 2023. - V. 24. - №. 5. - P. 5037.).
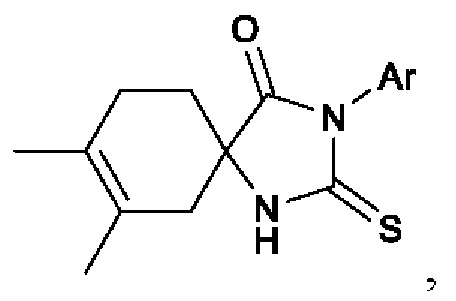
где Ar=2-ClC6H4, 4-MeOC6H4, 3-Cl,4-FC6H3
Эталонами сравнения противомикробной эффективности выбраны антибактериальный препарат диоксидин [Падейская Е. Н. Антибактериальный препарат диоксидин: особенности биологического действия и значение в терапии различных форм гнойной инфекции // Инфекции и антимикробная терапия. - 2001. - №. 5. - С. 105-155] и противогрибковый препарат флуконазол [Shilova I.B., Gus'kova Т.А., Glushkov R.G. Modern drags for treating dermatomycosis // Pharmaceutical Chemistry Journal. - 2004. - T. 38. - №. 4. - C. 175-180.], которые широко применяются в лечебной практике и являются аналогами по действию.
Задачей изобретения является поиск в ряду производных спиро-тиогидантоинов веществ с выраженным противомикробным действием и расширение арсенала средств воздействия на живой организм.
Поставленная задача достигается получением 8-гидрокси-6-(2-гидроксифенил)-9-ароил-1-(фениламино)-2-тиоксо-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-дионов, которые обладают противомикробной активностью.
Заявляемые соединения синтезируют путем взаимодействия 3-ароил-2,4-дигидро-1H-пирроло[2,1-с][1,4]бензоксазин-1,2,4-трионов (I) с 2-фенилгидразин-1-карботиамидом в соотношении 1:1 в среде безводного растворителя с последующим выделением целевых продуктов (II) по представленной схеме:
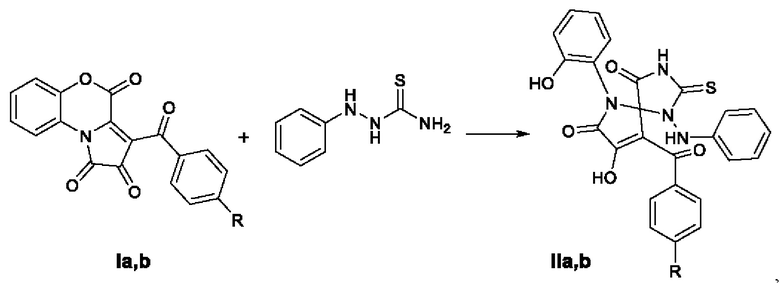
где R=СН3 (a), NO2 (b).
Процесс ведут при кипячении, а в качестве растворителя используют безводный ацетонитрил.
Изобретение иллюстрируется следующими примерами.
Пример 1. Получение 8-гидрокси-6-(2-гидроксифенил)-9-(метилбензоил)-1-(фениламино)-2-тиоксо-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-диона (IIa).
К раствору 0.3 ммоль 3-(4-метилбензоил)-1H-бензо[b]пирроло[1,2-d][1,4]оксазин-1,2,4-триона (Ia) в 1 мл безводного ацетонитрила добавляли 0.3 ммоль 2-фенилгидразин-1-карботиамида. Реакционную массу кипятили в течение 60 минут. Выход 79%, т.пл. 206-207°С. Соединение (IIa) C26H20N4O5S.
Найдено, %:
Вычислено, %: С, 62.39; Н, 4.03; N, 11.19; S, 6.41
Соединение (IIa) - желтое кристаллическое вещество, легкорастворимое в ДМСО, ДМФА, растворимое в дихлорметане, хлороформе, ацетоне, спиртах, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
В ИК спектре соединения (IIa), записанном в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний гидроксильных групп гидроксифенила и пиррол-2-она 3402, 3152 см-1, карбонильных групп пиррол-2-она, тиогидантоина и бензоила 1719, 1631, 1601 см-1.
Спектр ЯМР 1Н (400 МГц, DMSO-d6, δ, м.д.): 12.40 (с, 1Н), 10.74 (с, 1Н), 7.95-7.74 (м, 1Н), 7.33 (т, J=7.8 Гц, 1Н), 7.06 (с, 6Н), 6.97-6.81 (м, 4Н), 6.64-6.54 (м, 3Н), 2.31 (с, 3Н).
Пример 2. Получение 8-гидрокси-6-(2-гидроксифенил)-9-(4-нитробензоил)-1-(фениламино)-2-тиоксо-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-диона (IIb).
К раствору 0.3 ммоль 3-(4-нитробензоил)-1H-бензо[b]пирроло[1,2-d][1,4]оксазин-1,2,4-триона (Ib) в 1 мл безводного ацетонитрила добавляли 0.3 ммоль 2-фенилгидразин-1-карботиамида. Реакционную массу кипятили в течение 60 минут. Выход 63%, т.пл. 207-208°С. Соединение (IIb) C25H17N5O7S.
Найдено, %:
Вычислено, %: С, 56.50; Н, 3.22; N, 13.18; S, 6.03.
Соединение (IIb) - желтое кристаллическое вещество, легкорастворимое в ДМСО, ДМФА, растворимое в дихлорметане, хлороформе, ацетоне, спиртах, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях
В ИК спектре соединения (IIb), записанном в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний гидроксилыгых групп гидроксифенила и пиррол-2-она 3412, 3177 см-1, карбонильных групп пиррол-2-она, тиогидантоина и бензоила 1730, 1616, 1600 см-1.
Спектр ЯМР 1Н (400 МГц, DMSO-d6, δ, м.д.): 12.27 (с, 1Н), 9.63 (с, 1H), 8.26 (д, J=8.4 Гц, 2Н), 8.08 (д, J=8.4 Гц, 2Н), 7.42-7.28 (м, 2Н), 7.18 (т, J=7.9 Гц, 1H), 7.11-6.98 (м, 2Н), 6.97-6.88 (м, 3Н), 6.84-6.76 (м, 1H), 6.71-6.57 (м, 2Н).
Пример 3. Фармакологическое исследование 8-гидрокси-6-(2-гидроксифенил)-9-ароил-1-(фениламино)-2-тиоксо-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-дионов (IIa,b) на наличие противомикробной активности.
Противомикробные свойства химических веществ изучали на 2-х коллекционных условно-патогенных штаммах микроорганизмов: Staphylococcus aureus (АТСС 25923) и Candida albicans (РКПГY 1353/1277).
Для исследования противомикробного действия использовали общепринятый метод двукратных серийных разведений в жидкой питательной среде микрометодом [Хабриев Р.У. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. - М.: И-во Медицина, 2005. - 832 с.]. Готовили исходные разведения микроорганизмов в физиологическом растворе из суточной агаровой культуры по оптическому стандарту мутности (ОСО) на 5 ME с использованием денситометра. После ряда разведений конечная концентрация клеток в опыте составляла 2.5×105 клеток/мл.
В лунках стерильного 96 луночного плоскодонного микропланшета готовили два параллельных ряда двукратных серийных разведений химических соединений в бульоне РПБ, Сабуро. В каждой лунке содержалось 150 мкл определенной концентрации испытуемого вещества и 150 мкл инокулята культуры. В последних рядах содержалась питательная среда и культура в равных объемах (контроль). Максимально испытанная концентрация соответствовала 1000.0 мкг/мл, минимальная - 1.0 мкг/мл. Микропланшет помещали в термостат спектрофотометра Epoch и замеряли оптическую плотности (ОП) при длине волны 540 нм. Через 24 часа и 7 суток вновь регистрировали ОП культуральной жидкости.
Результаты оценивали с помощью программного обеспечения Gen 5 спектрофотометра для микропланшет Epoch. Последняя лунка ряда с задержкой роста и показателями ОП равной оптической плотности контрольной лунки соответствует минимальной подавляющей концентрацией соединения.
Проведенные исследования показали (Таблица 1), что соединения (IIa,b) проявляют ингибирующее действие относительно штамма Staphylococcus aureus при концентрации 250.0 мкг/мл, бактерицидное действие наступает в концентрациях 500.0 мкг/мл. В отношении культуры Candida albicans соединения (IIa,b) проявляют фунгистатическое действие в концентрации 62.5 мкг/мл, губительное действие наступает от концентрации 125.0-500.0 мкг/мл.
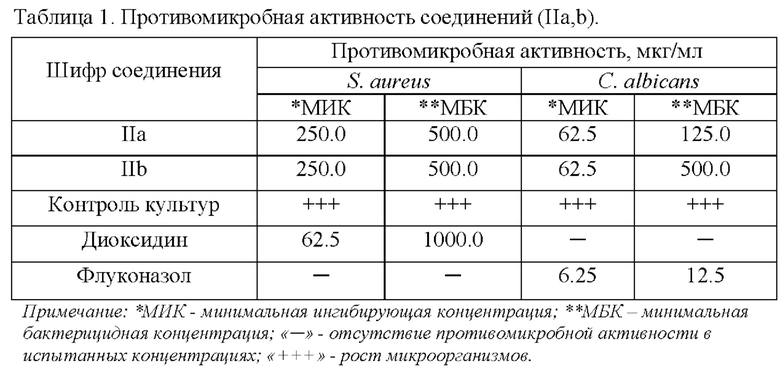
Заявляемые ранее неописанные в литературе 8-гидрокси-6-(2-гидроксифенил)-9-ароил-1-(фениламино)-2-тиоксо-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-дионы могут найти применение в фармакологии в качестве потенциальных лекарственных средств с противомикробными свойствами.
Изобретение относится к новым биологически активным соединениям класса спиро-тиогидантоинов а именно 8-гидрокси-6-(2-гидроксифенил)-9-ароил-1-(фениламино)-2-тиоксо-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-дионам общей формулы
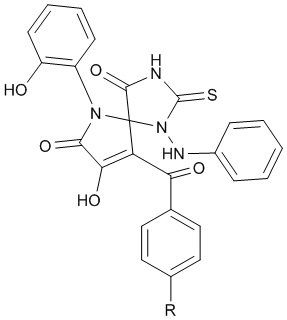
Технический результат: получены новые соединения, обладающие противомикробной активностью, которые могут быть использованы в фармакологии в качестве потенциальных лекарственных средств с противомикробными свойствами. 1 табл., 3 пр.
8-Гидрокси-6-(2-гидроксифенил)-9-ароил-1-(фениламино)-2-тиоксо-1,3,6-триазаспиро[4.4]нон-8-ен-4,7-дионы общей формулы:
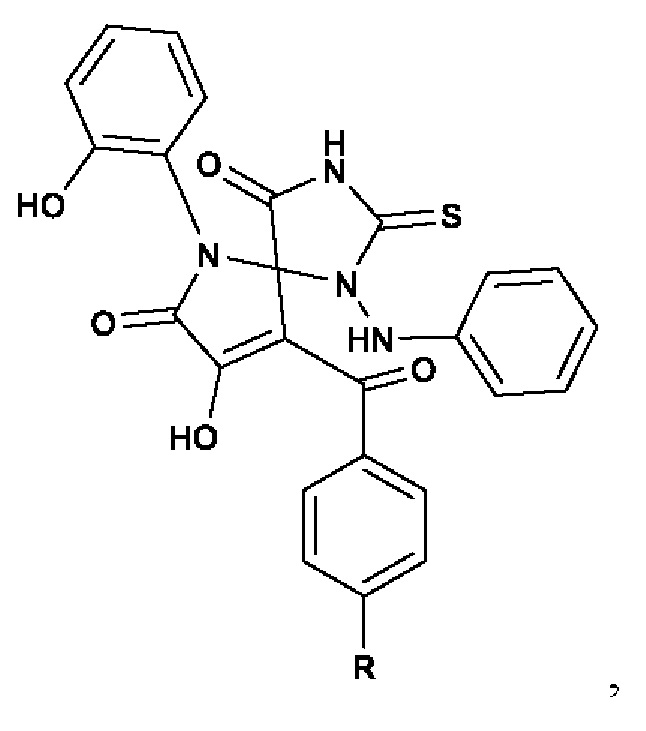
где R= CH3 (а), NO2 (b), обладающие противомикробной активностью.
| Aleksandr I | |||
| Kobelev et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Org | |||
| Chem., 15, 2864-2871, 2019 | |||
| A | |||
| V | |||
| Babenysheva et al | |||
| Spiro-Heterocyclization of Pyrrolobenzoxazinetriones Effected by Thiourea, Russian | |||
Авторы
Даты
2024-09-30—Публикация
2024-03-17—Подача