ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к композициям для местного уменьшения воспаления. Более конкретно, настоящее изобретение относится к композициям, содержащим экстракты семян тмина обыкновенного (Carum carvi) и розмарина лекарственного (Rosmarinus officinalis) для уменьшения воспаления кожи и/или слизистых оболочек.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Известен широкий спектр активных веществ для ухода за кожей, приемлемых для применения в композициях для личной гигиены. Примеры таких активных веществ для ухода за кожей включают экстракт листьев оливкового дерева, который, согласно описанию, проявляет антигипертензивную и гипогликемическую активность, противорадикальные свойства для питательных и косметических средств и противовоспалительную активность при пероральном введении (см., например, публикацию Leaf extract of Olea europea rich in oleuropeine, products from it, their application as medicines and compositions containing them. Combes, Georges; Escaut, Alexandre. Fr. Demande, FR 2507477 A1 19821217, 1982; Gonzalez M, et al, Hypoglycemic activity of olive leaf, Planta Med December 1992; 58(6):513-515; Use of an extract from the leaves of Olea Europea as an antiradical agent. Amari, Giorgio. Eur. Pat. Appl. (1999), EP 937455 A1 19990825; Fehri B, et al. Olea europaea L.: stimulant, anti-ulcer and antiinflammatory effects. Boll Chim Farm (1996) 135(1): 42-49), сигезбекию (чудо-трава), которая используется в качестве лекарства от малярии, ревматизма, почечной колики и в качестве средства от стригущего лишая в сочетании с глицерином, древесина растения саппан (Lignum Sappan), которая используется для улучшения кровообращения и устранения закупорки кровеносных сосудов, а также для уменьшения отека и облегчения боли, а также пиретрум, имеющий признанные значительные лекарственные свойства при пероральном введении и применяющийся в качестве общего жаропонижающего средства. Другие активные вещества для ухода за кожей включают масляные экстракты, такие как масляный экстракт босвеллии пильчатой (Boswellia Serrata (ладан)), для которого описаны противоопухолевые и антиартритные свойства, и экстракт овсяного масла, для которого описаны противораздражающие и антиоксидантные свойства.
Существует постоянная потребность в разработке комбинаций активных веществ для ухода за кожей в целях эффективного лечения, уменьшения и/или предотвращения воспаления кожи различного происхождения. Несмотря на то что существует множество активных веществ, которые, как правило, проявляют противовоспалительные свойства по существу трудно, если не невозможно, спрогнозировать комбинацию таких активных веществ, которая будет проявлять неожиданно высокие синергические противовоспалительные свойства и эффективность снижения воспаления.
Кроме того, в некоторых вариантах применения может быть желательно использовать относительно низкие количества активных веществ с точки зрения себестоимости, для уменьшения нежелательного цвета или запаха, ассоциирующегося с определенными активными веществами, по соображениям стабильности и т.п. Однако многие активные вещества или их комбинации, как правило, проявляют относительно малую эффективность или отсутствие эффективности для снижения воспаления при применении в относительно низких количествах. Соответственно, существует постоянная потребность в комбинациях активных веществ для ухода за кожей, которые проявляют относительно высокие синергические противовоспалительные свойства и эффективность, и в определенных комбинациях, которые могут также быть эффективными даже в относительно низких количествах.
ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Соответственно, один аспект изобретения предусматривает композицию, содержащую:
экстракт семян тмина обыкновенного (Carum carvi);
экстракт розмарина лекарственного (Rosmarinus officinalis); и
фармацевтически и/или косметически приемлемый носитель.
В одном или более вариантах осуществления композиция дополнительно содержит материал, выбранный из группы, состоящей из поверхностно-активных веществ, хелатирующих агентов, мягчителей, увлажнителей, кондиционеров, консервантов, замутнителей, ароматизаторов и комбинаций двух или более из них. В некоторых вариантах осуществления экстракт семян тмина обыкновенного (Carum carvi) и экстракт розмарина лекарственного (Rosmarinus officinalis), каждый независимо, содержат полярный экстракт. В дополнительных вариантах осуществления экстракт семян тмина обыкновенного (Carum carvi) и экстракт розмарина лекарственного (Rosmarinus officinalis) содержат полярные экстракты. В одном или более вариантах осуществления полярный экстракт экстрагировали одним или более растворителями, выбранными из группы, состоящей из C1-C8 спиртов, C1-C8 полиолов, C1-C8 гликолей и их комбинаций. В некоторых вариантах осуществления экстракт семян тмина обыкновенного (Carum carvi) и экстракт розмарина лекарственного (Rosmarinus officinalis), каждый независимо, содержат один или более растворителей, содержащих этанол и воду. В одном или более вариантах осуществления один или оба из экстракта семян тмина обыкновенного (Carum carvi) и экстракта розмарина лекарственного (Rosmarinus officinalis) по существу свободны от неполярных экстрактов. В некоторых вариантах осуществления один или оба из экстракта семян тмина обыкновенного (Carum carvi) и экстракта розмарина лекарственного (Rosmarinus officinalis) по существу свободны от эфирных масел. В одном или более вариантах осуществления композиция представлена в форме таблетки, пилюли или капсулы. В некоторых вариантах осуществления композиция представлена в форме раствора, суспензии, эмульсии, лосьона, крема, сыворотки, геля, карандаша, спрея, мази, жидкого средства для мытья, бруска мыла, шампуня, кондиционера для волос, пасты, пены, порошка, мусса, крема для бритья, гидрогеля или пленкообразующего продукта. В одном или более вариантах осуществления экстракт семян тмина обыкновенного (Carum carvi) и экстракт розмарина лекарственного (Rosmarinus officinalis) присутствуют в композиции в объединенной концентрации от около 0,1 до около 20 мас. % общей массы композиции. В некоторых вариантах осуществления экстракт семян тмина обыкновенного (Carum carvi) и экстракт розмарина лекарственного (Rosmarinus officinalis) присутствуют в соотношении от около 1:2 до около 1:100. В одном или более вариантах осуществления экстракт семян тмина обыкновенного (Carum carvi) присутствует в концентрации от около 50 до около 350 мкг/мл, а экстракт розмарина лекарственного (Rosmarinus officinalis) представляет собой экстракт листьев розмарина лекарственного (Rosmarinus officinalis), присутствующий в концентрации от около 0,5 до около 25 мкг/мл. В некоторых вариантах осуществления экстракт семян тмина обыкновенного (Carum carvi) присутствует в концентрации около 50 мкг/мл, а экстракт листьев розмарина лекарственного (Rosmarinus officinalis) присутствует в концентрации от около 0,5 до около 5 мкг/мл.
Другой аспект изобретения относится к способу уменьшения воспаления, включающему:
введение нуждающемуся в этом пациенту терапевтически эффективной дозы композиции, содержащей экстракт семян тмина обыкновенного (Carum carvi) и экстракт розмарина лекарственного (Rosmarinus officinalis).
В одном или более вариантах осуществления воспаление представляет собой опосредованное рецептором CCR2 воспаление. В некоторых вариантах осуществления экстракт семян тмина обыкновенного (Carum carvi) и экстракт листьев розмарина лекарственного (Rosmarinus officinalis), каждый независимо, содержат полярный экстракт. В дополнительных вариантах осуществления экстракт семян тмина обыкновенного (Carum carvi) и экстракт розмарина лекарственного (Rosmarinus officinalis) содержат полярные экстракты. В одном или более вариантах осуществления полярный экстракт экстрагировали одним или более растворителями, выбранными из группы, состоящей из C1-C8 спиртов, C1-C8 полиолов, C1-C8 гликолей и их комбинаций. В некоторых вариантах осуществления один или оба из экстракта семян тмина обыкновенного (Carum carvi) и экстракта листьев розмарина лекарственного (Rosmarinus officinalis) по существу свободны от неполярных экстрактов. В одном или более вариантах осуществления один или оба из экстракта семян тмина обыкновенного (Carum carvi) и экстракта листьев розмарина лекарственного (Rosmarinus officinalis) по существу свободны от эфирных масел. В некоторых вариантах осуществления композицию наносят на поверхность кожи пациента. В одном или более вариантах осуществления композицию наносят на слизистую оболочку пациента. В некоторых вариантах осуществления композицию вводят в форме раствора, суспензии, лосьона, крема, сыворотки, геля, карандаша, спрея, мази, жидкого средства для мытья, бруска мыла, шампуня, кондиционера для волос, пасты, пены, порошка, мусса, крема для бритья, гидрогеля или пленкообразующего продукта. В одном или более вариантах осуществления композицию вводят перорально. В некоторых вариантах осуществления композицию вводят в форме таблетки, пилюли, капсулы. В одном или более вариантах осуществления экстракт семян тмина обыкновенного (Carum carvi) и экстракт розмарина лекарственного (Rosmarinus officinalis) присутствуют в композиции в объединенной концентрации от около 0,1 до около 20 мас. % общей массы композиции. В некоторых вариантах осуществления экстракт семян тмина обыкновенного (Carum carvi) и экстракт розмарина лекарственного (Rosmarinus officinalis) присутствуют в соотношении от около 1:2 до около 1:100. В одном или более вариантах осуществления экстракт семян тмина обыкновенного (Carum carvi) присутствует в концентрации от около 50 до около 350 мкг/мл, а экстракт розмарина лекарственного (Rosmarinus officinalis) представляет собой экстракт листьев розмарина лекарственного (Rosmarinus officinalis), присутствующий в концентрации от около 0,5 до около 25 мкг/мл. В некоторых вариантах осуществления экстракт семян тмина обыкновенного (Carum carvi) присутствует в концентрации около 50 мкг/мл, а экстракт листьев розмарина лекарственного (Rosmarinus officinalis) присутствует в концентрации от около 0,5 до около 5 мкг/мл.
Еще один аспект изобретения предусматривает композицию, содержащую:
экстракт семян тмина обыкновенного (Carum carvi) в концентрации от около 50 до около 350 мкг/мл;
экстракт листьев розмарина лекарственного (Rosmarinus officinalis) в концентрации от около 0,5 до около 25 мкг/мл; и
фармацевтически и/или косметически приемлемый носитель, причем экстракт семян тмина обыкновенного (Carum carvi) и экстракт листьев розмарина лекарственного (Rosmarinus officinalis) представляют собой водно-спиртовые экстракты, и при этом композиция представлена в форме раствора, суспензии, эмульсии, лосьона, крема, сыворотки, геля, карандаша, спрея, мази, жидкого средства для мытья, бруска мыла, шампуня, кондиционера для волос, пасты, пены, порошка, мусса, крема для бритья, гидрогеля или пленкообразующего продукта. В некоторых вариантах осуществления экстракт семян тмина обыкновенного (Carum carvi) присутствует в концентрации около 50 мкг/мл, а экстракт листьев розмарина лекарственного (Rosmarinus officinalis) присутствует в концентрации от около 0,5 до около 5 мкг/мл.
Эти и прочие отличительные признаки и преимущества настоящего изобретения будут понятны из дальнейшего подробного описания изобретения.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящем документе термин «кожа, требующая уменьшения воспаления» означает участок или область кожи пациента, демонстрирующую красноту или эритему, отечность или реакцию, или чувствительность, на воздействие внешних элементов. Внешние элементы включают в себя, без ограничений, солнечные лучи (УФ-излучение, излучение видимого спектра, ИК-излучение), микроорганизмы, атмосферные загрязнители, такие как озон, выбросы в воздушную среду, хлор и соединения, продуцирующие хлор, сигаретный дым, холод, нагревание, мыла и моющие средства, косметические средства, украшения. Воспалительные расстройства и смежные состояния, которые могут подлежать лечению или профилактике с использованием композиций настоящего изобретения, включают в себя, без ограничений, артрит, бронхит, контактный дерматит, атопический дерматит, псориаз, себорейный дерматит, сумаховый дерматит, экзему, аллергический дерматит, полиморфные легкие высыпания, воспалительные дерматозы, фолликулит, алопецию, воздействие ядовитого плюща, укусы насекомых, угревое воспаление, раздражение под воздействием внешних факторов, включая, без ограничений, химические вещества, травмы, загрязнители (такие как сигаретный дым) и воздействие солнца, вторичные состояния, связанные с воспалением, включая, без ограничений, ксероз, гиперкератоз, зуд, поствоспалительную гиперпигментацию, рубцевание и т.п. В одном или более вариантах осуществления воспалительные расстройства и смежные состояния, которые могут подлежать лечению или профилактике с использованием способов, составляющих предмет настоящего изобретения, представляют собой артрит, воспалительные дерматозы, контактный дерматит, аллергический дерматит, атопический дерматит, полиморфные легкие высыпания, раздражение, включая эритему, обусловленную внешними факторами, угревое воспаление, псориаз, себорейный дерматит, экзему, воздействие ядовитого плюща, ядовитого дуба, ядовитого сумаха, укусы насекомых, фолликулит, алопецию, а также вторичные состояния и т.п.
В настоящем документе формулировка «косметически/дерматологически приемлемый» означает приемлемый для применения в контакте с тканями (например, кожей или волосами) без проявления чрезмерной токсичности, несовместимости, нестабильности, раздражения и/или аллергической реакции и т.п.
В настоящем документе термин «безопасное и эффективное количество» означает количество, достаточное для инициирования необходимого эффекта, но достаточно низкое для предотвращения серьезных побочных эффектов. Безопасное и эффективное количество соединения, экстракта или композиции меняется, например, в зависимости от возраста, состояния здоровья конечного потребителя, а также воздействия условий окружающей среды, длительности и характера лечения, конкретного используемого экстракта, компонента или композиции, конкретного используемого фармацевтически приемлемого носителя и прочих факторов.
Используемый в настоящем документе термин «эфирное масло» относится к продукту дистилляции, полученному из растения, предпочтительно посредством паровой дистилляции, который содержит характерное ароматическое вещество растения или конкретной части растения, из которого он получен. В некоторых вариантах осуществления эфирное масло представляет собой концентрированную полученную из растения гидрофобную жидкость, которая содержит смесь летучих масел (включая, например, летучие ароматические соединения).
В настоящем документе термин «по существу свободен от» ингредиента означает содержание менее 0,1 весового процентного содержания, или менее 0,01 весового процентного содержания, или отсутствие ингредиента.
Для обеспечения большей краткости описания некоторые количественные выражения, приведенные в настоящем документе, не уточняются с использованием термина «около». Подразумевается, что независимо от того, применяется ли термин «около» явным образом или нет, предполагается, что каждое приведенное в настоящем документе численное значение относится к фактическому данному значению, а также предполагается, что оно относится к приближению к такому данному значению, которое может в разумной мере оценивать на основании знаний среднего специалиста в данной области, включая приближения, связанные с условиями проведения эксперимента и/или измерения для такого данного значения.
Для обеспечения большей краткости описания некоторые количественные выражения в настоящем документе указаны как диапазон от около количества X до около количества Y. Понятно, что, когда указан диапазон, он не ограничен указанными верхней и нижней границами, а включает в себя полный диапазон значений от около количества X до около количества Y либо любое количество или диапазон в этих пределах.
Соответственно, один аспект изобретения предусматривает композицию, содержащую: экстракт семян тмина обыкновенного (Carum carvi); экстракт розмарина лекарственного (Rosmarinus officinalis); и фармацевтически и/или косметически приемлемый носитель. Неожиданно было обнаружено, что такие композиции, содержащие экстракты семян тмина обыкновенного (Carum carvi) и экстракт розмарина лекарственного (Rosmarinus officinalis), обеспечивают неожиданно хорошие противовоспалительные свойства. При объединении экстракты проявляют синергический противовоспалительный эффект. Все протестированные комбинации экстракта семян тмина обыкновенного (Carum carvi) и розмарина лекарственного (Rosmarinus officinalis) являются синергическими (проявляющими > 1-кратное увеличение относительно аддитивных уровней) и даже 1,5-кратное или 2-кратное увеличение в некоторых комбинациях. Фактически было показано, что существуют ситуации, когда один или оба экстракта могут не обеспечивать какого-либо значительного противовоспалительного результата для данного маркера, однако демонстрируют сильные противовоспалительные свойства при объединении двух экстрактов.
Экстракт семян тмина обыкновенного (Carum carvi)
Тмин обыкновенный (Carum carvi), обычно известный как тмин, является двухлетним растением, встречающимся в различных частях Азии, Европы и Африки.
Используемый в настоящем документе термин «экстракт семян тмина обыкновенного (Carum carvi)» обозначает экстракт семян из этого растения. Для настоящего изобретения можно применять любой приемлемый способ приготовления экстрактов семян тмина обыкновенного (Carum carvi). Приемлемые экстракты можно получить с применением традиционных способов, включая, без ограничений, прямое экстрагирование вещества из биомассы путем измельчения, мацерации, прессования, отжимания, сминания, центрифугирования и/или таких способов, как холодная перколяция, перемешивание/дистилляция, микроволновое экстрагирование, ультразвуковая обработка, экстрагирование газообразным СО2 при суперкритическом/субкритическом сжатии в присутствии или отсутствии модификатора полярности, экстрагирование растворителем под давлением, ускоренное экстрагирование растворителем, экстрагирование горячей водой при повышенном давлении в присутствии поверхностно-активного вещества, масляное экстрагирование, мембранное экстрагирование, экстрагирование в аппарате Сокслета, дистилляция/экстрагирование методом «золотого пальца», и/или процессы, раскрытые, например, в патентах США №7,442,391, 7,473,435 и 7,537,791, выданных компании Integrated Botanical Technologies, LLC и включенных в настоящий документ путем ссылки; и т.п., либо с использованием других способов, таких как экстрагирование растворителем и т.п. В частности, экстракт в соответствии с настоящим изобретением может являться продуктом экстрагирования, полученным путем измельчения или мацерации растительного материала в растворителе, как правило, органическом растворителе, таком как спирт, ацетон, жидкая двуокись углерода с модификатором полярности или без него, гексан или хлороформ. Полученный экстракт содержит преимущественно неполярные соединения. Растительную биомассу можно полностью отделить от экстракта и не использовать после экстрагирования.
В способах, включающих экстрагирование растворителем, можно применять любой из различных растворителей, включая полярные растворители, неполярные растворители или комбинации двух или более из них. В одном или более вариантах осуществления используется полярный растворитель. Приемлемые полярные растворители включают полярные неорганические растворители, такие как вода и т.п., полярные органические растворители, такие как спирты и соответствующие органические кислоты, например C1-C8 спирты, включая метанол, этанол, пропанол, бутанол и т.п., а также органические кислоты, включая уксусную кислоту, муравьиную кислоту, пропановую кислоту и т.п., полиолы и гликоли, включая C1-C8 полиолы/гликоли и т.п., а также комбинации двух или более из них. Приемлемые неполярные растворители включают неполярные органические растворители, такие как алканы, включая C1-C8 алканы, циклоалканы, включая C1-C8 алканы, алкилэфиры, включая C1-C8 алкилэфиры, петролейные эфиры, кетоны, включая C1-C8 кетоны, метиленхлорид, этилацетат, ксилол, толуол, хлороформ, растительное масло, минеральное масло и т.п. В другом варианте осуществления экстрагирование можно провести с применением неполярных растворителей, описанных выше, или путем сверхкритического жидкостного экстрагирования в присутствии или при отсутствии полярного модификатора, такого как C1-C8 спирты, вода, C1-C8 полиолы/гликоли или C1-C8 органические кислоты.
В одном или более вариантах осуществления экстракт представляет собой полярный экстракт. Полярный экстракт означает экстракт, полученный путем обработки растения или частей растения полярным растворителем. В определенных предпочтительных вариантах осуществления экстракт, приготовленный путем измельчения семян тмина обыкновенного (Carum carvi) и экстрагирования при помощи полярного растворителя со значением диэлектрической постоянной от 1 до 100 при 20°С, в частности с диэлектрической постоянной со значением от 4 до 60 при 20°С, в частности с диэлектрической постоянной со значением от 4 до 50 при 20°С и в частности с диэлектрической постоянной со значением от 4 до 40 при 20°С. Примеры приемлемых полярных растворителей включают в себя C1-C8 спирты, C1-C8 полиолы/гликоли, C1-C8 органические кислоты, воду и комбинации двух или более из них, имеющие значение диэлектрической постоянной от 1 до 100, в частности от 4 до 60, в частности от 5 до 40 при 20°С, включая, без ограничений, растворители и комбинации растворителей, имеющие требуемое значение диэлектрической постоянной, как раскрыто в работе Dielectric Constants of Some Organic Solvent-Water Mixtures at Various Temperatures, авторы Akerlof, Gosta; JACS, Vol. 54, No. 11 (Nov. 1932), pp. 4125-4139, полностью включенной в настоящую заявку путем ссылки. В некоторых вариантах осуществления полярный экстракт экстрагируют с применением одного или более C1-C8 спиртов, C1-C8 полиолов, C1-C8 гликолей и комбинации двух или более из них. В одном или более вариантах осуществления экстракт экстрагируют с применением одного или более С1-С4 спиртов, С1-С4 полиолов и/или С1-С4 гликолей.
В некоторых вариантах осуществления экстракт готовят с применением растворителя, содержащего метанол, этанол или их комбинацию при наличии или отсутствии воды. В одном или более предпочтительных вариантах осуществления экстракт можно дополнительно очистить, обработав древесным углем (также называемым активированным углем). В одном или более вариантах осуществления экстракт представляет собой водно-спиртовой экстракт (т.е. смесь спирта в воде). В некоторых вариантах осуществления водно-спиртовой экстракт содержит от около 5% до 10% спирта в воде. В некоторых вариантах осуществления экстракт изобретения представляет собой экстракт, приготовленный путем измельчения семян тмина обыкновенного (Carum carvi) и экстрагирования при помощи растворителя со значением диэлектрической постоянной от около 1 до около 80 при 20°С, конкретно, со значением диэлектрической постоянной от около 2 до около 60 при 20°С, более конкретно, со значением диэлектрической постоянной от около 2 до около 40 при 20°С, еще более конкретно, со значением диэлектрической постоянной от около 2 до около 35 при 20°С.
В некоторых вариантах осуществления композиция по существу не содержит экстракты других частей растения тмина обыкновенного (Carum carvi), кроме семян. В дополнительных вариантах осуществления композиция не содержит экстракты других частей растения тмина обыкновенного (Carum carvi), кроме семян. В некоторых вариантах осуществления композиция может содержать экстракты из клеточных культур растений тмина обыкновенного (Carum carvi). В одном или более вариантах осуществления экстракт семян тмина обыкновенного (Carum carvi) по существу свободен от неполярных экстрактов. В дополнительных вариантах осуществления экстракт семян тмина обыкновенного (Carum carvi) не содержит неполярных экстрактов. В некоторых вариантах осуществления как экстракт семян тмина обыкновенного (Carum carvi), так и экстракт розмарина лекарственного (Rosmarinus officinalis) по существу свободны от неполярных экстрактов. В дополнительных вариантах осуществления как экстракт семян тмина обыкновенного (Carum carvi), так и экстракт розмарина лекарственного (Rosmarinus officinalis) не содержит неполярных экстрактов. В одном или более вариантах осуществления экстракт семян тмина обыкновенного (Carum carvi) по существу свободен от эфирных масел. В одном или более вариантах осуществления экстракт семян тмина обыкновенного (Carum carvi) не содержит эфирных масел. В дополнительных вариантах осуществления как экстракт семян тмина обыкновенного (Carum carvi), так и экстракт розмарина лекарственного (Rosmarinus officinalis) по существу свободны от эфирных масел. В также дополнительных вариантах осуществления как экстракт семян тмина обыкновенного (Carum carvi), так и экстракт розмарина лекарственного (Rosmarinus officinalis) не содержат эфирных масел. В некоторых вариантах осуществления как экстракт семян тмина обыкновенного (Carum carvi), так и экстракт розмарина лекарственного (Rosmarinus officinalis) по существу свободны от летучих компонентов. В некоторых вариантах осуществления как экстракт семян тмина обыкновенного (Carum carvi), так и экстракт розмарина лекарственного (Rosmarinus officinalis) не содержат летучих компонентов.
В композициях для местного нанесения настоящего изобретения можно использовать любое приемлемое количество экстракта семян тмина обыкновенного (Carum carvi). В одном или более вариантах осуществления композиции содержат от более нуля до около 20% экстракта семян тмина обыкновенного (Carum carvi). В некоторых вариантах осуществления композиции содержат от около 0,0001 до около 20%, от около 0,001 до около 10%, от около 0,01 до около 5%, от около 0,1 до около 5% или от около 0,2 до около 2% экстракта семян тмина обыкновенного (Carum carvi). В одном или более вариантах осуществления композиции содержат от более нуля до около 1%, от около 0,0001 до около 1%, от около 0,001 до около 1% или от около 0,01 до около 1% экстракта семян тмина обыкновенного (Carum carvi). В некоторых вариантах осуществления композиции содержат от около 1% до около 5%, конкретно, от около 2% до около 5% экстракта семян тмина обыкновенного (Carum carvi).
Экстракт розмарина лекарственного (Rosmarinus officinalis)
Используемый в настоящем документе термин «экстракт розмарина лекарственного (Rosmarinus officinalis)» относится к экстракту из любой из надземных частей растения розмарина лекарственного (Rosmarinus officinalis), например одного или более из стебля или листьев. В других вариантах осуществления композиция по существу не содержит экстракты других частей растения розмарина лекарственного (Rosmarinus officinalis), кроме стебля и листьев.
Можно применять любой приемлемый способ приготовления экстрактов розмарина лекарственного (Rosmarinus officinalis) для применения в соответствии с настоящим изобретением. Приемлемые экстракты можно получить с применением традиционных способов, включая, без ограничений, прямое экстрагирование вещества из биомассы путем измельчения, мацерации, прессования, отжимания, сминания, центрифугирования и/или таких способов, как холодная перколяция, перемешивание/дистилляция, микроволновое экстрагирование, ультразвуковая обработка, экстрагирование газообразным СО2 при суперкритическом/субкритическом сжатии в присутствии или отсутствии модификатора полярности, экстрагирование растворителем под давлением, ускоренное экстрагирование растворителем, экстрагирование горячей водой при повышенном давлении в присутствии поверхностно-активного вещества, масляное экстрагирование, мембранное экстрагирование, экстрагирование в аппарате Сокслета, дистилляция/экстрагирование методом «золотого пальца», и/или процессы, раскрытые, например, в патентах США №7,442,391, 7,473,435 и 7,537,791, выданных компании Integrated Botanical Technologies, LLC и включенных в настоящий документ путем ссылки; и т.п., либо с использованием других способов, таких как экстрагирование растворителем и т.п. В частности, экстракт в соответствии с настоящим изобретением может являться продуктом экстрагирования, полученным путем измельчения или мацерации растительного материала в растворителе, как правило, органическом растворителе, таком как спирт, ацетон, жидкая двуокись углерода с модификатором полярности или без него, гексан или хлороформ. Полученный экстракт содержит преимущественно неполярные соединения. Растительную биомассу можно полностью отделить от экстракта и не использовать после экстрагирования.
В способах, включающих экстрагирование растворителем, можно применять любой из различных растворителей, включая полярные растворители, неполярные растворители или комбинации двух или более из них. В одном или более вариантах осуществления используются полярные растворители. Приемлемые полярные растворители включают полярные неорганические растворители, такие как вода и т.п., полярные органические растворители, такие как спирты и соответствующие органические кислоты, например C1-C8 спирты, включая метанол, этанол, пропанол, бутанол и т.п., а также органические кислоты, включая уксусную кислоту, муравьиную кислоту, пропановую кислоту и т.п., полиолы и гликоли, включая C1-C8 полиолы/гликоли и т.п., а также комбинации двух или более из них. Приемлемые неполярные растворители включают неполярные органические растворители, такие как алканы, включая C1-C8 алканы, циклоалканы, включая C1-C8 алканы, алкилэфиры, включая C1-C8 алкилэфиры, петролейные эфиры, кетоны, включая C1-C8 кетоны, метиленхлорид, этилацетат, ксилол, толуол, хлороформ, растительное масло, минеральное масло и т.п. В другом варианте осуществления экстрагирование можно провести с применением неполярных растворителей, описанных выше, или путем сверхкритического жидкостного экстрагирования в присутствии или при отсутствии полярного модификатора, такого как C1-C8 спирты, вода, C1-C8 полиолы/гликоли или C1-C8 органические кислоты. В одном или более вариантах осуществления экстракт представляет собой полярный экстракт. Полярный экстракт означает экстракт, полученный путем обработки растения или частей растения полярным растворителем. В определенных предпочтительных вариантах осуществления, экстракт, приготовленный путем измельчения листьев розмарина лекарственного (Rosmarinus officinalis) и экстрагирования при помощи полярного растворителя со значением диэлектрической постоянной от 1 до 100 при 20°С, конкретно, со значением диэлектрической постоянной от 4 до 60 при 20°С, более конкретно, со значением диэлектрической постоянной от 4 до 50 при 20°С и еще более конкретно, со значением диэлектрической постоянной от 4 до 40 при 20°С.
Примеры приемлемых полярных растворителей включают в себя C1-C8 спирты, C1-C8 полиолы/гликоли, C1-C8 органические кислоты, воду и комбинации двух или более из них, имеющие значение диэлектрической постоянной от 1 до 100, в частности от 4 до 60, в частности от 5 до 40 при 20°С, включая, без ограничений, растворители и комбинации растворителей, имеющие требуемое значение диэлектрической постоянной, как раскрыто в работе Dielectric Constants of Some Organic Solvent-Water Mixtures at Various Temperatures, авторы Akerlof, Gosta; JACS, Vol. 54, No. 11 (Nov. 1932), pp. 4125-4139, полностью включенной в настоящую заявку путем ссылки. В одном или более вариантах осуществления экстракт экстрагируют с применением одного или более C1-C8 спиртов, C1-C8 полиолов, C1-C8 гликолей и комбинации двух или более из них. В некоторых вариантах осуществления экстракт экстрагируют с применением одного или более С1-С4 спиртов, С1-С4 полиолов и/или С1-С4 гликолей.
В одном или более вариантах осуществления экстракт готовят с применением растворителя, содержащего метанол, этанол или их комбинацию при наличии или отсутствии воды. В некоторых вариантах осуществления экстракт можно дополнительно очистить, обработав древесным углем (также называемым активированным углем). В одном или более вариантах осуществления экстракт представляет собой водно-спиртовой экстракт (т.е. смесь спирта в воде). В некоторых вариантах осуществления водно-спиртовой экстракт содержит от около 5% до 10% спирта в воде.
В одном или более вариантах осуществления экстракт изобретения представляет собой экстракт, приготовленный путем измельчения листьев розмарина лекарственного (Rosmarinus officinalis) и экстрагирования при помощи растворителя со значением диэлектрической постоянной от около 1 до около 80 при 20°С, конкретно, со значением диэлектрической постоянной от около 2 до около 60 при 20°С, более конкретно, со значением диэлектрической постоянной от около 2 до около 40 при 20°С, еще более конкретно, со значением диэлектрической постоянной от около 2 до около 35 при 20°С.
В некоторых вариантах осуществления композиция может содержать экстракты из клеточных культур растения розмарин лекарственный (Rosmarinus officinalis). В одном или более вариантах осуществления экстракт розмарина лекарственного (Rosmarinus officinalis) по существу свободен от неполярных экстрактов. В дополнительных вариантах осуществления как экстракт семян тмина обыкновенного (Carum carvi), так и экстракт розмарина лекарственного (Rosmarinus officinalis) по существу свободны от неполярных экстрактов. В одном или более вариантах осуществления экстракт розмарина лекарственного (Rosmarinus officinalis) по существу свободен от эфирных масел. В одном или более вариантах осуществления экстракт розмарина лекарственного (Rosmarinus officinalis) не содержит эфирных масел. В дополнительных вариантах осуществления как экстракт семян тмина обыкновенного (Carum carvi), так и экстракт розмарина лекарственного (Rosmarinus officinalis) по существу свободны от эфирных масел. В дополнительных вариантах осуществления как экстракт семян тмина обыкновенного (Carum carvi), так и экстракт розмарина лекарственного (Rosmarinus officinalis) не содержат эфирных масел. В некоторых вариантах осуществления как экстракт семян тмина обыкновенного (Carum carvi), так и экстракт розмарина лекарственного (Rosmarinus officinalis) по существу свободны от летучих компонентов.
В композициях для местного нанесения настоящего изобретения можно использовать любое приемлемое количество экстракта розмарина лекарственного (Rosmarinus officinalis). В некоторых вариантах осуществления композиции содержат от более нуля до около 20% экстракта розмарина лекарственного (Rosmarinus officinalis). В одном или более вариантах осуществления композиции содержат от около 0,0001 до около 20%, от около 0,001 до около 10%, от около 0,01 до около 5%, от около 0,1 до около 5% или от около 0,2 до около 2% экстракта розмарина лекарственного (Rosmarinus officinalis).
В некоторых вариантах осуществления композиции содержат от более нуля до около 1%, от около 0,0001 до около 1%, от около 0,001 до около 1% или от около 0,01 до около 1% экстракта розмарина лекарственного (Rosmarinus officinalis). В одном или более вариантах осуществления композиции содержат от около 1% до около 5%, конкретно, от около 2% до около 5% экстракта розмарина лекарственного (Rosmarinus officinalis).
В композициях настоящего изобретения можно использовать любое приемлемое количество экстракта семян тмина обыкновенного (Carum carvi) и экстракта розмарина лекарственного (Rosmarinus officinalis). В одном или более вариантах осуществления композиции содержат безопасное и эффективное количество экстракта семян тмина обыкновенного (Carum carvi) и экстракта розмарина лекарственного (Rosmarinus officinalis). В частности, количества используемого экстракта семян тмина обыкновенного (Carum carvi) и экстракта розмарина лекарственного (Rosmarinus officinalis) можно выбрать таким образом, чтобы достичь желаемого результата лечения данного воспалительного состояния. В некоторых вариантах осуществления композиции содержат от около 0,0001 до около 20%, от около 0,001 до около 10%, от около 0,01 до около 5%, от около 0,1 до около 5% или от около 0,2 до около 2% экстракта семян тмина обыкновенного (Carum carvi) и экстракта розмарина лекарственного (Rosmarinus officinalis). В одном или более вариантах осуществления композиции содержат от более нуля до около 1%, от около 0,0001 до около 1%, от около 0,001 до около 1% или от около 0,01 до около 1% объединенных экстракта семян тмина обыкновенного (Carum carvi) и экстракта розмарина лекарственного (Rosmarinus officinalis). В некоторых вариантах осуществления композиции содержат от около 1% до около 5%, конкретно, от около 2% до около 5% объединенных экстракта семян тмина обыкновенного (Carum carvi) и экстракта розмарина лекарственного (Rosmarinus officinalis). Эти экстракты семян тмина обыкновенного (Carum carvi) и экстракты розмарина лекарственного (Rosmarinus officinalis) присутствуют в композиции в количествах, которые могут варьироваться в зависимости от конечной точки, соответствующей желаемому полезному эффекту. Например, в некоторых вариантах осуществления, в частности в тех, в которых желательно связывание с рецептором CCR2, массовое соотношение экстракта розмарина лекарственного (Rosmarinus officinalis) к экстракту семян тмина обыкновенного (Carum carvi) составляет от около 1:9 до около 1:70, более конкретно от около 1:17 до около 1:35 и более конкретно около 1:35. В некоторых вариантах осуществления, в частности в тех, в которых желательно снижение уровня интерлейкинов 6 и 8 (IL-6, IL-8), массовое соотношение экстракта розмарина лекарственного (Rosmarinus officinalis) к экстракту семян тмина обыкновенного (Carum carvi) составляет от около 1:2 до около 1:100, более конкретно от около 1:10 до около 1:100 и более конкретно около 1:100.
Носитель
В композициях можно использовать любой приемлемый носитель. В некоторых вариантах осуществления носитель представляет собой косметически приемлемый носитель. Как будет понятно специалисту в данной области, косметически приемлемые носители представляют собой носители, приемлемые для применения в контакте с телом человека, в частности с кожей, без проявления чрезмерной токсичности, несовместимости, нестабильности, раздражения, аллергической реакции и т.п. Безопасное и эффективное количество носителя составляет от около 50, 55, 60, 65, 70, 75, 80, 85, 90, 95 или 98% до около 85, 90, 95, 98, 99, 99,1, 99,5 или 99,9% по массе композиции.
Носитель может присутствовать в широком спектре форм. Например, в настоящем документе подходящими являются носители в форме эмульсий, включая, без ограничений, эмульсии типа «масло-в-воде», «вода-в-масле», «вода-в-масле-в-воде» и «масло-в-воде-в-силиконе». Данные эмульсии могут иметь вязкость в широком диапазоне значений, например, от около 100 сПз до около 200 000 сПз, при измерении с помощью вискозиметра Brookfield RVT.
Примеры подходящих косметически приемлемых носителей включают в себя косметически приемлемые растворители и материалы для косметических растворов, суспензий, лосьонов, кремов, сывороток, эссенций, гелей, тонеров, карандашей, спреев, мазей, жидких средств для мытья и брусков мыла, шампуней, кондиционеров для волос, паст, пен, муссов, пудр, кремов для бритья, влажных салфеток, пластырей, полосок, пропитанных пластырей, микроигольчатых пластырей, повязок, гидрогелей, пленкообразующих продуктов, масок для лица и кожи, декоративной косметики, жидких капель и т.п. Данные типы продуктов могут включать в себя несколько типов косметически приемлемых носителей, включая, без ограничений, растворы, суспензии, эмульсии, такие как микроэмульсии и наноэмульсии, гели, твердые вещества, липосомы, другие технологии инкапсуляции и т.п.
Ниже приведены не ограничивающие примеры носителей. Обычные специалисты в данной области могут вводить в составы другие носители. В одном из вариантов осуществления носитель содержит воду. В дополнительном варианте осуществления носитель может также содержать один или более водных или органических растворителей. Примеры органических растворителей включают в себя, без ограничений: диметил изосорбид; изопропилмиристат; поверхностно-активные вещества катионной, анионной и неионной природы; растительные масла; минеральные масла; воски; камеди; синтетические и натуральные гелеобразующие агенты; алканолы; гликоли; и полиолы. Примеры гликолей включают в себя, без ограничений, глицерин, пропиленгликоль, бутиленгликоль, пенталенгликоль, гексиленгликоль, полиэтиленгликоль, полипропиленгликоль, диэтиленгликоль, триэтиленгликоль, каприлгликоль, глицерин, бутандиол и гексантриол, а также их сополимеры или смеси. Примеры алканолов включают в себя, без ограничений, соединения, имеющие от около 2 атомов углерода до около 12 атомов углерода (например, от около 2 атомов углерода до около 4 атомов углерода), такие как изопропанол и этанол. Примеры полиолов включают в себя, без ограничений, соединения, имеющие от около 2 атомов углерода до около 15 атомов углерода (например, от около 2 атомов углерода до около 10 атомов углерода), такие как пропиленгликоль. Органические растворители могут присутствовать в носителе в количестве, составляющем в расчете на общий вес носителя, от около 1 процента до около 99,99 процентов (например, от около 20 процентов до около 50 процентов). Вода может присутствовать в носителе (перед использованием) в количестве, составляющем в расчете на общую массу носителя от около 5 процентов до около 95 процентов (например, от около 50 процентов до около 90 процентов). Растворы могут содержать любые приемлемые количества растворителя, в том числе от около 40 до около 99,99%. Некоторые растворы содержат от около 50 до около 99,9%, от около 60 до около 99%, от около 70 до около 99%, от около 80 до около 99% или от около 90 до 99% растворителя.
Из такого раствора может быть изготовлен лосьон. Как правило, в дополнение к растворителю лосьоны содержат по меньшей мере один мягчитель. Лосьоны могут содержать от около 1% до около 20% (например, от около 5% до около 10%) мягчителя (-ей) и от около 50% до около 90% (например, от около 60% до около 80%) воды.
Другой тип продукта, который может быть изготовлен из раствора, - это крем. Как правило, крем содержит от около 5% до около 50% (например, от около 10% до около 20%) мягчителя (-ей) и от около 45% до около 85% (например, от около 50% до около 75%) воды.
Еще один тип продукта, который может быть приготовлен из раствора, - это мазь. Мазь может содержать простую основу из животных, растительных или синтетических масел или полутвердых 10 углеводородов. Мазь может содержать от около 2% до около 10% мягчителя (-ей) плюс от около 0,1% до около 2% загустителя (-ей). Композиции, используемые в настоящем изобретении, могут также быть приготовлены в виде эмульсий. Если носитель представляет собой эмульсию, то он содержит от около 1% до около 10% (например, от около 2% до около 5%) эмульгатора (-ов).
Эмульгаторы могут быть неионными, анионными или катионными.
Лосьоны и кремы могут быть изготовлены в виде эмульсий. Как правило, такие лосьоны содержат от 0,5% до около 5% эмульгатора (-ов), тогда как такие кремы, как правило, содержат от около 1% до около 20% (например, от около 5% до около 10%) мягчителя (-ей); от около 20% до около 80% (например, от 30% до около 70%) воды; и от около 1% до около 10% (например, от около 2% до около 5%) эмульгатора (-ов). Препараты для ухода за кожей на основе односторонней эмульсии, такие как лосьоны и кремы типа «масло-в-воде» и типа «вода-в-масле», хорошо известны в данной области и подходят для использования в настоящем изобретении. Композиции на основе многофазной эмульсии, например типа «вода-в-масле-в-воде» или типа «масло-в-воде-в-масле», также используются в заявленном изобретении. Обычно такие одно- или многофазные эмульсии в качестве основных ингредиентов содержат воду, мягчители и эмульгаторы.
Композиции настоящего изобретения также могут быть составлены в виде геля (например, водного, спиртового, водно-спиртового или масляного геля с применением приемлемого (-ых) гелеобразующего (-их) агента (-ов)). Приемлемые гелеобразующие агенты для водных и/или спиртовых гелей включают в себя, без ограничений, природные камеди, акриловую кислоту и акрилатные полимеры и сополимеры, а также производные целлюлозы (например, гидроксиметилцеллюлозу и гидроксипропилцеллюлозу). Приемлемые гелеобразующие агенты для масел (таких как минеральное масло) включают в себя, без ограничений, гидрогенизированный сополимер бутилена/этилена/стирола и гидрогенизированный сополимер этилена/пропилена/стирола. Такие гели, как правило, содержат от около 0,1% до 5% по массе таких гелеобразующих агентов. Композиции настоящего изобретения также можно приготовить в твердой форме (например, в форме карандаша на основе воска, композиции бруска мыла, порошка или влажной салфетки). Композицию настоящего изобретения также можно комбинировать с твердым, полутвердым или растворимым субстратом (например, влажной салфеткой, маской, прокладкой, перчаткой или полоской).
Другие добавки
Композиции настоящего изобретения могут дополнительно содержать любой из ряда дополнительных косметически активных агентов. Примеры приемлемых дополнительных активных агентов включают в себя агенты для осветления кожи, затемняющие агенты, дополнительные агенты, замедляющие старение, стимуляторы тропоэластина, стимуляторы коллагена, противоугревые агенты, агенты для контроля блеска кожи, противомикробные агенты, такие как противодрожжевые агенты, противогрибковые и антибактериальные агенты, противовоспалительные агенты, противопаразитарные агенты, наружные обезболивающие средства, солнцезащитные средства, фотопротекторы, антиоксиданты, кератолитические агенты, очищающие средства/поверхностно-активные вещества, увлажнители, питательные вещества, витамины, агенты, повышающие энергию, антиперспиранты, вяжущие вещества, дезодоранты, средства для удаления волос, агенты для усиления роста волос, агенты для замедления роста волос, агенты для укрепления кожи, усилители гидратации, усилители эффективности, агенты против огрубения кожи, агенты для кондиционирования кожи, антицеллюлитные агенты, агенты для контроля запаха, такие как агенты, маскирующие запах, или агенты, изменяющие рН, и т.п.
Примеры различных приемлемых дополнительных косметически приемлемых активных агентов включают гидроксикислоты; перекись бензоила; D-пантенол; УФ-фильтры, такие как, без ограничений, авобензон (Parsol 1789), бисдисулизол динатрия (Neo Heliopan АР), диэтиламиногидроксибензоилгексилбензоат (Uvinul A Plus), экамсул (Mexoryl SX), метилантранилат, 4-аминобензойная кислота (РАВА), циноксат, этилгексилтриазон (Uvinul Т 150), гомосалат, 4-метилбензилиденкамфора (Parsol 5000), октилметоксициннамат (Octinoxate), октилсалицилат (Octisalate), падимат О (Escalol 507), фенилбензимидазолсульфоновая кислота (Ensulizole), полисиликон-15 (Parsol SLX), троламинсалицилат, бемотризинол (Tinosorb S), бензофеноны 1-12, диоксибензон, дрометризолтрисилоксан (Mexoryl XL), искотризинол (Uvasorb НЕВ), октокрилен, оксибензон (Eusolex 4360), сулизобензон, бисоктризол (Tinosorb М), диоксид титана, оксид цинка; каротиноиды; акцепторы свободных радикалов; спиновые ловушки; ретиноиды и предшественники ретиноидов, такие как ретинол, ретиноевая кислота и ретинилпальмитат; церамиды; полиненасыщенные жирные кислоты; незаменимые жирные кислоты; ферментов; ингибиторы ферментов; минеральные вещества; гормоны, такие как эстрогены; стероиды, такие как гидрокортизон; 2-диметиламиноэтанол; соли меди, такие как хлорид меди; пептиды, содержащие медь, такие как Cu:Gly-His-Lys, кофермент Q10; аминокислоты, такие как пролин; витаминов; лактобионовую кислоту; ацетил-кофермент А; ниацин; рибофлавин; тиамин; рибозу; переносчики электронов, такие как NADH (никотинамидадениндинуклеотид) и FADH2 (восстановленная форма флавинадениндинуклеотида); и другие растительные экстракты, такие как экстракты овса, алоэ вера, пиретрума девичьего, сои, грибов шиитаке, а также их производные и смеси.
Дополнительный косметически активный агент, если он присутствует, может присутствовать в композиции в любом приемлемом количестве, например в количестве от около 0,0001% до около 20% по массе композиции, например от около 0,001% до около 10%, в частности от около 0,01% до около 5%. В некоторых вариантах осуществления - в количестве от 0,1% до 5%, а в других вариантах осуществления - от 1% до 2%.
Композиции настоящего изобретения могут включать в себя косметически эффективное количество одного или более дополнительных противовоспалительных соединений. Примеры приемлемых противовоспалительных агентов включают замещенные резорцины, (Е)-3-(4-метилфенилсульфонил)-2-пропеннитрил (такой как Bay 11-7082 производства компании Sigma-Aldrich, г. Сент-Луис, штат Миссури), тетрагидрокуркуминоиды (такие как Tetrahydrocurcuminoid CG производства компании Sabinsa Corporation, г. Пискатауэй, штат Нью-Джерси), экстракты и вещества, полученные из следующего сырья: экстракта коры (Phellodendron amurense (РСЕ)), неденатурированной сои (Glycine max), пиретрума девичьего (Tanacetum parthenium), имбиря (Zingiber officinale), гинкго (Ginkgo biloba), мадекассосида (ингредиент экстракта Centella asiatica), скумпии (Cotinus coggygria), экстракта белокопытника (Petasites hybridus), плодов годжи (Lycium barbarum), экстракта расторопши пятнистой (Silybum marianum), жимолости (Lonicera japonica), перуанского бальзама (Myroxylon pereirae), шалфея (Salvia officinalis), экстракта клюквы (Vaccinium oxycoccos), амарантового масла (Amaranthus cruentus), граната (Punica granatum), мате (экстракта листьев Ilexparaguariensis), экстракта цветков белой лилии (Lilium candidum), экстракта листьев маслины (Olea europaea), флоретина (экстракт яблок), овсяной муки (Aveena sativa), экстракта Lifenol (хмель: Hamulus lupulus), Bugrane P (Ononis spinosa), ликохалькона (солодка: компонент экстракта Glycyrrhiza inflate), симрелифа (бисаболол и экстракт имбиря), комбинации двух или более из них и т.п. В одном варианте осуществления противовоспалительным агентом является резорцин.
Особенно приемлемые замещенные резорцины включают 4-гексилрезорцин и 4-октилрезорцин, особенно 4-гексилрезорцин. 4-Гексилрезорцин под торговым названием SYNOVEA HR производит компания Sytheon, г. Линкольн-Парк, штат Нью-Джерси. 4-Октилрезорцин доступен в продаже в компании City Chemical LLC, г. Уэст-Хейвен, штат Коннектикут.
Под «экстрактами пиретрума девичьего» подразумевают экстракты растения пижма девичья (Tanacetum parthenium), которые можно получить, например, в соответствии с подробной информацией, приведенной в патенте США №7,537,791 под названием PARTHENOLIDE FREE BIOACTIVE INGREDIENTS FROM FEVERFEW (TANACETUM PARTHENIUM) AND PROCESSES FOR THEIR PRODUCTION. Один особенно приемлемый экстракт пиретрума девичьего в форме, содержащей около 20% активного пиретрума девичьего, доступен в продаже в компании Integrated Botanical Technologies, г. Оссининг, штат Нью-Йорк.
В композициях настоящего изобретения может также присутствовать ряд других материалов. В одном или более вариантах осуществления композиция содержит один или более компонентов для местного применения, которые выбраны из группы, состоящей из поверхностно-активных веществ, хелатирующих агентов, мягчителей, увлажнителей, кондиционеров, консервантов, замутнителей, ароматизаторов и т.п. Под мягчителем понимают соединение, помогающее поддерживать мягкость, гладкость и пластичность кожи (например, путем обеспечения на поверхности кожи или в роговом слое в качестве смазывающего вещества). Примеры приемлемых мягчителей включают мягчители, представленные в главе 35, стр. 399-415 (Skin Feel Agents, G Zocchi) в издании Handbook of Cosmetic Science and Technology (под ред. A. Barel, M. Paye и H. Maibach, опубликовано в 2001 г., Marcel Dekker, Inc, г. Нью-Йорк, штат Нью-Йорк), и включают, без ограничений, вазелин, гексилдецилстеарат и растительные и ореховые масла, а также масла растительного происхождения, такие как масло орехов макадамии, масло рисовых отрубей, масло косточек винограда, пальмовое масло, масло примулы, гидрогенизированное арахисовое масло и масло авокадо.
Под увлажнителем понимают соединение, предназначенное для повышения содержания воды в верхних слоях кожи (например, гигроскопические соединения). Примеры приемлемых увлажнителей включают увлажнители, представленные в главе 35, стр. 399-415 (G. Zocchi, Skin Feel Agents) в издании Handbook of Cosmetic Science and Technology (под ред. A. Barel, M. Paye и H. Maibach, опубликовано в 2001 г., Marcel Dekker, Inc, г. Нью-Йорк, штат Нью-Йорк), и включают, без ограничений, глицерин, сорбит или трегалозу (например, α,α-трегалозу, β,β-трегалозу, α,β-трегалозу) или их соль или сложный эфир (например, трегалозу-6-фосфат).
Под поверхностно-активным веществом понимают поверхностно-активный агент, предназначенный для очищения или эмульгирования. Примеры приемлемых поверхностно-активных веществ включают поверхностно-активные вещества, представленные в главе 37, стр. 431-450 (Oldenhove de Guertechin, Classification of surfactants) в издании Handbook of Cosmetic Science and Technology (под ред. A. Barel, M. Paye и H. Maibach, опубликовано в 2001 г., Marcel Dekker, Inc, г. Нью-Йорк, штат Нью-Йорк), и включают, без ограничений, анионные поверхностно-активные вещества, такие как сульфаты, катионные поверхностно-активные вещества, такие как бетаины, амфотерные поверхностно-активные вещества, такие как кокоглицинат натрия, неионные поверхностно-активные вещества, такие как алкилполиглюкозиды.
Примеры приемлемых хелатирующих агентов включают агенты, которые способны защищать и сохранять композиции этого изобретения. В одном или более вариантах осуществления хелатирующий агент представляет собой этилендиаминтетрауксусную кислоту (EDTA) и более конкретно, тетранатриевую соль EDTA, доступную в продаже в компании Dow Chemical Company, г. Мидленд, штат Мичиган, США, под торговым названием Versene 100XL.
Приемлемые консерванты включают, например, парабены, четвертичные аммониевые соединения, феноксиэтанол, бензоаты, DMDM гидантоин, органические кислоты, и они присутствуют в композиции в количестве от около 0 до около 1 процента или от около 0,05 процента до около 0,5 процента в расчете на общую массу композиции.
Для применения в целях настоящего изобретения можно использовать любой из ряда кондиционеров, которые приводят к появлению дополнительных характеристик, таких как блеск волос. Примеры включают, без ограничений, летучий силиконовый кондиционирующий агент с температурой кипения при атмосферном давлении менее около 220°С. Примеры приемлемых летучих силиконов включают, без ограничений, полидиметилсилоксан, полидиметилциклосилоксан, гексаметилдисилоксан, циклометиконовые текучие среды, такие как полидиметилциклосилоксан производства компании Dow Corning Corporation, г. Мидленд, штат Мичиган, США, доступный в продаже под торговым названием DC-345, и их смеси, а они конкретно включают циклометиконовые текучие среды. Другие приемлемые кондиционеры включают катионные полимеры, включая поликватерниумы, катионную гуаровую смолу и т.п.
Для применения в композиции приемлем любой из ряда доступных в продаже перлесцентных агентов или замутнителей. Примеры приемлемых перлесцентных агентов или замутнителей включают, без ограничений, сложные моно- или диэфиры (а) жирных кислот, имеющих от около 16 до около 22 атомов углерода, и (b) этилен- или пропиленгликоля; сложные моно- или диэфиры (а) жирных кислот, имеющих от около 16 до около 22 атомов углерода, и (b) полиалкиленгликоля формулы: НО-(JO)а-Н, где J - алкиленовая группа, имеющая от около 2 до около 3 атомов углерода; и а равно 2 или 3; жирные спирты, содержащие от около 16 до около 22 атомов углерода; сложные эфиры жирных кислот формулы: KCOOCH2L, где K и L независимо содержат от около 15 до около 21 атома углерода; неорганические твердые вещества, не растворимые в композиции шампуня, и смеси перечисленных веществ.
Любые ароматизирующие композиции, приемлемые для нанесения на кожу, можно применять в композиции в соответствии с настоящим изобретением.
Способы и форма продукта
Настоящее изобретение дополнительно включает способ уменьшения воспаления путем введения нуждающемуся в этом пациенту терапевтически эффективной дозы композиции, содержащей экстракт семян тмина обыкновенного (Carum carvi) и экстракт розмарина лекарственного (Rosmarinus officinalis). В некоторых вариантах осуществления воспаление представляет собой опосредованное рецептором CCR2 воспаление.
Композицию можно наносить местно. Такое местное нанесение можно выполнять на кожу, нуждающуюся в лечении, в любой части тела, например на кожу лица, губ, шеи, грудной клетки, спины, ягодиц, рук, подмышек и/или ног. Композицию также можно наносить на слизистую оболочку (например, в ротовую полость). В некоторых вариантах осуществления экстракты представляют собой полярные экстракты из экстрактов семян тмина обыкновенного (Carum carvi) и экстракта розмарина лекарственного (Rosmarinus officinalis).
В некоторых вариантах осуществления настоящее изобретение представлено в форме субстрата, содержащего композицию настоящего изобретения. Можно использовать любой приемлемый субстрат. Примеры приемлемых субстратов и материалов субстратов раскрыты, например, в патентах США № US 7452547 и US 2009/0241242, содержание которых полностью включено в настоящий документ путем ссылки. В некоторых вариантах осуществления композиция представлена в форме таблетки, пилюли или капсулы. В одном или более вариантах осуществления композиция представлена в форме раствора, суспензии, эмульсии, лосьона, крема, сыворотки, геля, карандаша, спрея, мази, жидкого средства для мытья, бруска мыла, шампуня, кондиционера для волос, пасты, пены, порошка, мусса, крема для бритья, гидрогеля или пленкообразующего продукта.
Можно применять любой приемлемый способ нанесения композиции на кожу, требующую ухода. Например, композицию можно наносить непосредственно из упаковки на кожу, требующую ухода, наносить рукой на кожу, требующую ухода, либо можно переносить на кожу с субстрата, такого как салфетка или маска, либо использовать комбинацию двух или более вариантов из перечисленного. В других вариантах осуществления композицию можно наносить посредством пипетки, тубы, ролика, аэрозоля и пластыря или можно добавлять в ванну или иным образом в воду для нанесения на кожу и т.п. Композицию можно наносить различными способами и в различных формах, включая, без ограничений, несмываемый крем, маску и/или сыворотку.
Хотя предшествующее описание представляет собой примеры вариантов осуществления настоящего изобретения, следует понимать, что в него могут быть внесены различные дополнения, модификации и замены, не выходящие за пределы сущности и объема настоящего изобретения. В частности, специалистам в данной области будет понятно, что настоящее изобретение может быть осуществлено в иных конкретных формах, структурах, конструкциях, пропорциях, а также с другими элементами, из других материалов и компонентов, не затрагивая дух и существенные характеристики настоящего изобретения. Специалисту в данной области будет понятно, что изобретение можно использовать с многочисленными модификациями структуры, конструкции, пропорций, материалов, компонентов и т.д. для создания примеров реализации настоящего изобретения, специально адаптированных для использования в конкретных условиях эксплуатации и в соответствии с эксплуатационными требованиями без отхода от принципов настоящего изобретения.
Таким образом, описанные в настоящем документе варианты осуществления следует рассматривать во всех отношениях как иллюстративные, а не ограничивающие объем настоящего изобретения, который обозначен прилагаемой формулой изобретения и не ограничен предшествующим описанием. Следует понимать, что в формуле изобретения термин «содержит/содержащий» не исключает наличия других элементов или этапов.
Кроме того, ссылки в единственном числе не исключают множественное число.
Термины, определяющие единственное число, «первый», «второй» и т.д., не исключают множественного числа.
Если не указано иное, все процентные доли, части и соотношения основаны на общей массе композиции настоящего изобретения. Если не указано иное, все подобные весовые доли, относящиеся к перечисленным компонентам, основаны на дозировке конкретного упомянутого компонента и, следовательно, не учитывают содержание носителей или побочных продуктов, которые могут быть включены в состав коммерчески доступных материалов.
ПРИМЕРЫ
В примерах использовали следующие способы испытания и материалы.
Анализ 1. Анализ антагонизма к рецептору С-С Chemokine Receptor Туре 2 (CCR2)
Клетки ТНР1 (American Type Culture Collection, г. Манассас, штат Виргиния, США, кат. № ТНР-1 (АТСС® TIB-202™) сеяли в 384-луночный полистироловый плоскодонный микропланшет, покрытый поли-d-лизином с крышкой и черным прозрачным дном, продаваемый под торговым наименованием CELLCOAT™ (Greiner Bio-One, г. Монро, штат Северная Каролина, США, кат. №781946), с плотностью 15 тыс.клеток/лунка в 40 мкл буфера для анализа (HBSS/20 мМ HEPES/0,001% Tween® 20) с использованием комбинированного диспенсера для реагентов, продаваемого под торговым наименованием Multidrop™ (ThermoFisher Scientific, г. Уолтем, штат Массачусетс, США), смешивая клетки с плотностью 7,5Е5 клеток/мл в буфере 1:1, с буфером, содержащим реагенты для окрашивания на кальций из набора для анализа на кальций, продаваемого под торговым наименованием Screen Quest™ Fluo-8 No Wash Calcium Assay Kit (AAT Bioquest, г. Саннидейл, штат Калифорния, США, кат. №36316).
Планшеты центрифугировали при 800 об/мин в течение 2 мин без торможения. Затем клетки инкубировали при 37°С в инкубаторе в течение 45 мин, а затем помещали в комнатную температуру на 15 мин. Антагонизм к CCR2 оценивали с использованием системы FLIPR Penta High Throughput Cellular Screening System (Molecular Devices, г. Сан-Хосе, штат Калифорния, США) путем измерения потока кальция, вызванного активацией рецептора CCR2 его лигандом МСР1 (Peprotech, Inc., г. Роки Хилл, штат Нью-Джерси, США, кат. №300-04) при дозе ЕС80 200 нМ. Используя протокол 2 добавлений с настройками возб./испуск. 490/525, считывали фоновые значения (5x1 с), затем к клеткам добавляли по 10 мкл содержащих буфер экстрактов и измеряли поток кальция (60x1 с, затем 40x3 с). Затем добавляли 10 мкл агониста (МСР1 с конечной концентрацией 200 нМ) и измеряли поток кальция (сканирования 60x1 с, а затем 40x3 с).
В анализе первую фазу, в которой добавляли экстракты, считали фазой агонизма и в ней определяли, имеют ли экстракты какой-либо агонистический эффект на поток кальция. Поток, наблюдаемый в контрольных лунках, обработанных безводным DMSO (Sigma-Aldrich, г. Сент-Луис, штат Миссури, США), считали 0% агонизмом, а поток, наблюдаемый в контрольных лунках, обработанных агонистом МСР1, считали 100% агонизмом. Во второй фазе, в которой к каждой лунке планшета добавляется доза ЕС80 МСР1, определяли антагонизм экстрактов. Поток, наблюдаемый в лунках, обработанных DMSO (из первой фазы), считали 0% антагонизмом, а поток, наблюдаемый в лунках, обработанных контрольным антагонистом (из первой фазы), считали 100% антагонизмом. Поток как в фазе агонизма, так и в фазе антагонизма представляет собой разность между наибольшим уровнем кальция, наблюдаемым в этой фазе, и исходным уровнем.
Для анализа синергии использовали 2 планшета с двумя наборами экспериментов по синергии на каждом из этих планшетов, и каждое условие в эксперименте имело три повторности.
Анализ 2. Анализ высвобождения цитокинов
Нормальные эпидермальные кератиноциты человека, Р2, партия ЕР-ВА, получали (Sterlab, г. Валлорис, Франция) и высевали в 96-луночный планшет в восстановленной среде для выращивания кератиноцитов, продаваемой под торговой маркой (KGM™ Gold Keratinocyte Growth medium Bulletkit™, Lonza, г. Вервье, Бельгия) с концентрацией 30 000 клетках/лунке. На следующий день среду заменяли средой для выращивания кератиноцитов, содержащей растительные экстракты и термоинактивированные бактерии P. acnes (109 КОЕ, штамм ID АТСС® 6919), поставляемые компанией LGC Standards, г. Мольсем, Франция. На следующий день собирали кондиционированную среду для измерения высвобождения IL6, IL8 и TNFa с использованием системы суспензионной матрицы Bio-Plex, продаваемой под торговой маркой BIOPLEX 200, Bio-Rad Laboratories, Inc., г. Марн-ла-Кокетт, Франция, с соответствующими наборами стандартных эталонных материалов, а жизнеспособность клеток оценивали с помощью теста МТТ. Каждое условие имело 4 повторности.
Тестируемые экстракты включали экстракт листьев розмарина с конечной концентрацией 0,5, 5 и 25 мкг/мл, экстракт семян тмина с конечной концентрацией 50 мкг/мл и комбинации этих двух экстрактов. В анализах на высвобождение цитокинов влияние P. acnes нормализовали к 100%. Относительное ингибирование при комбинированных обработках рассчитывали по следующей формуле:
1 - {(наблюдаемое значение - обработка DMSO)/(P. Acnes - обработка DMSO)}.
Экстракт листьев розмарина
Экстракт листьев розмарина лекарственного (Rosmarinus officinalis) был получен от компании Ungerer & Company, штат Нью-Джерси, США. Экстракт листьев розмарина готовили с использованием органической/водной среды, состоящей из смеси воды и спирта. Типичное приготовление заключалось в смешивании биомассы со смесью воды/денатурированного этилового спирта (2:8, соответственно) при комнатной температуре в течение 24 ч, фильтровании и высушивании фильтрата при пониженном давлении с получением нужного материала - экстракта. Экстракт суспендировали в безводном DMSO (Sigma-Aldrich) с концентрацией маточного раствора 100 мг/мл. Впоследствии готовили последовательные разведения маточного раствора для проведения тестирования эффективности в соответствии с описанными выше протоколами анализа.
Экстракт семян тмина
Экстракт семян тмина обыкновенного (Carum carvi) был получен от компании Ungerer & Compan, штат Нью-Джерси, США. Экстракт семян тмина готовили с использованием органической/водной среды, состоящей из смеси воды и спирта. Типичное приготовление заключалось в смешивании биомассы со смесью воды/этилового спирта (2:8, соответственно) при комнатной температуре в течение 24 ч, фильтровании и высушивании фильтрата при пониженном давлении с получением нужного материала - экстракта. Экстракт суспендировали в безводном DMSO (Sigma-Aldrich) с концентрацией маточного раствора 100 мг/мл. Впоследствии готовили последовательные разведения маточного раствора для проведения тестирования эффективности в соответствии с описанными выше протоколами анализа.
ПРИМЕР 1. Ингибирование рецепторов CCR2
Экстракт листьев розмарина и экстракт семян тмина тестировали по отдельности и в комбинации в различных концентрациях и оценивали ингибирование рецептора CCR2 в соответствии с описанным выше анализом 1. Рецептор CCR2 представляет собой хемокиновый рецептор, который связан с широким спектром воспалительных заболеваний/состояний. Таким образом, ингибирование этого рецептора связано с уменьшением воспаления. Результаты эксперимента показаны в таблице 1 ниже.
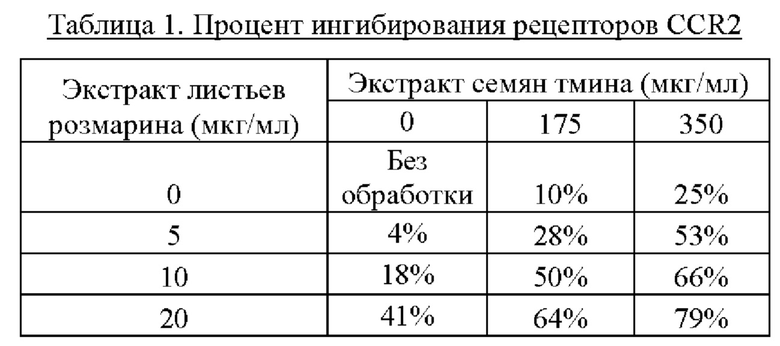
Как видно из приведенной выше таблицы, все протестированные комбинации экстракта листьев розмарина лекарственного (Rosmarinus officinalis) и экстракта семян тмина обыкновенного (Carum carvi) демонстрируют синергический эффект в отношении ингибирования рецептора CCR2 (>1-кратное увеличение от аддитивных уровней).
Синергия особенно выражена в случае комбинаций 5 и 10 мкг/мл экстракта листьев розмарина лекарственного (Rosmarinus officinalis) с 175 мкг/мл или 350 мкг/мл экстракта семян тмина обыкновенного (Carum carvi) (>1,5-кратное увеличение от аддитивных уровней). Синергический эффект был наиболее выраженным в случае комбинации 5 мкг/мл экстракта листьев розмарина лекарственного (Rosmarinus officinalis) с 175 мкг/мл экстракта семян тмина обыкновенного (Carum carvi) (2-кратное увеличение от аддитивных уровней).
Эти результаты неожиданны, с одной стороны, тем, что для достижения синергического эффекта требуется относительно небольшое количество экстракта.
Например, при использовании 175 мкг/мл экстракта семян тмина обыкновенного (Carum carvi) отдельно (без экстракта листьев розмарина лекарственного (Rosmarinus officinalis)) ингибирование рецепторов CCR2 составляло 10%. Даже удвоение количества экстракта семян тмина обыкновенного (Carum carvi) до 350 мкг/мл приводило только к 25%-му ингибированию. Однако при добавлении всего 5 мкг/мл экстракта листьев розмарина лекарственного (Rosmarinus officinalis), процент ингибирования скачком увеличивался до 28%, притом что концентрация экстракта семян тмина обыкновенного (Carum carvi) оставалась на уровне 175 мкг/мл. Результаты являются особенно неожиданными, учитывая, что отдельно экстракт листьев розмарина лекарственного (Rosmarinus officinalis) в концентрации 5 мкг/мл (без экстракта семян тмина обыкновенного (Carum carvi)) давал ингибирование рецепторов всего в 4%. Это означает, что даже в концентрациях, в которых экстракт листьев розмарина лекарственного (Rosmarinus officinalis) сам по себе обладает очень низкой активностью, его присутствие значительно повышает ингибирование экстрактов семян тмина обыкновенного (Carum carvi).
Судя по продемонстрированному ингибированию рецепторов CCR2, неожиданно было обнаружено, что комбинация экстракта листьев розмарина лекарственного (Rosmarinus officinalis) и экстракта семян тмина обыкновенного (Carum carvi) превосходит (а в некоторых случаях значительно превосходит) любой из экстрактов по отдельности.
Соответственно, синергическая комбинация экстракта листьев розмарина лекарственного (Rosmarinus officinalis) и экстракта семян тмина обыкновенного (Carum carvi) может быть эффективна для лечения, уменьшения и/или облегчения симптомов воспаления, в частности, когда воспаление представляет собой опосредованное CCR2 воспаление.
ПРИМЕР 2. Влияние на высвобождение цитокина IL-6
Экстракт листьев розмарина лекарственного (Rosmarinus officinalis) и экстракт семян тмина обыкновенного (Carum carvi) тестировали отдельно и в комбинации в различных концентрациях и оценивали снижение высвобождения цитокина IL-6 в соответствии с анализом 2, описанным выше. IL-6 представляет собой интерлейкин, действующий как провоспалительный цитокин. Таким образом, снижение высвобождения IL-6 связано с уменьшением воспаления. Результаты эксперимента показаны в таблице 2 ниже.
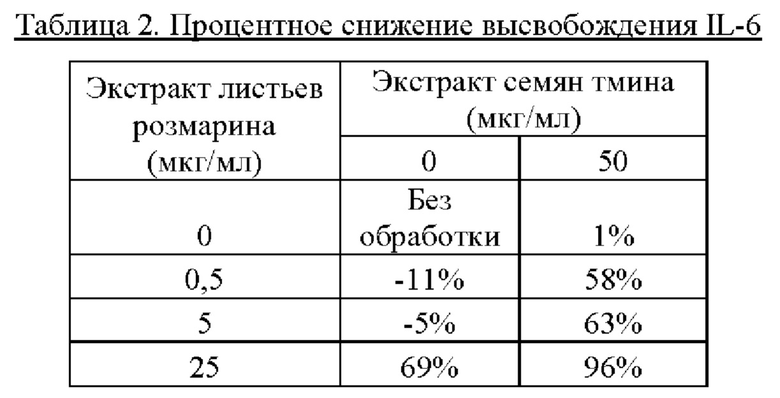
Как видно из приведенной выше таблицы, все протестированные комбинации экстракта листьев розмарина лекарственного (Rosmarinus officinalis) и экстракта семян тмина обыкновенного (Carum carvi) демонстрируют синергический эффект в отношении уменьшения высвобождения IL-6 (>1-кратное увеличение от аддитивных уровней).
Синергический эффект особенно выражен в случае комбинаций 0,5 и 5 мкг/мл экстракта листьев розмарина лекарственного (Rosmarinus officinalis) с 50 мкг/мл экстракта семян тмина обыкновенного (Carum carvi).
Эти результаты неожиданны, с одной стороны, тем, что большинство протестированных концентраций экстракта семян тмина обыкновенного (Carum carvi) и экстракта листьев розмарина лекарственного (Rosmarinus officinalis), при тестировании по отдельности, практически не оказывали влияния или даже оказывали отрицательное влияние на снижение высвобождения IL-6. Тем не менее те же концентрации приводили к резкому снижению высвобождения на 50%, если два экстракта объединяли. Например, при использовании 50 мкг/мл экстракта семян тмина обыкновенного (Carum carvi) (без экстракта листьев розмарина лекарственного (Rosmarinus officinalis)) ингибирование высвобождения IL-6 составляло 1%. Более того, при концентрации экстракта листьев розмарина лекарственного (Rosmarinus officinalis) 0,5 и 0,5 мкг/мл (без экстракта семян тмина обыкновенного (Carum carvi)), результаты фактически показали отрицательное процентное снижение. Аддитивный эффект, ожидаемый от комбинации этих концентраций, должен был бы оставаться отрицательным. Тем не менее процентное снижение увеличивалось до 58% (0,5 мкг/мл экстракта листьев розмарина лекарственного (Rosmarinus officinalis) и 50 мкг/мл экстракта семян тмина обыкновенного (Carum carvi)) и до 63% (5 мкг/мл экстракта листьев розмарина лекарственного (Rosmarinus officinalis) и 50 мкг/мл экстракта семян тмина обыкновенного (Carum carvi)). Это означает, что даже в концентрациях, в которых экстракт листьев розмарина лекарственного (Rosmarinus officinalis) и экстракт семян тмина обыкновенного (Carum carvi) по отдельности проявляют очень слабую (или вовсе не проявляют) активность, присутствие обоих экстрактов приводит к желаемому свойству снижения высвобождения IL-6. Даже при концентрации 25 мкг/мл экстракта листьев розмарина лекарственного (Rosmarinus officinalis), которая демонстрировала снижение высвобождения IL-6 на 69%, значение увеличивалось почти до 100% при объединении с 50 мкг/мл экстракта семян тмина обыкновенного (Carum carvi).
Судя по продемонстрированному снижению высвобождения IL-6, неожиданно было обнаружено, что комбинация экстракта листьев розмарина лекарственного (Rosmarinus officinalis) и экстракта семян тмина обыкновенного (Carum carvi) превосходит (а в некоторых случаях значительно превосходит) любой из экстрактов по отдельности.
Соответственно, синергическая комбинация экстракта листьев розмарина лекарственного (Rosmarinus officinalis) и экстракта семян тмина обыкновенного (Carum carvi) может быть эффективна для лечения, уменьшения и/или облегчения симптомов воспаления, в частности, когда воспаление связано с высвобождением IL-6.
ПРИМЕР 3. Влияние на высвобождение цитокина IL-8
Экстракт листьев розмарина лекарственного (Rosmarinus officinalis) и экстракт семян тмина обыкновенного (Carum carvi) тестировали отдельно и в комбинации в различных концентрациях и оценивали снижение высвобождения цитокина IL-8 в соответствии с анализом 2, описанным выше. IL-8 представляет собой цитокин-хемоаттрактант, связанный с воспалением. Таким образом, снижение высвобождения IL-8 связано с уменьшением воспаления. Результаты эксперимента показаны в таблице 3 ниже.
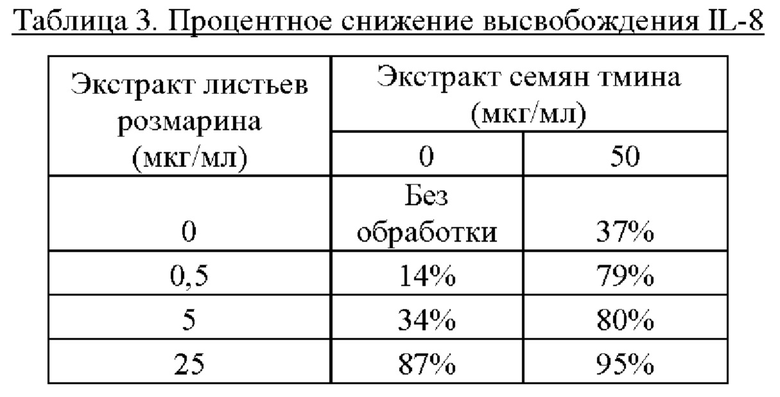
Как видно из приведенной выше таблицы, все протестированные комбинации экстракта листьев розмарина лекарственного (Rosmarinus officinalis) и экстракта семян тмина обыкновенного (Carum carvi) демонстрируют синергический эффект в отношении уменьшения высвобождения IL-8 (>1-кратное увеличение от аддитивных уровней).
Синергетический эффект был особенно выражен в случае комбинации 0,5 мкг/мл экстракта листьев розмарина лекарственного (Rosmarinus officinalis) с 50 мкг/мл экстракта семян тмина обыкновенного (Carum carvi) (>1,5-кратное увеличение от аддитивных уровней).
Эти результаты неожиданны, с одной стороны, тем, что для достижения синергического эффекта требуется относительно небольшое количество экстракта.
Например, при использовании 50 мкг/мл экстракта семян тмина обыкновенного (Carum carvi) (без экстракта листьев розмарина лекарственного (Rosmarinus officinalis)), процентное значение снижения составляло 37%. При объединении всего с 0,5 мкг/мл экстракта листьев розмарина лекарственного (Rosmarinus officinalis), величина резко увеличивалась до 79%, несмотря на то что та же концентрация экстракта листьев розмарина лекарственного (Rosmarinus officinalis) при отдельном использовании демонстрировала лишь умеренное процентное снижение на 14%. Это означает, что даже в концентрациях, в которых экстракт листьев розмарина лекарственного (Rosmarinus officinalis) сам по себе обладает умеренной активностью, его присутствие значительно повышает ингибирование экстрактом семян тмина обыкновенного (Carum carvi).
Судя по продемонстрированному снижению высвобождения IL-8, неожиданно было обнаружено, что комбинация экстракта листьев розмарина лекарственного (Rosmarinus officinalis) и экстракта семян тмина обыкновенного (Carum carvi) превосходит (а в некоторых случаях значительно превосходит) любой из экстрактов по отдельности.
Соответственно, синергическая комбинация экстракта листьев розмарина лекарственного (Rosmarinus officinalis) и экстракта семян тмина обыкновенного (Carum carvi) может быть эффективна для лечения, уменьшения и/или облегчения симптомов воспаления, в частности, когда воспаление связано с высвобождением IL-8.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ЭКСТРАКТЫ ТМИНА ОБЫКНОВЕННОГО (CARUM CARVI) И РОЗМАРИНА ЛЕКАРСТВЕННОГО (ROSMARINUS OFFICINALIS), И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2021 |
|
RU2837617C1 |
| РАСТИТЕЛЬНЫЕ И БАКТЕРИАЛЬНЫЕ ЭКСТРАКТЫ, ДЕМОНСТРИРУЮЩИЕ РЕТИНОЛОПОДОБНУЮ АКТИВНОСТЬ | 2019 |
|
RU2833927C2 |
| КОМПОЗИЦИЯ ДЛЯ ПОЛУЧЕНИЯ ЧАЙНОГО НАПИТКА ИЛИ ТРАВЯНОГО И РАСТИТЕЛЬНОГО ОТВАРОВ | 2014 |
|
RU2690651C2 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ЭКСТРАКТЫ AMPELOPSIS GROSSEDENTATA И ЭКСТРАКТЫ ALBIZIA JULIBRISSIN, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2731561C2 |
| КОМПОЗИЦИИ ДЛЯ МЕСТНОГО НАНЕСЕНИЯ, СОДЕРЖАЩИЕ ЭКСТРАКТЫ ACMELLA OLERACEA, И ВАРИАНТЫ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2703299C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ ГЛАЗ | 2020 |
|
RU2802625C2 |
| . | 2011 |
|
RU2571691C2 |
| КОМПОЗИЦИЯ ДЛЯ СТИМУЛИРОВАНИЯ РОСТА КОСТЕЙ И ПОДДЕРЖАНИЯ ЗДОРОВЬЯ КОСТЕЙ | 2002 |
|
RU2314717C2 |
| СПОСОБ ИНДУКЦИИ ИММУННОГО ОТВЕТА ОРГАНИЗМА | 2001 |
|
RU2229890C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ ГЛАЗ | 2019 |
|
RU2802365C2 |
Изобретение относится к фармацевтической и/или косметической промышленности, а именно к композиции для местного уменьшения воспаления. Композиция для местного уменьшения воспаления содержит: водно-спиртовой экстракт семян тмина обыкновенного (Carum carvi), причем экстракт семян тмина обыкновенного (Carum carvi) присутствует в концентрации от 50 до 350 мкг/мл; водно-спиртовой экстракт листьев розмарина лекарственного (Rosmarinus officinalis), причем экстракт листьев розмарина лекарственного (Rosmarinus officinalis) присутствует в концентрации от 0,5 до 25 мкг/мл; и фармацевтически и/или косметически приемлемый носитель. Вышеописанная композиция обладает синергетическим противовоспалительным эффектом при местном воспалении. 14 з.п. ф-лы, 3 табл., 3 пр.
1. Композиция для местного уменьшения воспаления, содержащая:
водно-спиртовой экстракт семян тмина обыкновенного (Carum carvi), причем экстракт семян тмина обыкновенного (Carum carvi) присутствует в концентрации от 50 до 350 мкг/мл;
водно-спиртовой экстракт листьев розмарина лекарственного (Rosmarinus officinalis), причем экстракт листьев розмарина лекарственного (Rosmarinus officinalis) присутствует в концентрации от 0,5 до 25 мкг/мл; и
фармацевтически и/или косметически приемлемый носитель.
2. Композиция по п. 1, дополнительно содержащая материал, выбранный из группы, состоящей из поверхностно-активных веществ, хелатирующих агентов, мягчителей, увлажнителей, кондиционеров, консервантов, замутнителей, ароматизаторов и комбинаций двух или более из них.
3. Композиция по п. 1 или 2, в которой экстракт семян тмина обыкновенного (Carum carvi) и экстракт розмарина лекарственного (Rosmarinus officinalis), каждый независимо, содержит полярный экстракт.
4. Композиция по любому из пп. 1-3, в которой полярный экстракт экстрагировали одним или более растворителями, выбранными из группы, состоящей из C1-C8 спиртов, C1-C8 полиолов, С1-С8 гликолей и их комбинаций.
5. Композиция по любому из пп. 1-4, причем один или более растворителей выбраны из группы, состоящей из этанола, воды и их комбинаций.
6. Композиция по любому из пп. 1-5, в которой экстракт семян тмина обыкновенного (Carum carvi) и экстракт розмарина лекарственного (Rosmarinus officinalis), каждый независимо, содержит менее 0,1 весового процентного содержания, или менее 0,01 весового процентного содержания эфирных масел, или не содержит эфирных масел.
7. Композиция по любому из пп. 1-6, которая представлена в форме раствора, суспензии, эмульсии, лосьона, крема, сыворотки, геля, карандаша, спрея, мази, жидкого средства для мытья, бруска мыла, шампуня, кондиционера для волос, пасты, пены, порошка, мусса, крема для бритья, гидрогеля или пленкообразующего продукта.
8. Композиция по любому из пп. 1-7, в которой экстракт семян тмина обыкновенного (Carum carvi) и экстракт розмарина лекарственного (Rosmarinus officinalis) присутствуют в объединенной концентрации от 0,1 до 20 мас. % общей массы композиции.
9. Композиция по любому из пп. 1-8, в которой экстракт розмарина лекарственного (Rosmarinus officinalis) и экстракт семян тмина обыкновенного (Carum carvi) присутствуют в массовом соотношении от 1:2 до 1:100.
10. Композиция по любому из пп. 1-9, в которой экстракт семян тмина обыкновенного (Carum carvi) присутствует в концентрации 50 мкг/мл, а экстракт листьев розмарина лекарственного (Rosmarinus officinalis) присутствует в концентрации от 0,5 до 5 мкг/мл.
11. Композиция по п. 1, в которой экстракт семян тмина обыкновенного (Carum carvi) и экстракт листьев розмарина лекарственного (Rosmarinus officinalis), каждый независимо, представляет собой водно-спиртовой экстракт, и
при этом композиция представлена в форме раствора, суспензии, эмульсии, лосьона, крема, сыворотки, геля, карандаша, спрея, мази, жидкого средства для мытья, бруска мыла, шампуня, кондиционера для волос, пасты, пены, порошка, мусса, крема для бритья, гидрогеля или пленкообразующего продукта.
12. Композиция по п. 11, в которой экстракт семян тмина обыкновенного (Carum carvi) присутствует в концентрации 50 мкг/мл, а экстракт листьев розмарина лекарственного (Rosmarinus officinalis) присутствует в концентрации от 0,5 до 5 мкг/мл.
13. Композиция по п. 11 или 12, в которой экстракт семян тмина обыкновенного (Carum carvi) и экстракт розмарина лекарственного (Rosmarinus officinalis) присутствуют в объединенной концентрации от 0,1 до 20 мас. % общей массы композиции.
14. Композиция по любому из пп. 11-13, в которой экстракт розмарина лекарственного (Rosmarinus officinalis) и экстракт семян тмина обыкновенного (Carum carvi) присутствуют в массовом соотношении от 1:2 до 1:100.
15. Композиция по любому из пп. 11-14, дополнительно содержащая материал, выбранный из группы, состоящей из поверхностно-активных веществ, хелатирующих агентов, мягчителей, увлажнителей, кондиционеров, консервантов, замутнителей, ароматизаторов и комбинаций двух или более из них.
| US 20180064775 A1, 08.03.2018 | |||
| Спортивный тренажер | 1989 |
|
SU1743620A1 |
| EP 2949362 А1, 02.12.2015 | |||
| КОМПОЗИЦИИ ДЛЯ УХОДА ЗА ПОЛОСТЬЮ РТА, СОДЕРЖАЩИЕ РАСТИТЕЛЬНЫЕ ЭКСТРАКТЫ | 2008 |
|
RU2440821C2 |
Авторы
Даты
2025-04-02—Публикация
2021-03-24—Подача