Изобретение относится к области неорганической химии, а именно к способу получения кристаллических двойных ортофосфатов церия(IV), которые могут быть использованы для различных оптических применений, в том числе в качестве компонентов солнцезащитных средств.
Класс ортофосфатов четырехвалентных металлов наиболее широко представлен двойными солями, имеющими богатый кристаллохимический состав из-за возможности объединения различных катионов в своих структурах. Можно выделить, в частности, двойные ортофосфаты общего состава BIIMIV(PO4)2 (BII=Cd, Ca, Sr, Pb, Ba; MIV=Ge, Ti, Mo, Sn, Hf, Zr, Pu, Np, U, Th) [Bregiroux D. et al. J. Solid State Chem. 2015, 230, 26-33], AIMIV2(PO4)3 (A=Li, Na, K, Rb, Cs, 1/2Mg, 1/2Са, 1/2Sr, 1/2Ba, M=Ti, Zr, Hf, Ge, Sn, актиниды Th, U) [Pet'kov V.I., Asabina E.A. Glass and Ceramics. 2004, 61(7-8), 233-239; Козлова Т.О. и др. Журн. неорган, химии. 2021, 66(12), 1647-1665], AI2Th(PO4)2 [Patkare G. et al. Eur. J. Inorg. Chem. 2023, 26(17), e202300140], кристаллизующиеся в различных структурных типах в зависимости от ионного радиуса катионов. Двойные ортофосфаты четырехвалентных металлов обычно имеют кристаллические структуры с туннелями, что позволяет рассматривать их в качестве ионообменных материалов, сорбентов и матриц для захоронения радиоактивных отходов [Neumeier S. et al. Radiochim. Acta. 2017, 105(11), 961-984].
В отличие от ортофосфатов других четырехвалентных металлов, таких как Ti, Zr, Hf, Th и U, информация о двойных солях церия(IV) крайне скудна, несмотря на близость кристаллохимических свойств этих элементов [Marsac R. et al. Dalton Trans. 2017, 46(39), 13553-13561; Usman M. et al. J Solid State Chem. 2019, 270, 19-26]. Так, класс двойных ортофосфатов церия(IV) на сегодняшний день насчитывает менее 10 достоверно охарактеризованных кристаллических структур, содержащих однозарядные катионы натрия - Na1.97Ce1.03(PO4)2⋅xH2O [Baranchikov А.Е. et al. ChemistrySelect. 2024, 9(17), e202401010], Na10Ce2(PO4)6 [Lai Y. et al. Inorg. Chem. 2013, 52(23), 13639-13643], калия - K2Ce(PO4)2 [Bevara S., et al. Inorg. Chem. 2017, 56(6), 3335-3348], KCe2(PO4)3 [Kozlova Т.О. et al. Nanosystems: Phys. Chem. Math. 2023, 14(1), 112-119] или аммония - (NH4)2Ce(PO4)2⋅H2O [Salvado M.A. et al. J. Am. Chem. Soc. 2007, 129(36), 10970-10971], NH4Ce2(PO4)3 [Shekunova Т.О. et al. Eur. J. Inorg. Chem. 2019, 2019(27), 3242-3248].
Помимо областей практического использования двойных ортофосфатов церия(IV), в целом присущих классу ортофосфатов четырехвалентных металлов, недавно на примере КСе2(PO4)3 и NH4Ce2(PO4)3 была продемонстрирована возможность применения данного класса соединений в качестве неорганических компонентов солнцезащитной косметики ввиду высокого поглощения в УФ-диапазоне [Kozlova Т.О. et al. Nanosystems:Phys. Chem. Math. 2024, 15(2), 215-223].
Основным методом синтеза двойных ортофосфатов церия(IV), содержащих однозарядные катионы металлов, является гидротермальная обработка церийфосфатных прекурсоров. Что касается способа получения двойных ортофосфатов церия(IV), содержащих в составе двухзарядные катионы металлов, то можно отметить публикации только одного авторского коллектива, посвященные соединениям общего состава В0.5Се2(РО4)3, B1.5Ce1.5(PO4)3 и ВСе(PO4)2 (В=Mg, Cа, Sr, Ba и Cd) [Orlova A.I. et al. Radiochemistry. 2002, 44(4), 326-331]. В качестве промежуточного продукта синтеза использовали аморфные гели, полученные в результате смешения раствора ортофосфорной кислоты с водными растворами соли церия (NH4)2Се(NO3)6 и хлоридами или нитратами щелочноземельных металлов. Данные гели высушивали и подвергали термической обработке до 1100°С. Однако достоверность описания продуктов синтеза вызвала некоторые сомнения у других исследователей, в т.ч. ввиду склонности ортофосфатов церия(IV) к превращению в ортофосфаты церия(III) в условиях высокотемпературной обработки. В частности, авторы статьи [Рора К. et al. J. Solid State Chem. 2007,180(8), 2346-2355] с целью получения фазы ВаСе(PO4)2 воспроизвели методику из работы [Orlova A.I. et al. Radiochemistry. 2002, 44(4), 326-331]. В отличие от предполагаемого однофазного соединения полученный продукт представлял собой смесь аморфной барийсодержащей фазы и монацита (СеРО4), сформированного в связи с восстановлением Се4+до Се3+. Таким образом, применимость предложенного высокотемпературного метода синтеза для получения двойных ортофосфатов церия(IV) и щелочноземельных металлов остается сомнительной.
Наиболее близкое техническое решение, обеспечивающее, на наш взгляд, возможность гидротермального синтеза двойных ортофосфатов церия(IV), содержащих также щелочноземельный металл, изложено в статье [Kozlova Т.О. et al. J. Mater. Chem. В. 2022, 10(11), 1775-1785] и принято за прототип. Для получения двойного ортофосфата церия(IV) состава NH4Ce2(PO4)3 готовили церий фосфатный раствор путем растворения 0.1 г нанокристаллического диоксида церия в 5 мл 85 масс. % ортофосфорной кислоты при 80°С. После остывания к полученному раствору добавляли 35 мл 1.5 М водного раствора аммиака в качестве осадителя. Реакционную смесь количественно переносили в тефлоновый автоклав объемом 100 мл и подвергали гидротермальной обработке при 180°С в течение 24 ч. Полученный осадок многократно промывали дистиллированной водой и высушивали при температуре 60°С. Значение солнцезащитного фактора для полученного соединения оказалось относительно высоким и составило 2.7.
Основным недостатком прототипа является его неприменимость для синтеза двойных ортофосфатов церия(IV) иного состава, обусловленная специфическими экспериментальными условиями и типом осадителя. Кроме того, безопасность применения аммоний содержащего соединения в составе косметического средства, предполагаемого к нанесению на кожу, требует тщательного изучения.
Изобретение направлено на расширение арсенала УФ-поглощающих неорганических компонентов на основе двойных ортофосфатов церия(IV) для дальнейшего применения в составе солнцезащитной косметики.
Техническим результатом изобретения является разработка способа получения двойного ортофосфата церия(IV), содержащего в качестве второго катиона кальций. Выбор последнего обусловлен тем, что фосфаты кальция обладают собственным УФ-протекторным действием и относятся к классу биомиметических материалов, широко используемых в медицинских целях благодаря их полной биосовместимости [Carella F. et al. Materials. 2021, 14(21), 6398].
Технический результат достигается тем, что предложен способ получения двойного ортофосфата церия(IV), включающий приготовление церийфосфатного раствора путем растворения 0.1 г нанокристаллического диоксида церия в 5 мл 85 масс. % ортофосфорной кислоты при 80°С, добавление к полученному остывшему церийфосфатному раствору 35 мл водного раствора осадителя, гидротермальную обработку реакционной смеси в тефлоновом автоклаве объемом 100 мл при 180°С в течение 24 ч, многократную промывку осадка дистиллированной водой и его сушку при 60°С, отличающийся тем, что в качестве водного раствора осадителя используют водный раствор нитрата кальция с концентрацией от 0.1 до 0.5 М.
Применение в качестве источника катионов кальция именно нитрата кальция обусловлено проведенными дополнительными исследованиями по анализу влияния различных анионов в составе реакционной среды на фазовый состав продуктов гидротермальной обработки церийфосфатных гелей.
Концентрация водного раствора нитрата кальция менее 0.1 М не приводит к формированию двойного ортофосфата церия(IV)-кальция, а использование концентрации более 0.5 М ведет к избыточному содержанию кальция в продукте и снижению его солнцезащитных свойств.
Сущность предлагаемого способа заключается в том, что в результате использования осадителя определенного состава и концентрации формируется оптимальный состав реакционной среды, обеспечивающий кристаллизацию однофазного продукта, представляющего собой двойной ортофосфат церия(IV)-кальция, в гидротермальных условиях.
Изобретение проиллюстрировано следующими фигурами.
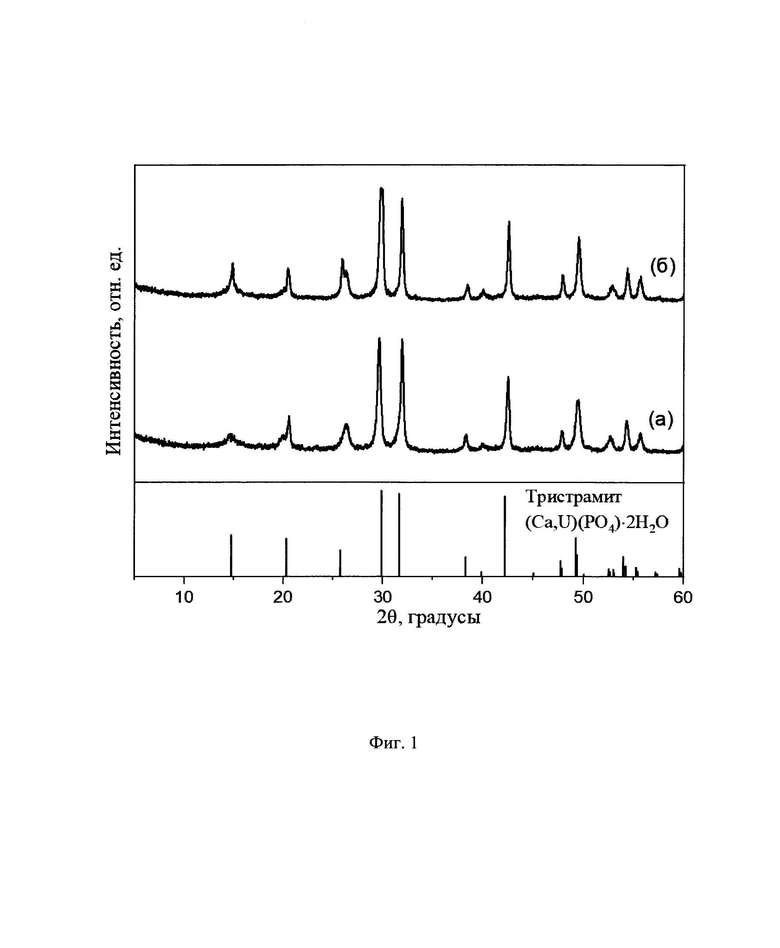
Фиг. 1. Дифрактограмма продукта, полученного по примеру 1 (а), по примеру 2 (б) добавлением 0.1 М или 0.5 М водного раствора Са(NO3)2, соответственно, к церийфосфатному раствору с последующей гидротермальной обработкой реакционной смеси. Внизу отражены положения брэгговских пиков для тристрамита (Са,U)(PO4)⋅2Н2О (PDF-2, №35-0613).
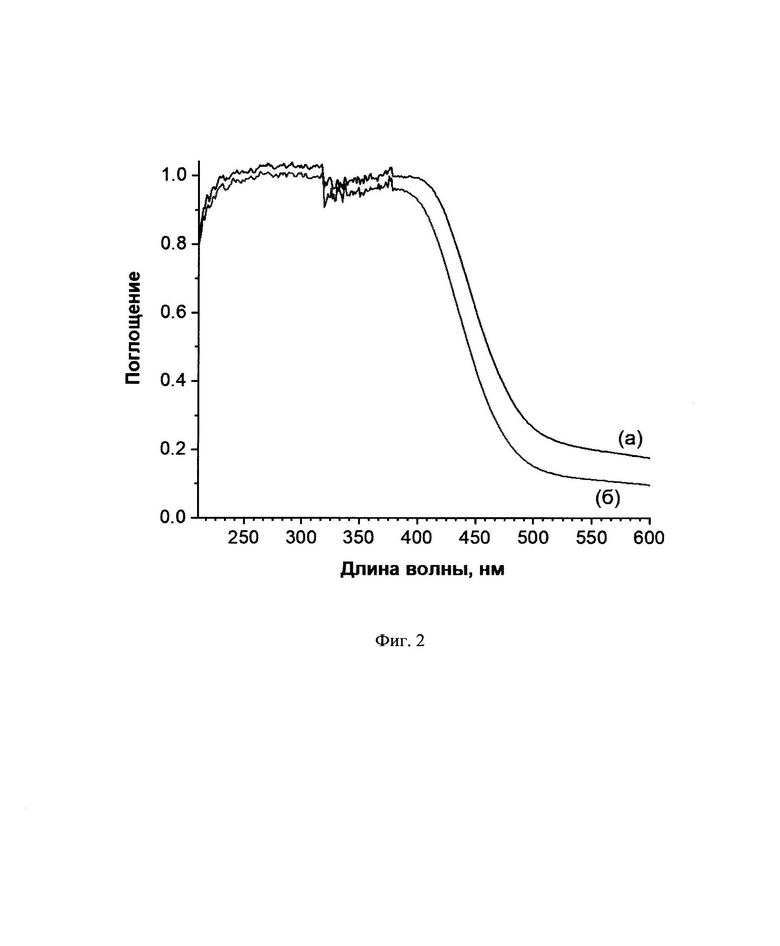
Фиг. 2. Спектр оптического поглощения продукта, полученного а) по примеру 1, б) по примеру 2 добавлением 0.1 М или 0.5 М водного раствора Са(NO3)2, соответственно, к церийфосфатному раствору с последующей гидротермальной обработкой реакционной смеси.
Фиг. 3. Результаты дифференциального окрашивания клеточной культуры мезенхимальных стволовых клеток человека с использованием флуоресцентных красителей без добавления (а), с добавлением продукта, полученного по примеру 1, в концентрации 0.1 мг/мл (б) или 1 мг/мл (в).
Ниже приведены примеры реализации заявляемого способа. Примеры иллюстрируют, но не ограничивают предложенный способ.
Пример 1
Для синтеза нанокристаллического диоксида церия использовали методику, опубликованную в работе [Baranchikov А.Е. et al. CrystEngComm. 2010, 12, 3531-3533]. Навеску 0.1 г синтезированного нанокристаллического СеО2 растворяли в 5 мл 85 масс. % ортофосфорной кислоты при 80°С. К полученному церийфосфатному раствору после остывания добавляли 35 мл 0.1 М водного раствора нитрата кальция. Реакционную смесь подвергали гидротермальной обработке при 180°С в течение 24 ч в тефлоновом автоклаве объемом 100 мл. Осадок многократно промывали дистиллированной водой, затем высушивали при 60°С. Результаты рентгенофазового анализа представлены на Фиг. 1 и указывают на однофазность продукта; положения основных рефлексов продукта близки положению брэгговских пиков для структуры минерала тристрамита (PDF № 35-0613, (Ca,U)(PO4)-2H2O). Согласно данным рентгеноспектрального микроанализа соотношение Се:Са составляет 1.1, Р:Са - 2.1, Р:Се - 2.0, что соответствует брутто-формуле СаСе(PO4)2. Результаты термогравиметрического анализа указывают на наличие структурной воды в продукте, а ее количество, рассчитанное через потерю массы между 120°С и 600°С, составляет около 1. Таким образом, формула полученного двойного ортофосфата церия(IV)-кальция может быть записана в виде СаСе(PO4)2⋅Н2О. Соединение такого состава является новым и ранее в литературе описано не было. На Фиг. 2а представлен спектр оптического поглощения СаСе(PO4)2⋅H2O. Можно видеть, что диапазон поглощения полученного продукта покрывает весь ультрафиолетовый диапазон. Значение солнцезащитного фактора для СаСе(PO4)2⋅Н2O определяли аналогично методике, представленной в прототипе, в соответствии с международным стандартом ГОСТ ИСО 24443-2016. Оно составило 1.6, что ниже значения, полученного для NH4Ce2(PO4)3 в прототипе, однако превышает показатель SPF=1 для CePO4, также рассматриваемого в качестве потенциального неорганического УФ-фильтра [Kozlova Т.О. et al. Molecules. 2024, 29, 2157].
Анализ токсичности у веществ, предлагаемых к использованию в составе косметических препаратов, является крайне важным параметром.
Оценку цитотоксичности и жизнеспособности мезенхимальных стволовых клеток человека в присутствии полученного продукта проводили методом Live/Dead assay. Посев проводили в 96-луночные планшеты в среде ДМЕМ/F12 (1:1) с добавлением 10% эмбриональной телячьей сыворотки (FBS) и 100 Ед/мл пенициллин/стрептомицина и 2 мМ L-глютамина. Плотность посева - 25 тыс/см2. Культивирование проводили при 37°С в атмосфере 5% СО2. Через 10 ч к клеткам добавляли полученный продукт в концентрации 0.1 или 1 мг/мл. В качестве контроля использовали лунки с клетками без добавления образца. Для анализа использовали дифференциальное окрашивание флуоресцентными красителями Hoechst33342 и Propidium Iodide через 24 ч после внесения образца. Интеркалирующий реагент Propidium Iodide в режиме исследования λ(возб)=546 нм, λ(эмисс)=575-640 нм окрашивает в красный цвет ядра погибших клеток. Флуоресцентный краситель Hoechst 33342 в режиме исследования λ(возб)=355 нм, λ(эмисс)=460 нм окрашивает в синий цвет ДНК живых и мертвых клеток. После окрашивания клеток осуществляли их фотосъемку на приборе Bio Rad Fluorescent Cell Imager с последующей количественной оценкой жизнеспособных (по синему фильтру) и нежизнеспособных клеток (по красному фильтру) в программе ImageJ. Анализ соотношения числа мертвых и живых клеток не выявил статистически достоверного увеличения мертвых клеток через 24 ч соинкубации с образцом для обеих исследованных концентраций, что продемонстрировано на Фиг. 3.
Пример 2
По примеру 1, отличающийся тем, что использовали водный раствор нитрата кальция с концентрацией 0.5 М. Согласно данным рентгеноспектрального микроанализа соотношение Се:Са составило 0.9, Р:Са - 1.9, Р:Се-2.1. Результаты рентгенофазового анализа представлены на Фиг. 1б, положения основных рефлексов и соотношение их интенсивностей совпадают с данными для продукта, полученного по примеру 1. На Фиг. 2б представлен спектр оптического поглощения образца, покрывающий весь ультрафиолетовый диапазон. Значение солнцезащитного фактора равнялось 1.5.
Таким образом, заявляемый способ позволяет получить новый двойной ортофосфат церия(IV), перспективный в качестве неорганического УФ-фильтра для применения в составе солнцезащитной косметики.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения композитных материалов на основе фосфата и оксида церия | 2022 |
|
RU2799468C1 |
| СПОСОБ ПОЛУЧЕНИЯ НЕОРГАНИЧЕСКОГО ИНДИКАТОРА ТЕМПЕРАТУРЫ | 2020 |
|
RU2750694C1 |
| КОМПОЗИЦИЯ ДЛЯ ТРАНСДЕРМАЛЬНОЙ ДОСТАВКИ НАНОЧАСТИЦ | 2021 |
|
RU2753699C1 |
| Способ получения золя диоксида церия в неводной среде | 2022 |
|
RU2798099C1 |
| Способ получения стабильных водных коллоидных растворов наночастиц диоксида церия | 2016 |
|
RU2615688C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОКРИСТАЛЛИЧЕСКОГО КРЕМНИЙЗАМЕЩЕННОГО ГИДРОКСИАПАТИТА | 2012 |
|
RU2500840C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИТНОГО ТЕРМОСТАБИЛЬНОГО КАТАЛИЗАТОРА КАРКАСНОГО СТРОЕНИЯ ДЛЯ ДЕГИТРАТАЦИИ МЕТАНОЛА В ДИМЕТИЛОВЫЙ ЭФИР (ВАРИАНТЫ) | 2019 |
|
RU2717686C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОКРИСТАЛЛИЧЕСКОГО МАГНИТНОГО ПОРОШКА ДОПИРОВАННОГО ОРТОФЕРРИТА ИТТРИЯ | 2013 |
|
RU2574558C2 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОЧАСТИЦ ОКСИДА ЦЕРИЯ | 2019 |
|
RU2698679C1 |
| СПОСОБ ИММОБИЛИЗАЦИИ ТОРИЯ(IV) ИЗ ВОДНЫХ РАСТВОРОВ СОРБЕНТОМ НА ОСНОВЕ ГИДРООРТОФОСФАТА ЦЕРИЯ(IV) | 2018 |
|
RU2676624C1 |

Изобретение относится к области неорганической химии, а именно к способу получения кристаллических двойных ортофосфатов церия(IV), которые могут быть использованы для различных оптических применений, в том числе в качестве компонентов солнцезащитных средств. Способ получения двойного ортофосфата церия(IV) включает приготовление церийфосфатного раствора путем растворения 0.1 г нанокристаллического диоксида церия в 5 мл 85 масс. % ортофосфорной кислоты при 80°С. К полученному остывшему церийфосфатному раствору добавляют 35 мл водного раствора осадителя. Далее проводят гидротермальную обработку реакционной смеси в тефлоновом автоклаве объемом 100 мл при 180°С в течение 24 ч, многократно промывают осадок дистиллированной водой и сушат при 60°С. В качестве водного раствора осадителя используют водный раствор нитрата кальция с концентрацией от 0.1 до 0.5 М. Обеспечивается получение двойного ортофосфата церия(IV), содержащего в качестве второго катиона кальций, пригодного для использования в составе солнцезащитной косметики в качестве УФ-поглощающего компонента. 3 ил., 2 пр.
Способ получения двойного ортофосфата церия(IV), включающий приготовление церийфосфатного раствора путем растворения 0.1 г нанокристаллического диоксида церия в 5 мл 85 масс. % ортофосфорной кислоты при 80°С, добавление к полученному остывшему церийфосфатному раствору 35 мл водного раствора осадителя, гидротермальную обработку реакционной смеси в тефлоновом автоклаве объемом 100 мл при 180°С в течение 24 ч, многократную промывку осадка дистиллированной водой и его сушку при 60°С, отличающийся тем, что в качестве водного раствора осадителя используют водный раствор нитрата кальция с концентрацией от 0.1 до 0.5 М.
| Kozlova T.O., Popov A.L., Kolesnik I.V., Kolmanovich D.D., Baranchikov A.E., Shcherbakov A.B., Ivanov V.K | |||
| Amorphous and crystalline cerium phosphates: biocompatible ROS-scavenging sunscreens, Journal of Materials Chemistry B, 2022, 10(11), p | |||
| Приемник и передатчик звука | 1924 |
|
SU1775A1 |
| Способ получения люминесцентного ортофосфата кальция, активированного церием | 2021 |
|
RU2779453C1 |
| RU 2018121797 A, 16.12.2019 | |||
| Способ получения композитных материалов на основе фосфата и оксида церия | 2022 |
|
RU2799468C1 |
| WO | |||
Авторы
Даты
2025-04-23—Публикация
2024-07-09—Подача