Настоящее изобретение относится к химии, биологии, медицине, ветеринарии, сельском хозяйстве, а именно, к определению флавоноидов в траве горца перечного и траве горца птичьего. Заявленное изобретение может быть применено в химико-фармацевтичекой, биотехнологической, аграрной и смежных отраслях.
Уровень техники
Важной проблемой на современном этапе развития химико-фармацевтической, биотехнологической, аграрной и смежных отраслей, является расширение сырьевой базы для получения лекарственных растительных препаратов.
Решение этой проблемы заключается в применении лекарственного растительного сырья, представленного близкородственными видами, к которым относятся, в частности, представители рода горец - Persicaria Mill. семейства гречишных - Polygonaceae Juss., широко распространенные на территории Российской Федерации (РФ).
Особый интерес для исследования и практического применения представляют: официнальные трава горца перечного и трава горца птичьего (спорыш).
Траву горца птичьего (спорыш) и траву горца перечного применяют в качестве кровоостанавливающего, повышающего свертываемость крови, вяжущего, болеутоляющего, мочегонного, антимикробного средства и др.
Однако вышеуказанные представители семейства Polygonaceae Juss., обладают и отличиями, в частности, трава горца птичьего (спорыш) содержит большое количество кремниевой кислоты, что является противопоказанием при мочекаменной болезни, в отличие от горца перечного. При этом, горец перечный для некоторых сельскохозяйственных животных является ядом, в то время как горец птичий используется в качестве корма, богатого протеином и другими биологически активными веществами (БАВ).
Трава горца перечного и птичьего при своем близком химическом составе имеют отличия: в траве горца птичьего содержатся основные флавоноиды авикулярин и рутин, а в траве горца перечного - флавоноид гиперозид.
Актуальной задачей в области обеспечения качества лекарственных средств растительного происхождения, является разработка современных, высокоточных методов анализа, способных достоверно (объективно) определять действующие вещества.
Одним из перспективных методов в химико-фармацевтической, биотехнологической, аграрной и других смежных отраслей является тонкослойная хроматография (ТСХ).
Метод ТСХ применяется для контроля качества лекарственного растительного сырья (ЛРС) и лекарственных растительных препаратов (ЛРП) и может быть использован в анализе различных биологически активных соединений (БАС) растительного происхождения, например, фенольных соединений, флавоноидов, гидроксикоричных кислот, алкалоидов. Данный метод позволяет проводить идентификацию того или иного лекарственного растительного препарата по профилю основной группы БАС, оказывающей фармакологическое действие, а также определять примеси других видов ЛРС.
Из уровня техники известен способ определения флавоноидов в траве горца перечного методом ТСХ, раскрытый в источнике [8]. Недостатком данного способа является использование подвижной фазы бутанол, уксусная кислота ледяная, вода в соотношении 4:1:2, соответственно, которая не позволяет обеспечить достаточное разделение зон адсорбции. Также, для обработки хроматограммы применяется спиртовой раствор алюминия хлорида, который не относится к чувствительным реагентам для детектирования/дериватизации и не позволяет оценивать цвет флуоресценции полученных хроматограмм.
Из уровня техники известен другой способ определения флавоноидов в траве горца птичьего (спорыша), раскрытый в источнике [9]. Недостатками раскрытого способа является применение аналогичных, вышеизложенному способу, реактивов подвижной фазы, которые в заданной комбинации не могут обеспечить должного разделения исследуемых веществ.
Из уровня техники известен способ определения флавоноидов в лекарственных растительных препаратах, раскрытый в источнике [10]. Недостатками известного способа является то, что иная структура флавоноидов и морфологическое строение травы горца перечного и травы горца птичьего, не позволяют использовать указанные, в раскрытом способе, условия экстракции, и таким образом не способствуют получению ожидаемого объективного результата.
Из уровня техники известен другой способ количественного определения биологически активных соединений в лекарственном растительном сырье, представляющих собой экстракт травы термопсиса, листьев толокнянки, где используют высокоэффективную тонкослойную хроматографию (ВЭТСХ) [11-12]. Данный метод не подходит для идентификации и анализа флавоноидов, содержащихся в траве горца перечного и траве горца птичьего, из-за различного морфологического строения ЛРС и другого качественного состава активных веществ.
Другим известным способом идентификации биологически активных веществ в ЛРС, используемый в анализе лекарственных растительных препаратов, является метод ВЭЖХ [13]. В качестве объекта исследования использовались препараты «Валерианы настойка» в лекарственной форме «настойка», или в лекарственном препарате «Валерианы экстракт» в лекарственной форме «таблетки, покрытые пленочной оболочкой», или в фармацевтической субстанции «Валерианы экстракт густой». Данный способ не позволяет проводить идентификацию флавоноидов, так как в раскрытом способе используются условия проведения для количественного анализа сесквитерпеновых кислот.
Трудоемкие этапы выделения исследуемой группы биологически активных соединений (флавоноидов), долгая очистка от сопутствующих и балластных веществ, длительность анализа, дороговизна стандартного образца авикулярина не позволяют применять метод ВЭЖХ для идентификации флавоноидов в траве горца птичьего и траве горца перечного.
К общим недостаткам известных способов относятся: условия проведения пробоподготовки образцов, в частности, для каждого вида лекарственного растительного сырья требуется различное время насыщения камеры подвижной фазы; необходимость использования разной концентрации реактива для проведения детектирования, представляющего собой спиртовой раствор алюминия хлорида. Таким образом, условия проведения пробоподготовки, раскрытые в известных способах, не позволяют в полной мере проводить объективную оценку качества, исследуемых близкородственных видов ЛРС в одинаковых условиях. Кроме того, в лаборатории не всегда возможно осуществление известных способов в условиях ограниченности финансовых, временных и кадровых ресурсов.
В связи с вышеизложенным, для лекарственного растительного сырья из семейства Polygonaceae Juss. была выявлена потребность в разработке технического решения, обладающего чувствительностью и селективностью, позволяющего идентифицировать флавоноиды в официнальных траве горца перечного и траве горца птичьего (спорыша).
Раскрытие сущности изобретения
Технической задачей является разработка способа идентификации (определения) флавоноидов в траве горца перечного и траве горца птичьего для осуществления контроля качества лекарственного растительного сырья, обладающего чувствительностью и селективностью.
Техническим результатом заявленного технического решения, обладающего чувствительностью и селективностью, является идентификация флавоноидов для нескольких видов лекарственного растительного сырья в одинаковых условиях проведения контроля качества, что может способствовать производительности и экономической эффективности в научных организациях, и на промышленных предприятиях химико-фармацевтической, биотехнологической, аграрной и смежных отраслей.
Технический результат заявленного изобретения достигается благодаря следующим признакам:
- возможность проведения анализа в одинаковых условиях для нескольких видов лекарственного растительного сырья;
- использование специфичного реактива для детектирования зон адсорбции:
- применение смеси растворителей (подвижной фазы) толуол - этил ацетат - муравьиная кислота безводная - вода в соотношении 10:20:5:2, соответственно, с помощью которой возможно провести достаточно четкое разделение зон адсорбции:
- использование стандартных образцов рутина и или гиперозида;
- экстракция 96% и 70% этиловым спиртом.
Способ идентификации флавоноидов в лекарственном растительном сырье с применением восходящей тонкослойной хроматографии, отличающийся тем, что в траву горца перечного или траву горца птичьего экстрагируют этиловым спиртом 96% и 70% и соответственно, фильтруют затем фильтраты извлечений и растворенные в спирте этиловом 70% стандартные образцы рутина и гиперозида до концентрации 0.5 мг/мл, наносят на хроматографические пластинки, затем разделяют в хроматографической камере насыщенной в течение 30 мин подвижной фазой, представляющей собой смесь растворителей толуола, этил ацетата, муравьиной кислоты и воды в соотношении 10:20:5:2. соответственно, высушивают до удаления следов подвижной фазы, при нагревании пластинки в течение 3 мин при температуре 105°С, проявляют путем поочередного опрыскивания 1% раствором дифенилборной кислоты аминоэтилового эфира в 96% этиловом спирте и 5% раствором полиэтиленгликоля 400 в 96% этиловом спирте, детектируют в ультрафиолетовом свете при длине волны 365 нм, определяют зону адсорбции.
Способ, отличающийся тем, что хроматографическне пластинки со слоем силикагеля с флуоресцентным индикатором.
Способ, отличающийся тем, что стандартные образцы рутина и гиперозида наносят на хроматографические пластинки по 2 мкл.
Способ, отличающийся тем, что фильтраты извлечений наносят на хроматографическне пластинки по 10 мкл.
Краткое описание чертежей и иных материалов (Приложение):
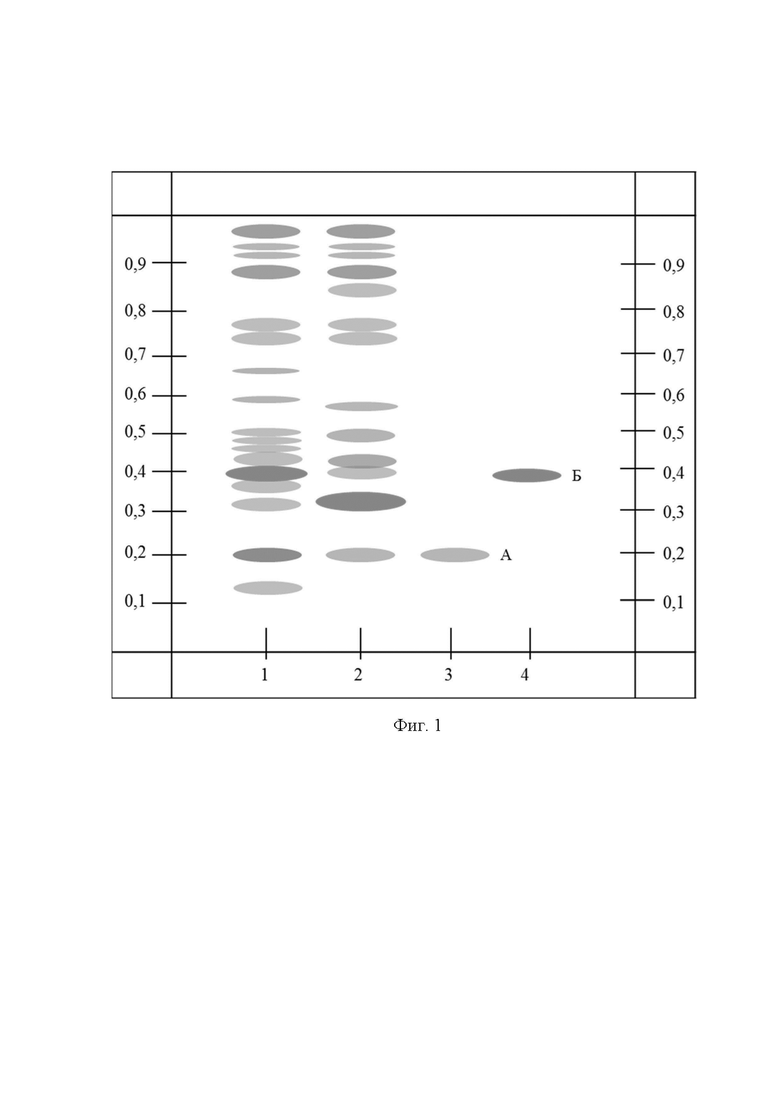
Фиг. 1. - 1. Спирто-водное извлечение из травы горца перечного; 2. Спирто-водное извлечение из травы горца птичьего (спорыша); 3. Раствор стандартного образца рутина 0,5 мг/мл в 70% спирте этиловом; 4. Раствор стандартного образца гиперозида 0,5 мг/мл в 70% спирте этиловом; А - рутин, стандартный образец, Б - гиперозид, стандартный образец.
Осуществление изобретения
В качестве объектов исследования были выбраны: официнальные трава горца перечного и трава горца птичьего (спорыш).
В области обеспечения качества лекарственных средств растительного происхождения, актуальной задачей является разработка современных методов анализа, обладающих селективными и чувствительными свойствами, способных достоверно (объективно) определять действующие вещества.
Основным флавоноидом травы горца перечного является гиперозид (кверцетин-3-О-галактозид), имеющий следующую структурную формулу:
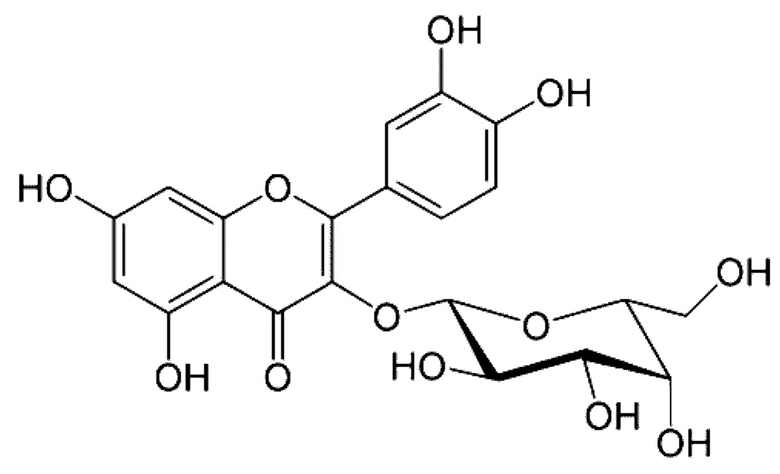
Одним из основных флавоноидов травы горца птичьего является рутин (кверцетин-3-О-рутинозид), имеющий структурную формулу:
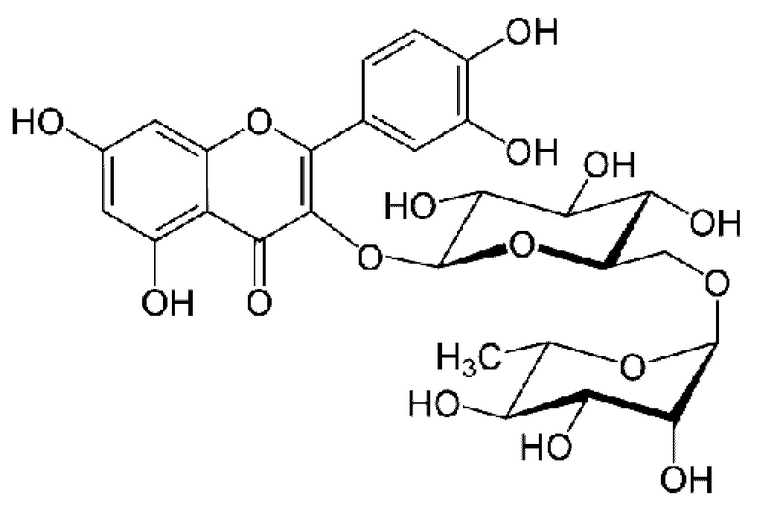
Оба соединения являются гликозидами (содержат сахарный остаток) флавоноида кверцетина.
Основным флавоноидом травы горца птичьего является авикулярин, имеющий структурную формулу:
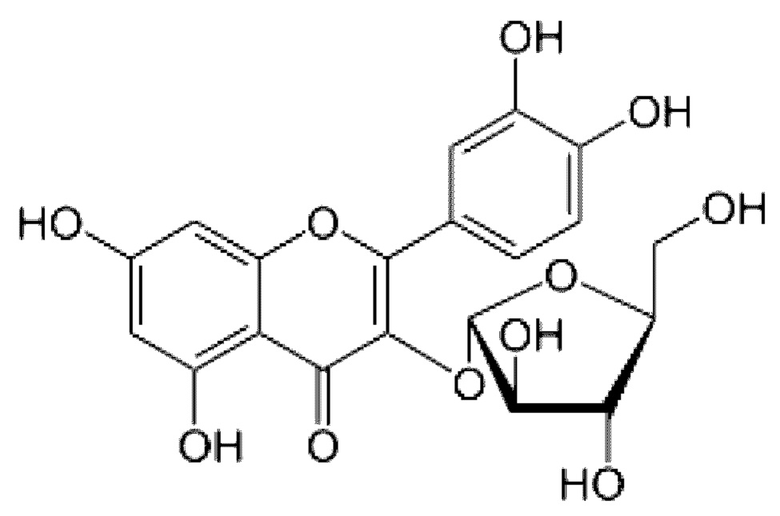
Тонкослойная хроматография (ТСХ) зарекомендовала себя как быстрый и эффективный способ идентификации лекарственного растительного сырья в дополнение к определению внешних и микроскопических признаков [11].
Данный вид хроматографии основан на различии в скорости перемещения компонентов смеси в плоском тонком слое сорбента при их движении в потоке подвижной фазы. Разделение происходит по адсорбционному, распределительному или ионообменному механизму, или какой-либо их комбинации. ТСХ используется для исследования как однокомпонентных, так и многокомпонентных лекарственных средств при испытаниях на подлинность (идентификация анализируемых веществ), родственные примеси (испытание на чистоту) полуколичественным и количественным методами, а также, для количественного определения анализируемых веществ [11-13].
Заявленный способ идентификации флавоноидов в траве горца перечного и траве горца птичьего (спорыш) включает наиболее полную экстракцию лекарственного растительного сырья (препарата) спиртом этиловым с оптимальной концентрацией для каждого из вышеописанных лекарственных растительных препаратов (сырья).
Получают спиртовое извлечение (экстракт) травы горца перечного или травы птичьего (спорыш), содержащий флавоноиды группы кверцетина. Растворенные в спирте этиловом 70% стандартные образцы рутина и гиперозида до концентрации 0,5 мг/мл наносят одновременно с испытуемыми растворами по 10 мкл на хроматографические пластинки со слоем силикагеля с флуоресцентным индикатором. Испытуемые растворы -10 мкл, растворы стандартных образцов - 2 мкл. Проводят восходящую хроматографию в смеси растворителей толуола, этилацетата, муравьиной кислоты и воды в соотношении 10:20:5:2, соответственно, с насыщением хроматографической камеры в течение 30 мин и до прохождения смесью растворителей около 90% длины хроматографической пластины, высушивают до удаления следов растворителей, детектируют путем нагревания на нагревательной плитке в течение 3 мин при температуре 105°С, проявляют путем поочередного опрыскивания 1% раствором дифенилборной кислоты аминоэтилового эфира в 96% спирте и 5% раствором полиэтиленгликоля 400 в 96% спирте теплую хроматографическую пластину, затем просматривают в ультрафиолетовом свете при длине волны 365 нм, определяют зону адсорбции для каждого из вышеперечисленных лекарственных растительных препаратов.
Предлагаемый способ, в отличие от прототипов, позволяет получить индивидуализированные зоны адсорбции для каждого вида действующих веществ, представляющие собой флавоноиды травы горца перечного и травы горца птичьего, и таким образом различить два вышеперечисленных вида лекарственных растений друг от друга. Известные способы идентификации, описанные в прототипах, не позволяют это сделать.
Возможность осуществления заявленного способа раскрыта в следующих примерах.
Пример 1. Идентификация флавоноидов в траве горца перечного.
Около 1,0 г сырья, измельченного до величины частиц, проходящих сквозь сито с отверстиями 1,0 мм, кипятят на водяной бане с 50 мл спирта 96% в течение 10 мин, затем охлаждают и фильтруют.
На пластинку ТСХ со слоем силикагеля с флуоресцентным индикатором наносят 10 мкл полученного раствора и 2 мкл раствора стандартного образца (СО) рутина и раствора СО гиперозида. Хроматографируют в смеси растворителей толуол - этилацетат - муравьиная кислота - вода в соотношении 10:20:5:2, соответственно, при насыщении камеры в течение 30 мин. После прохождения подвижной фазой около 90% длины пластинки, ее вынимают, сушат на воздухе до удаления следов растворителей, нагревают при температуре от 100°С до 105°С и еще теплую пластинку последовательно опрыскивают 1% раствором дифенилборной кислоты аминоэтилового эфира в 96% спирте этиловом и 5% раствором полиэтиленгликоля 400 в 96% спирте этиловом, затем просматривают в ультрафиолетовом свете (УФ-свете) при длине волны 365 нм.
На хроматограммах стандартных растворов обнаруживается зона адсорбции коричневато-желтого цвета (рутин), выше нее - зона адсорбции коричневато-желтого цвета (гиперозид).
На хроматограмме испытуемых растворов травы горца перечного обнаруживаются: в нижней трети пластинки зона адсорбции коричневато-желтого цвета ниже зоны СО рутина, синяя зона на уровне зоны СО рутина, голубая зона чуть выше нее; в средней трети - зоны адсорбции коричневато-желтого и желтого цвета на уровне, чуть ниже и чуть выше зоны СО гиперозида; в верхней трети - зоны желтовато-зеленого, сине-голубого и синего цвета. Также в верхней трети пластинки наблюдаются другие зоны адсорбции.
Примечание. Приготовление раствора стандартного образца рутина: около 5 мг рутина растворяют в 8 мл спирта этилового 70% в мерной колбе вместимостью 10 мл, доводят объем раствора тем же спиртом до метки и перемешивают.
Приготовление раствора стандартного образца гиперозида: около 5 мг гиперозида растворяют в 8 мл спирта этилового 70% в мерной колбе вместимостью 10 мл, доводят объем раствора тем же спиртом до метки и перемешивают.
Пример 2. Идентификация флавоноидов в траве горца птичьего.
Около 1,0 г сырья, измельченного до величины частиц, проходящих сквозь сито с отверстиями 1,0 мм, кипятят на водяной бане с 10 мл спирта 70% в течение 10 мин, затем охлаждают и фильтруют.
На пластинку ТСХ со слоем силикагеля с флуоресцентным индикатором наносят 10 мкл полученного раствора и 2 мкл раствора стандартного образца (СО) рутина и раствора СО гиперозида. Хроматографируют в смеси растворителей толуол - этилацетат - муравьиная кислота - вода в соотношении 10:20:5:2, соответственно, при насыщении камеры 30 мин. После прохождения подвижной фазой около 90% длины пластинки, ее вынимают, сушат на воздухе до удаления следов растворителей, нагревают при температуре от 100°С до 105°С и еще теплую пластинку последовательно опрыскивают 1% раствором дифенилборной кислоты аминоэтилового эфира в 96% спирте этиловом и 5% раствором полиэтиленгликоля в 96% спирте этиловом, затем просматривают в УФ-свете при длине волны 365 нм.
На хроматограммах стандартных растворов обнаруживается зона адсорбции коричневато-желтого цвета (рутин), выше нее - зона адсорбции коричневато-желтого цвета (гиперозид).
На хроматограмме испытуемых растворов травы горца птичьего обнаруживаются: в нижней трети - зона адсорбции коричневато-желтого цвета на уровне зоны СО рутина; в средней трети - две зоны адсорбции коричневато-желтого и зеленовато-желтого цвета чуть ниже и на уровне зоны СО гиперозида, над ними - зона зеленого цвета; в верхней трети - зоны адсорбции синего цвета. Также наблюдаются другие зоны адсорбции.
Примечание. Приготовление раствора стандартного образца рутина: около 5 мг рутина растворяют в 8 мл спирта в мерной колбе вместимостью 10 мл при нагревании на водяной бане, охлаждают, доводят объем раствора тем же спиртом до метки и перемешивают.
Приготовление раствора стандартного образца гиперозида: около 5 мг гиперозида растворяют в 8 мл спирта в мерной колбе вместимостью 10 мл при нагревании на водяной бане, охлаждают, доводят объем раствора тем же спиртом до метки и перемешивают.
На фиг. 1 приведены результаты идентификации флавоноидов в траве горца перечного и траве горца птичьего предлагаемым способом.
Вывод. Заявленный способ позволяет получить индивидуальные зоны адсорбции, для каждого из вышеперечисленных лекарственных растительных препаратов, действующих веществ - флавоноидов травы горца перечного и травы горца птичьего, и таким образом различить два вышеперечисленных вида растений друг от друга.
Заявленное техническое решение раскрыто довольно подробно, с целью ясности понимания, и не должно рассматриваться, как ограничивающее объем притязаний.
Представленные примеры служат только для цели иллюстрации и раскрытия заявленного способа, и не должны рассматриваться как ограничивающие объем притязаний настоящего изобретения.
Промышленная применимость.
Все представленные примеры подтверждают возможность применения заявленного способа в фармации, химии, биологии, медицине, ветеринарии, сельском хозяйстве, а также то, что заявленное изобретение может быть применено в химико-фармацевтической, биотехнологической, аграрной и смежных отраслях.
Таким образом, поставленная техническая задача, а именно, разработка способа идентификации флавоноидов в траве горца перечного и траве горца птичьего выполнена.
Список литературы
1. Пименова И.А, Гудкова А.А., Чистякова А.С.Количественное содержание суммы флавоноидов в некоторых представителях рода Polygonum L. Пути и формы совершенствования фармацевтического образования. Актуальные вопросы разработки и исследования новых лекарственных средств. Материалы 7-й Международной научно-методической конференции «Фармобразование-2018». 28-30 марта 2018. г. Воронеж; 2018.С.287-290.
2. Haraguchi Н, Hashimoto Ж, Yagi A. Antioxidative substances in leaves of Polygonum hydropiper. J. Agric. Food Chem 1992; 40: 1349-351. (URS: https://doi.org/10.1021/jf00020a011. Дата обращения 02.09.2024).
3. Peng ZF, Strack D, Baumert A, Subramaniam R, Goh NK, Chia TF et al. Antioxidant flavonoids from leaves of Polygonum hydropiper L. Phytochemistry 2003;62:219-28. (URS: https://doi.org/10.1016/S0031-9422(02)00504-6. Дата обращения 02.09.2024).
4. Жаркеева A.M., Шевченко А.С., Корулькин Д.Ю., Музычкина Р.А. Выделение полифлаванов из травы горца перечного для использования в фармацевтической промышленности. Вестник Казахского Национального медицинского университета. 2018;3:241-3.
5. Zanwar АА, Badole SL, Shende PS, Hegde MV, Bodhankar SL. Role of gallic acid in cardiovascular disorders. In: Polyphenols Human Health Dis 2014. Academic Press. 2014:1045-7. (URS: http://dx.doi.org/10.1016/B978-0-12-3984562.00080-3. Дата обращения 02.09.2024).
6. Cai Y, Wu L, Lin X, Hu X, Wang L. Phenolic profiles and screening of potential a-glucosidase inhibitors from Polygonum aviculare L. leaves using ultrafiltration combined with HPLC-ESI-qTOF-MS/MS and molecular docking analysis. Indust Crops and Prod. 2020;154:112673. (URS: https://doi.org/10.1016/j.indcrop.2020.112673. Дата обращения 02.09.2024).
7. Yu Y, Liu G, Piao M, Lang M, Wang Y, Jin M et al. Chemical constituents of Polygonum aviculare L. and their chemotaxonomic significance. Biochem Syst and Ecol. 2022;105:104529. (URS: https://doi.org/10.1016/j.bse.2022.104529. Дата обращения 02.09.2024).
8. ФС.2.5.0067.18. Фармакопея. Издание XIV. Том IV. Биологические лекарственные препараты, Растительные средства и препараты, Гомеопатические фармацевтические субстанции. Стр. 5990-5991.
9. ФС.2.5.0069.18. Фармакопея. Издание XIV. Том IV. Биологические лекарственные препараты, Растительные средства и препараты, Гомеопатические фармацевтические субстанции. Стр. 6007-6008.
10. ФС.2.5.0095. Фармакопея. Издание XV. Сушеницы топяной трава. Электронное издание. (URS:https://pharmacopoeia.regmed.ru/pharmacopoeia/izd anie-15/2/2-3/sushenitsy-topyanoy-trava-/. Дата обращения 02.09.2024).
11. Патент № 2796599 Российской Федерации. МПК G01N 30/90 (2006.01). Способ определения алкалоидов в экстракте термопсиса. Заявка RU2022132871A. Дата подачи 15.12.2022. Дата опубл. 26.05.2023. Моргунов И.М., Антонова Н.П., Прохватилова С.С., Шефер Е.П., Голомазова Т.А.
12. Патент № 2802173 Российской Федерации. МПК G01N 30/90 (2006.01). Способ определения арбутина в листьях толокнянки. Заявка RU2023102202A. Дата подачи 01.02.2023. Дата опубл. 22.08.2023. Моргунов И.М., Антонова Н.П., Шефер Е.П., Прохватилова С.С, Голомазова Т.А., Евдокимова О.В.
13. Патент № 2744231 Российской Федерации. МПК А61К 36/84 (2006.01), А61К 9/20 (2006.01), А61К 9/06 (2006.01), G01N 1/28 (2006.01), G01N 1/38 (2006.01), G01N 30/06 (2006.01). Способ определения суммы сесквитерпеновых кислот в пересчете на валереновую кислоту методом ВЭЖХ в лекарственных средствах. Заявка RU2020115945A. Дата подачи 15.05.2020. Дата опубл. 03.03.2021. Антонова Н.П., Шефер Е.П., Калинин A.M., Семенова Н.Е., Прохватилова С.С., Моргунов И.М.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ГИПОТЕНЗИВНОЙ АКТИВНОСТЬЮ | 2000 |
|
RU2182487C2 |
| СРЕДСТВО ДЛЯ ПРОПИТКИ ГИГИЕНИЧЕСКОГО ТАМПОНА, ОБЛАДАЮЩЕЕ АНТИМИКРОБНОЙ АКТИВНОСТЬЮ, И СПОСОБ ПОЛУЧЕНИЯ ФИТОТАМПОНА, ОБЛАДАЮЩЕГО АНТИМИКРОБНОЙ АКТИВНОСТЬЮ | 2020 |
|
RU2740284C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ИММУНОМОДУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 2012 |
|
RU2496510C2 |
| СРЕДСТВО "ЧАЙ БАЙКАЛЬСКИЙ-6", ОБЛАДАЮЩЕЕ ДИУРЕТИЧЕСКОЙ АКТИВНОСТЬЮ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2004 |
|
RU2237488C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ГИПОГЛИКЕМИЧЕСКОЙ АКТИВНОСТЬЮ | 1999 |
|
RU2141841C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОВОСПАЛИТЕЛЬНЫМ И АНТИБАКТЕРИАЛЬНЫМ ДЕЙСТВИЕМ | 2009 |
|
RU2413527C1 |
| Биологически активная добавка к пище капсулированной формы | 2020 |
|
RU2752781C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО АДАПТОГЕННОЙ АКТИВНОСТЬЮ | 1997 |
|
RU2135198C1 |
| СБОР ЛЕКАРСТВЕННЫХ РАСТЕНИЙ "ФИТОМОРОЗКО", ОБЛАДАЮЩИЙ ФРИГОПРОТЕКТОРНЫМ ДЕЙСТВИЕМ | 2006 |
|
RU2336896C2 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ГИПОЛИПИДЕМИЧЕСКОЙ АКТИВНОСТЬЮ | 2000 |
|
RU2173161C1 |
Настоящее изобретение относится к химии, биологии, медицине, ветеринарии, сельскому хозяйству, а именно к определению флавоноидов в траве горца перечного или траве горца птичьего. Способ идентификации флавоноидов рутина и гиперозида в лекарственном растительном сырье с применением восходящей тонкослойной хроматографии, в котором траву горца перечного или траву горца птичьего экстрагируют этиловым спиртом 96% и 70%, соответственно, фильтруют, затем на хроматографические пластинки наносят фильтраты извлечений по 10 мкл и растворенные в 70% спирте этиловом до концентрации 0,5 мг/мл стандартные образцы рутина и гиперозида по 2 мкл, затем разделяют в хроматографической камере насыщенной в течение 30 мин подвижной фазой, представляющей собой смесь растворителей толуола, этилацетата, муравьиной кислоты и воды в соотношении 10:20:5:2, соответственно, высушивают до удаления следов подвижной фазы, при нагревании пластинки в течение 3 мин при температуре 105°С, проявляют путем поочередного опрыскивания 1% раствором дифенилборной кислоты аминоэтилового эфира в 96% этиловом спирте и 5% раствором полиэтиленгликоля 400 в 96% этиловом спирте, детектируют в ультрафиолетовом свете при длине волны 365 нм, определяют зону адсорбции. Вышеописанный способ идентификации флавоноидов рутина и гиперозида в траве горца перечного или траве горца птичьего является чувствительным и селективным 1 з.п. ф-лы, 1 ил., 2 пр.
1. Способ идентификации флавоноидов рутина и гиперозида в лекарственном растительном сырье с применением восходящей тонкослойной хроматографии, отличающийся тем, что траву горца перечного или траву горца птичьего экстрагируют этиловым спиртом 96% и 70%, соответственно, фильтруют, затем на хроматографические пластинки наносят фильтраты извлечений по 10 мкл и растворенные в 70% спирте этиловом до концентрации 0,5 мг/мл стандартные образцы рутина и гиперозида по 2 мкл, затем разделяют в хроматографической камере насыщенной в течение 30 мин подвижной фазой, представляющей собой смесь растворителей толуола, этилацетата, муравьиной кислоты и воды в соотношении 10:20:5:2, соответственно, высушивают до удаления следов подвижной фазы, при нагревании пластинки в течение 3 мин при температуре 105°С, проявляют путем поочередного опрыскивания 1% раствором дифенилборной кислоты аминоэтилового эфира в 96% этиловом спирте и 5% раствором полиэтиленгликоля 400 в 96% этиловом спирте, детектируют в ультрафиолетовом свете при длине волны 365 нм, определяют зону адсорбции.
2. Способ по п. 1, отличающийся тем, что хроматографические пластинки со слоем силикагеля с флуоресцентным индикатором.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Фармакопея | |||
| Издание XIV | |||
| Том IV | |||
| Биологические лекарственные препараты, Растительные средства и препараты, Гомеопатические фармацевтические субстанции | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| КИРПИЧНАЯ СТЕНКА С ЖЕЛЕЗОБЕТОННЫМИ СТОЛБАМИ | 1927 |
|
SU6007A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Фармакопея | |||
| Издание XIV | |||
| Том IV | |||
| Биологические лекарственные препараты, Растительные средства и препараты, Гомеопатические | |||
Авторы
Даты
2025-04-28—Публикация
2024-09-03—Подача