Изобретение относится к области медицины, а именно к кардиологии, и может быть использовано для определения острой окклюзии интермедиарной ветви (ИМВ; синоним: интермедиарной артерии) левой коронарной артерии (ЛКА) как причины острого коронарного синдрома и показания к немедленной (в течение 2-х часов) коронароангиографии (КАГ).
Ствол ЛКА отходит от левого коронарного синуса и в большинстве случаев делится на 2 ветви (бифуркация) – переднюю межжелудочковую артерию (ПМЖА) и огибающую артерию (ОА). Однако в ряде случает случаев имеет место трифуркация - ствол ЛКА делится на 3 ветви – ПМЖА, ОА и ИМВ. Частота данного варианта коронарной анатомии сердца варьирует, по разным источникам, от 15 до 30% [1-3], а размер ИМВ - от очень малого до достаточно крупного; сама ИМВ также может делиться на ветви [4].
Острая окклюзия коронарной артерии, согласно современным клиническим рекомендациям [5, 6], требует немедленной (в течение 2 часов) КАГ с целью выполнения первичного чрескожного коронарного вмешательства (ЧКВ) на инфаркт-связанной артерии. Какую именно артерию считать инфаркт-связанной при многососудистом поражении, определяют в подавляющем большинстве случаев по электрокардиограмме (ЭКГ) в 12 стандартных отведениях (I-III, aVR, aVL, aVF, V1-V3, V4-V6) [5-7].
Сказанное выше обосновывает актуальность корректного определения инфаркт-связанной артерии для ЧКВ не только при наиболее частой коронарной анатомии, но также и при ее вариантах.
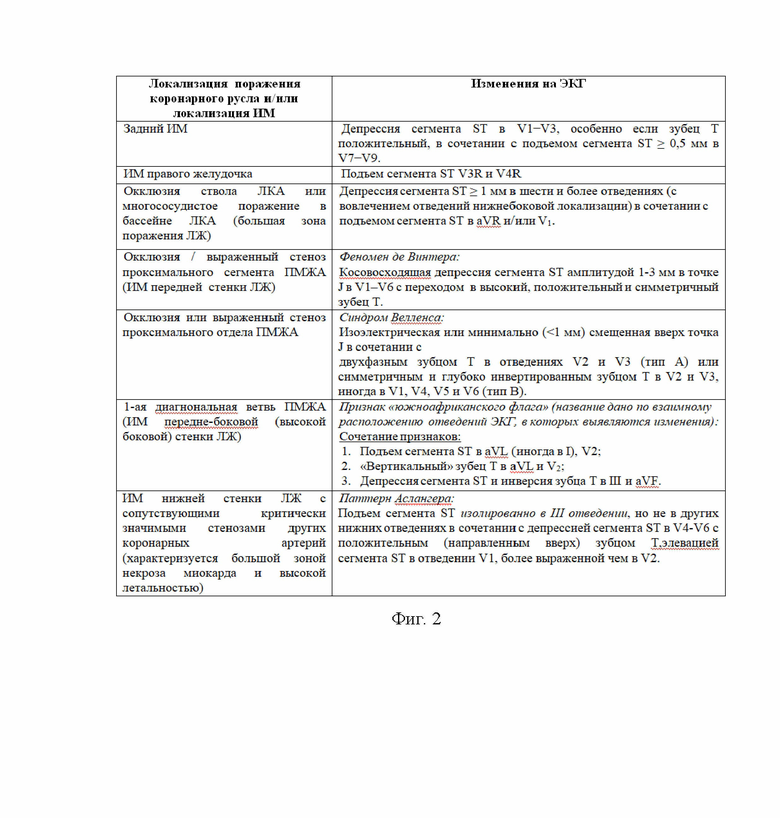
Диагностические ЭКГ-критерии для определения инфаркт-связанной коронарной артерии при стандартной анатомии коронарного русла хорошо известны, и их можно разделить на две группы: (1) критерии инфаркта миокарда (ИМ) с подъемом сегмента ST (независимо от локализации) (фиг.1) [7] и (2) критерии окклюзии конкретных коронарных артерий при отсутствии диагностически значимого подъема сегмента ST на ЭКГ (фиг. 2) [5, 8-17].
Каких-либо ЭКГ-феноменов при поражении ИМВ ранее описано не было. Это можно объяснить следующим. Либо ожидается классический, диагностически значимый, подъем сегмента ST (в таком случае он сам по себе является показанием к КАГ / ЧКВ, локализация поражения на ЭКГ не имеет решающего значения), либо ЭКГ-картина при поражении ИМВ приравнивается к таковой для других ветвей ЛКА (т.е. уже описана – фиг. 2). Так, в ряде литературных источников ИМВ рассматривается как более высокое отхождение первой диагональной ветви (D1) ПМЖА или первой ветви тупого края (ВТК1) ОА. Соответственно, по умолчанию ЭКГ-критерии поражения ИМВ приравниваются к таковым для поражения D1 или ВТК1.
Например, Kim T.Y., et al. (1999) рассматривали ИМВ как ответственную за строго боковую локализацию инфаркта миокарда (ИМ) наравне с D1 и ВТК1 [14] (что должно определяться на ЭКГ как диагностически значимые ишемические изменения в I, aVL, V6 [18]). Singh A., et al. (2021) также не выявили отличий в ЭКГ-картине между поражением ИМВ, D1 и ВТК1, объединив их в группу диагностически значимого подъема сегмента ST в I и aVL [19]. Кроме того, ограничением практического применения выводов данного авторского коллектива [19] следует считать использование для оценки подъема сегмента ST точки, следующей за точкой J через 60 мс (так называемая точка J60), тогда как для современной клинической практики оценка подъема сегмента ST рекомендована непосредственно в точке J (фиг. 1) [7].
Sarıçam E., et al. (2023) приравняли по ЭКГ-критериям ИМВ к ВТК1: «у шестидесяти пациентов в качестве инфаркт-связанной артерии была ВТК1 и/или ИМВ. ЭКГ-изменения в этих случаях - депрессия сегмента ST в V2 и подъем сегмента ST не менее 1 мм в II, III, aVF и V6» [20]. Существенным ограничением данной работы следует считать включение в анализ только случаев с диагностически значимым подъемом сегмента ST, которые сами по себе независимо от локализации поражения являются показанием к неотложной КАГ, т.е. работа не дает представления о том, есть ли другие ЭКГ-варианты окклюзионного поражения ИМВ.
В указных работах часто фигурирует вовлечение отведений I и aVL. Выполнен поиск и систематизация вариантов ЭКГ-феноменов с вовлечением этих отведений (фиг. 3) [21-25].
Работа Sarıçam E., et al. (2023) [20] демонстрирует в том числе и ограничения классификации острого коронарного синдрома по критерию подъема сегмента ST. К настоящему моменту уже описаны варианты поражения коронарного русла с окклюзией коронарной артерии (т.е. требующие неотложного вмешательства), но без подъема сегмента ST (фиг. 2) [5, 8-17] и все более широкое распространение получает термин «окклюзионный ИМ» (или «ИМ с окклюзионным поражением коронарной артерии») [26-31]. Накопление информации по этому вопросу позволило в Клинических рекомендациях Европейского кардиологического общества 2023 г. вынести ЭКГ-феномены окклюзионного поражения коронарного русла, протекающие без диагностически значимого подъема ST, но требующие неотложной КАГ [5].
Таким образом, собственные ЭКГ-феномены острой окклюзии ИМВ к настоящему моменту в отечественной и международной печати (выполнен поиск в системах PubMed, eLibrary, SCOPUS, Google Scholar без ограничений по времени и типе публикации) не описаны.
При этом, известно, что острый коронарный синдром, как таковой, не диагностируется по ЭКГ, тогда как ЭКГ является основанием для реперфузионной терапии, ее вида и сроков.
Технический результат — определение острой окклюзии интермедиарной ветви левой коронарной артерии с помощью стандартной электрокардиограммы в покое.
Технический результат достигается выявлением на стандартной электрокардиограмме (12 стандартных отведений) в покое следующих критериев:
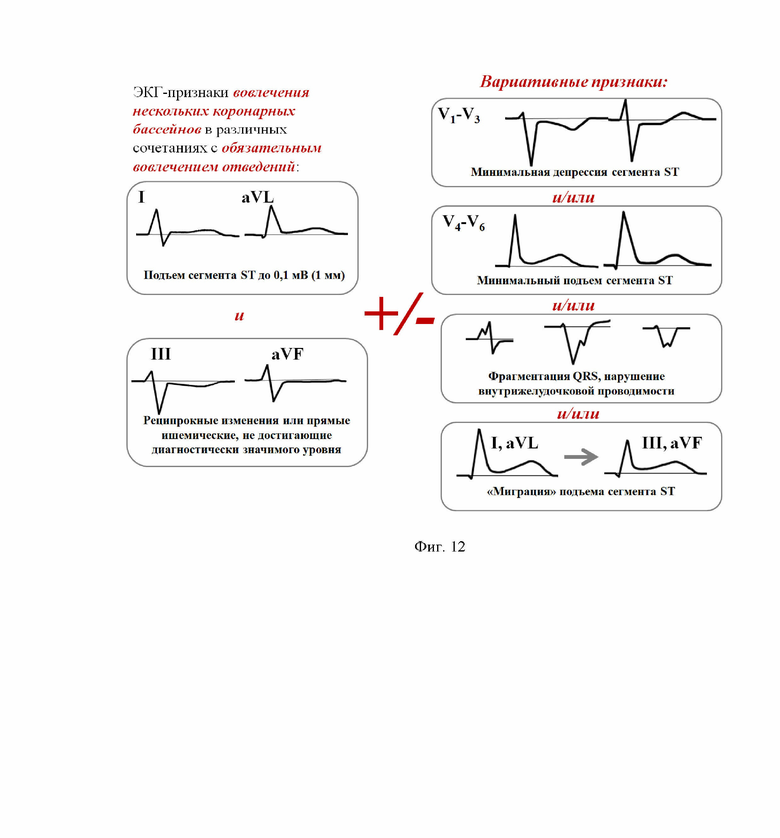
а) Постоянный критерий: признаки вовлечения нескольких коронарных бассейнов в различных сочетаниях с обязательным вовлечением отведений (1) I, aVL (подъем сегмента ST, не достигающий 0,1 мВ) и (2) III, aVF (ишемические изменения, как прямые, так и реципрокные; в случае прямых - не достигающие в острый период диагностически значимого уровня).
б) Вариативные критерии (в любых комбинациях в дополнение к изменениям в I, aVL, III, aVF, соответствующим постоянному критерию):
- минимальная депрессия сегмента ST в V1-V3 (передние отведения);
- минимальный подъем сегмента ST в V4-V6 (боковые отведения);
- фрагментация комплекса QRS или нарушения внутрижелудочковой проводимости;
- «миграция» в течение нескольких часов подъема сегмента ST из I, aVL в III, aVF (± II) без медицинских воздействий с целью реперфузии (фиг. 12).
Осуществление изобретения: Для изучения изолированной острой окклюзии ИМВ были отобраны пациенты, госпитализированные в Региональный сосудистый центр по поводу острого коронарного синдрома, у которых (1) по результатам КАГ была выявлена острая окклюзия или значимый стеноз (≥ 70%) ИМВ при отсутствии гемодинамически значимого сужения других крупных коронарных артерий (для ужесточения критериев в рамках данной работы под гемодинамически незначимым поражением других коронарных артерий понималось сужение их просвета менее 50%); (2) были в наличии и достаточном для анализа качестве ЭКГ первого медицинского контакта в 12 стандартных отведениях (не менее 2-х полных сердечных циклов в каждом отведении). Вольтаж 1 мВ = 10 мм. Скорость ЭКГ 25 или 50 мм/сек.
Критериев исключения не было.
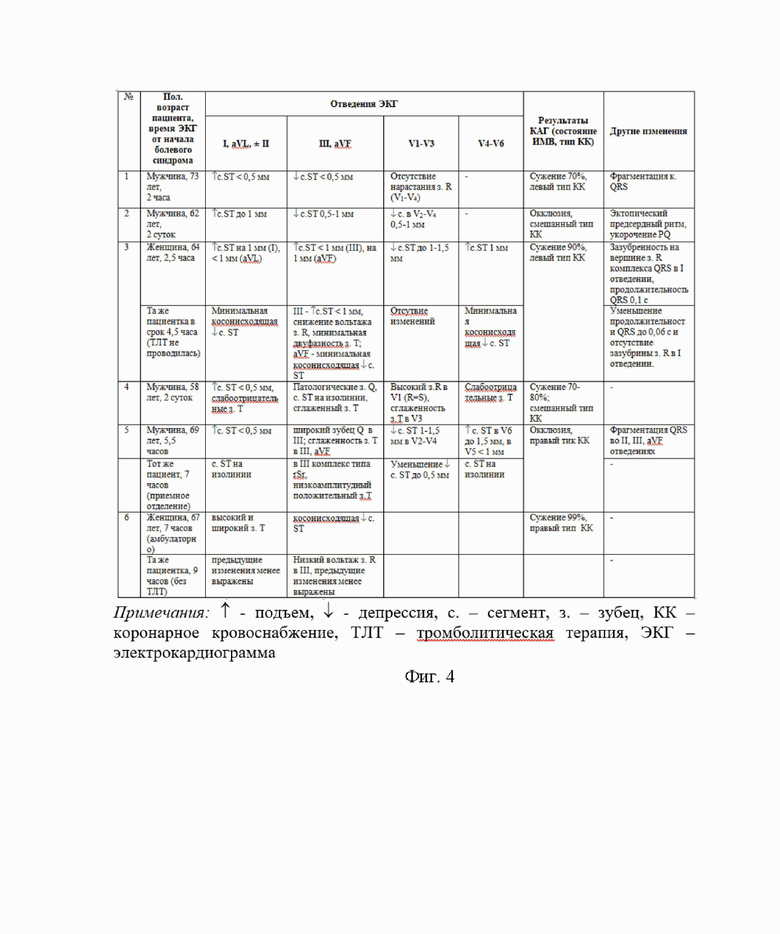
В результате в анализ было включено 6 клинических случаев (4 мужчины и 2 женщины); возраст от 58 до 73 лет, время первой ЭКГ от начала болевого синдрома – от 2-х часов до 2-х суток (фиг. 4). Относительно небольшое количество наблюдений определяется тем, что (1) ИМВ – это вариант нормы, но не рутинная находка, соответственно имеет нечастое распространение; (2) при наличии ИМВ далеко не всегда имеется острая окклюзия именно этой артерии как причина ОКС. Тем не менее, наличие даже небольшого количества таких пациентов требует оптимальной стратегии их ведения.
Для систематизации результатов и с учетом относительной однотипности изменений в определенных отведениях у этих пациентов, все отведения были разбиты на 4 группы: I, aVL, ± II (высокая боковая локализация); III, aVF (нижняя локализация); V1-V3 (передняя локализация); V4-V6 (боковая локализация).
КАГ проводилась по стандартному протоколу для острого коронарного синдрома. В трех случаях степень сужения ИМВ была на уровне 70-90% и еще в трех случаях – 99-100% (окклюзия). При этом, были представлены все варианты коронарного кровоснабжении: правый (n = 2), левый (n = 2), смешанный (n = 2).
Сводные данные по ЭКГ-изменениям представлены на фиг. 4, а клинические примеры – на фиг. 5-11.
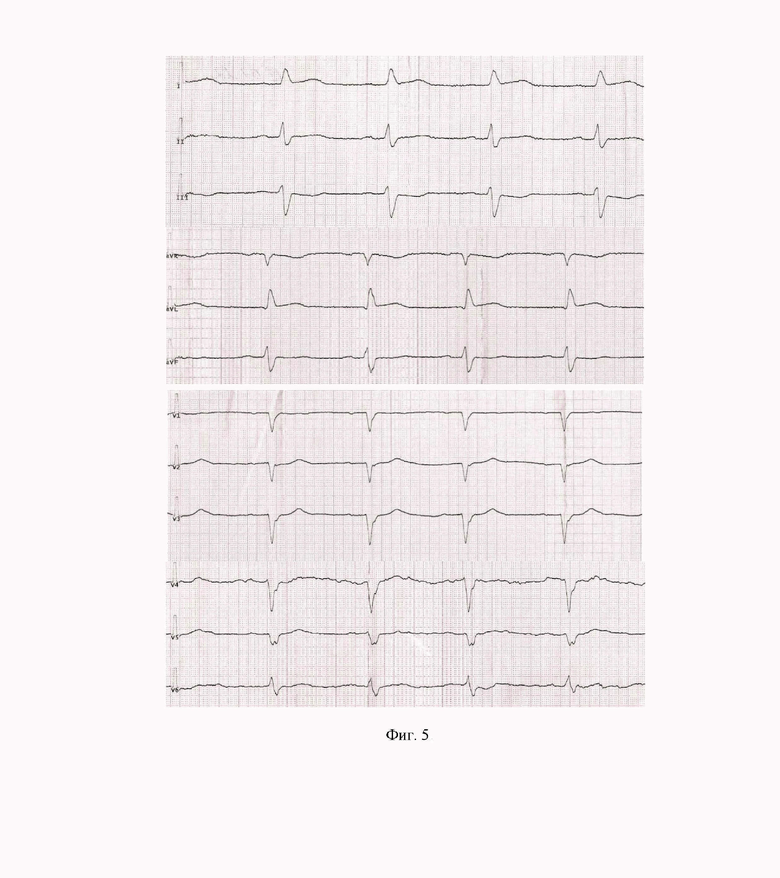
Клинический пример 1. Пациент Т., 73 года. Через 2 часа от начала болевого синдрома. Отклонение ЭОС влево, подъем с. ST в I, aVL отведениях менее 0,5 мм в сочетании с депрессией с. ST в III, aVF отведениях менее 1 мм, отсутствие нарастания зубца R в V1-V4 и фрагментация комплекса QRS (фиг. 5). На ЭКГ в приемном отделении уменьшение подъема сегмента ST в I, aVL отведениях, сглаженность и слабо выраженная отрицательная фаза зубца T, в III и aVF отведениях сегмент ST на изолинии (что можно расценить как эффективность тромболитической терапии), а также сохранялось отсутствие нарастания зубцов R и фрагментация QRS в V1-V4, кроме того, выявлен подъем cегмента ST менее 0,5 мм в отведениях V5-V6 с двухфазным зубцом T.
В дальнейшем на ЭКГ отмечалось углубление отрицательных зубца T I, aVL, V4-V6, сохранялся регресс зубца R V1-V3, в III отведении – небольшая, менее 0,5 мм депрессия с. ST в III отведении (со слабоположительным зубцом Т) и сглаженность зубца Т в aVF, в динамике уменьшилась выраженность фрагментации QRS в грудных отведениях – в V3 зарегистрирована небольшая зазубрина в начале восходящей части зубца S, но также появилась в отведениях II, III, aVF, чего не было на первичной ЭКГ.
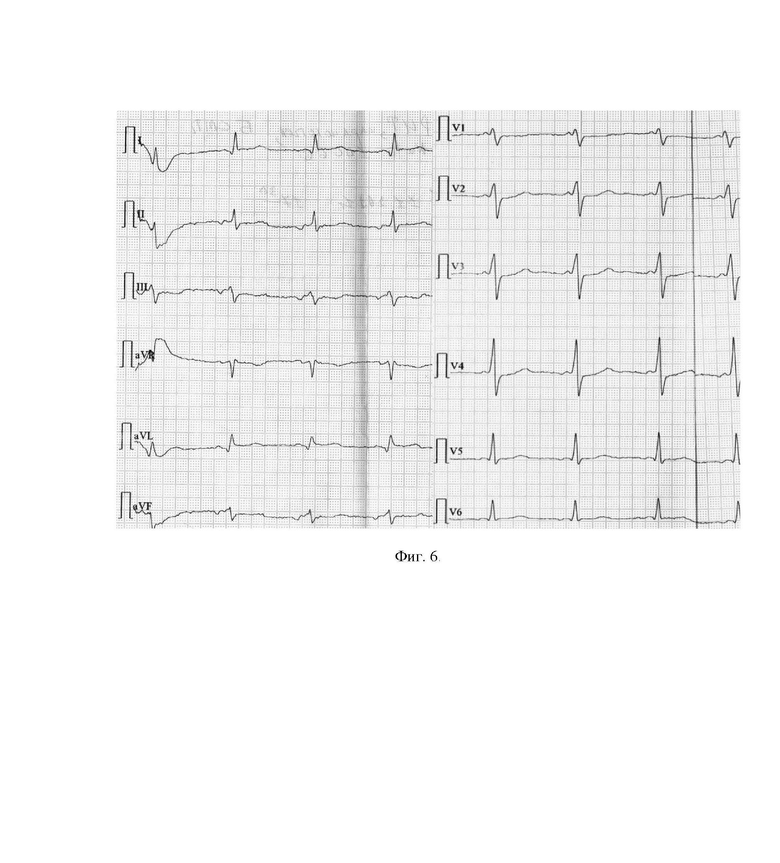
Клинический пример 2. Пациент А., 62 года. Через 2 суток от начала болевого синдрома. Эктопический предсердный ритм, укорочение PQ, подъем сегмента ST в I, aVL отведениях до 1 мм, депрессия с. ST III, aVF, V2-V4 0,5-1 мм (фиг. 6). Последующие 3 суток существенной динамики ЭКГ не отмечалось, что можно объяснить поздними сроками реваскуляризации (более 48 часов). На 2 и 3 сутки у пациента была зарегистрирована фибрилляция предсердий. В дальнейшем отмечалось восстановление синусового ритма, снижение сегмента ST к изолинии и формирование отрицательного зубца Т в I, aVL отведениях, сглаженность зубца Т в V6, уменьшение депрессии сегмента ST и увеличение амплитуды положительного зубца Т в III и aVF отведениях.
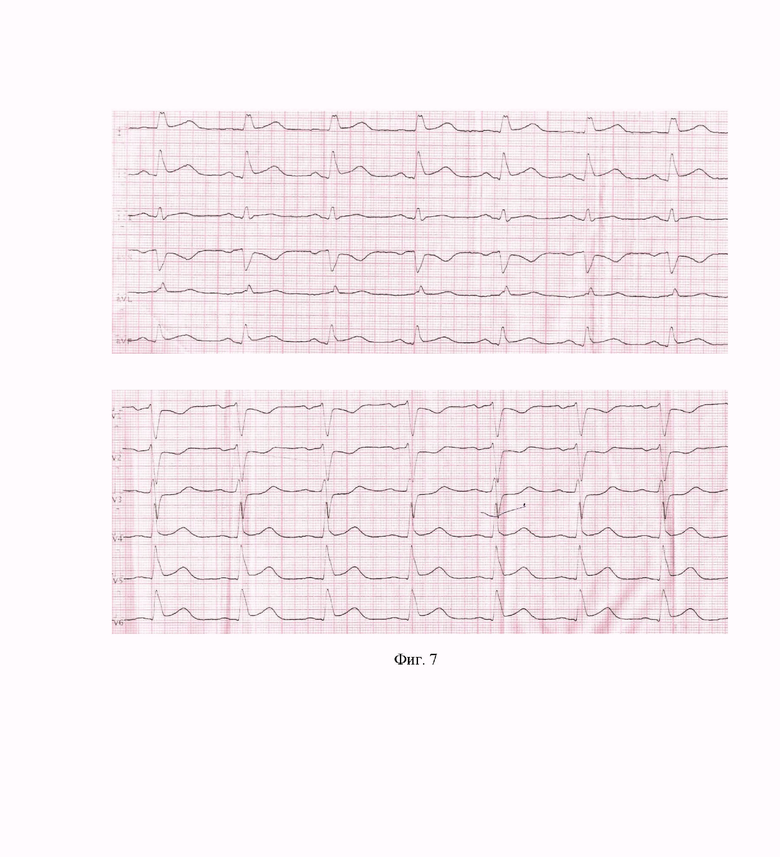
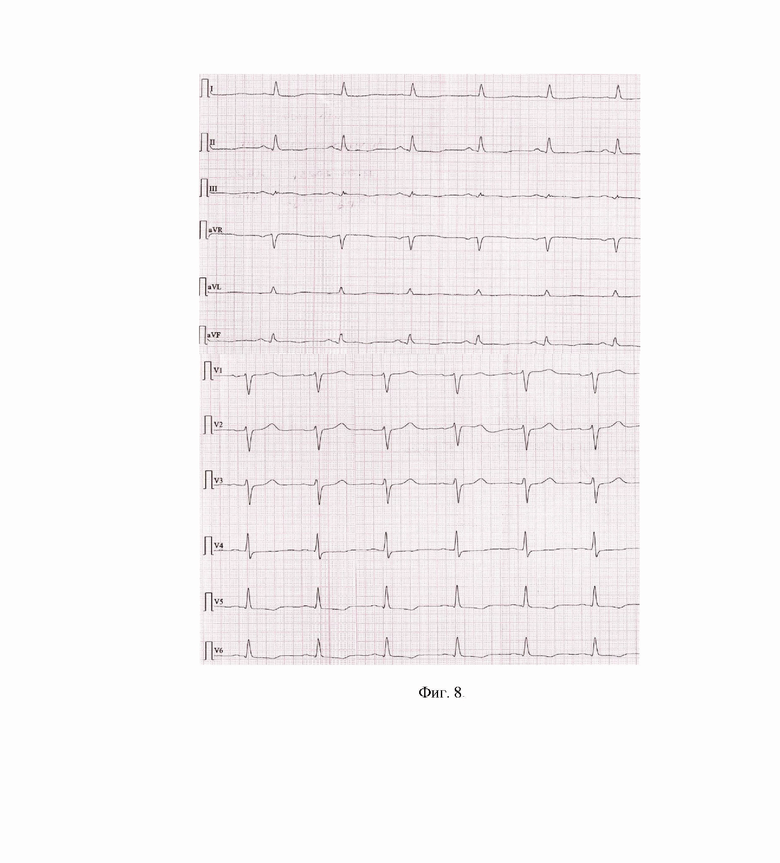
Клинический пример 3. Пациентка А., 64 лет. Через 2,5 часа от начала болевого синдрома. Синусовый ритм, подъем сегмента ST в отведениях I, II, aVF, V4-V6 - 1 мм, в III и aVL – менее 1 мм, депрессия сегмента ST в V1-V3 до 1-1,5 мм. Продолжительность QRS 0,1 мс и зазубренность на вершине зубца R комплекса QRS в I отведении (фиг. 7). При поступлении в стационар (через 4,5 часа от начала болевого синдрома) ЭКГ отличалась от исходной: подъем сегмента ST в I, II, aVL, AVF, V4-V6 сменился депрессией с. ST до 1 мм косонисходящего характера со слабоотрицательными зубцом Т в V5-V6, подъем с. ST регистрировался изолированно в III отведении с двухфазным зубцом Т, обращало на себя внимание снижение вольтажа зубца R в III отведении и уменьшение продолжительности QRS до 0,06 с и отсутствие зазубрины зубца R в I отведении, отсутствие депрессии сегмента ST V1-V3 (фиг. 8). На ЭКГ после ЧКВ – появление отрицательного зубца Т II, III, aVF, уменьшение депрессии сегмента ST в I и aVL отведениях, увеличение амплитуды положительного зубца Т в отведении aVL. В динамике на ЭКГ – сегмент ST на изолинии, появление патологического зубца Q в III отведении, небольшой зубец q в aVF, регресс зубца R в III отведении, углубились отрицательные зубцы Т – в отведениях II, III, aVF, V4-V6, сглаженность зубца Т в отведении I.
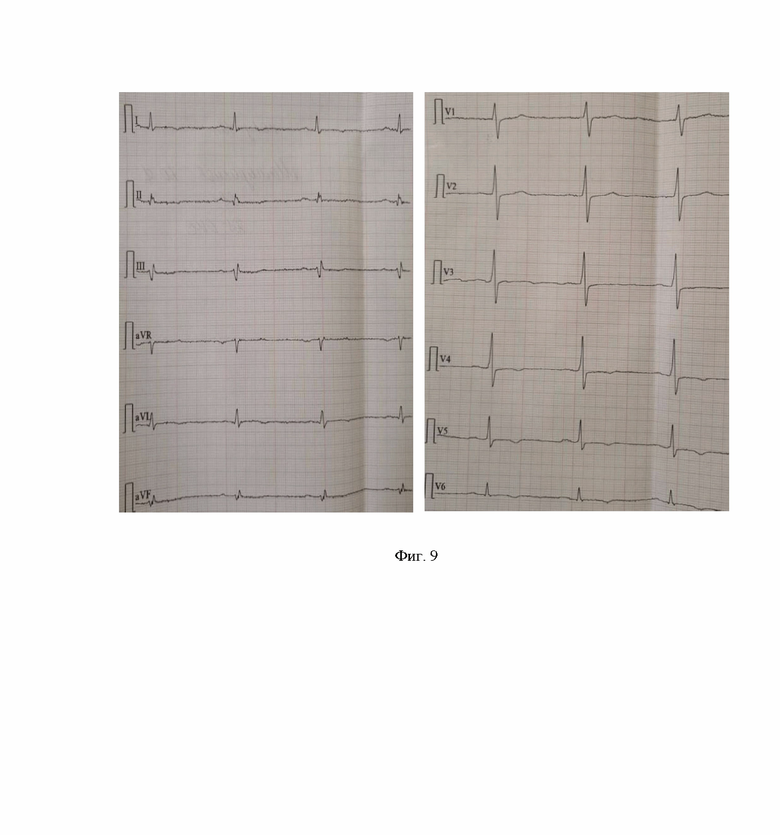
Клинический пример 4. Пациент М., 58 лет. Через 2 суток от начала болевого синдрома. Синусовый ритм, патологические зубцы Q в III, aVF отведениях, сегмент ST на изолинии, сглаженный зубец Т в III, aVF, высокий зубец R в V1 (R = S), сегмент ST приподнят в I, aVL менее 0,5 мм, слабоотрицательные зубцы Т I, aVL, V4-V6, сглаженность зубца Т в V3 (фиг. 9). На ЭКГ в динамике после ЧКВ – более глубокий отрицательный зубец Т I, aVL, V5-V6, положительный зубец Т в III отведении, V3, слабоположительный зубец Т в V4.
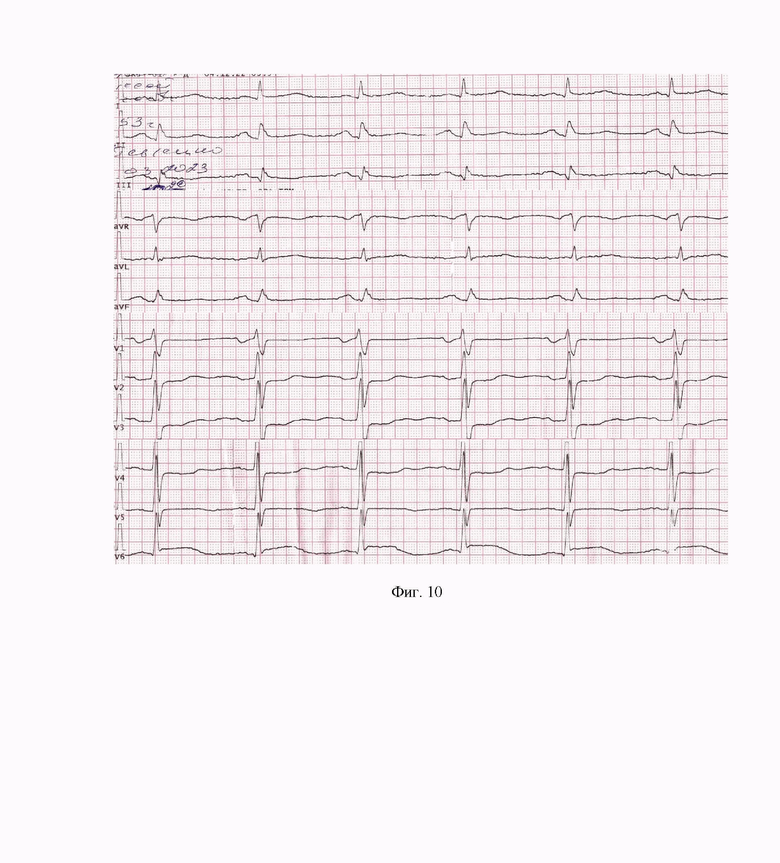
Клинический пример 5. Пациент Б., 69 лет. Через 7 часов от начала болевого синдрома. Синусовый ритм, сегмент ST «приподнят» в отведениях I, aVL менее 0,5 мм, в III отведении – широкий зубец Q в III отведении, сглаженность зубца Т в III, aVF, депрессия сегмента ST V2-V4 1-1,5 мм, подъем сегмента ST в отведении V6 до 1,5 мм, в V5 – менее 1 мм. Отмечается фрагментация QRS во II, III, aVF отведениях (фиг. 10). На ЭКГ при поступлении в приемное отделение – сглаженность сегмента ST I, aVL, aVF, V5-V6, уменьшение депрессии сегмента ST V2-V4 до 0,5 мм, комплекс типа rSr в III отведении, низкоамплитудный зубец Т в III отведении. Сразу после ЧКВ на ЭКГ: синусовый ритм, в сравнении с зарегистрированной в приемном отделении ЭКГ сегмент ST «приподнят» в отведении aVL менее 1 мм, в III и aVF - сглаженность зубца Т, в отведениях V4-V6 - сегмент ST на изолинии, в динамике отмечается отрицательный зубец Т в V4-V6; в V2-V3 cегмент ST на изолинии, депрессии SТ нет. На ЭКГ при выписке (19 сутки) – синусовый ритм, отрицательные зубцы Т I, aVL, V5-V6, сглаженность зубца Т в V4, III, aVF, глубокий зубец Q в III отведении, фрагментация QRS II, III, aVF.
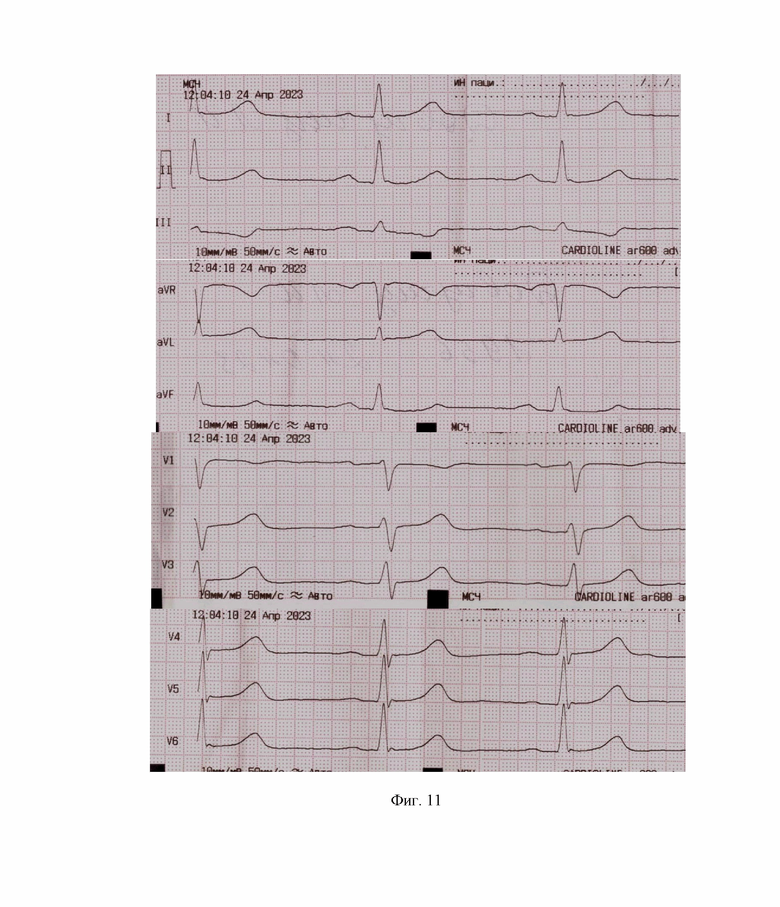
Клинический пример 6. Пациентка Д., 67 лет. Через 7 часов от начала болевого синдрома. Синусовый ритм, высокий и широкий зубец Т в I, aVL отведениях, косонисходящая депрессия сегмента ST – более выражена в III отведении, с отрицательным с. T, менее выражена в aVF, при этом зубец Т положителен (фиг. 11). На ЭКГ в приемном отделении – вышеуказанные изменения менее выражены, а также низкий вольтаж в III отведении. На ЭКГ при выписке – синусовый ритм, горизонтальная ЭОС, без очаговых изменений. В сравнении с первичной ЭКГ – отсутствует депрессия сегмента ST в III и aVF отведениях, в aVL – зубец Т сглажен.
Результаты проведенного анализа:
1) Изменения ЭКГ при острой окклюзия ИМВ не соответствуют ранее описанным критериям ИМ с подъемом сегмента ST (фиг. 1);
2) Изменения ЭКГ при острой окклюзия ИМВ не совпадают также с ранее описанными ЭКГ-феноменами других ветвей ЛКА (фиг. 2).
3) Изменения ЭКГ при острой окклюзия ИМВ включают смещение сегмента ST в I и aVL, но ранее не были описаны (фиг. 3).
1) Для острой окклюзии ИМВ характерными являются ЭКГ-признаки вовлечения нескольких «классических» коронарных бассейнов в динамике у одного пациента в различных сочетаниях, при этом в отдельных отведениях изменения не достигают диагностически значимого уровня. Обязательным является вовлечение отведений: (1) I и aVL (подъем сегмента ST без достижения диагностически значимого уровня по амплитуде и по продолжительности — транзиторный, относительно кратковременный) и (2) III, aVF (ишемические изменения, как прямые, так и реципрокные; в случае прямых - не достигающие диагностически значимого уровня).
2) Сформулированы ЭКГ-критерии острой окклюзии ИМВ (фиг. 12).
Краткое описание чертежей:
Фиг. 1. Критерии диагностически значимых подъема сегмента ST, депрессии сегмента ST и инверсии зубца T [7].
Фиг. 2. ЭКГ-феномены окклюзивного поражения коронарных артерий при отсутствии классических критериев ОКС с подъемом сегмента ST [5, 8-17].
Фиг. 3. ЭКГ-феномены поражения коронарного русла при вовлечении отведений I и aVL [21-25].
Фиг. 4. Серия клинических случаев острой изолированной окклюзии ИМВ: анализ изменений в стандартных 12 отведениях ЭКГ.
Фиг. 5. Клинический случай 1. Пациент Т., 73 года. ЭКГ через 2 часа от начала болевого синдрома.
Фиг. 6. Клинический случай 2. Пациент А., 62 года. ЭКГ через 2 суток от начала болевого синдрома.
Фиг. 7. Клинический случай 3. Пациентка А., 64 лет. ЭКГ через 2,5 часа от начала болевого синдрома.
Фиг. 8. Клинический случай 3, продолжение.
Фиг. 9. Клинический случай 4. Пациент М., 58 лет. ЭКГ через 2 суток от начала болевого синдрома.
Фиг. 10. Клинический случай 5. Пациент Б., 69 лет. ЭКГ через 7 часов от начала болевого синдрома.
Фиг. 11. Клинический случай 6. Пациентка Д., 67 лет. ЭКГ через 7 часов от начала болевого синдрома.
Фиг. 12. Способ диагностики острой окклюзии интермедиарной ветви левой коронарной артерии с помощью стандартной электрокардиограммы в покое
Список литературы:
1. Bhimalli S, Dixit D, Siddibhavi M, Shirol VS. A study of variations in coronary arterial system in cadaveric human heart. World Journal of Science and Technology 2011; 1(5): 30-35.
2. Cademartiri F, La Grutta L, Malagò R, Alberghina F, Meijboom WB, Pugliese F, et al. Prevalence of anatomical variants and coronary anomalies in 543 consecutive patients studied with 64-slice CT coronary angiography. EurRadiol. 2008; 18: 781-791.
3. Saja M. Ali.Angiographical study of ramus intermedius coronary artery in Basrah. The Medical Journal of Basrah University, 2017, Volume 35, Issue 2, Pages 91-96.
4. Koşar P, Ergun E, Öztürk C, Koşar U. Anatomic variations and anomalies of the coronary arteries: 64-slice angiographic appearance. Journal of he Turkish ociety of Radiology 2009; 15(4): 275-283.
5. Byrne RA, Rossello X, Coughlan JJ, Barbato E, Berry C, Chieffo A, Claeys MJ, Dan GA, Dweck MR, Galbraith M, Gilard M, Hinterbuchner L, Jankowska EA, Jüni P, Kimura T, Kunadian V, Leosdottir M, Lorusso R, Pedretti RFE, Rigopoulos AG, Rubini Gimenez M, Thiele H, Vranckx P, Wassmann S, Wenger NK, Ibanez B; ESC Scientific Document Group. 2023 ESC Guidelines for the management of acute coronary syndromes. Eur Heart J. 2023 Oct 12;44(38):3720-3826. doi: 10.1093/eurheartj/ehad191. PMID: 37622654.
6. О. В. Аверков, Д. В. Дупляков, М. Ю. Гиляров и др. Острый инфаркт миокарда с подъемом сегмента ST электрокардиограммы. Клинические рекомендации 2020 // Российский кардиологический журнал. – 2020. – Т. 25, № 11. – С. 251-310. – DOI 10.15829/1560-4071-2020-4103. – EDN KNQWWK.
7. Thygesen K, Alpert JS, Jaffe AS, Chaitman BR, Bax JJ, Morrow DA, White HD; Executive Group on behalf of the Joint European Society of Cardiology (ESC)/American College of Cardiology (ACC)/American Heart Association (AHA)/World Heart Federation (WHF) Task Force for the Universal Definition of Myocardial Infarction. Fourth Universal Definition of Myocardial Infarction (2018). J Am Coll Cardiol. 2018 Oct 30;72(18):2231-2264. doi: 10.1016/j.jacc.2018.08.1038. Epub 2018 Aug 25. PMID: 30153967.
8. Swarath S, Maharaj N, Hall A, Frederick JM, Seecheran R, Seecheran V, Seecheran NA. The South African Flag Sign: An Electrocardiographic Flag for All Coronary Territories? J Investig Med High Impact Case Rep. 2023 Jan-Dec;11:23247096231192861. doi: 10.1177/23247096231192861. PMID: 37559377; PMCID: PMC10413884.
9. Littmann L. South African flag sign: a teaching tool for easier ECG recognition of high lateral infarct. Am J Emerg Med. 2016 Jan;34(1):107-9. doi: 10.1016/j.ajem.2015.10.022. Epub 2015 Oct 23. PMID: 26527178.
10. Miyauchi E, Kuwazuru K, Arikawa R, Tokutake D, Chaen H, Oketani N, Ohishi M. Clinical Features of the Aslanger Pattern to Compensate for the Limitation of ST-Elevation Myocardial Infarction (STEMI) Criteria. Cureus. 2023 Jan 1;15(1):e33227. doi: 10.7759/cureus.33227. PMID: 36601361; PMCID: PMC9805815.
11. Kainat A, Ain NU, Boricha H, Gulzar M, Dueweke EJ. Atypical de Winter Presentation of Critical Left Anterior Descending Coronary Artery Occlusion. Cureus. 2022 May 4;14(5):e24724. doi: 10.7759/cureus.24724. PMID: 35673311; PMCID: PMC9165533.
12. Zhan ZQ, Li Y, Wu LH, Han LH. A de Winter electrocardiographic pattern caused by left main coronary artery occlusion: A case report. J Int Med Res. 2020 May;48(5):300060520927209. doi: 10.1177/0300060520927209. PMID: 32475184; PMCID: PMC7263117.
13. Winter MP, Goliasch G, Bartko P, Siller-Matula J, Ayoub M, Aschauer S, Distelmaier K, Gebhard C, Mashayekhi K, Ferenc M, Hengstenberg C, Toma A. Left Main Coronary Artery Disease and Outcomes after Percutaneous Coronary Intervention for Chronic Total Occlusions. J Clin Med. 2020 Mar 30;9(4):938. doi: 10.3390/jcm9040938. PMID: 32235416; PMCID: PMC7231249.
14. Zhou L, Gong X, Dong T, Cui HH, Chen H, Li H. Wellens' syndrome: incidence, characteristics, and long-term clinical outcomes. BMC Cardiovasc Disord. 2022 Apr 16;22(1):176. doi: 10.1186/s12872-022-02560-6. PMID: 35429969; PMCID: PMC9013025.
15. Okobi OE, Bakare IO, Evbayekha EO, Olawoye A, Umeh CC, Sowemimo A. Wellens Syndrome: A Possible Precursor. Cureus. 2022 Nov 28;14(11):e31963. doi: 10.7759/cureus.31963. PMID: 36582578; PMCID: PMC9795536.
16. Obi MF, Namireddy V, Noel C, O'Brien A, Sharma M, Frederick A, De Gale B, Ubhi M, Cho R. The Comparative Assessment of Wellens' Syndrome With Proximal Left Anterior Descending Artery (LAD) Stenosis Versus Right Coronary Artery (RCA) or Circumflex Coronary Artery Stenosis and Its Prevalence: A Systematic Review. Cureus. 2023 Apr 22;15(4):e37991. doi: 10.7759/cureus.37991. PMID: 37228569; PMCID: PMC10208002.
17. Macherey-Meyer S, Halbach M, Mauri V. Posterior Myocardial Infarction-a Hidden ECG Emergency Presentation. Dtsch Arztebl Int. 2023 Jun 9;120(23):404. doi: 10.3238/arztebl.m2023.0057. PMID: 37561007; PMCID: PMC10433363.
18. Kim TY, Alturk N, Shaikh N, Kelen G, Salazar M, Grodman R. An electrocardiographic algorithm for the prediction of the culprit lesion site in acute anterior myocardial infarction. Clin Cardiol. 1999 Feb;22(2):77-83. doi: 10.1002/clc.4960220205. PMID: 10068843; PMCID: PMC6655669.
19. Singh A, Dwivedi S, Pradhan A, Narain VS, Sethi R, Chandra S, Vishwakarma P, Chaudhary G, Bhandari M, Sharma A. Isolated ST-Elevation Myocardial Infarction Involving Leads I and aVL: Angiographic and Electrocardiographic Correlations from a Tertiary Care Center. Cardiol Res Pract. 2021 Jun 21;2021:7638020. doi: 10.1155/2021/7638020. PMID: 34239726; PMCID: PMC8241503.
20. Sarıçam E, Erdol MA, Bozkurt E, Ilkay E, Cantekin ÖF. New ECG Algorithm for the Prediction of Culprit Vessel in Acute Myocardial Infarction Involving Lateral Part of the Ventricle: Ilkay Classification. Int J Gen Med. 2023 Jun 22;16:2643-2651. doi: 10.2147/IJGM.S416376. PMID: 37377781; PMCID: PMC10292609.
21. Birnbaum Y, Drew BJ. The electrocardiogram in ST elevation acute myocardial infarction: correlation with coronary anatomy and prognosis. Postgrad Med J. 2003 Sep;79(935):490-504. doi: 10.1136/pmj.79.935.490. PMID: 13679544; PMCID: PMC1742828.
22. Parker AB 3rd, Waller BF, Gering LE. Usefulness of the 12-lead electrocardiogram in detection of myocardial infarction: electrocardiographic-anatomic correlations--part I. Clin Cardiol. 1996 Jan;19(1):55-61. doi: 10.1002/clc.4960190111. PMID: 8903539.
23. Vives-Borrás M, Maestro A, García-Hernando V, Jorgensen D, Ferrero-Gregori A, Moustafa AH, Solé-González E, Noriega FJ, Álvarez-García J, Cinca J. Electrocardiographic Distinction of Left Circumflexand Right Coronary Artery Occlusion in PatientsWith Inferior Acute Myocardial Infarction. Am J Cardiol. 2019 Apr 1;123(7):1019-1025. doi: 10.1016/j.amjcard.2018.12.026. Epub 2019 Jan 4. PMID: 30658918.
24. Bayés de Luna A, Wagner G, Birnbaum Y, Nikus K, Fiol M, Gorgels A, Cinca J, Clemmensen PM, Pahlm O, Sclarovsky S, Stern S, Wellens H, Zareba W; International Society for Holter and Noninvasive Electrocardiography. A new terminology for left ventricular walls and location of myocardial infarcts that present Q wave based on the standard of cardiac magnetic resonance imaging: a statement for healthcare professionals from a committee appointed by the International Society for Holter and Noninvasive Electrocardiography. Circulation. 2006 Oct 17;114(16):1755-60. doi: 10.1161/CIRCULATIONAHA.106.624924. PMID: 17043179.
25. Sadanandan S, Hochman JS, Kolodziej A, Criger DA, Ross A, Selvester R, Wagner GS. Clinical and angiographic characteristics of patients with combined anterior and inferior ST-segment elevation on the initial electrocardiogram during acute myocardial infarction. Am Heart J. 2003 Oct;146(4):653-61. doi: 10.1016/S0002-8703(03)00369-7. PMID: 14564319.
26. Fiol M, Carrillo A, Cygankiewicz I, Velasco J, Riera M, Bayés-Genis A, Gómez A, Peral V, Bethencourt A, Goldwasser D, Molina F, Bayés de Luna A. A new electrocardiographic algorithm to locate the occlusion in left anterior descending coronary artery. Clin Cardiol. 2009 Nov;32(11):E1-6. doi: 10.1002/clc.20347. PMID: 19816974; PMCID: PMC6652907.
27. Aslanger EK, Meyers HP, Smith SW. Recognizing electrocardiographically subtle occlusion myocardial infarction and differentiating it from mimics: Ten steps to or away from cath lab. Turk Kardiyol Dern Ars. 2021 Sep;49(6):488-500. doi: 10.5543/tkda.2021.21026. PMID: 34523597.
28. Aslanger EK. Beyond the ST-segment in Occlusion Myocardial Infarction (OMI): Diagnosing the OMI-nous. Turk J Emerg Med. 2022 Sep 28;23(1):1-4. doi: 10.4103/2452-2473.357333. PMID: 36818946; PMCID: PMC9930387.
29. Meyers HP, Bracey A, Lee D, Lichtenheld A, Li WJ, Singer DD, Kane JA, Dodd KW, Meyers KE, Thode HC, Shroff GR, Singer AJ, Smith SW. Comparison of the ST-Elevation Myocardial Infarction (STEMI) vs. NSTEMI and Occlusion MI (OMI) vs. NOMI Paradigms of Acute MI. J Emerg Med. 2021 Mar;60(3):273-284. doi: 10.1016/j.jemermed.2020.10.026. Epub 2020 Dec 9. PMID: 33308915.
30. Pendell Meyers H, Bracey A, Lee D, Lichtenheld A, Li WJ, Singer DD, Rollins Z, Kane JA, Dodd KW, Meyers KE, Shroff GR, Singer AJ, Smith SW. Accuracy of OMI ECG findings versus STEMI criteria for diagnosis of acute coronary occlusion myocardial infarction. Int J Cardiol Heart Vasc. 2021 Apr 12;33:100767. doi: 10.1016/j.ijcha.2021.100767. PMID: 33912650; PMCID: PMC8065286.
31. Aslanger EK, Meyers HP, Smith SW. Time for a new paradigm shift in myocardial infarction. Anatol J Cardiol. 2021 Mar;25(3):156-162. doi: 10.5152/AnatolJCardiol.2021.89304. PMID: 33690129; PMCID: PMC8114732.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ выполнения аспирационной тромбэмболэктомии проводниковым катетером у пациентов с острым коронарным синдромом | 2023 |
|
RU2805970C1 |
| СПОСОБ И СИСТЕМА ДЛЯ ВЫЯВЛЕНИЯ ИШЕМИИ МИОКАРДА С ИСПОЛЬЗОВАНИЕМ ЭКГ | 2016 |
|
RU2719017C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ И ИСХОДА ОСТРОГО КОРОНАРНОГО СИНДРОМА | 2009 |
|
RU2401053C1 |
| Способ лечения больных острым инфарктом миокарда с массивным тромбозом инфаркт-связанной коронарной артерии | 2017 |
|
RU2649572C1 |
| Способ профилактики феномена "no-reflow" при стентировании коронарной артерии у пациентов с острым инфарктом миокарда с подъемом сегмента ST, обусловленным массивным тромбозом | 2021 |
|
RU2786150C1 |
| АВТОМАТИЗИРОВАННАЯ ИДЕНТИФИКАЦИЯ МЕСТОПОЛОЖЕНИЯ ОККЛЮЗИИ В ИНФАРКТ-ЗАВИСИМОЙ КОРОНАРНОЙ АРТЕРИИ | 2011 |
|
RU2598049C2 |
| Способ выполнения ручной тромбаспирации у пациентов с острым коронарным синдромом | 2024 |
|
RU2829204C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ НЕБЛАГОПРИЯТНЫХ КАРДИОВАСКУЛЯРНЫХ ИСХОДОВ ОСТРОГО КОРОНАРНОГО СИНДРОМА В ТЕЧЕНИЕ ГОСПИТАЛЬНОГО ПЕРИОДА У ПАЦИЕНТОВ С ОНКОЛОГИЧЕСКИМИ ЗАБОЛЕВАНИЯМИ | 2020 |
|
RU2751808C1 |
| Способ неинвазивной диагностики стеноза правой коронарной артерии | 2019 |
|
RU2714171C1 |
| Способ определения послеоперационной тактики ведения пациентов с ишемической болезнью сердца на основе выделенных классов ангиографических результатов чрескожного коронарного вмешательства | 2022 |
|
RU2802854C1 |


Изобретение относится к области медицины, а именно к кардиологии. Выполняют диагностирование у пациента с острым коронарным синдромом на электрокардиограмме в покое обязательного сочетания наличия подъема сегмента ST амплитудой менее 0,1 мВ в отведениях I, aVL, ишемических изменений в отведениях III, aVF, как прямых, не достигающих в острый период диагностически значимого уровня, так и реципрокных, и дополнительного сочетания этих признаков по меньшей мере с одним из признаков в виде депрессии сегмента ST в отведениях V1-V3 амплитудой 0,5-1,5 мм, диагностически незначимого подъема сегмента ST в отведениях V4-V6, фрагментации комплекса QRS, нарушения внутрижелудочковой проводимости, изменения локализации подъема сегмента ST на электрокардиограмме в виде подъема сегмента ST в отведениях боковой локализации I, aVL на первичной электрокардиограмме, и подъема сегмента ST в отведениях нижней локализации III, aVF в динамике. Способ позволяет повысить эффективность диагностики, сократить сроки диагностики и определить показания к немедленной в течение 2-х часов коронароангиографии. 12 ил., 6 пр.
Способ диагностики острой окклюзии интермедиарной ветви левой коронарной артерии с помощью электрокардиограммы в покое, включающий диагностирование у пациента с острым коронарным синдромом на электрокардиограмме в покое обязательного сочетания наличия подъема сегмента ST амплитудой менее 0,1 мВ в отведениях I, aVL, ишемических изменений в отведениях III, aVF, как прямых, не достигающих в острый период диагностически значимого уровня, так и реципрокных, и дополнительного сочетания этих признаков по меньшей мере с одним из признаков в виде депрессии сегмента ST в отведениях V1-V3 амплитудой 0,5-1,5 мм, диагностически незначимого подъема сегмента ST в отведениях V4-V6, фрагментации комплекса QRS, нарушения внутрижелудочковой проводимости, изменения локализации подъема сегмента ST на электрокардиограмме в виде подъема сегмента ST в отведениях боковой локализации I, aVL на первичной электрокардиограмме, и подъема сегмента ST в отведениях нижней локализации III, aVF в динамике.
| Серафинович И.А., Корнелюк Д.Г., Электрокардиографическая диагностика локализации критической окклюзии в коронарной артерии часть 1 | |||
| Теоретические основы и диагностические критерии, Журнал Гродненского государственного медицинского университета, 2008, 2 (22), с | |||
| Ударно-долбежная врубовая машина | 1921 |
|
SU115A1 |
| СПОСОБ ДИАГНИСТИКИ Q-ИНФАРКТА МИОКАРДА ПРИ НЕИНВАЗИВНОМ ЭЛЕКТРОКАРДИОГРАФИЧЕСКОМ КАРТИРОВАНИИ ПОВЕРХНОСТИ СЕРДЦА | 2006 |
|
RU2315556C1 |
| Счетчик оборотов с червячной установкой в начальное положение | 1925 |
|
SU12070A1 |
| АВТОМАТИЗИРОВАННАЯ ИДЕНТИФИКАЦИЯ МЕСТОПОЛОЖЕНИЯ ОККЛЮЗИИ В ИНФАРКТ-ЗАВИСИМОЙ КОРОНАРНОЙ АРТЕРИИ | 2011 |
|
RU2598049C2 |
Авторы
Даты
2025-05-05—Публикация
2024-05-02—Подача