Изобретение относится к усоверше ствованной композиции для отверждения непредельных полиэфирных смол, состоящей из перекиси цйклогексанон и растворителя, в частности к жидкой композиции, не расслаивающейся при температурах ниже , которая может найти применение для отверждения не предельных полиэфирных смол. Перекиси цйклогексанона получают путем взаимодействия цйклогексанона с перекисью водорода. В зависимости от услов1(гй реакции, могут быть получены различные соединения, например (бис-1-оксициклогексил)-пероксид, {1-ОКСИ-1 -гидропероксидициклогексил)-пероксид и бис-(1-гидроперокси диклогекс ш)-пероксид Г1 . По причинам безопасности .вышеука занные соединения, плавящиеся при €9-71, 78 и 82-83 С соответственно и являющиеся, следовательно, твердыми ПР.И комнатной температуре, выпускают не в чистом виде, а исключитель но в десенсибилизированной форме. Так, например, известны пастообразные композиции, в которых в качестве десенсибилизирующего агента использу ют сложные эфиры фталевой кислоты, например, дибутил или диметилфталат Однако вышеуказанные перекиси цйклогексанона плохо растворяются в этих десенсибилизирующих агентах и поэто.му не пригодны для получения жидких композиций, содержащих перекись в применяемых на практике количествах Известно использование в качестве растворителя для перекиси дицикло гексанона алкилфосфатов, алкильная группа или группы которых содержат не более 4 атомов углерода, в частности триэтилфосфат. С использованием этого десенсибилизирующего агента .можно получить растворы перекиси 1-ОКСИ-1 -гидропероксидициклогексила в триэтилфосфате, концентрация которых при комнатной температуре равна 50% С23. Известна композиция, представляющая собой смесь перекисей бис-(1-оксициклогексила) и 1-окси-1-гидропероксидициклогексила, растворенных в триэтилфосфате ЗJ. Известен способ получения маслянистой смеси различных перекисей циклогексанона, согласно которому очен-ь чистые кристаллические перекиси дициклогексанона этой маслянистой смеси довольно хорошо растворяются в спиртах, например метаноле, сложных эфирах, например дибутилфталате, кетонах, например циклогексаноне, и углеводородах, например бензоле и толуоле 4. Известна порошковая композиция на основе перекиси циклогексанона и воды, в которую в целях улучшения растворимости ее в органических жид костях вводят поверхностно-активное веществе а также органическую жидкость типа пластификатора с т. вспышки выше l. и т. кип. вьше СЗ.Недостатком известной композиции ; является то/ что композиция циклогексанона плохо растворяется в используемом пластификаторе. Общими недостатками Bcejjизвестных композиций, содержащих перекиси циклогексанона, являются низкая растворимость этих перекисей в используем1лх органических растворителях (не превышающая 50%), что снижает, например, эффективность их применения для отверждения непредельных полиэфирных смол, а также их незначитель- ная стабильность, особенно при температурах ниже . Цель изобретения - повышение концентрации перекисного компонента и повышение стабильности композиции. Поставленная цель достигается тем, что композиция для отверждения непредельных полиэфирных смол, содержащая перекись циклогексанона и растворитель, в качестве перекиси циклогексанона содержит 9-60 мас.% 1,1-дигидропероксициклогексана, а в качестве растворителя 40-9i мас.% воды, одно-или многоатомного спирта, простого эфира спирта, сложного эфира одно-или многоосновной алифатической или ароматической карбоновой кислоты, кетоспирта или их смеси В качестве растворителя используют сложный эфир многоосновной алифатической или ароматической карбоновой кислоты. Композиция обычно дополнительно содержит О,1-10 мас.% 0,2-5 мас.% бис( l-гидpoпepоксициклогексил)-пероксида. , Установлено, что 1,1-дигидропероксициклогексан прекрасно растворяется в несодержащих фосфор растворителях, таких как вода, одно-или многоатомные спирты, простые эфиры спиртов, эфиры одно-или многоосновных алифатических или ароматических каобоновых кислот, кетоспирты и кетоэфиры, или смесях этих растворителей. Установлен также, что при охлаждеНИИ этих растворов в соответствии с изобретением до температуры ниже О с, на узимер до , они не рас лаиваются и из них не выпадают кристал-. лы. В качестве примеров растворите- . лей, которые могут использоваться в композиции в соответствии с изобретением, можно указать следующие соединения: сложные эфиры фталевой кислоты, например диметилфталат, ди-нбутилфталат, диизобутилфталат и бис{-2-этилгексил)-фталат; сложные эфиры адипиновой кислоты, например диметиловый эфир адипиновой кислоты; сложные эфиры уксусной кислоты, например этилацетат, н-бутил-или изо утилацетат,н -амил-нли изоамилацетат; спирты, например н-бутиловый, изобутиловий, этиленгликоль, пропи- ленгликоль, диэтиленгликоль, дипропиленгликоль , гекеиленгликоль, тэтра-и гексаметилёнгликоль; неполные эфиры многоатомных спиртов, например 2-метоксиэтанол, 2-этоксиэтанол-, диэтиленгликоль, дипропиленгликоль и их моноэфиры; кетоспирты, например диацетоновый спирт, и кетоэфиры, например 4-метокси-4-метил-2-пентанон. Могут использоваться также двойные или тройные смеси этих соединений.
В состав предлагаемых композиций могут вводиться также при желании разбавители, загустители (если хотят получить вязкие, пастообразные или тестообразные композиции),, пленкообразующие агенты, например нитроцеллюлозу, стабилизаторы и внутренние красители или. пигменты, которые могут служить индикаторами качества перемешивания при приготовлении гомогенных смесей. К растворам в соответствии с изобретением могут добавляться также и другие перекисные соединения или составы, например Н-О д У1,1-дигидропероксициклогексан получают, используя известный способ C5J, путем обработки циклогексанона избытком коцентрированной перекиси водорода в триэтилфосфате.
Содержание 1,1-дигидропероксициклогексана в предлагаемых композициях может колебаться в широких пределах. Предпочтительными являются композиции, в которых содержится 9-60 мас.% 1,1-дигидропероксициклогексана,| что соответствует содержанию активного Кислорода примерно 2-13 вес.%. Предпочтительно .предлагаемые композиции могут содержать примерно 9-60 мас.% 1Д-дигидропероксициклогексана, до 5 мас.% био-(1-гидропероксициклогексил)-пероксида, 0,1-10 мас.% Н202 и остальное растворитель. .Для определения содержания 1,1-дигидропероксициклогексана в концентрированных растворах (более 50%) требуется со- блюдать особые меры безопасности. Поэтому при определении концентраций этих растворов используют метод, позволяющий установить, что они содержат более 50% основного пероксида.
Пр едлагаемые композиции пригодны для использования в химических реакциях, протекающих под действием свободных радикалов. В комбинации с соединениями, действующими как каталйзаторы, такими как соли переходных метёшлов, например ре, Мг, Со, ванадия. Се и т.д., органические и неорганические кислоты.они особенно подХОДЯ1Ф1 для использования в качестве инициатора отверждения смесей ненасыщенных полиэфирных смол и COOT-
ветствующих мономеров. Под ненасыщенными полиэфирнЕлми смолами в данном случае понимают продукты конденсации смесей малеинового ангидрида и многоосновной алифатической и/или ароматической карбоновой кислоты или их ангидридов, например, фталевого ангидрида и диэтиленгликоля или дипропиленгликоля, или смеси этихДиолов. .
В. качестве примеров подходящих дл сополимеризации мономеров.можно указать стирол, дивинилбензол, ме илмётакрилат, винилацетат, дпаллилфталат, триаллилизоцианурат, N-винилпирролидон, алкилдигликолькарбонат/ тримети л ол пропан, моно-и диаллиловый эфир.
Пример 1 (сравнительный). Смесь из 90 вес.% бис(-1-ОКСИЦИКЛогексил)-пероксида, 0,08 вес.% и примерно 10 вес.% вода (содержание активного кислорода 6,3 вес.%) добавляют в течение часа при перемешивании при к такому количеству диметилтерефталата, чтобы по окончании этого времени оставалось бы значительное количество нерастворенного материала. ,
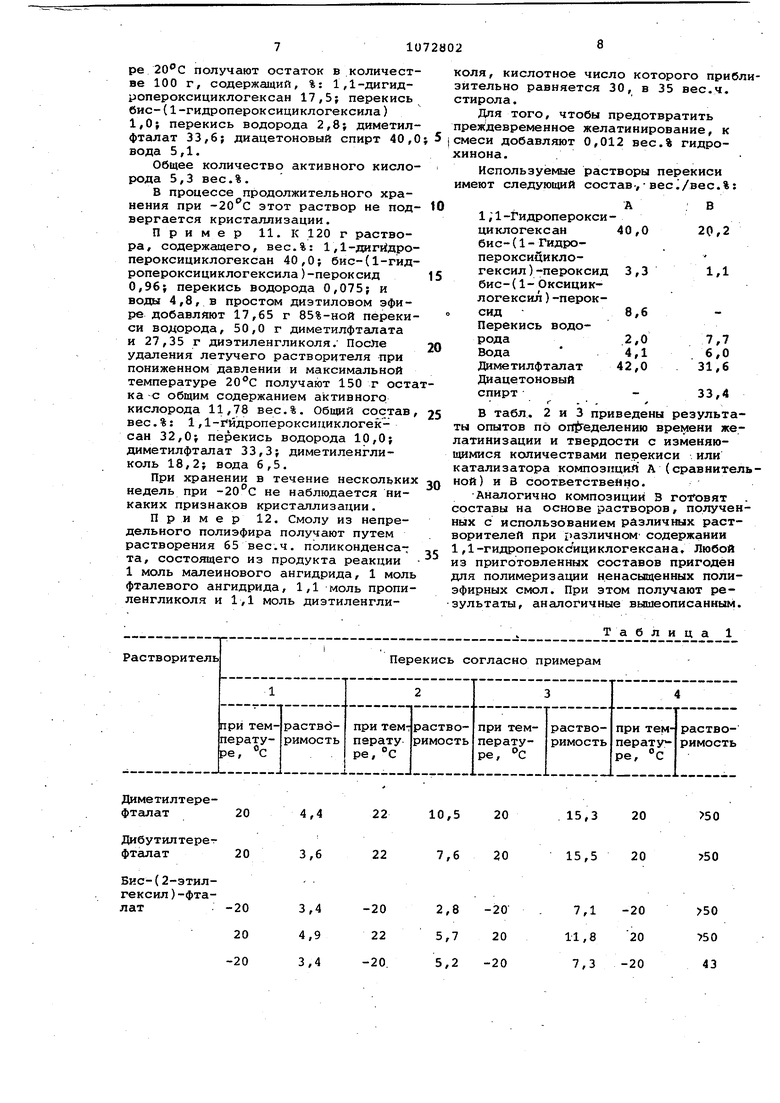
Затем этот нерастворенный ма териал отфильтровывают при 20°С. В полученном насыщенном растворе определяют содержание активного кислорода, по которому определяют растворимость бис-(1-оксициклогексил)-пероксида в диметилфталате при 20с.
Таким же образом определяют растворимость бис-(1-оксициклогексил)пероксида в других растворителях при.+20 и -20°С.
Пример 2 (сравнительный). Смесь из 91 вес.% (1-гидропероксиl -оксидициклогексил)-пероксида, 0,04 вес.% Н2О2 и около 9 вес.% в.оды (содержание активирго кислорода 11,85 вес.%) добавляют при интенсивном перемешивании в течение часа при 22с к такому количеству диметилфталата, чтобы по окончании этого времени оставалось бы значительное количество нерастворенного материала.
Затем этот нерастворенный материал отфильтровывают при 22с. В полученном таким образом насыщенном растворе определяют содержание, активного кислорода, по которому рассчитывают растворимость (1-гидроперокси-1 оксидициклогексил)-пероксида в диметилфталате при 22°С.
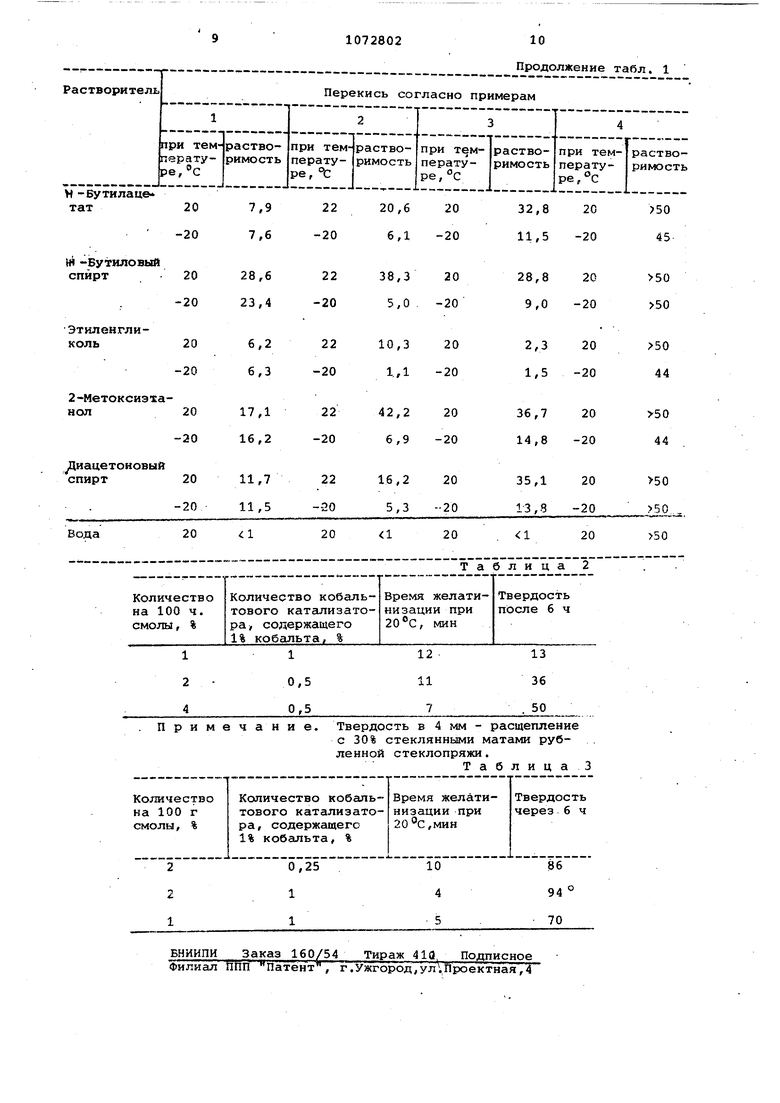
Подобным образом определяют растворимость (1-гидроперокси-1 -оксидициклогексил ) -пероксида в других растворителях при +22 и .Пример 3 (сравнительный). Смесь из 97 вес.% бис-(1-гидроперокс;ициклогексил) -пероксида, О /06. вес.% , 1,5 вес.% (1-гидроперокси-1 -оксидициклогексил)-пероксида 0,5 вес.%- циклического димера циклогексанонпероксида и менее 1 вес.% воды (содержание активного кислорода 18,0 вес.%) добавляют при интенсивном перемешивании в течение часа при к такому количеству диметил фталата, чтобы по окончании этого времени оставалось бы значительное количество нерастворенного материала Затем .этот нерастворенный материал отфильтровывают при . В полученном насыщенном растворе определяют содержание активного кислорода, по которому рассчитывают растворимость бис-(1-гидропероксициклогексила)-пероксида в диметилфталате при 20 с. Подобным образом определяют растворнмость бис-(1-гидропероксициклогексил)-пероксида в других растворителях при +20 и -20°С. Пример 4. 100 г 43%-ного (вес;.) раствора 1,1-дигидропероксициклогексана вдиэтйловом эфире смеиИ вают до получения гомогенной смеси с примерно 40 г диметилфталата. Эфир отгоняют из смеси при пониженном дав лении при температуре не выше 20с. Полз -ченный в результате этого раствор 1Д-дигидропероксициклогексана в диметилфталате содержит примерно 50 вес.% этой перекиси. После хранения в течение нескольких недель при 20С1 из раствора не выпадают кристаллы. Подобным образом определяют растворимость этой перекиси в других растворителях при +20 и -20с. Результаты полученные в примерах 1-4 приведены в табл. 1. Пример 5. К120г раствора 40,0 вес.% 1,1-дигидропероксициклогексана, 0,96 вес.% бис-(1-гидроперокск:1 ;иклогексил )-пероксида, О ,075 вес.% и 4,8 вес.% воды в диэтиловом эфире добавляют 50,7 г н-бутилс.цетата. После этого диэтиловый эфир отгоняют при пониженном давлеНИИ. Выход составляет 105,7 г растBopci перекиси в н-бутилацетате, соде жаще:го, вес.%: активный кислород 10 ,С; 1,1-дигидропероксициклогексан 45,4-} бис- (1-гидропероксициклогексил )-пероксид 1,1; перекись водорода 0,1} циклогексанон 0,3; вода 5,1 и н-бутилацетат 48. При длительном хранении раствора при О и -20°С не наблюдается рассла вание и выпадение из него кристалло К 30 г этого раствора добавляют 15,4 г н-бутилацетата и 45,4 г 30%ного раствора (вес.%) нитроцеллюлозы в и-бутилацетате. В результате получают прозрачную жидкость с соде жанием активного кислорода 3,2 вес.%, прозрачность которого, а также содержание активного кислорода не изменились после 8-недельного хранения при 20с. Пример 6. Осуществляют согласно примеру 4, только вместо 40 добавляют г диметилфталата, получая раствор, содержащий 9 вес.% 1,1-дигидропероксициклогексана. После хранения в течение нескольких недель при из раствора не выпадают кристаллы.. Пример 7i Осуществляют согласно примеру 5, заменяя бутилацетат тем же количеством следующих растворителей: простой моноэтиловый эфир диэтиленгликоля, простой моноэтиловый эфир пропиленгликоля, 2-этил . гексанол, З-метилпентанол-2, метилвале ат, амилацетат. Со всеми этими растворителями получают растворы, содержащие более используемого пероксида. При длительном хранении полученных растворов при О и -20°С не наблюдается расслаивание и выпадение из них кристаллов. Пример 8. К 120 г раствора 40 вес.% 1,1-дигидропероксициклогексана, 0,96 вес.% бис-(1-гидропероксициклогексил)-пероксида, 0,075 вес.% HgO и 4,8,вес.% воды в простом диэтиловом эфире добавляют 383,6 г Н-бутилацетата. Затем простой эфир отгоняют при пониженном давлении. Выход составляет 438,6 г .раствора, состоящего, %: 1,1-дигидропероксициклогексан 9,2; бис-(1-гидроперокеициклогексил)-пероксид 0,22; перекись .водорода 0,02; циклогексанон 0,6; вода 1,03; бутилацетат 89,47. После 4-недельной выдержки при -20°С никакой кристаллизации не наблюдают. Пример 9. Готовят состав, содержащий, %: дигидропероксициклогексан 37,1; бис-(1-гидропероксициклогексил ) -пероксид 4,9; перекись водорода 2,4; вода 4,2; циклогексанон 1,9; диизобутилфталат 49,5, смешением, г: 70%-ной 70,75; диизобутилфталата 72,5. 2н, 0,56 мл; циклогексанона 57,3. Температура реакции 25°С. После завершения реакции состав нейтрализуют и сушат. После длительной выдержки при -20с никакой кристаллизации не наблюдают. Пример 10. К 42,8 г 43%-ного раствора 1,1-дигидрапероксицик- логексана в простом диэтиловом эфире добавляют 4,0 г 70%-ной 33,6 г диметилфтсшата и 40,0 г диаце тонового спирта. После удаления эфира путем перегонки при поннж нном давдавлении при максимальной температуре получают остаток в количест ве 100 г, содержащий, %: 1,1-дигидропероксициклогексан 17,5; перекись бис-(1-гидропероксициклогексила) 1,0; перекись водорода 2,8; диметил фталат 33,6; диацетоновый спирт 40, вода 5,1. Общее количество активного кисло рода 5,3 вес.%. В процессе продолжительного хранения при этот раствор не под вергается кристаллизации. Пример 11. К 120 г раствора, содержащего, вес.%: 1,1-дигйдро пероксициклогексан 40,0; бис-(1-гид ропероксициклогексила)-пероксид 0,96; перекись водорода 0,075; и воды 4,8, в простом диэтиловом эфире добавляют 17,65 г 85%-ной переки си водорода, 50,0 г диметилфталата и 27,35 г диэтиленгликоля. После удаления летучего растворителя при пониженном давлении и максимальной температуре получают 150 г ост ка с общим содержанием активного кислорода 11,78 вес.%. Общий состав вес.%: 1,1-гйдропероксиииклогексан 32,0; перекись водорода 10,0; диметилфталат 33,3; диметилен 7ликоль 18,2; вода 6,5. При хранении в течение нескольки недель при не наблюдается никаких признаков кристаллизации. Пример 12. Смолу из непредельного полиэфира получают путем растворения 65 вес.ч. поликонденсата, состоящего из продукта реакции 1 моль малеинового ангидрида, 1 мол фталевого ангидрида, 1,1 моль пропи ленгликоля и 1,1 моль диэтиленгликоля, кислотное число которого приблизительно равняется 30, в 35 вес.ч. стирола. Для того, чтобы предотвратить преждевременное желатинирование, к смеси добавляют 0,012 вес.% гидрохинона. Используемые растворы перекиси имеют следующий состав-, .%: 1;1-Гидропероксициклогексан 40,0 20,2 бис- (1 - Гидропероксициклогексил)-пероксид 3,3 1,1 бис-( 1-Оксициклогексил)-пероксид 8,6 Перекись водорода .2,0 7,7 Вода 4,1 ,6,0 Диметилфталат 42,0 31,6 Диацетоновый спирт - 33,4 f . , f В табл. 2 и 3 приведены результаты опытов по оп геделению желатинизации и твердости с изменяювдамися количествами перекиси или катализатора композиций А (сравнительной) и В соответственно. Аналогично композиций В готовят составы на основе растворов, полученных с использованием различных растворителей при различном содержании 1,1-гидроперокСицикЛогексана Любой из приготовленных составов пригоден для полимеризации ненасыщенных полиэфирных смол. При этом получают результаты, аналогичные вышеописанным. Таблица


1. КОМПОЗИЦИЯ ДЛЯ ОТВЕРЖ ДЁН11Я НЕПРЕДЕЛЬНЫХ ПОЛИЭФИРНЫХ СМОЛ, содержащая перекись цйкдогексанона и растворитель, о тличающаяс я тем, что, с целью повг.лиения ко нцентрации перекисного компонента .и повышения стабильности композиции, в качестве перекиси циклогексанона она содержит 9-60 мас.% 1,1-дигидропероксициклогексана,, а в качестве раствор11теля 40-91 мас.% воды, одноили многоатомного спирта, простого эфира спирта, сложного эфира одноили многоосновной .алифатической или ароматической карбоновсэй кисло ы, кетоспирта или их смеси. О)
20 20
4,4 3,6
3,4
-20
20 4,9 3,4
-20
50
20 20
10,520
2 22
15,3 50
15,5
50
7,1 -20
2,8-20
11,8 20
50
43 5,2-20
7,3 -20
Авторы
Даты
1984-02-07—Публикация
1978-07-03—Подача