т мин
ii.f Изобретение относится к биологи и медицине и предназначено для определения антиоксидантной активности веществ. Известен способ определения анти оксидантной активности химических соединений хемилюминесцентным способом, заключающимся в том, что в окислительной ячейке с термостатиру мой рубашкой проводят окисление этилбензола при 37°С в присутствии инициатора - дициклогексилпероксиди карбоната, для усиления квантового выхода хемилюминесценции добавляют Э,10-дибромантрацен в концентрации м. Выделенные экстракцией смесью хлороформ фир (1:1) липиды вводят в ячейку, что способствует снижению интенсивности хемилюминесценции. Действующую концентрацию антиоксиданта определяют по соотношению площадей под кривой хемилюминесценции в присутствии и в отсут ствие ингибитора tl. Недостатками способа являются не высокая точность и возможность регистрации антиоксидантной активност только тех препаратов, которые обла дают антиоксидантным действием. Наиболее близким к изобретению по технической сущности и достигае.мому результату является способ опр деления антиоксидантной активности еществ на основе олеи новокислых Э13итрограмм, заключающийся в том,,, что в кювету , содержащую взвесь эритр цитов стандартной концентрации, вводят испытуемое вещество и раствор оки,с;1енного олеата, продукты окисления олеата вызывают повреждение мембраны эритроцитов с последующим гемолизом, что регистрируют фотометрически, при наличии антиоксидант ной активности интенсивность гемоли за уменьшается, что приводит к увел чению в сравнении с контролем времени 50% гемолиза Сз. Недостатком способа является то что антиоксидантную активность определяют в экспериментах in vitr которую может проявлять не само вещество, а продукты его метаболизм или активация антиоксидантных сиетем организма. Цель изобретения - повышение точности измерений. Поставленная цель достигается тем, что согласно способу определен антиоксидантной активности веществ включа-ющему взятие крови, введение испытуемого вещества и раствора оки ленного олеата с последующей регист рацией эритрограмм,испытуемое вещест во вводят перитонеапьно животному и антиоксидантную активность определяют по соотношению между двумя стадиями гемолиза эритроцитов - окисленным и неокисленным олеатом. , На фиг. 1 представлена эритрограмма, полученная при гемолизе окисленным олеатом натрия на кровь 1 онтрольных животных млшей) , которым перито- неально вводят 0,9%-ный раствор NaCt; на фиг. 2 - эритрограмма,полученная при гемолизе неокисленным олеатом натрия на кровь мышей, которым перитонеапьно вводят тот же раствор соли; на фиг. 3 - эритрограмма, полученная при гемолизе окисленным олеатом натрия на кровь л«шей, которым перитонеально вводят феназан натрия. Пример. Олеат натрия растворяют в изоосмотическом фосфатном буфере рН 7,4 в концентрации 12 мг% в течение 30 мин при 20°С. Окисление олеата натрия проводят при 90°С, пропуская воздух через раствор. В процессе окисления отбирают пробы для определения степени окисления методом эритрогрс1мм.Окисление оста-навливают при равенстве двух стадий гемолиза - быстрой и медленной. Подопытному животному перитонеально вводят феназан натрия (натриевая соль-4-окси-З,5-дитретбутил-фенилпропионовой кислоты) из расчета 100 мг/кг живого веса и через 30 мин из хвостовой вены берут кровь для анализа (экспериментально установлено, что оптимальное время проявления препарата в крови 30 мин). Контрольным животным перитонеально вводят 0,9%-ный раствор NaC2. Эритрограмму записывают в следующих условиях: 2 МП взвеси.эритроцитов в физиологическом растворе (1600 шт/мм) смешивают с 2 мл раствора окисленного олеата натрия в термостатированной ячейке при 24°С. Гемолиз непрерывно регистрируют по изменению оптической плотности взвеси эритроцитов при длине волны 630 нм. Графический материал, отражающий опыты с феназаном натрия, изображен в следукяцих координатах: ось абсцисс соответствует времени лизиса в минутах; ось ординат - процент эритроцитов в опытной кювете. За 100% принимают содержание эритроцитов, соответствующее значению, устанавливающемуся после смешивания всех компонентов в опытной кювете (процент эр1Лроцитов, лизированных в фазе быстрого и медленного гемолиза в сумме), В условиях эксперимента лизис заканчивается к 3 мин. Результатом опыта является двухступенчатая эритрограмма с соотношением между ступенями быстрого (1) и медленного (,П) гемолиза: для гемолиза окисленным олеатом натрия эритроцитов контрольных животных, которым перитонеапьно вводят 0,9%ный раствор хлористого натрия, соот ношение стадий ,83 (фиг,1); для гемолиза неокисленным олеатом натрия эритроцитов контрольных животных, которьм перитонеашьно вводя 0,9%-ный раствор хлористого натр.чя, соотношение ступеней ,3 (фиг.2 для гемолиза окисленным олеатом натрия эритроцитов животных, которы перитонеально вводят раствор фенази на натрия из расчета 100 мг/кг живо го веса, соотношение ступеней 1:11 0,17 (фиг.З), Таким образом, из результатов эксперимента следует, что эритрограмки, полученные с помощью окисленного олеата наТрия при введении животному феназана натрия, приобретают вид эритрбграммм, полученных с помощью неокисленного олеата натрия при введении животному физиологическогр раствора, что указывает на згицитное действие препарата от продуктов окисления олеата натрия, т.е.о его антиоксидантном эффекте. Экспериментальные результаты по тестированию феназана натрия способом-прототипом с концентрацией в кювете до 10 г/л (на 2 порядка превьнпает испытываемую) не выявили антиоксидантной активности. Для сравнения влияния химических соединений на данные эритрограммы, полученные при действии окисленного олеата натрия на эритроциты мышей непосредственно в процессе лизиса и недоокисленного олеата натрия опоередственно - после введения препара животным, проведены эксперименты, кроме феназана натрия (препарат А), с 1-0-(1-силатранил)-2,3; 4,5-ди-О-изопропилиден-р-В-фруктопиранозой(препарат В), дийодметилатом ди-р-диметиламино-этилового эфира 2,7-диэтило:стандиловой-1,8-кислоты (препарат С) и винилоксиэтиламинной солью 2,4-дихлорфеноксиуксусной кис лоты (препарат D). Результаты приведены в табл. 1 и 2. В табл 1 показаны результаты дв экспериментов. В первом узучают не посредственно действие препаратов на соотношение процентов эритроцито лизированных в результате, быстрого и медленного лизисов при проведении опытов путем смешивания в экспериме тальной кювете 2 мл суспензии эритр цитов, 1 мл 40 мМ раствора испытыва мого вещества и 1 мл 12 мг%-ного раствора недоокисленного с1леата натрия, приготовленных на физраство ре (суспензии эритроцитов и раствора испытываемого вещества) и па нат рий-фосфатном буфере с рН 7,4 (для олеата натрия). Конечная концентрац препаратов 10 мМ, Во втором эксперименте исследуют опосредованное действие изучаемых препаратов путем введения их животным и последующей регистрацией олеиновокислых эритрограмм. Разработанный способ тестирования химических соединений на антиоксидантную активность позволяет повысить точность измерений и получить возможность определять антиоксидантную активность препаратов не только при прямом действии, но и опосредованно, в частности при действии их метаболитов. Представленные данные указывают на отсутствие достоверных изменений соотношений фаз гемолиза при непосредственном действии. Для препаратов Вид получено значительное ускорение быстрого гемолиза, причем для препарата В все эритроциты лизировали в фазу быстрого лизиса, а для препарата Д - более 80% эритроцитов, в то время как в контроле только 36%. Пол ченные результаты указывают на возможное альтерирующее действие отмеченных препаратов на эритроциты, но не об их антиоксидантной активности. При опосредственном действии наблюдается статистически достоверное уменьшение соотношения частей эритроцитов, лизированных при двух стадиях гемолиза от 0,59+0,04 для препарата В до 0.17+0,04 для препаратов А и Д.Испчтанные концентрации для экспериментов с опосредованным действием в 15-30 раз меньше, чем для эксперимента с непосредственным действием. Полученное уменьшение соотношения частей эритроцитов, лизированных в фазах быстрого и медленного гемолиза в экспериментах с ОпосредоБанным, действием вплоть до соотношения, наблюдаемого для лизиса неокисленным олеатом (0,12+ +0,02), свидетельствует о защитном действии на эритроциты продуктов метаболизма изучаемых препаратов от окисленного олеата, т.е. об их антиоксидантном действии. В табл.2 представлены результаты двух экспериментов, полученных при непосредственном и опосредованном действии изучае1)х препаратов на время 50%-ного лизиса эритроцитов кьшей под влиянием окисленного олеата натрия. Представленные результаты указывают на отсутствие антиоксидантного эффекта изучаемых препаратов ПРИ проведении анализа путем использования способа-прототипа. Препараты В и Д в концентргщиях 10 мМ оказали альтерирующее воздействие на эритроциты. В то же время при испытанных концентрациях ни один из изучаемых препаратов не выявил достоверного увеличения времени 50%-ного лизиса.
Сравнение данных табл. 1 и 2 покаэ«лвает, что проведение анализа по предлагаемому способу дает уйеличение точности по сравнению со способом-прототипом и, в частности, позволяет регистрировать антиоксидантную активность метаболитов.
Таблица



| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕЧЕБНОЕ СРЕДСТВО ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ХРОНИЧЕСКИХ ЗАБОЛЕВАНИЙ ПЕЧЕНИ | 2012 |
|
RU2526172C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИГИПОКСИЧЕСКОЙ И АНТИОКСИДАНТНОЙ АКТИВНОСТЬЮ | 2001 |
|
RU2191592C1 |
| СПОСОБ ПРОФИЛАКТИКИ ПОВРЕЖДЕНИЯ БИОЛОГИЧЕСКИХ МЕМБРАН | 2013 |
|
RU2549449C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АНТИОКИСЛИТЕЛЬНОЙ АКТИВНОСТИ АНТИОКСИДАНТНЫХ ПРЕПАРАТОВ | 1999 |
|
RU2160898C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ФУНКЦИОНАЛЬНОГО СОСТОЯНИЯ ОРГАНИЗМА ПО СТЕПЕНИ РЕЗИСТЕНТНОСТИ КРОВИ К КИСЛОТНОМУ ГЕМОЛИЗУ | 2000 |
|
RU2179315C1 |
| МЕМБРАНОПРОТЕКТОРНОЕ СРЕДСТВО | 2013 |
|
RU2538803C1 |
| Средство, обладающее антиагрегантной, цитопротекторной и антиоксидантной активностью | 2018 |
|
RU2694061C1 |
| СПОСОБ ПОВЫШЕНИЯ УСТОЙЧИВОСТИ К ГЕМОЛИЗУ ЭРИТРОЦИТОВ И ВОССТАНОВЛЕНИЯ ИХ ПОВРЕЖДЕННОЙ ФОРМЫ | 1998 |
|
RU2162698C2 |
| ЭНЕРГЕТИЧЕСКИЙ БЕЗАЛКОГОЛЬНЫЙ НАПИТОК | 2010 |
|
RU2423887C1 |
| ДИГИДРОБРОМИД 2-(3,4-ДИГИДРОКСИФЕНИЛ)-9-ДИЭТИЛАМИНОЭТИЛИМИДАЗО[1,2-a] БЕНЗИМИДАЗОЛА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2008 |
|
RU2391979C2 |

СПОСОБ ОПРЕДЕЛЕНИЯ АНТИ- I ОКСИДАНТНОЙ АКТИВНОСТИ ВЕЩЕСТВ, включакяций взятие крови, введение испытуемого ветдества и раствора окисленного олеата с последующей регистрацией эритрограмм, отличающийся тем, что, с целью повышения точности измерений, испытуемое вещество вводят перитонеашьно животному и антиоксидантную активность определяют по соотношению между двумя стадиями гемолиза эритроцитов-) окисленным и неокисленным олеатом.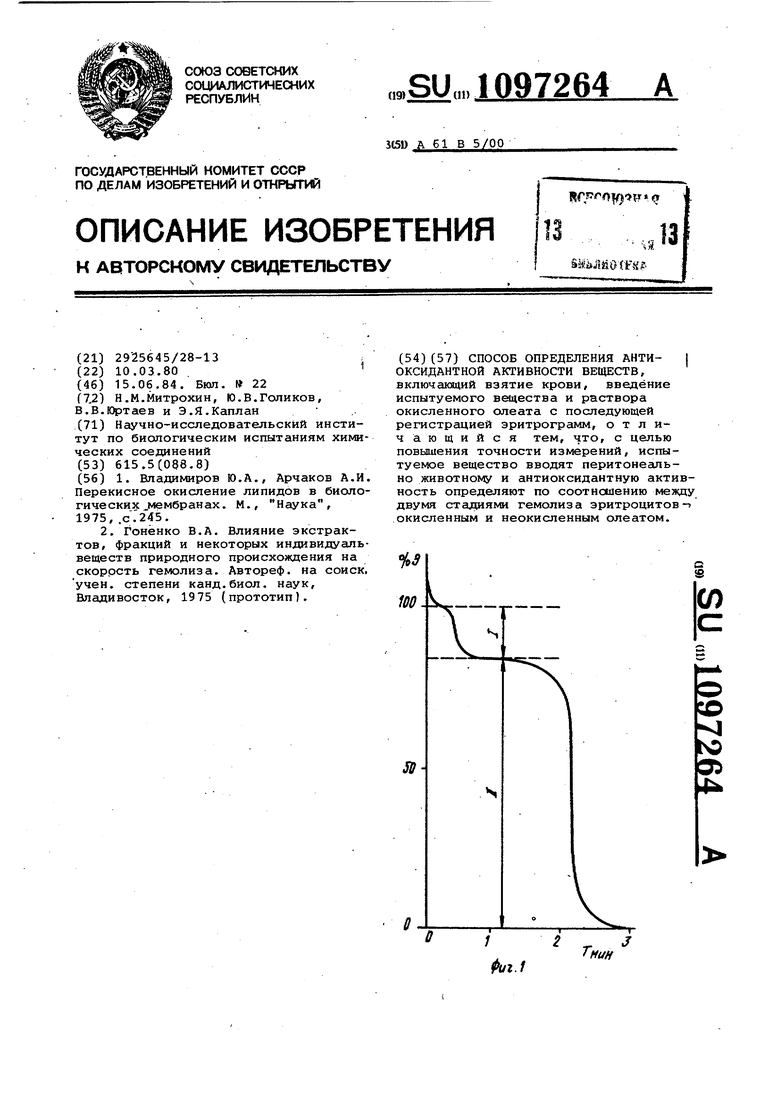
достоверное отличие (р/0,05).
Таблица 2
Продолжение табл. 2
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Владимиров Ю.А., Арчаков А.И Перекисное окисление липидов в биоло гических мембранах | |||
| М., Наука, 1975,.с.245 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Гонёнко В.А | |||
| Влияние экстрактов, фракций и некоторых индивидуаль веществ природного происхождения на скоррсть гемолиза | |||
| Автореф | |||
| на соиск учен, степени канд.биол | |||
| наук, Владивосток, 1975 (прототип). | |||
Авторы
Даты
1984-06-15—Публикация
1980-03-10—Подача