О СП
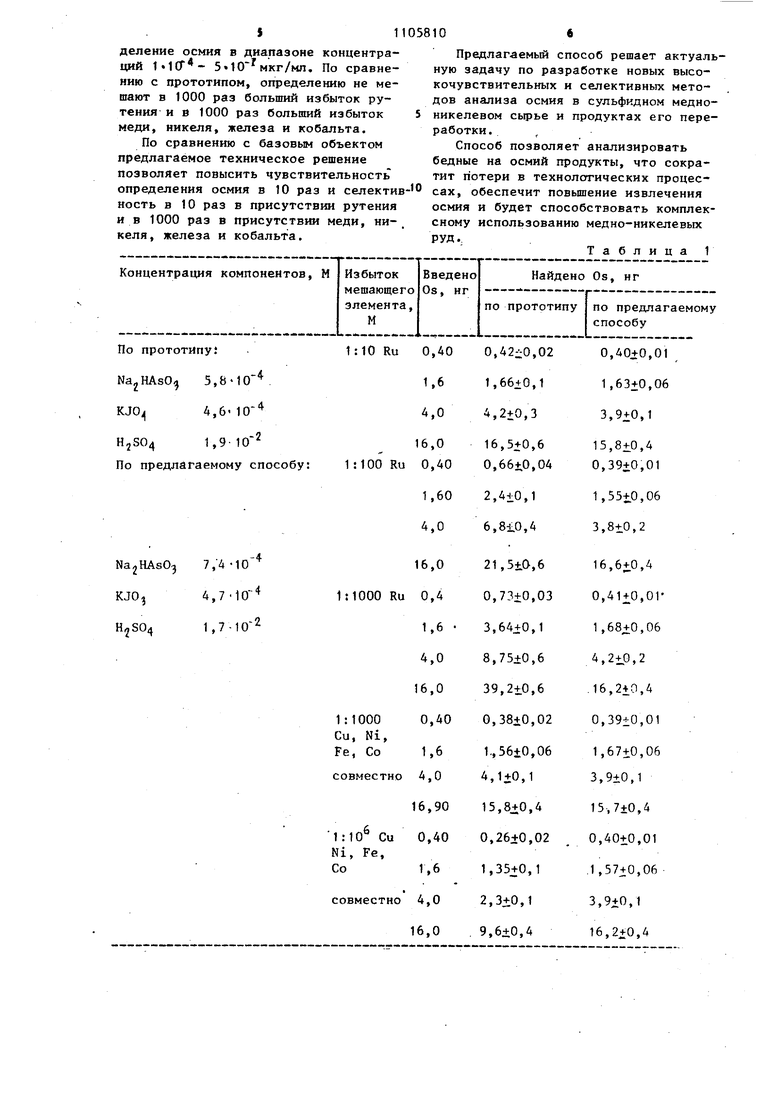
00 Изобретение относится к аналитической химии платиновых металлов и может быть использовано для анали за объектов, содержащих следы осмия и большие количества других элемент например рутения, меди, никеля, жел за, кобальта. Известен способ определения осми основанный на индикаторной реакции между арсенитом натрия и броматом к ЛИЯ lj , Недостатком известного .способа является низкая чувствительность: предел обнаружения составляет 510°мкг/мл. Определение можно проводить в присутствии не более чем 1000-кратных количеств Си, Ni, Fe, Со и 100-кратных количеств рутения, тогда как в природных и промьшшенкых объектах рутений сопутствует осмию в гораздо более высоких избытках. Наиболее близким по технической сущности и достигаемому результату к предлагаемому является способ опре деления осмия по его каталитическому действию в индикаторной окислительно восстановительной реакции между арсе нитом натрия и периодатом калия 2j Эта реакция протекает с индукционным периодом, длительность .которого зава сит от концентрации катализатора - . осмия. Для измерения индукционного периода применяют амперометр)(1ческий метод. Предел -обнаружения составляет 510 мкг/мл. Определение осмия проводят в присутствии Си, Ni, Fe, Со до 1000-кратного избытка и рутения до 10-кратного избытка. Недостатком известного способа является низкая селективность определения осмия в присутствии таких элементов, как рутений, медь, никель железо, кобальт. Цель изобретения - повышение селективности определения осмия при со хранении высокой чувствительности способа. Поставленная цель достигается тем что согласно способу определения осмия, основанному на его каталитическом действии в окислительно-восстано вительной реакции между арсенитом натрия и галогенатом калия в присутствии серной кислоты, в качестве галогената калия используют йодат каЛИЯ и окислительно-восстановительную реакцию проводят при следующих концентрациях компонентов, М: Йодат калия (4,65-4,74)-10 Арсенит натрия (7,35-7,44)- 10 Серная кислота (1,65-1,74)10. Введение иодата калия определенной концентрации вместо периодата калия позволяет исключить каталитическое действие рутения в индикаторной реакции при содержании, рутения в 1000кратном и менее избытке по отношению к осмию. Это объясняется тем, что действие катализатора (осмия) в реакции окисления арсенита натрия йодатом калия протекает по одному из основных механизмов каталитического действия комплексных соединений переходных металлов в гомогенных каталитических реакциях - по Переменному окислению - восстановлению катализатора. Для этого необходимо, чтобы катализатор (осмий) являлся окислителем по отношению к арсениту натрия и восстановителем - к йодату калия, что возможно благодаря существованию соединений осмия с различными степенями окисления и легкости их перехода из одной формы в другую. Условиями для этого являются определенные реальные окислительно-восстановительные потенциалы всех участвующих в реакции редокс-систем. Величины этих потенциалов находятся в зависимости от соотношения концентраций компонентов реакции: иодата KJO, арсенита , ионов водорода и влияют на проявление каталитического действия осмия в данной реакции. Способ осуществляют следующим образом. В сосуд-смеситель вносят: в 1-й отросток - раствор арсенита натрия Na2HAsO в серной кислоте; во 2-й отросток раствор иодата калия KJO и анализируемый раствор осмия; в 3-й отросток - воду. Растворы, общий объем которых составляет 50 мл, перемешивают. Концентрации компонентов индикаторной реакции в смеси составляют (4,65-4, 74) иодата калия, (7,35-7,44) арсенита натрия, (1,65-1,74) 10 М серной кислоты. Далее раствор помещают в электролизер и по истечении .1 мин записывают кинетическую кривую амперометрическим методом по диффузионному току восстановления йода, вьщеляющегося в ходе реакции. Для записи кинетичесих кривых используют полярограф LP-7 и электролитическую ячейку с платиновым вращающимся микроэлектродом. Потенциал электрода +0,4 В (нас.к.э.). Кинетическая кривая характеризуется индукционным, периодом, обратная величина которого рропорциональна концентрации осмия. Концент-рацию осмия определяют методом калибровочного графика, которы строят в координатах обратная длительность индукционного периода концентрация осмия. Для построения градуиррвочного графика во 2-й отросток сосуда-смесителя помещают 0,5 мл; 1,0 мл; 3,0 на; 5,0 мл ЫОМ раствора осмия и записывают кинетические кривые. Результаты определения осмия в различных растворах предлагаемым и известным методом приведены в табл.1 в которой представлена также селективность определения осмия в присутствии рутения, а также меди, никеля железа, кобальта. Из данных таОл. 1 следует, ;что результаты анализа растворов, содержащих 10-кратный и менее избыток рутения и 1000-кратный и менее избыток меди, никеля, железа, кобальта, полученные по предлагаемому способу и по прототипу, имеют достаточно хорошую селективность, а следовательно, точность, правильность, воспроиз водимость. Но результаты анализа растворов, содержащих 100- и 1000кратный избыток рутения и 10 -кратный избыток меди, никеля, железа, кобальта, полученные по прототипу, содержат систематическую ошибку в сторону завышение для рутения и зани жения для меди, :г;келя-, железа, кобальта результатов по содержанию осмия, в то время как результаты, полу ченные предлагаемым способом, имеют по-прежнему достаточно хорошую селек тивность, точность и воспроизводимость. Обоснование средних и граничных значений концентраций компонентов, участвующих в индикаторной окислител но-восстановительной реакции определения осмия, представлено в табл. 2 Из табл. 2 видно, что при указанных граничных значениях концентраций реагентов чувствительность и селективность предлагаемого способа определения осмия сохраняются на уровне достигаемом при средних значениях концентраций реагентов. При концентрациях йодата калия, арсенита натрия и серной кислоты менее 4,65-10 ; 7,33«10 и 1,65Чб М соответственно каталитическая активность -осмия мала. При концентрациях йодата калия и арсенита натрия более 4, и 7, в присутствии серной кислоты в количестве, превышающем 1,, индукционный период некаталитической реакции уменьшается, что ведет к значительному снижению чувствительности способа определения осмия. Ухудшается также селективность определения осмия, так как каталитическое действие рутения проявляется при меньшем его избытке при увеличении концентрации окислителя в индикаторной реакции. Таким образом, интервалы значений концентраций реагентов в индикаторной каталитической реакции определения осмия составляют, М: , (7,35-7,44) 10(4,65-4,74) (1,65-1,74) Пример. Для опредедения осмия в сосуд-смеситель вносят растворы: в первый отросток - 18,5 мл 210 М раствора арсеннта натрия в 0,05 М H2S04; во второйотросток 2,0 мл 1 раствора йодата калия и анализируемьй раствор осмия; в третий отросток - вода до общего объема 50 мл, где концентрация реагентов составляют; 7, ; 4,7ПО-м KJO и 1,7.10-2 М . Введено 0,4 нг осмия. Избыток сопутствующих элементов составляет 10 для Си, Ni, Fe и Со и 10 для Ru. По КИ7 нетической зависимости, измеренной амперометрическим методом, находят индукционный период реакции и далее по калибровочной кривой - концентрацию осмия, которая составляет 0,40 + ±0,01 нг. Предел обнаружения осмия в данной реакции 5 мкг/мл. Из представленных данных следует, что предлагаемый способ определения осмия обладает высокой селективностью: определению не мешают 1000- ., кратный и менее избыток рутения и 10кратный и менее избыток меди, никеля, железа, кобальта при сохранении вы- сокой чувствительности способа (510 мкг/мл осмия). Возможно определение осмия в диапазоне концентраций ( 5 10 мкг/ип. По сравнению с прототипом, определению не мешают в 1000 раз больший избыток рутения- и в 1000 раз больший избыток меди, никеля, железа и кобальта. По сравнению с базовым объектом предлагаемое техническое решение позволяет повысить чувствительность определения осмия в 10 раз и селекти ность в 10 раз в присутствии рутения ив 1000 раз в присутствии меди, никеля, железа и кобальта. Предлагаемый способ решает актуальную задачу по разработке новых высокочувствительных и селективных методов анализа осмия в сульфидном медноникелевом сырье и продуктах его переработки. Способ позволяет анализировать бедные на осмий продукты, что сократит потери в технологических процессах, обеспечит повьшгение извлечения осмия и будет способствовать комплексному использованию медно-никелевых Таблица 1


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ ОСМИЯ | 1991 |
|
RU2050541C1 |
| Способ определения осмия | 1978 |
|
SU701946A1 |
| СПОСОБ КИНЕТИЧЕСКОГО ОПРЕДЕЛЕНИЯ РОДИЯ | 1994 |
|
RU2102744C1 |
| Способ полярографического определения кобальта в биологических материалах | 1988 |
|
SU1518768A1 |
| Способ определения иридия | 1979 |
|
SU775690A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ОСМИЯ (VIM) | 1972 |
|
SU353191A1 |
| Способ кинетического определения родия | 1987 |
|
SU1543340A1 |
| Способ определения палладия | 1982 |
|
SU1087889A1 |
| Способ подготовки проб к определению осмия кинетическим методом | 1991 |
|
SU1825417A3 |
| СПОСОБ ПОДГОТОВКИ ПРОБ ДЛЯ ОПРЕДЕЛЕНИЯ ИРИДИЯ | 1994 |
|
RU2096754C1 |
СПОСОБ ОПРЕДЕЛЕНИЯ ОСМИЯ, основанный на его каталитическом действии в окислительно-восстановительной реакции между арсенитом натрия и галогенатом калия в присутствии серной кислоты, отличающийс я тем, что, с целью повышения селективности определения осмия при сохранении высокой чувствительности способа, в качестве галогената калия используют йодат калия и окислительно-восстановительную реакцию проводят при следующих.концентрациях компонентов, М: -4 Йодат калия 
По прототипу: 5,В10 4,6- 10
KJO
1,9-10
По предлагаемому способу:
7,4-10
Г 4
4, 710 г 2
1,7-10
Таблица
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Журнал аналитической химии, 19-74, 24, с | |||
| Способ получения коричневых сернистых красителей | 1922 |
|
SU335A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ определения осмия | 1978 |
|
SU701946A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1984-07-30—Публикация
1982-11-12—Подача