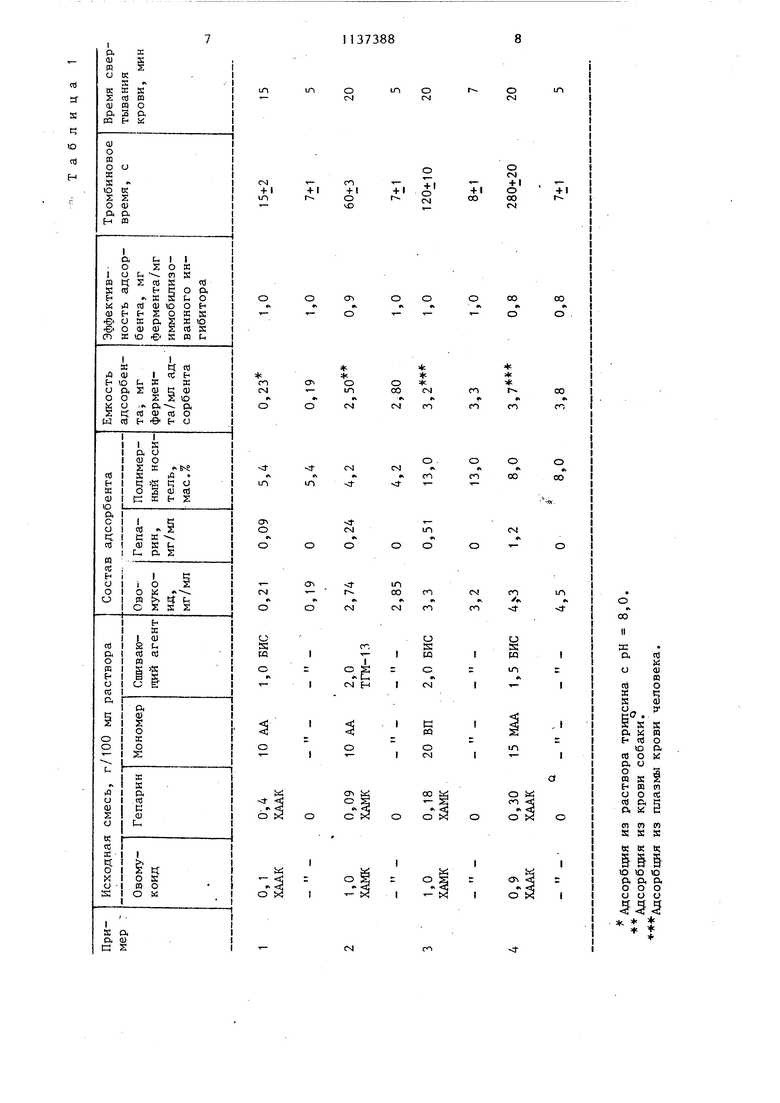
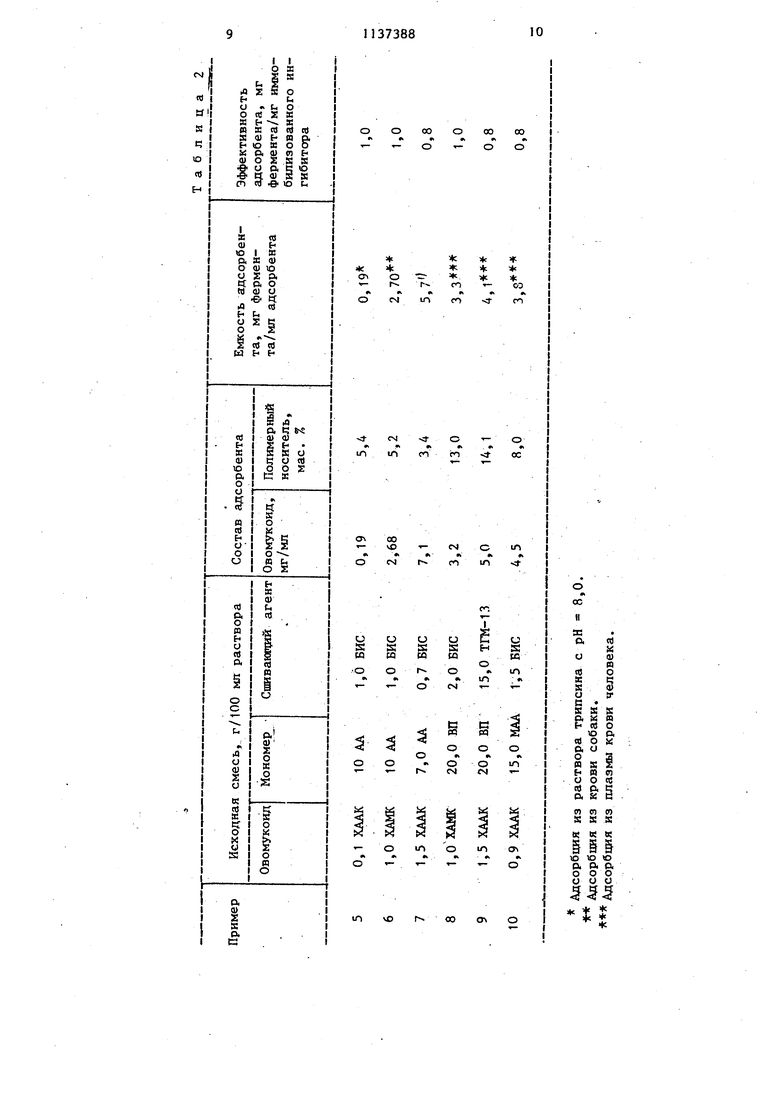
Изобретение относится к химии полимеров и биохимии, а именно к биоспецифическому полимерному адсор бенту для выделения протеиназ из биологических жидкостей, и может быть использовано для получения высокоочшценных препаратов протеиназ, а также для очистки биологических жидкостей от этих ферментов. Послед нее необходимо для предотвращения ферментативного разрушения белковых веществ в процессе их выделения из объектов животного происхождения. Для выделения протеиназ из биоло гических жидкостей известны биоспецифические адсорбенты, содержащие полимерный носитель с ковалентно иммобилизованным белковым ингибитором протеиназ и воду и получаемые активацией полимерного носителя сшитого полисахарида (сефарозы) бромцианом с последующим ковалентны присоединением к активированной сефарозе белкового ингибитора протеиназ l . Для этого к набухшей в воде сефа розе, содержащей4-6% твердого полимера, при рН 11,0 добавляют бромциан. Полученную суспензию пере мешивают в течение 8 мин, поддерживая рН равным 10,8-11,2 добавление 5N раствора гидроокиси натрия. Затем активированную сафарозу промыва ют водой и бикарбонатным буфером (рН 9,5), и к ней добавляют раствор ингибитора. Суспензию перемешивают 18 ч при 4с, многократно промьгоают буферными растворами с рН 2,2 и 8,0 и непрореагировавшие груп пы активированной сефарозы нейтрали зуют раствором глицина. Известен биоспецифический полиме ньй адсорбент для вьщелення протеиназ из биологических жидкостей, содержащий полимерный носитель с ковалентно иммобилизованным белковым ингибитором протеиназ и воду. В качестве полимерного носителя, концентрация 1соторого в адсорбенте составляет 4 мае. %, адсорбент содержит сшитый полисахарид сефарозу, а в качестве белкового ингибитора протеиназ - ингибитор трипсина из .соио Концентрация ингибитора соетавляет 25 мг/мл адсорбента. Адсор бент способен поглощать трипсин в количестве 5 мг/мл адсорбента 1.2Т. Недостатками этого адсорбента являются невысокая эффективность адсорбента, составляющая 0,2 мг трипсина на 1 мг иммобилизованного ингибитора, лабильность химических и биологических свойств адсорбента, который в качестве полимерного носителя содержит способный разрушаться под действием ферментов полисахарид - сефарозу, а также низкая гемосовместимость адсорбента. Последнее не позволяет использовать адсорбент для извлечения протеиназ из крови. Кровь при контакте с таким адсорбентом свертьшается в течение 5-6 мин. Наиболее близким к изобретению является биоспедифический полимерный адсорбент для выделения протеиназ, содержащий полимерный носитель с ковалентно иммобилизованным белковым ингибитором протеиназ и воду. В качестве полимерного носителя, концентрация которого в адсорбенте составляет 4-6 мас„%, адсорбент содержит сшитый полисахарид - сефарозу, а в качестве белкового ингибитора протеиназ - ингибитор трипсина из лимской фасоли. Концентрация ингибитора, составляет 5,4 мг/мл адсорбента. Адсорбент способен поглощать 1,6 мг трипсина/мл адсорбента З. Недостатками этого адсорбента являются невысокая эффективность адсорбента по протеиназам, составляющая 0,3 мг трипсина на 1 мг иммобилизованного ингибитора, лабильность химических и биологических свойств а.цсорбента, а также низкая гемосовместимость адсорбента. Время свертывания крови при контакте с таким адсорбентом составляет 5-6 мин Целью изобретения является повышение емкости адсорбента по протеиназам. Поставленная цель достигается тем, что биоспецифический полимерный адсорбент для выделения протеиназ, содержащий полимерньй носитель, связанный с белковым ингибитором протеиназ, и воду, в качестве колимерного носителя, связанного с ингибитором, содержит сшитый сополимер .овомукоида из белка утиных яиц, ацилированного хлорангидридом ненасыщенной кислоты, акриламида или метакрнпамида, или N-винилпирролидона и биофункционального смешивающего агента, взятых соответственно в количествах: 0,35-6,35, 77,80 90,60 и 8,60-15,60 мае. % при содержании указанного сополимера в адсорбенте 4,2-13,0 мас.%, вода остальное, Кроме того, в качестве полимерно го носителя, связанного с ингибитором, адсорбент содержит сшитьй сополимер овомукоида из белка утиных яиц, актированного хлорангидридом ненасыщенной кислоты, акриламида, или метакриламида, или Ы-винилпирролидона и бифункционального сшиваю щего агента, взятых соответственно в количествах: 0,35-17,30, 55,2090,55, 8,60-41,40 мае. % при содержании указанного сополимера в адсорбенте 3,4-14,1 мас.7о, вода остальное. Используемый овомукоид является гликопротеином с мол. массой около 22000. Его вьщеляют из белка.утиных яиц по методике З J. Гепарин являет ся мукополисахаридом, который применяют для предотвращения свертьшания крови. Биоспецифический адсорбент получ ют раздельным ацилированием овому- коида и гепарина хлорангидридом акр ловой или метакриловой кислоты при рН 6,0-8,0, температуре 0-30°С и мольным отношении овомукоид (гепарин):клорангидрид равном 1:10-100. Затем полученные растворы смешивают и к ним добавляют акриламнд, метак- риламид или N-винилпирролидон в количестве 7-20 мае. %, бифункциональный сшивающий агент, например N,N -метилеибисакриламид или диэфир метакриловой кислоты, в количестве 0,7-15 мае. % и инициатор радикальной полимеризации. Полученный раствор вакуумируют или продувают инерт ным газом для удаления растворенного кислорода. Полимеризацию проводят вьщерживанием раствора при 020 С в течение 10-20 мин. Полученный продукт измельчают до частиц- с размерами 0,1-1,0 мм и промывают бикарбонатным буфером с рН 8,0 до полного удаления непрореагировавших соединений. Полноту удаления контр лируют,спектрофотометрически.-Коли чество связанного с полимером гепа рина и овомукоида определяют по ра 8 нице между исходной концентрацией этих веществ и их концентрацией в промьганых водах. Содержание полимера в адсорбенте определяют высуши-. ванием адсорбента в вакууме при комнатной температуре до постоянного веса. Для выделения протеиназ из биологичееких жидкостей адсорбент помещают в колонку объемом 10-50 мл, и через колонку пропускают жидкость. Количество адсорбированного фермента определяют по разнице между его исходной концентрацией в жидкости и конечной концентрацией или путем элюции адсорбированного фермента буферным раствором с рН 1,52,0. Промывание адсорбента указанным буфером обеспечивает полнзгю элюцию фермента и многократное использование адсорбента. Гемосовместимость адсорбента оценивают по времени образования фибринового сгустка (тромбиновое время) при реакции фибриногена с тромбином в присутствии адсорбента или путем измерения времени свертывания крови при ее контакте с адсорбентом. Пример 1.В 80 мл бикарбонатного буфера (рН 8,0) растворяют 100 мг овомукоида из белка утиных яиц. К раствору при добавляют 0,01 мл хлорангидрида акриловой кислоты. Реакционную смесь перемешивают при в течение 15 мин. В 20 мл бикарбонатного буфера (рН 8,0) растворяют 20 мг гепарина, к раствору добавляют 0,003 мл хлорангидрида акриловой кислоты. Раствор перемешивают при 4°С в течение 15 мин. Оба раствора смешивают и к ним добавляют 10 г акриламида, 1,0 г К,ы-метиленбисакрш1амида и инициатор полимеризации - 0,01 г персульфата аммония и 0,2 ил 0,4%-ного раствора N,N,N ,N-TeTpaметилзтилендиамина. Через раствор в течение 10 мин пропускают аргон для удаления растворенного кислорода. Полимеризацию проводят вьздерживанием реак1р1онной смеси при 10°С в течение 20 мин. После окончания полимеризации адсорбент, который представляет собой хорошо набухающий в воде полимерный гидрогель, измельчают и промывают бикарбонатным буфером до полного удаления иепрореагировавших соединений. Свойства адсорбента приведены в табл. 1. Аналогичным образом получают адсорбент без гепарина. Свойства этого адсорбента также приведены в таблице о П р и м. е р ы 2-4. Процесс получения адсорбента проводят по примеру 1, используя различные мономеры и сшиваюгше. агенты„ Состав исходной реакционной смеси и свойства адсорбентов приведены в табл. 1, Пример 5, BlOt-ui бккарбонатного буфера (рН 8,0) растворяют 10 мг овомукоида из утиных яиц. К раствору при добавляют 0,001 мл хлорангидрида акриловой кислоты. Реакционную смесь перемешивают при 0°С 15 мин. Затем к пол ченному раствору добавляют 1,0 г ак риламида, 0,1 г N,N-метиленбйсакриламида и инициатор полимеризации 0,01 г персульфата аммония и 0,1 мл 0,4%-ного раствора NjNjN,Ы-тетраметиленэтилендиамина. Через раствор в течение 5 мин пропускают аргон. Полимеризацию проводят при 15 С в течение 10 мин. После окончания полимериза Д1и адсорбент измельчают и промывают бикарбонатным буфером (рН 8,0). Свойства адсорбента при ведены в табл. 2. Примеры 6-10, Процесс получения адсорбента проводят по примеру 5, используя различные мономеры и сшивающие аге-.яты„ Состав исход ной реакционной смеси и свойства ад сорбентов приведены в табл, 2. В табл. 1 и 2 приняты еледующие обозначения: ХААК - овомукоиДгацилированный хлорангидридом акриловой кислоты, XAInK - овомУкоид, ацилированньм хлорангидридом метакриловой 86 кислоты, АА - акриламид, ВП - N-винилпирролидон, МАА - метакриламид, БИС - N,N-метиленбисакриламид, ТГМ-13 - диэфир метакриловой кислоты и полизтиленгликоля со степенью полимеризации 13. Таким образом, предлагаемый адсорбент обладает повышенной эффективностью. Так, емкость адсорбентапрототипа, который одновременно является базовым объектом, составляет 0,3 мг трипсина на 1 мг иммобилизованного ингибитора. Емкость адсорбента по изобретению составляет 0,8-1,0 мг трипсина на 1 мг иммобилизованного ингибитора, т.е. этот адсорбент является в 3-4 раза более эффективным, чем адсорбент-прототип. Повышенная эффективность адсорбента позволяет в 3-4 раза сократить расход наиболее дорогостоящего компонента адсорбента - белкового ингибитора протеиназ с. Использование в качестве полимерного носителя синтетического полимера карбоцепного строения на основе легко доступных мономеров, кроме того повышает устойчивость адсорбента к деградации под действием кислот, щелочей и различньсс ферментных систем по сравнению с адсорбентом-прототипом, который является полисахаридом и содержит в основной цепи легко гидролизуемые связи углерод-кислород. Состав , адсорбента, а следовательно, и набухаемость адсорбента, можно легко регулировать путем изменения состава исходной реакционной смеси. Изобретение характеризуется также доступностью и простотой выделения овомукоида из белка утиных яиц.
rt
Я
s R
Ю
пЗ
н


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ БИОСПЕЦИФИЧЕСКОГО ГИДРОГЕЛЕВОГО СОРБЕНТА ДЛЯ ВЫДЕЛЕНИЯ ПРОТЕИНАЗ | 2012 |
|
RU2484475C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСПЕЦИФИЧЕСКОГО ГЕМОСОРБЕНТА ДЛЯ ВЫДЕЛЕНИЯ ПРОТЕИНАЗ | 2018 |
|
RU2681883C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСПЕЦИФИЧЕСКОГО ПОЛИМЕРНОГО СОРБЕНТА ДЛЯ ВЫДЕЛЕНИЯ ПРОТЕИНАЗ | 2010 |
|
RU2420739C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСПЕЦИФИЧЕСКОГО ГИДРОГЕЛЕВОГО СОРБЕНТА ДЛЯ ВЫДЕЛЕНИЯ ПРОТЕИНАЗ | 2014 |
|
RU2567623C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕРНЫХ ГИДРОГЕЛЕЙ, СОДЕРЖАЩИХ ФИЗИОЛОГИЧЕСКИ АКТИВНЫЕ ВЕЩЕСТВА | 2007 |
|
RU2342147C1 |
| Способ получения овомукоида | 1986 |
|
SU1404513A1 |
| Способ очистки ингибиторов протеиназ | 1981 |
|
SU964533A1 |
| СПОСОБ ПОЛУЧЕНИЯ ИНСУЛИНСОДЕРЖАЩЕЙ КОМПОЗИЦИИ | 2020 |
|
RU2752509C1 |
| АФФИННЫЙ АДСОРБЕНТ ДЛЯ УДАЛЕНИЯ ИЗ КРОВИ БИЛИРУБИНА И ДРУГИХ ТОКСИЧНЫХ ПРОДУКТОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1978 |
|
SU731750A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ИНСУЛИНА | 1994 |
|
RU2076733C1 |
1. Биоспецифический полимерНьй адсорбент для выделения протеиназ, содержащий полимерный носитель. связанный с белковым ингибитором протеиназ, и воду, отличающийся тем, что, с целью повышения емкости адсорбента по протеи- назам, он содержит в качестве полимерного -носителя, связанного с ингибитором, сшитый сополимер овомукоида из белка утиных яиц, ацилированного хпорангидридом ненасыщенной кислоты, акриламида или метакрил- амида, или N-винилпирролидона и бифункционального схци ающего агента, взятых соответственно в количествах: 0,35-6,35, 77,80-90,60 и 8,60-15,60 мас.%, при содержании указанного сополимера в адсорбенте 4,2-13,0 мас.%, вода - остальное. 2. Биоспецифйческий полимерный адсорбент, содержащий полимерный носитель, связанный С белковым ингибитором протеиназ, и воду, отличающийся тем, что, с целью повьшения емкости адсорбента по протеиназам, он содержит в качестве полимерного носителя, связанного с СО ингибитором, сшитый сополимер ofib мукоида из белка утиных яиц, ацилиоо , рованного хлорангидридом ненасыщен00 00 ной кислоты, акриламида, или метакриламида, или N-виниапирролидона и бифункционального сшивающего агента, взятых соответственно в количествах; 0,35-17,30, 55,20-90,55, 8,6041,40 мае. %, при содержании указанного сополимера в адсорбенте 3,414,1 мае. %, вода остальное.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Liepnieks J.J., Light А | |||
| Preparation of -Trypsin by Affinity Chroraatography of Enterbkinose Activav..;d Bovine Trypsinigen | |||
| - Analytical Biochemistry, 1974, V | |||
| Способ получения молочной кислоты | 1922 |
|
SU60A1 |
| 395-404, | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Isolation of starfish trypsin by affinity chromatography | |||
| - Сопфагаtive Biochemistry and Physiology, 1976, V | |||
| Видоизменение прибора для получения стереоскопических впечатлений от двух изображений различного масштаба | 1919 |
|
SU54A1 |
| Выбрасывающий ячеистый аппарат для рядовых сеялок | 1922 |
|
SU21A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Свойства утиного овомукоида, очищенного методом афинной хроматографии на трипсин-сефарозе | |||
| - Биохимия, т | |||
| Способ изготовления звездочек для французской бороны-катка | 1922 |
|
SU46A1 |
| Способ смены деревянных мостовых ферм | 1922 |
|
SU473A1 |
Авторы
Даты
1985-01-30—Публикация
1982-04-15—Подача