Изобретение относится к усовершенствованному способу получения 2-замещенных 2-циклопентенонов общей формулы (1) где R - алкил С3-С7 или
где R - алкил С3-С7 или 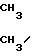 C=CH-CH2 которые обладают запахом жасмина и пригодны для использования в парфюмерных композициях, а также могут найти применение в качестве исходных веществ в синтезе стероидов, простагландинов, пиретринов, используемых как лекарственные препараты и вещества сельскохозяйственного назначения.
C=CH-CH2 которые обладают запахом жасмина и пригодны для использования в парфюмерных композициях, а также могут найти применение в качестве исходных веществ в синтезе стероидов, простагландинов, пиретринов, используемых как лекарственные препараты и вещества сельскохозяйственного назначения.
Известен способ получения 2-замещенных 2-циклопентенонов формулы 1 путем пиролиза при 500-600оС этиловых эфиров 3-циклопропил-3-оксопропионовых кислот.
Недостаток этого способа заключается в низком выходе целевого продукта, который не превышает 60%.
Известен также способ получения 2-замещенных 2-циклопентенонов формулы 1 путем взаимодействия алкилциклопропилкетонов с концентрированной серной кислотой. Образующиеся γ-гидроксикетоны окисляют хлорхроматом пиридина в γ-кетоальдегиды, которые действием оснований превращают в 2-алкил-2-циклопентеноны.
Выход целевого продукта при этом составляет лишь 50-60%. Кроме того, этот способ многостадиен и предусматривает использование химически агрессивных реагентов.
Наиболее близким к предлагаемому способу является способ получения 2-замещенных 2-циклопентенонов формулы 1 путем внутримолекулярной циклизации γ-кетоальдегидов в щелочной среде при комнатной температуре.
С целью предотвращения окисления γ-кетоальдегидов процесс осуществляют в инертной атмосфере, а уменьшение доли продуктов межмолекулярных конденсаций достигается проведением реакции в гомогенной среде путем использования воднометанольных растворов. Выход целевого продукта составляет около 60%.
Недостатком этого способа является низкий выход целевого продукта.
Целью изобретения является увеличение выхода целевого продукта.
Поставленная цель достигается тем, что при осуществлении способа получения 2-замещенных 2-циклопентенов общей формулы (1)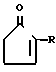 где R - алкил С3-С7 или
где R - алкил С3-С7 или 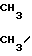 C=CH-CH2 путем внутримолекулярной циклизации карбонильных соединений в щелочной среде, в качестве карбонильного соединения используют 2-хлорциклопропилкетоны общей формулы (II)
C=CH-CH2 путем внутримолекулярной циклизации карбонильных соединений в щелочной среде, в качестве карбонильного соединения используют 2-хлорциклопропилкетоны общей формулы (II)
R-CH2-
 Cl где R - имеет указанное значение, а процесс проводят при 80-100оС.
Cl где R - имеет указанное значение, а процесс проводят при 80-100оС.
Отличительными особенностями данного способа являются использование в качестве карбонильного соединения 2-хлорцик- лопропилкетонов общей формулы

 где R - имеет указанное значение, и проведение процесса при 80-100оС.
где R - имеет указанное значение, и проведение процесса при 80-100оС.
Процесс осуществляют в гетерогенной среде без использования органического растворителя, что способствует увеличению выхода целевого продукта благодаря протеканию реакции в водной фазе, где концентрация субстрата мала, или на границе раздела фаз, что способствует протеканию внутри-, а не межмолекулярных конденсаций.
2-Замещенные 2-циклопентеноны формулы (1) где R-C4H9, C5H11, C6H13, C7H15, CH2-CH= C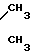 получают путем кипячения соответствующих транс-2-хлорциклопропилкетонов с водным раствором едкого натра. Температура реакционной смеси при ее кипячении 100оС. Проведение реакции при более низких температурах приводит к значительному увеличению времени реакции. Так, например, взаимодействие 5,2 г транс-амил (2-хлорциклопропил)кетона с 75 мл 5% -ного водного раствора едкого натра завершается при 80оС в течение 10 ч. Выход 2-бутил-2- циклопентен-1-она 3,4 г (82%), т.кип. 69-70оС (2 мм рт.ст. , nD21 1,4726.
получают путем кипячения соответствующих транс-2-хлорциклопропилкетонов с водным раствором едкого натра. Температура реакционной смеси при ее кипячении 100оС. Проведение реакции при более низких температурах приводит к значительному увеличению времени реакции. Так, например, взаимодействие 5,2 г транс-амил (2-хлорциклопропил)кетона с 75 мл 5% -ного водного раствора едкого натра завершается при 80оС в течение 10 ч. Выход 2-бутил-2- циклопентен-1-она 3,4 г (82%), т.кип. 69-70оС (2 мм рт.ст. , nD21 1,4726.
2-Пропил-2-циклопентен-1-он получают путем перемешивания бутил (2-хлорциклопропил)кетона с водным раствором едкого натра при 80оС. Проведение реакции при температуре кипения реакционной смеси приводит к частичному осмолению продуктов реакции и снижению выхода целевого продукта (пример 7). Выход увеличивается при осуществлении процесса при более низких температурах, что однако приводит к увеличению времени реакции (пример 8). Удовлетворительный выход продукта достигается при проведении реакции при 80оС в течение 3 ч (пример 2).
Целевые соединения получают данным способом с выходом 75-85%.
Способ иллюстрируется следующими примерами.
П р и м е р 1. 2-Бутил-2-циклопентен-1-он.
Смесь 5,2 г транс-амил (2-хлорциклопропил)кетона и 75 мл 5%-ного водного едкого натра перемешивают в течение 3 ч при 100оС. Реакционную массу охлаждают до комнатной температуры, продукт экстрагируют эфиром (3х30 мл). Эфирные вытяжки промывают водой и сушат безводным сульфатом натрия. После отгонки растворителя получают 3,5 г 2-бутил-2-циклопентенона. Выход 85%, т. кип. 70-72оС/3 мм рт.ст., nD20 1,4729.
П р и м е р 2. 2-Пропил-2-циклопентен-1-он.
Смесь 4,8 г (0,03 моль) транс-бутил (2-хлорциклопропил)-кетона и 75 мл 5% -ного водного раствора едкого натра перемешивают в течение 2 ч при 80оС. Реакционную массу охлаждают до комнатной температуры. Продукт экстрагируют эфиром (3х30 мл). Эфирные вытяжки промывают водой и сушат безводным сульфатом натрия. Растворитель удаляют, остаток перегоняют в вакууме. Получают 2,8 г (75%) 2-пропил-2-циклопентен-1-она т.кип. 77-78оС/12 мм рт.ст., nD20 1,4731.
П р и м е р 3. 2-Амил-2-циклопентен-1-он.
Смесь 5,65 г (0,03 моль) транс-гексил (2-хлорциклопропил)-кетона и 75 мл 5% -ного водного раствора едкого натра перемешивают в течение 4 ч при 100оС. Реакцион- ную смесь обрабатывают аналогично примеру 2 и перегонкой в вакууме получают 3,5 г (78%) 2-амил-2-циклопентен-1-она, т.кип. 76-78оС/2 мм рт.ст., nD20 1,4738.
П р и м е р 4. 2-Гексил-2-циклопентен-1-он.
Смесь 6,07 г (0,03 моль) транс-гептил(2-хлорциклопропил)-кетона и 75 мл 5%-ного водного раствора едкого натра перемешивают в течение 6 ч при 100оС. Реакционную смесь обрабатывают аналогично примеру 2 и перегонкой в вакууме получают 4,0 г (80%) 2-гексил-2-циклопентен-1-она, т.кип. 89-90оС/2 мм рт. ст., nD20 1,4749.
П р и м е р 5. 2-Гептил-2-циклопентен-1-он.
Смесь 6,5 г (0,03 моль) транс-октил(2-хлорциклопропил)-кетона и 75 мл 5% -ного водного раствора едкого натра перемешивают в течение 10 ч при 100оС. Реакционную смесь обрабатывают аналогично примеру 2 и перегонкой в вакууме получают 4,4 г (81%) 2-гептил-2-циклопентен-1-она, т.кип. 95-96оС/2 мм рт.ст., nD20 1,4730.
П р и м е р 6. 2-(3-Метил-2-бутен-1-ил)-2-циклопентен-1-она.
Смесь 5,6 г (0,03 моль) транс-(4-метил-3-пентен-1-ил)-(2-хлорциклопропил)кетона и 75 мл 5%-ного водного раствора едкого натра перемешивают в течение 3 ч при 100оС. Реакционную смесь обрабатывают аналогично примеру 2 и перегонкой в вакууме получают 3,7 г (83%) 2-(3-метил-2-бутен-1-ил)-2-циклопентен-1-она, т.кип. 79-80оС/2 мм рт.ст., nD20 1,4885.
П р и м е р 7. 2-Пропил-2-циклопентен-1-он.
Смесь 4,8 г (0,03 моль) транс-бутил(2-хлорциклопропил)-кетона и 75 мл 5% -ного водного раствора едкого натра перемешивают в течение 1,5 ч при 100оС. Реакционную смесь обрабатывают аналогично примеру 2 и перегонкой в вакууме получают 2,2 г 2-пропил-2-циклопентен-1-она (60%), nD18 1,4734, т. кип. 77-78оС/12 мм рт.ст.
П р и м е р 8. 2-Пропил-2-циклопентен-1-он. Смесь 4,8 г (0,03 моль) транс-бутил(2-хлорциклопропил)-кетона и 75 мл 5% -ного водного раствора едкого натра перемешивают в течение 8 ч при 60оС. Реакционную смесь обрабатывают аналогично примеру 2 и перегонкой в вакууме получают 2,7 г (73%) 2-пропил-2-циклопентен-1-она, т.кип. 77-79оС/12 мм рт.ст., nD18 1,4733.
Таким образом, температурный интервал 80-100оС представляется оптимальным с точки зрения достижения максимальных выходов целевых продуктов при возможно меньшем времени проведения процесса.
Предлагаемый способ позволяет увеличить выход целевого продукта до 85% по сравнению с 60% в известном способе.
| название | год | авторы | номер документа |
|---|---|---|---|
| БИС-[3- (3,5-ДИМЕТИЛ- 4-ОКСИФЕНИЛ)- ПРОПИЛ-1] -СУЛЬФИД КАК ТЕРМОСТАБИЛИЗАТОР СЭВИЛЕНА И 3-(3,5 -ДИМЕТИЛ-4- ОКСИФЕНИЛ)- ПРОПАНОЛ-1 В КАЧЕСТВЕ ПРОМЕЖУТОЧНОГО ПРОДУКТА В СИНТЕЗЕ БИС-[3-(3,5- ДИМЕТИЛ-4- ОКСИФЕНИЛ) -ПРОПИЛ-1] -СУЛЬФИДА - ТЕРМОСТАБИЛИЗАТОРА СЭВИЛЕНА | 1991 |
|
SU1833606A3 |
| Способ получения 2-(6 @ -карбоксигексил)-циклопент-2-ен-она | 1985 |
|
SU1334644A1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-МЕТОКСИИЗОБУТИЛИЗОЦИАНИДА | 1990 |
|
RU2026857C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-МЕТОКСИИЗОМАСЛЯНОЙ КИСЛОТЫ | 1990 |
|
RU2026855C1 |
| N-АЛКИЛ- N-АЦЕТИЛКАРБОНАМИДЫ, ОБЛАДАЮЩИЕ ИНСЕКТО- И АКАРОРЕПЕЛЛЕНТНОЙ АКТИВНОСТЬЮ | 1993 |
|
RU2047598C1 |
| 2-АЦЕТОНИЛ-5,5-ДИМЕТИЛ-1,2,3,4,5,6,7,8-ОКТАГИДРОНАФТАЛИН В КАЧЕСТВЕ КОМПОНЕНТА ПАРФЮМЕРНОЙ КОМПОЗИЦИИ, СПОСОБ ЕГО ПОЛУЧЕНИЯ, 2,6-ДИМЕТИЛ-2,6,10-ТРИДЕКАТРИЕН-12-ОН В КАЧЕСТВЕ ПРОМЕЖУТОЧНОГО ПРОДУКТА В СИНТЕЗЕ 2-АЦЕТОНИЛ-5,5-ДИМЕТИЛ-1,2,3,4,5,6,7,8-ОКТАГИДРОНАФТАЛИНА | 1992 |
|
RU2035448C1 |
| Способ получения метиловых эфиров @ -кетокарбоновых кислот | 1985 |
|
SU1325843A1 |
| ВСЕСОЮЗНАЯnAl?HTBQ-T:XHH'iKHAfi | 1973 |
|
SU386502A1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРИАЛКИЛФОСФИТОВ | 1993 |
|
RU2026298C1 |
| Способ получения производных @ -дигалоидвинилциклопропана | 1978 |
|
SU1075972A3 |
СПОСОБ ПОЛУЧЕНИЯ 2-ЗАМЕЩЕННЫХ-2-ЦИКЛОПЕНТЕНОНОВ общей формулы
где R - алкил С3 - С7 или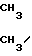 C=CH-CH2
C=CH-CH2
путем внутримолекулярной циклизации карбонильных соединений в щелочной среде, отличающийся тем, что, с целью увеличения выхода целевого продукта, в качестве карбонильного соединения используют 2-хлорциклопропилкетоны общей формулы
R-CH2-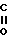
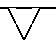 Cl
Cl
где R имеет указанные значения,
а процесс проводят при 80 - 100oС.
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| M.Laroheveque, G.Valltte, Th | |||
| Guligny | |||
| Tetrahedror, 35, 1745-1749, 1979. | |||
Авторы
Даты
1994-07-15—Публикация
1983-09-14—Подача