o:i
00
ел
СП
Изобретение относится к произв ным 1-нитро-9-гидроксиалкиламиноакридинам общей формулы NH-CHlCH.bOH N0, , где при R Н п 1,2 или 3 при R п 1 , а именно к их гидрохлоридам, проявляющим противоопухолевую активность. Цель изобретения - получение но соединений в акридиновом ряду, обладающих высокой противоопухолевой активностью. Пример 1. 6,4 г 1-нитро-9-феноксиакридина растворяют в. 20 г фенола, добавляют 2 г хлоргидрата -аминэтанола, после чего подогрева при 80°С в течение 40 мин. После охлаждения смесь, полученную в результате реакции, разбавляют эфиро и медленно вьшивают в излишек сухо го эфира, подкисленного эфирным раствором хлористого водорода. Выпавший осадок фильтруется и промыв ется сухим эфиром и кристаллизуется из безводного этанола. Получают темно-желтые кристаллы хлоргидрата 1-нитро-9-(2-гидроксиэтиламино) ак ридина с ТоПл. 170 С, с разложением. Выход 91%. Хроматографический анализ; На нейтральной окиси алюминия 60F254 (фирмы Merck) по системе бензол:ацетон:метанол 3:1:1 К/ 0 На силикагеле (фирмы Merck) по системе бутанол:уксусная кислота: да 4:1:1 Rf-0,45. Вычислено,%: С 56,47 Н 4,42j N 13,17. едЛОзС . Найдено,%: С 56,44 Н 4,40; N 13,03. Прим ер 2. 3,16 г 1-нитро -9-феноксиакридина растворяют в 15 мл ,-добавляют 1 г хлоргидрата 3-аминпропанола, после чего подогревают при 60 С в течение 0,5 ч. После охлаждения смесь полученную в результате реакции, растворяют в сухом бензоле и медл но вьтивают в излишек сухого бенз ла. Выпавший оранжевый осадок фил труется, несколько раз промывается на воронке сухим эфиром и выкристаллизовывается из смеси этанол/эфир. Таким образом, получают хлоргидрат 1-нитро-9-гидроксипропиламиноакридина ст. пл. 180°С, с разложением. Выход 88%. Хроматографический анализ. На нейтральной окиси алюминия (Merck) по системе бензол : ацетон : метанол 3: 1: 1 R 0,35. На силикагеле (Merck) по системе бутанол : уксусная кислота : вода 4:1:1 .R 0,45. Вычислено,%: С 57,53; Н 4,83; N 12,58. Найдено,%: С 57,63; Н 4,97; N 12,43. Приме рЗ.З,9г 1-нитро-9-феноксиакридина растворяют в 20 мл фенола, добавляют 1,1 мп 2-амино-1-бутанола, после чего подогревают в течение 20 мин при 90°С. Затем смесь, полученную в результате реакции, медленно вьтивают в охлажденный эфир, часть растворителя отгоняют, а вьтавший осадок кристаллизуется из смеси петрол.ейный эфир/бензол. Получают основание 1-нитро-9(1-этил-2-гидроксиэтиламино) акридина с т.пл. . Выход 99%. Основание затем переводят в хлоргидрау. Хроматографический анализ. На нейтральной окиси алюминия (Merck) по системе бензол : ацетон: метанол 3:1:1 Rp 0,7. На силикагеле (Merck) по системе бутанол : уксусная кислота : вода 4:1:1 Кл 0,6. Вычислено,%: С 58,67; Н 5,21j N 19,08. . Найдено,%: С 58,80; Н 5,17; N 11,84. Пример 4. 6,4 г 1-HrfTpo-9-феноксиакридина растворяют в 30 мл фенола, добавляют 2,4 г хлоргидрата 4-амино-1-бутанола, после чего нагревают смесь в течение 20 мин при 100°С, После охлаждения смесь, олученную в результате реакции, выливают в излишек (1,5 л) сухого охлажденного эфира. Вьшавший оранжевый осадок кристаллизуется из метанола с добавкой эфира. Получают хлоргидрат 1-нитро-9(4-гидрокси3
бутиламино)акридина с т.пл.168С с разложением. Выход 90%,
Хроматографический анализ.
На нейтральной окиси алюминия (Merck) по системе бензол : ацетон : метанол 3:1:1 Rp 0,65.
На силикагеле (Merck) по систем бутанол : уксусная кислота : вода 4:1:1 R 0,50.
Вычислено,%: С 58,67 Н 5,21; N 12,08.
Ц,Н,,ОэЫзС1
Найдено,%: С 58,69; Н. 5,20; N 12,16.
Группа предлагаемых соединений обладает противоопухолевой активностью, которая является подобной, а в большинстве тестов даже более высокой по сравнению с известными соединениями этой группы, кроме того, не проявляет рвотных свойств а также не влияет на периферическую кровь. Это свойство необыкновено редкое и ценное среди этой груп соединений.
Противоопухолевые свойства рассматриваемой группы соединений, а именно 1-нитро-9-гидроксиалкиламинакридинов, многократно исследуют тестами in vitro и in vivo.
Метод in vitro . Торможение прорастания семян сердечника-- тест роста.
На чашке Петри диаметром 80 мм по возможности равномерно размещают 20-25 семян сердечника на двух слоях промокательной- бумаги, затем наливают 30 мл раствора исследуемого соединения с концентрацией 1 мг/мл, а на контрольные чашки дистиллированную воду. Чашки инкубируют в течение суток при 20-30 С после чего измеряют длину ростков.
Эффект торможения выражается в процентах уменьшения средней длины исследуемых ростков по сравнени с контрольными.
Процент торможения прорастания семян сердечника для рассматриваемой группы соединений составляет 87-94%.
Метод Миямуры (раковые клетки Эрлиха).
Метод состоит в определении торможения активности дегидрогенов раковьк клеток Эрлиха (5 х 10 в мл исследуемыми соединениями, мерилом чего является диаметр зоны невосст85574
новленного окислительно-восстлновительного красителя (ресязуриня), образовавшегося вокруг цилиндра с 1%-ным раствором исследуемого соединения после 5 ч инкубации при ..
В соответствии с общепринятыми принципами соединения, для которых зона торможения составляет не менее 20 мм, считаются активными.
О Предлагаемые соединения выявляют исключительно высокую активность по этому тесту, причем она составляет в среднем 31-33 мм.
Тканевая культура, так называемая линия КВ.
Исследования проводят по методу тканевой культуры, разработанному Иглем и Фоули, модифицированному Смитом и его сотрудниками.
20 Опыт проводят на опухолевых клетках человеческого происхождения (линии KB), с использованием питательной среды Игла с добавкой 10% телячьей сыворотки-.
25 Тесты производят в пробирках с прививаемых клеток (40-80 тыс) взвеси (4 мл), что равнозначно-с 40-80 мг клеточного белка.
Рост культуры определяют приростом клеточного белка фотометрически с использованием реактива Фолина-Сикальтана методом, разработан.ньгм Оямой и др.
Одновременно с привитием пробирок
j-j клетками добавляют 0,9 t-in водного раствора исследуемого соединения таким образом, чтобы концентрация составляла 100, 10, 1, 0,1, 0,01, 0,001, 0,0001 мг/мп питательной
40 среды. Пробирки инкубируются при 37 С. Через 72 ч определяют прирост клеточного белка в пробирках, в которые добавлялся препарат из контрольных пробирок.
45 Каждую концентрацию исследуют параллельно по двум пробам.
Определяют такие концентрации вещества, при которых обеспечивается торможение прироста клеточного белка на 50%, LDj, или EDjj.
Процент торможения определяют из соотношения остаточного количества клеточного белка по контролю - концевое количество белка клеточного
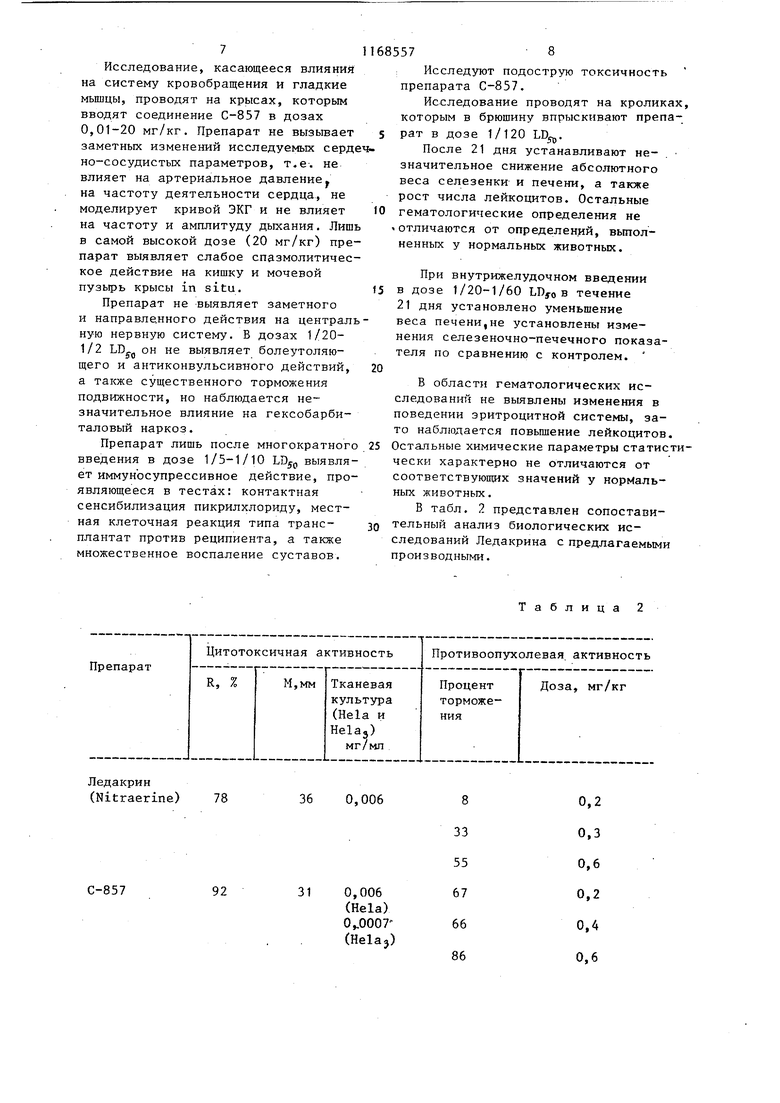
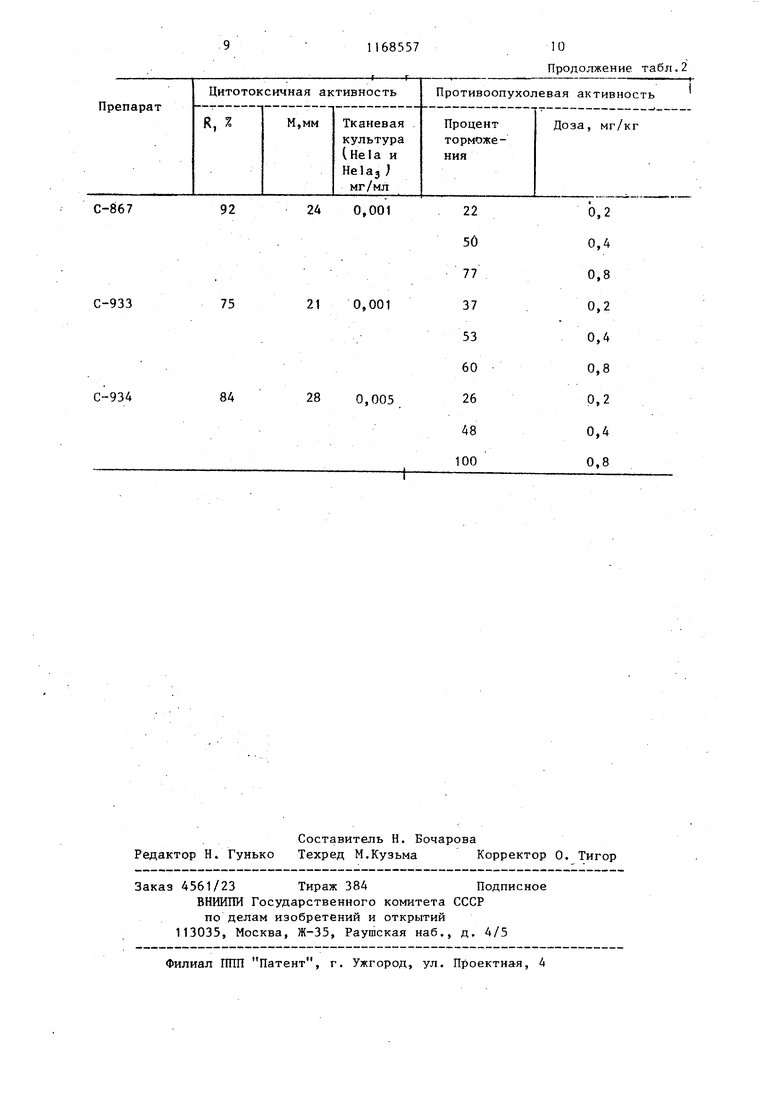
55 в тесте к остаточному количеству клеточного белка по контролю - начальное количество клеточного белка по контролю. В соответствии с общепринятыми нормами активными считаются такие соединения для которых LD fKD-J 1 мг/мп.. Предлагаемые соединения тестирую ся этим методом несколько раз. Например , EDjQ для одного препарата из этой группы с кодовым символом С-857, т.е. 1-нитро-9-гидроксиэтиламиноакридина, составляет 0,0007 мг/ Метод in vivo. Торможение роста мьшшной саркомы Крокера (Sa-180). Для опытов применяют мышей в воз расте около 3 мес, весом около 25 г Их прививают срезом опухоли (Sa-180 после чего разделяют на группы: одну контрольную (18 шт.) и две до четырех групп (леченных по 8 шт каждая). Исследуемые соединения в соответствующих дозах вводят в брюшину после предварительного определения максимальной переносимой дозы (MTD). В качестве критерия оценки противоопухолевого действия исследуемых соединений применяют процентную разницу между средними весами опухолей контрольных мьшей и мышей, по лучающих препарат, с учетом при . ЭТОМ токсических эффектов исследуемого соединения. Оценка токсичности охватывает потерю веса леченных животных по сравнению с контролем, число павших животных по сравнению с контролем, а также микроскопические гистопатологические исследовани Активными считаются такие соединения, которые по крайней мере дваж ды тормозят рост опухолей более 40%, не вызывая при этом падежа животных (2 шт.) и средних потерь веса 4 г. Исследования in vivo в этом тесте предлагаемой группы соединений проводят многократно. Так, например для препарата с кодовым символом С-857, т.е. 1-нитро-9-гидроксиэтиламиноакридина, установлено торможение роста саркомы Sa-180 в зависимости от следующей дозы: при 0,20,8 мг/кг процент торможения 44-86. Лля препарата С-934, т.е. 1-нитро-9-гидроксибутиламиноакридина, при дозах 0,2-0,4 процент торможения 45-60. Фармакологические исследования. Анализ биологической активности подтвержден подробными фармакологическими исследованиями. Проводят исследования токсичности острой и кумулятивной, а также основных фармакологических свойств в следующих тестах: острая токсичность и определение максимальной переносимой дозы, кумулятивная токсичность, влияние на систему кровообращения, на гладкие мьш1цы, на центральную нервную систему, иммуносупрессивное действие. Острую токсичность bDso J и максимальную переносимую дозу (MTD) определяют на крысах Wister, кроликах (обоего пола) и мышах Albino Swiss (самки). Соединения вводят в брюшину (у всех трех видов животных) и желудок (у крыс и кроликов). Продолжительность наблюдения составляет 48 ч. Полученные значения LD.. и MTD сведены в табл. I Таблица 1 Кумулятивная токсичность. Опыт проводят на нескольких- группах крыс (по 20 шт.), которым исследуемое соединение вводят в течение- .14 дней в дозах 1/100 LDj5 . Затем животных умерщвляют, после чего производят микроскопическую оценку мьш1ечных органов и брюшной полости. Исследуемый препарат кумулируется в минимальной степени - смертельность животных, получавших лекарство, по сравнению с контролем составляет около 5%. Не наблюдаются также потери веса животных и изменения в lix внешнем виде и поведении. Исследование, касающееся влияния на систему кровобращения и гладкие мышцы, проводят на крысах, которым вводят соединение С-857 в дозах 0,01-20 мг/кг. Препарат не вызывает заметных изменений исследуемых серд но-сосудистых параметров, т.е-, не влияет на артериальное давление на частоту деятельности сердца, не моделирует кривой ЭКГ и не влияет на частоту и амплитуду дыхания. Лиш в самой высокой дозе (20 мг/кг) пре парат выявляет слабое спазмолитичес кое действие на кишку и мочевой пузырь крысы in situ. Препарат не выявляет заметного и направленного действия на централ ную нервную систему. В дозах 1/201/2 LD.. он не выявляет болеутоляющего и антиконвульсивяого действий, а также существенного торможения подвижности, но наблюдается незначительное влияние на гексобарбиталовый наркоз. Препарат лишь после многократног введения в дозе 1/5-1/10 выявля ет иммуносупрессивное действие, про являющееся в тестах: контактная сенсибилизация пикрилхлориду, местная клеточная реакция типа трансплантат против реципиента, а также множественное воспаление суставов. Исследуют подострую токсичность препарата С-857. Исследование проводят на кроликах, которым в брюшину впрыскивают препарат в дозе 1/120 LDjp. После 21 дня устанавливают незначительное снижение абсолютного веса селезенки и печени, а также рост числа лейкоцитов. Остальные гематологические определения не отличаются от определений, выполненных у нормальных животных. При внутрижелудочном введении в дозе 1/20-1/60 LDyoв течение 21 дня установлено уменьшение веса печени,не установлены изменения селезеночно-печечного показателя по сравнению с контролем. В области гематологических исследований не выявлены изменения в поведении эритроцитной системы, зато наблюдается повьш1ение лейкоцитов. стальные химические параметры статистически характерно не отличаются от соответствующих значений у нормальных животных. в табл. 2 представлен сопоставительный анализ биологических исследований Ледакрина с предлагаемыми производными.


Гидрохлориды 1-нитро-9-гидроксиалкиламиноакридинов общей Лормулы NH-CH(CH2)OH г где при R Н п 1,2 или З; при R . п 1, проявляющие противоопухолевую активность.
Ледакрин (Nitraerine)
36
78
С-857
92
31
Таблица 2
0,2
8 0,3
33 55 67 66 86 0,6 0,2 0.4 0,6
| Кулачково-рычажный механизм | 1983 |
|
SU1093844A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Naterie Medice Polone | |||
| Планшайба для точной расточки лекал и выработок | 1922 |
|
SU1976A1 |
Авторы
Даты
1985-07-23—Публикация
1981-04-14—Подача