3,f
3.0
4 г,в
Нойьное отношение .t
yittt. 1
Изобретение относится к технологии специальных материалов для нужд электронной техники и связанных с ней отраслей керамической технологии и может быть использовано для получения 5 компонентов электронных устройств, а также в производстве конструкционных и контейнерных материалов (нитридной керамики).
Целью изобретения является повыше- ние степени чистоты нитрида алюминия и упрощение процесса.
Сущность способа заключается в том, что в способе получения нитрида алюминия, включающем нагрев алю- 5 миния с хлоридом аммония в атмосфере азота процесс ведут при нормальном давлении с использованием смеси алюминия с хлоридом аммония, взятой в молярном соотношении хлорида к алю- 20 минию 2,4-3, которую нагревают до 550-595 К с вьзделением водорода и аммиака, а затем, после того, как металлический алюминий полностью прореагирГует с образованием промежу- 5 точного продукта, этот продукт прокаливают при температуре выше 1100 К.
Процессы, развивающиеся в ходе обработки, по предлагаемому способу существенно отличаются от тех, кото- 30 рые имеют место при работе по известному способу. В реакторе отсутствуют кислородсодержащие вещества и, тем самым, загрязнение оксидом алюминия исключается. При 550 К начи- 35 нается. диссоциация хлорида аммония и, как следствие, начинается реакция с алюминием, с вьщелением водорода. Образуется жидкий расплав хлоридаммиакатов алюминия. Остав- Ю шийся алюминий полностью реагирует с расплавом, образуя твердый промежуточный продукт сложного состава, включающий алюминий, азот и водород-хлорамид алюминия, Взаимодейст- 45 вие алюминия с азотом газовой фазы при этом отсутствует.
В интервале температур 550-695 К хлоридаммиакат и хлорамид алюминия 50 сосуществуют в виде двухфазной смеси, При 695 К хлоридаммиакат отгоняется из смеси, поскольку наступает его кипение. Остается твердый промежуточный продукт - хлорамид алюми- 55 ния. Вьше 1100 К хлорамид распадается. При этом хлор полностью отгоняется в виде хлорводорода и в
итоге образуется чистый нитрид алюминия .
Способ позволяет получать указанный продукт при соблюдении определенных условий ведения процесса, обоснованных рядом теоретических и экспериментальных выводов. Состав реакционной смеси должен удовлетворять молярному соотношению 2,4хлоридаммония и алюминия 3. Такой интервал составов обоснован экспериментально.
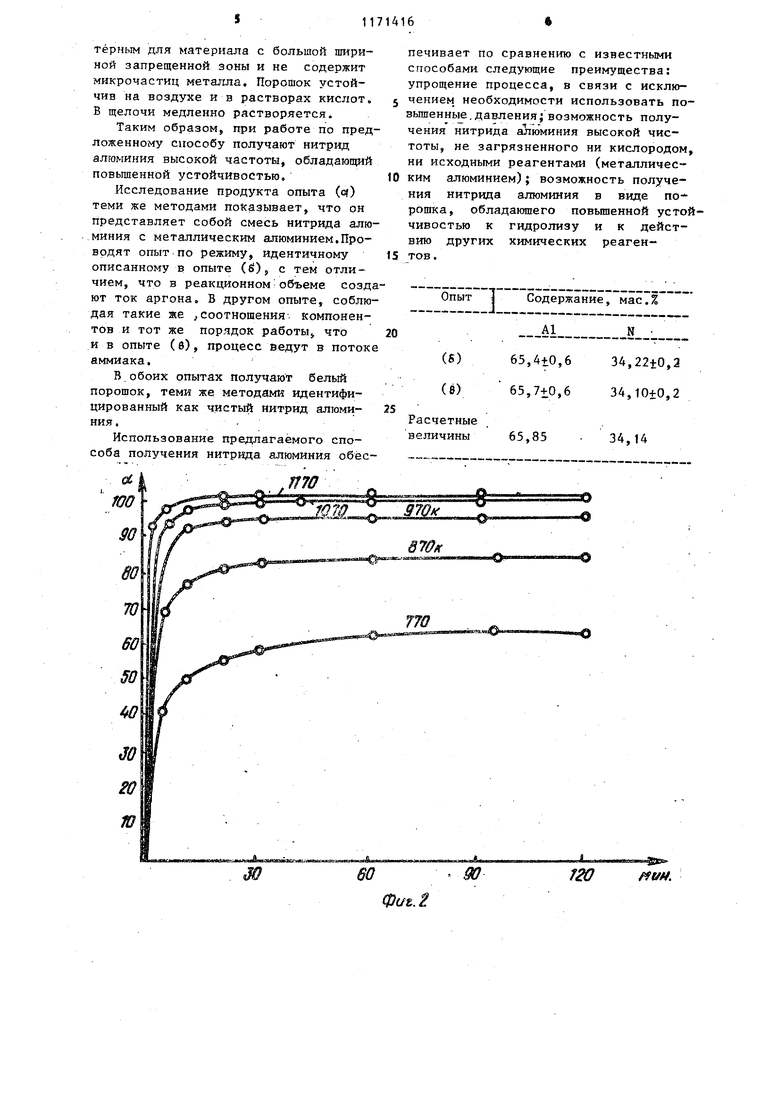
На фиг. 1 приведены результаты экспериментов,выполненных при различных молярньос соотношениях в реакциционной смеси; на фиг. 2 - зависимость степени превращений :Хлорамида алюминия в нитрид от времени вьщержки, при раэличньпс температурах.
По вертикальной оси (фиг.1) отложна величина выхода реакции по алюминию. Светлые кружки соответствуют продукту, не содержащему металлического алюминия.Зачерненные сегменты указывют на загрязнение продукта непрореагровавшим алюминием. Приведенные результаты показывают, что нижншпределом молярного соотношения является величина 2, 4 так как при меньших значениях этого отношения наступает загрязнение продукта алюминием, вследствие недостатка хлорида аммония для его полного связьшания. Верхним пределом молярного соотношения является величина 3, так как при больших значениях этого отношения выход нитрида алюминия уменьшается до нуля. Непосредственное наблюдение за ходом процесса показывает, что уменьшение выхода, а затем и полное прекращение образования порошка нитрида алюминия в реакторе обусловлено повьшением доли летучих соединений в составе реакционной массы и, как следствие, потерями алюминия в газовую фазу. При значениях молярного отношения более 3 хлорамида алюминия не образуется и реакционная смесь при 695 К полностью испаряется. Оптимальное молярное соотношение составляет 2,45.
Интервал температур, в котором ведут первую стадию процесса 550695 К обоснован как теоретически, так и экспериментально. Нижний предел 550 К соответствует температуре при которой диссоциация хлорида аммония становится заметной и газооб разные продукты, в особенности хлорводород, активно взаимодействуют с металлами. При более низких температурах вз имодействие- между твердыми фазами алюминием и хлоридом аммония, как по казывает опыт, практически отсутствует. Верхний предел 695 К соответствует точке кипения хлоридаммиаката алюминия, присутствующего в многофазной реакционной массе. Попытки перегреть реакционную массу выше 695 К не могут быть успешными, так как наступает кипение одного из ее компоненT08,QnbiT подтверждает это заключение Лишь после отгонки избыточного хлорид дш йак;а1 а появляется возможность перейти ко второй стадии процесса - пиролитическому разложению хлорамида алюминия.. , Температура, при которой пиролиз хлорамида алюминия протекает с заметной скоростью, определена экспериментально, на основании излучения кинетики этого процесса. Как видно из фиг, 2 по вертикальной оси отложена степень превращения oi(%), по горизонтальной оси время опыта (мин). Каждая кинетическая кривая соответствует определенной температуре. При использовании температурвьппе 1100 К превращение (100%) достигается в течение короткого времени (30-40 мин). При более низких температурах кинетические кривые выходят на участок насьщения, соответствующий d 100% и, таким образом, достижение полного превращения в практически приемлемый промежуток времени невозможно. Проведение обеих стадий процесса :возможно не только в атмосфере азота но и в атмосфере инертного газа или аммиака. Суть происходящих реакций такова, что основным азотирующим реагентом является хлорид аммония. Из приведенных экспериментальных данных 1ясно, что в интервале 550-695 К алюминий полностью связывается с хлорадом аммония и поэтому газовая среда выполняет лишь защитную функциюо В качестве защитной среды используют инертный газ. Это может оказаться целесообразным, так как азбТрпоставляемый промьшшенностью, соответствует менее высоким требованиям по чистоте, чем аргон. Аммиак обладает защитным действием и способствует полноте превращения.| Пример. В кварцевый реактор, снабженный патрубками для подвода и отвода газов и обогреваемый печью сопротивления помещают 20 г алюминия в виде стружки ft (d) 91,1 г, либо (Т)-97,1, либо (в) 114,8 г,, либо (-t) 120,8 г хлорида аммония, что соответствует молярным отношениям хлорида аммония к алюминию соответственно (о) 2,3, либр (&) 2,45, либо (6) 2,9, либо (i) 3,05. Пропуская ток азота (расход 8 л/ч), разогревают смесь до 550 К. Начинается разложение хлорида аммония и его взаимодействие с алюминием, в .отходящих газах появляется водород. По мере дальнейщего повышения температуры смесь претерпевает ряд превра щений, в ходе которых выделяется аммиак. Б (5) , (б) , (г) металлический алюминий полностью вступает в реакцию и образуется вязкая масса. В (о) в вязкой массе остается непрорёагировавший остаток алюминия.При. 695 К жидкость, входящая в состав вязкой массы, активно испаряется. При этом в опыте (с() остается белый РЫХЛЫЙ спек, содержащий остаточный алюминий; в опытах () и (в) остается однородный белый спек, масса которого в опыте (б) существенно меньше, чем в опыте (б); в опыте (г) происходит практически полное испарение жидкости, спека не.образуется. Температуру повьш1ают в опыте (а) и (6) до 1100 К, а в опыте (в) до 1300 К. Проводят двухчасовую выдержку и охлаждают реактор. Опыт (г) прекращают ввиду отсутствия материала в рабочей зоне реактора. Получают в опытах (S) и (в) соответственно 21,2 и 4,6 г белого порошка; в опыте (с) получают 24,7 г такого же порошка, содержащего металлический алюминий в виде мелких корольков. Проводят анализ на азот и хлор. Проба на хлор дает отрицательный результат. Результаты анализа приведены в таблице. Измерение показателя диффузного отражения, выполненное в широком диапазоне длин волн с помощью приставки ЦЦО-1 и спектрометра СФ-26, показывает, что полученный порошок обладает спектром отражения, харак-

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ АЛЬФА-ФАЗЫ НИТРИДА КРЕМНИЯ МЕТОДОМ СВС | 2014 |
|
RU2550882C1 |
| СПОСОБ ПОЛУЧЕНИЯ НИТРИДА АЛЮМИНИЯ В РЕЖИМЕ ГОРЕНИЯ | 2013 |
|
RU2531179C1 |
| Способ получения раствора неорганического полисилазана в дибутиловом эфире | 2020 |
|
RU2745823C1 |
| РЕНИЙСОДЕРЖАЩИЕ КАТАЛИЗАТОРЫ ТРАНСАЛКИЛИРОВАНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ КСИЛОЛА | 2007 |
|
RU2412759C2 |
| Способ получения уксусной кислоты,этанола,ацетальдегида и их производных | 1979 |
|
SU1064864A3 |
| СПОСОБ СИНТЕЗА ВЫСШИХ ЭТАНОЛАМИНОВ | 2010 |
|
RU2573637C2 |
| УСТОЙЧИВЫЙ К ВОЗДЕЙСТВИЮ ТЕМПЕРАТУРЫ КАТАЛИЗАТОР ДЛЯ ОКИСЛЕНИЯ ХЛОРОВОДОРОДА В ГАЗОВОЙ ФАЗЕ | 2008 |
|
RU2486006C2 |
| СПОСОБ ПЕРЕРАБОТКИ НИТРАТНЫХ СОЛЕЙ | 2013 |
|
RU2522343C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСИДА ХРОМА (III) | 2011 |
|
RU2568112C9 |
| СПОСОБ ПОЛУЧЕНИЯ N, N-ЗАМЕЩЕННЫХ 3-АМИНОПРОПАН-1-ОЛОВ | 2009 |
|
RU2522761C2 |

СПОСОБ ПОЛУЧЕНИЯ НИТРИДА АЛЮМИНИЯ, включающий нагревание алюминия в смеси с хлоридом аммония в атмосфере азота, отличающийся тем, что, с целью повьшения степени чистотыконечного продукта и упрощения процесса, процесс ведут с протоком газа при поддержании молярного соотношения, хлорида аммония и алюминия 254-3,0, нагревание ведут до 550-695 К с вьщелением водорода и аммиака с последующей выдержкой образующегося продукта при температуре выше 1100,К.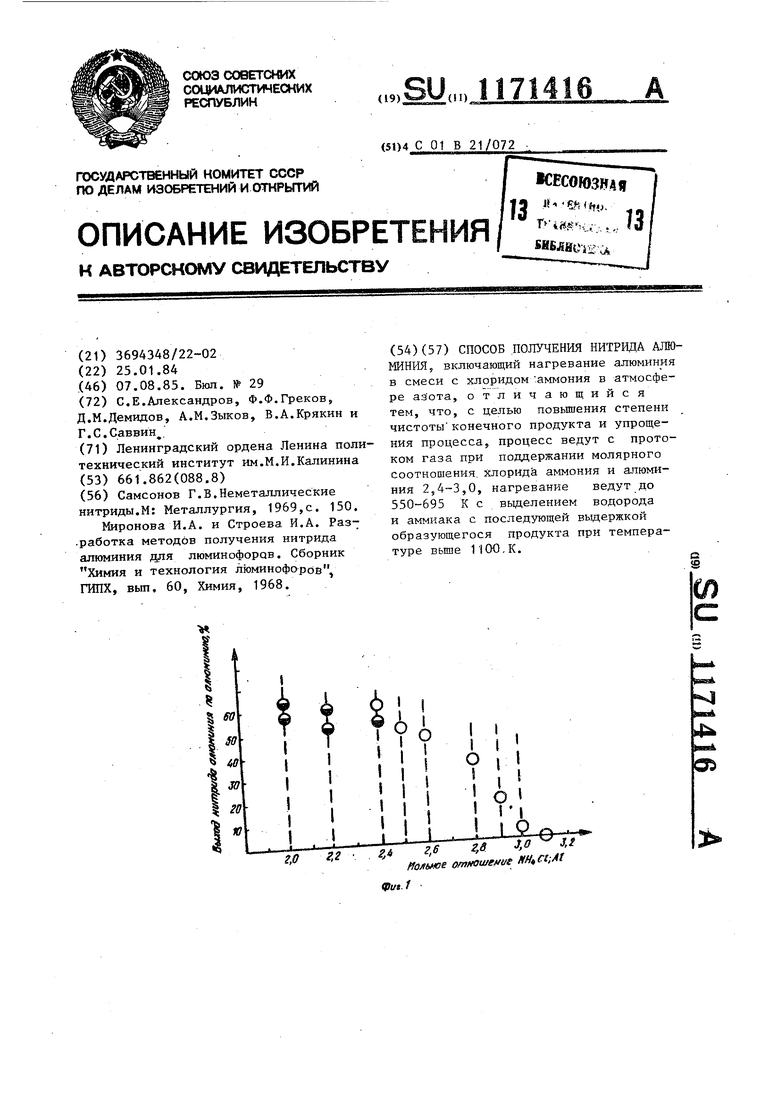
| Самсонов Г.В.Неметаллические нитриды.М: Металлургия, 1969,с | |||
| Деревянный коленчатый рычаг | 1919 |
|
SU150A1 |
| Миронова И.А | |||
| и Строева И.А | |||
| Раз.работка методов получения нитрида алюминия для люминофоров | |||
| Сборник Химия и технология люминофоров ГИПХ, вьт, 60, Химия, 1968. | |||
Авторы
Даты
1985-08-07—Публикация
1984-01-25—Подача