11
Изобретение относится к способу получения новых производных имидайолина общей формулы
(1)
где R, - метил, этил,Н -пропил, Н-пройенил, циклоалкенил C4-Cg или фенил, обладающих физиологической активностью.
Цель изобретения - синтез новых производных имидазолина, обладающих ценными свойствами.
Пример 1. Гидрохлбрид (2-метил-1,4-бензодиоксанил) 2-имидазолина..
; а) 2-Метил-1,4-бёнзодиоксан-2-карбоновая кислота.
Смесь (,23,7 г) 2-оксиметил-2-метил-1,4-бензодиоксана и 3-окси-З-меТИЛ-2Н-1,5-бензодиоксепина (соотношение приблизительно 3:1) перемещивают с 1 н.водным раствором гидроокиси натрия (135 мл) и охлаждают до . Медленно добавляют раствор перманганата калия (42 г) в вод (165 мл), так что температура поддерживается ниже 10 С. После 48 часовой вьщержки при комнатной температуре смесь фильтруют, фильтрат подкисляют 1М водной серной кислотой и экстрагируют метиленхлоридом. Экстракты промывают водным растворо бикарбоната натрия, водный слой подкисляют серной кислотой. Экстрагирование метиленхлоридом с последующей промывкой, сушкой и упариванием экстрактов дает карбоновую кислоту (11,5 г); т.пл. 125-129,5°С.
S) 2-Метил-1,4-бензодиоксан-2-.
-карбоксамид.
.
Смесь 2-метил-1,4-бензодиоксан-2-карбоновой кислоты (10,28 г) и тионилхлорида (7,8 мл), в безводном толуоле (40 мл) нагревают в течение 1 ч при 90-100 с. Удаление раствори теля и избыточного тионилхлорида в вакууме дает неочищенный карбонилхлорид, который медленно затвердевает. Раствор данного промежуточного продукта в безводном диоксане (25 мл) добавляют медленно к перемешиваемому водному аммиаку (d 0,88 26 мл) при охлаждении (0-10°С). Через 1 ч добавляют воду (300 мл), твердое вещество собирают фильтро)Ванием, промывают вбдой, а затем
62
сушат,.получают карбоксамид (8,3 г) т.пл. 127-128,.
2-Циано-2-метил-1,4-бензо- ; диоксан.
Перемешиваемую смесь 2-метил-1,4-бензодиоксан-2-карбоксамида (8,17 г), пятиокиси фосфора (17 г) и безводного толуола (175 мл) нагревают с обратным холодильником в течение 4 ч. При охлаждении поверх- . ностный слой декантируется с остатка, последний промывают декантацией дополнительным количеством толуола. Фильтрование и упаривание растворителя дает твердый остаток (5,18 г) Кристаллизация из этанола дает цианосоединение (4,4 г); т.пл. 88-89с.
J Гидрохлорид (2-метил-1,4-бензодиоксанил)3 -2-имидазолина.
Смесь 2-циано-2-метил-1,4-бензодио ссана (0,61 г), метилата. натрия (16 мг) и метанола (2,3 мл) перемешивают в течение 18 ч, получая почти чистый раствор. При охлаждении
до 0-10 С по каплям при перемешива,нии добавляют раствор этилендиамида (0,235 г) в метаноле (1 мл). Через несколько минут добавляют по каплям раствор хлористого водорода в метаноле (0,65 мл 5,6 М раствора), и смеси затем дают возможность подо- , греться до комнатной температуры. Спустя 16 ч смесь слегка подкисляют метанольным хлористым водородом и
фильтруют для удаления твердого вещества. Добавление дизтилового эфира к фильтрату дает твердое вещество, которое собирак1Т фильтрованием (о,84 г; 2 сбора). Перекристаллизация из смеси этанола и диэтилового эфира, содержащей хлористый водород, дает после сушки гидрохлорид
имидазолина; т.пл. 258-261°С (анаизируется в виде 1/4 гидрата).
П р и м е р 2. 2-|;2-С2-Этил-1 ,4-бензодиоксанил)-2-имидазолин.
а 2-Оксиметил-2-этш1-1,4-бензодиоксан.
Перемешиваемую смесь пирокатехина
(l4,0 г),. 2-этилэпихлоргидрина
(15,3 г), гидроокиси натрия (5,1 г) и воды (50 мл) нагревают при 90 С в атмосфере азота в течение 4 ч. При охлаждении добавляют воду, продукт
экстрагируют метиленхлоридом. Объег диненные экстракты промывают 2 н.водным раствором гидроокиси натрия, водой и солевым раствором, сушат
3
и упаривают, получая масло (10,8 г) ИКд(акс 3650-3200, 3000-2850 .
в) (2-Этил-1,4.-бензодиоксанил) -2-имидазолин.
Полученный 2-этил-бензодиоксан метанол превращают в соответствующее имидазолиновое соединение по примеру 1, После добавления метанольного раствора хлористого водорода по примеру 1 г большую часть растворителя удаляют в вакууме, остаток распределяют между водным раствором бикарбоната натрия,и этилацетатом, Сущка органической фазы с последующим упариванием растворителя дает твердое вещество, которое растворяют легким бензином (6080 с), получая свободное имидазолиновое основание; т,пл. 98-100 С.
Примерз. (2-Фенил-1,4-бензодиоксанил)}-2-имидазолин.
Пирокатехин и 2-фенилэпихлоргидрин вводят в реакцию, получая промежуточный 2-оксиметш1-2-фенил-1,4-беизодиоксан (по примеру 2а, который превращают в имидазолиновое соединение по примеру 26. Свободное основание перекристаллизовывают из легкого бензина (60-80с) ; т.пл. 114,5-116°С.
П р и м е р 4. (2- Изопропенил-1,4-бензодиоксанил) -2-имидазолин.а) 2-Циано-2- (l -окси-1 -метилэтил)-1,4-бензодиоксан.
Суспензию 2-циано-1,4-бензодиок{сана (40 г) и безводного карбоната (калия (176 г) в.ацетоне (500 мл) |пере1у ешивают и нагревают с обрат ным холодильником в течение 5 дн. Смесь охлаждают и неорганические соли удаляют фильтрованием. После упаривания ацетона в вакууме остаток распределяется между метиленхло РИДОМ и 2 н.водным раствором гидроокиси натрия. Органический слой промьтают 2 н.водным раствором гидроокиси натрия (2 раза), 5%-ной соляной кислотой, рассолом, а затем сушат пропусканием его через абсорбент из хлопка и шерсти. Упаривание в вакууме дает оранжевое масло (37 Требуемый нродукт вьщеляют пропусканием его через колонку из кремнезе,ма (ЗОО г) с использованием метиленхлорида в качестве элюента. Те фракции, которые по данным проверки с помощью тех имеют величину Rf 0,2 (СНСГз) объединяют и упаривают 7
75664
в вакууме, получая желаемое оксисоединение (14,5 г); т.пл. 63-69 С (18 г непрореагировавшего 2-циано-1,4-бензодиоксана регенерируют с 5 колонки) .
б 2-Циано-2-изопропенил-1,4-бензодиоксан.
Раствор указанного оксисоединения (0,80 г) в сухом пиридине (8. мл при
0 комнатной температуре обрабатывают добавлением по каплям хлорокиси фосфора (1 мл) на протяжении 5 мин. Раствор затем нагревают при 60-70°С в течение 18 ч, охлаждают и выливают
5 осторожно на смесь льда с водой. Смесь экстрагируют метиленхлоридом (3 раза по 50 мл), экстракты промы-- вают солевым раствором, сушат и упаривают, получая требуемое изопро0 пенильное соединение (0,62 г); Rf 0,75 (CHCF ).
в)(2-Изопропенил-1 ,4-бензодиоксанил) -2-имидазолин.
Указанное изопропенильное соединение вводят в реакцию с этилендиамином по примеру 1г-. После добавления метанольного раствора хлористого водорода большую часть раствори теля удаляют в вакууме , остаток расQ пределяют между водным раствором
бикарбоната натрия.и метиленхлоридом. Сушка органической фазы с последующим упариванием растворителя дает твердое вещество, которое перекристаллизовывают из легкого бензина (60-80°с), получая имидазолиновое свободное основание; т.пл. 108-110 С.
П р и м е р 5. (2-Изопропил-1,4-бензодиоксанил) -2-имидазолин.
0 Раствор (2-изопропенил-1,4-бензодиоксанил)} -2-имидазолина (0,80 г) в этаноле (О мл) с 10%-ным палладием на угле (80 г) гидрируют при атмосферном давлении и комнатной температуре в течение 6,5 ч.
Смесь фильтруют, палладиевые остатки промывают этанолом (2 раза по 10 мл) и объединеннные фильтраты упаривают досуха при пониженном .давлении. Полученное в результате твердое вещество (0,8 г) перекристаллизовывают из легкого бензина 6080 С), получая изопропилбензодиоксан (0,3 г); т.пл. 124-125°С.
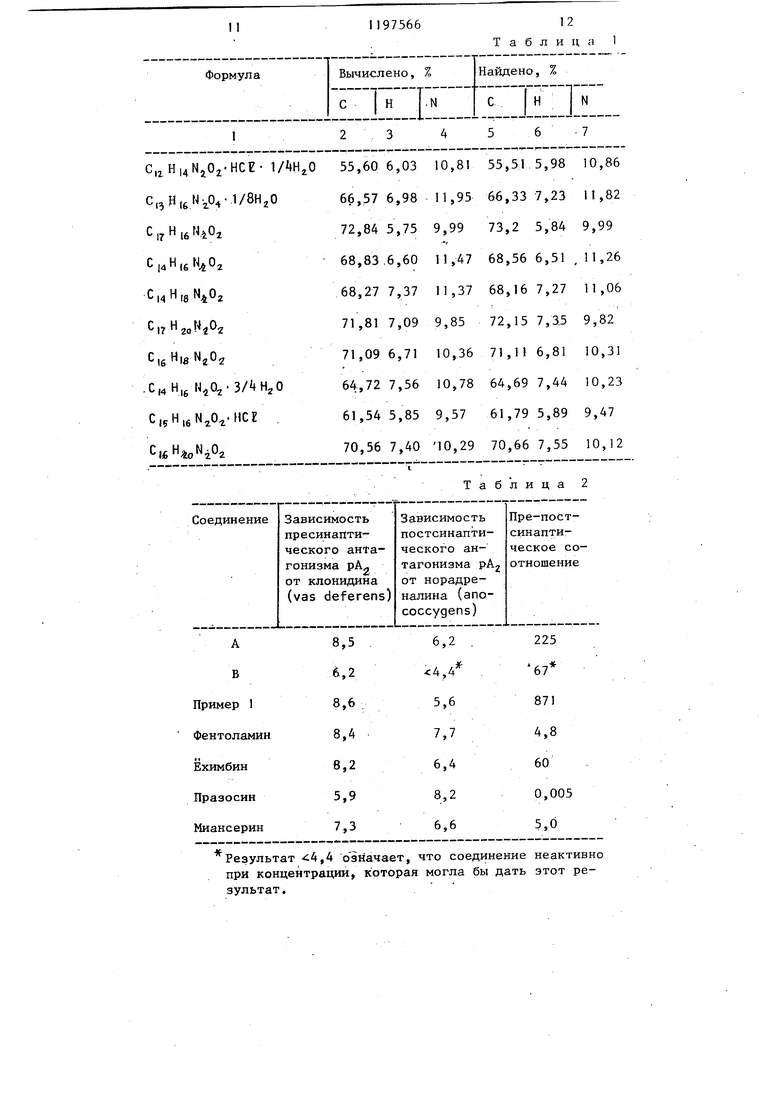
5 П р и м е р 6. (2-Циклогекс-1 -енил-1,4-бензодиоксанил) -2-имидазолин. Получают по примеру 4 с использованием циклогексанона вместо ацетона по реакции при примерно . Продукт имеет т.пл. 122-124 0. Пример. (2-Циклопен -1 -анил-1 ,4-бeнзoдиoкcaншI)3-2-имидaзoлин. Приготавливают по примеру 4 с ис пользованием циклопентанона вместо ацетона при проведении реакции при примерно 90 С. Продукт имеет т.пл. 83-85°С. . Примере. .(2-Пропил-1,4-6ензодиоксанил) -2-имидазолин. Приготавливают по примеру 2 с ис пользованием 2-н-пропилэпихлоргидрина приготовленного с помощью обработки .основанием 1-хлор-2-окси-2-хлорметилпентана, полученного по реакции н-пропилмагнийбромида с 1,З-дихлорацетойом в безводном толу оле) , продукт имеет т.пл. 113-115 С П р и м е р 9. Гидрохлорид (2-циклобут-1 -енил-1,4-бензодиоксанил) -2-имидазолина. Приготавливают по примеру 4с ис пользованием циклобутанона с тетрагидрофураном в качестве сорастворителя вместо ацетона с проведением реакции при приблизительно 65 С. Пр дукт имел величину Rf 0,38 (CHCfj) метанол 4:1 (объем/объем). П р и м 8 р 10. 2-{;2-(2-Циклопён тил-1 ,4-бензодиокс.анил)1 -2-имидазолин . Раствор (2-циклопент-1 -енш -1,4-бензодиоксанил)-2-имидазолина (0,50 г) в этаноле (10 мл) с 10%-ны палладием на угле (80 мг) гидрируют при атмосферном давлении и комнатной температуре в течение 3,5 ч. Смесь фильтруют, фильтрат упаривают досуха при пониженном давлении, получая коричневое масло (0,5 г). Мас ло распределяют между 2 н.водной соляной кислотой и диэтиловьш эфиром. Водный слой подщелачивают бикарбонатом натрия, а затем экстрагируют диэтиловым эфиром. ВысущенHjTo органическую фазу упаривают при пониженном давлении, получают твердое вещество (0,15 г), которое перекристаллизовывают из гексана, что дает твердое вещество (0,10 г), т.пл. .}35-136°С. Данные элементного анализа представлены в табл. I . Фармакологическую активность соединений, получаемых предлагаемым способом, определяют следующим образом. 1. Антагонизм пре- и постсинаптических tsf -адренорецепторов в экс- , Периментах с выделенной тканью. Антагонизм пресинаптического о 2 адренорецептора оценивают с; помощью определения величин рА по отношению к ингибиторным действиям клонидина, хорошо известного . агониста пресиноптического ,ренорецептора на вьгоодящих сосудах крыс, стимулированных при частоте О,I Гц. Данная модель in vitro является особенно полезной в качестве начального экрана для изучения пресинаптической активности в изоляции, поскольку физиологическая природа тканей выводящих сосудов такова, что постсинаптические рецепторы, расположенные в них, особенно недоступны для экзогенных агентов. Вследствие этого, для установления активности постсинаптического oi -адренорецептора используется альтернативная ткань, anococcugeus мьшца крыс. Антагонизм противодействий норадреналина используется , для определения величин pAg У постсинаптических о, -адренорецепторов. Соотношение антагонизма пресинаптического ЛJ-адренорецептора (по сравнению с клонидином на выводящих сосудах крыс) и антагонизма постсинаптического oi) -адренорецептора (в сравнении с противодействиями норадреналина на anococcugeus мьппце крыс) используется для оценки селективности адренорецептора. I В табл. 2 представлены данные испытаний соединения примера 1 и стандартных лекарственных препаратов: неселективного антагониста oi-адренорецептора фентоламина) , селективного пресинаптического антагониста (ёхимбина), высоко селективно|го постсинаптического антагониста (празосина) и антидепрёссанта (миансерина), который показывает свойства антагониста неселективного пре- и постсинаптического адренорецептора как часть его фармакологического профиля.Таблица дополнена результатами для известного соединения В формулы
9 сят с активностью соединения формулы А.
Постсинаптические исследования(е,
Как для исследований агонистов так и йнтагонистов, используют апоcoccygeus мьшщу крыс. Способность соединений вызывать противодействия мышцы anococcygeus отражает постсинаптическую активность агониста oti-адренорецептора. Активности соединений с контрактильными свойствами определяют в сравнении с фенильнином, который является селективным постсинаптическим O6f -адренорецепторным агонистом.
Антагонистическую активность проверяют с помощью определения ингибиторных действий соединений на противодействия, вызванные норадреналином, на anococcygeus. мышце.
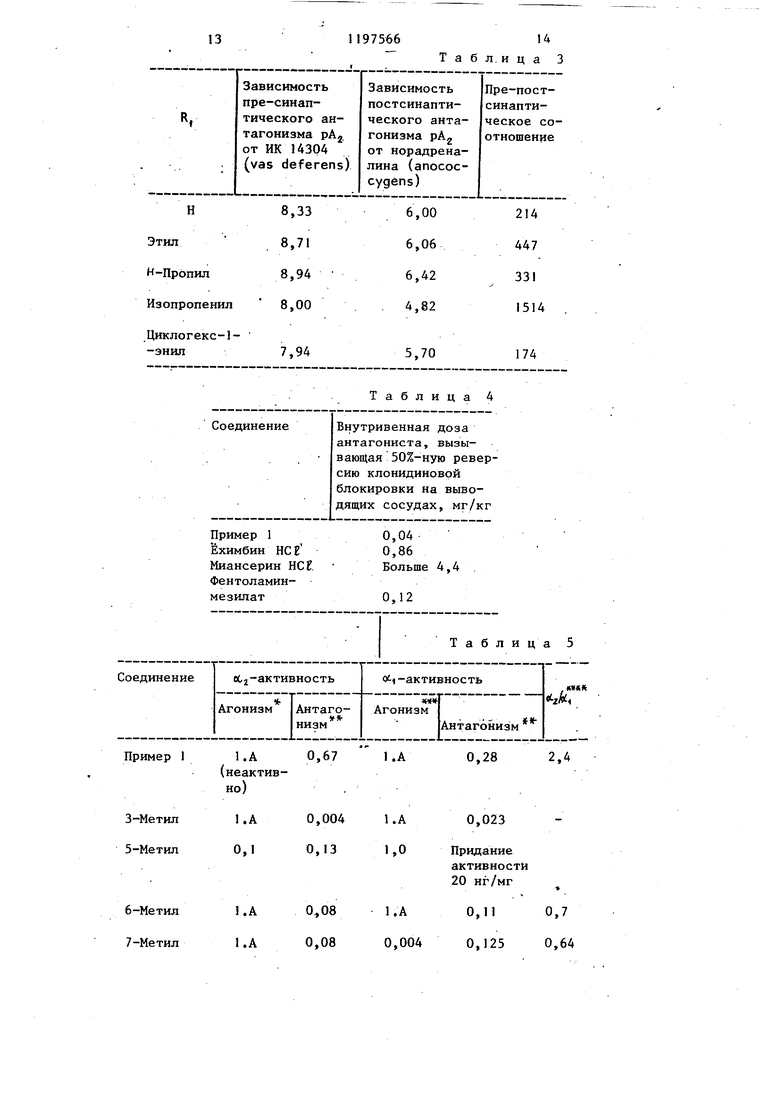
Результаты определений представлены в табл. 5, (первая колонка покзывает положение метильного заместителя в формуле А).
Из табл. 5 видно, что соединение примера 1 является более селективным (более чем в 2 раза) по сравнению с соединением формулы А. Ни одно из остальных семи соединений не является таким же селективным, как соединение формулы А, они, как 0 2 антагонисты, обладают значительно пониженной активностью. В некоторых случаях об2-агонизм становится признаком их профиля.
. Соединения формулы (1) или их нетоксичные соли используются при лечении депрессии. Способ лечения депрессии включает назначение людям противодепрессантно эффективного количества соединения формулы (Г) или его нетоксичной соли.
Фармацевтические композиции могут быть представлены в форме, подходящей для орального, ректального или парэнтерального назначения. Оральные композиции могут быть в виде капсул, таблеток,, гранул или жидких препаратов (эликсиры, сиропы или суспензии).
Таблетки содержат соединение формулы 1Г) или его нетоксичную соль в смеси с эксципиентами, кото9756610
рые являются, подходящими для производства таблеток. Этими эксципиентами могут быть инертные разбавители фосфат кальция, микрокристаллическая
5 целлюлоза, лактоза, сахароза или декстроза) , гранулирующие и дезынтегрирующие агенты (крахмал), связующие агенты (крахмал, желатин, поливинилпирролидон или камедь акации)
10 и смазочные агенты (стеарат магния, стеариновая кислота или тальк).
Композиции в виде капсул могут содержать соединение или его нетоксичную соль, смешанные с инертным твердым разбавителем, таким как фосфат кальция, лактоза или каолин, в твердой желатиновой капсуле.
Композиции для парэнтерального . назначения могут быть в виде стерильных инъецируемых препаратов, таких как растворы или суспензии, например, в воде, солевом растворе или 1,3-бутандиоле.
Для удобства и точности дозировки
композиции преимущественно применяют-ся в форме дозированных единиц. Для орального назначения формы дозированных единиц содержат 1-200 мг Гпредпочтительно 10-50 мг) соединения формулы (1) или его нетоксичной соли. Парэнтеральные формы дозиро-. ванных единиц содержат 0,1-10 мг соединения формулы (1) или его нетоксичной соли на 1 мл препарата.
35 Ниже приведены примеры композиций, в которых все части даны по весу.
Пример 1. Смесь 1 ч. гидрохлорида (2-метил- ,А-бензодиок40 санил) -2-имидазолина и 4 ч. микрокристаллической целлюлозы вместе с 1% CTeaipaTa магния прессуется в таблетки, которые содержат 10, 25 или 50 мг активного ингредиента.
45 Пример 11. Смесь 1 ч. гидрохлорида (2-метил-1 ,4-бензодиоксанил) -2-имидазолина и А ч. высушенной распылением о актозы вместе с 1 % стеарата магния заполняется в
50 твердые желатиновые капсулы, которые содержат 10,25 или 50 мг активного ингредиента.
Таблица 2





СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВ НЫХ ИМИДАЗОЛИНА общей формулы 1 где R -метил, этил,и -пропил,н пенил, циклоалкенил С4-Сб или фе ТЕНИЯ отличающийся темТ соединение общей формулы 11 , где RI - имеет указанные значения; R - метил или этил; ЫХ - хлористый водород, подвергают взаимодействию и спирте общей формулы по крайней мере с 1 молярным эквивалентом ятилендиамина с вьщелением целевого продукта или соединение формулы (l), где R -Н-пропенил, подвергают 1идрогенизации в присутствии катализаторапалладия на угле для получения соединения формулы (т), в которой Р./Ч-пропил. Приоритет по признг)кам: 30.01.81 - при RJ-метил, этил,К-пропил или н -пропенил. 28.07.81.- при R -циклoaлк и ш или фенил.
Результат AjA означает, что соединение неактивно при концентрации, которая могла бы дать этот результат.
Активность относительно клонидина 1.
-л
Активность относительно соединения формулы А Активность относительно фенилэфрина 1 .
#-IHt
Селективность относительно соединения формулы
| Эльдерфильд Р | |||
| Гетероциклические соединения, т | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Фотореле для аппарата, служащего для передачи на расстояние изображений | 1920 |
|
SU224A1 |
Авторы
Даты
1985-12-07—Публикация
1982-01-28—Подача