Изобретение относится к генетнче кой инженерии, а именно к получению г-мкроорганизмов, содержапшх генети- ческиГ код фермента термостойкой ал ь фа амил азы. Пример 1. Получение плазМИД, содержащих гены альфа-амилазы, стойких к антибиотику. Вся ДНК, содержащая гены альфаамилазы выделяется из леток штамма Bacillus stearotherraophilus АТСС № 31783 с помощью известного метода Бернса и Томаса. В соответст вии с предлагаемым способом клетки i-yi:no; M,inivioi(:H в смеси 50 мМ хлоргидрата тр ..с (оксиме1ил) аминометана (трис-НС1;, 0,6 мМ этилендиаминтетрауксусной кислоты (ЭДТК) и 25%-ног pacib.jpa сахарозы стандартного соляного цитрата при рН 8,0. Кроме того, клетки обрабатываются лизоцимом (2 мг/мл) в течение 1 ч при 0°С перед лизисом. Плазмида pBR 322 ДНК, фермент ограничения Hind III и ДНК лигаза фага Т4 получены из лаборачорий Исследовательского центра в Бета еде, Мэриленд, . Смесь 7,5/и г от всей ДНК штамма Вас. stcajothermophilus фермент ограничения Hind III и 10 /U г альбуми на сывороткибыка в 100 ju л раствора который содержит 50 мМ NaCl, 6 мМ при рН 7,5 и 6 мМ MgQ , инкубирую при 37С в течение Г 30 НИН. 2,2 щг ДНК-плазмиды pBR 322 и 7 единиц (Е) Hind Ш вывариваются в 20 m л того же раствора в течение 1 ч при 37 С, Анализ ДНК на агарово геле показывает, что процесс вывар ваш-1я закончен. Затем 6,75/иг обработанной ДНК Вас. stearothermophilus и l. обработанной ДНК pBR 322 смешиваютс ь 0,3 мл раствора, содержащего 6,6 Трио-НС 1 (рН 7,6), 6,6 мМ Mga2 , 10 мМ дитиотрейтола и 0,067 мМ триф сфата аденозина(АТП), и комбинируются с использованием 0,28 единиц ДНК-лигазы фага Т. Анализ на агаровых гелях ДНК после лигации показывает, что лигация завершена и оставшихся линейных молекул ДНК рВ 322 не обнаружено. Пример 2. Трансформация плазмид, содержащих гены альфа-амилазы и маркер, стойкий к воздействи антибиотика, в К, Coli. 53 Культура Е. со 1 i RH. , полученная в виде штамма PRC 399 из Центра видов плазмид. Медицинский центр Университета в Стэнформе, Калифорния, выращивается .в среде, содержащей г/л;; триптон 10,0; экстракт дрожжей 5,0 хлорид натрия 5,Оглюкоза ,0. Культура выращивается в пробирке в течение ночи при . Затем она разбавляется 9 частями такой же среды и инкубируется при 37°С еще в течение 135 мин при энергичном перемешивании. Клетки собираются центрифуг1-1рованием и промываются 0,1 М холодным раствором NaCl. Собранные клетки E.coli обрабатываются перед трансформацией в соответствии с известной процедурой, предложенной Козном и др. Половина ДНК, которую подверга ют лигации (получена в примере 1) переносится в клетки Е. со 1i RRI, Клетки культивируются на пластинках, содержащих ту же среду, на которой выраш 1вались клетки E.coli, за тем исключением, что среда содержит ампициллин с концентрацией 50 Л( г/мл. В результате получают только клетки E.coli, содержащие плазмиду pBR 322 (с генами, отвечающими за стойкость к ампициллину). В качестве средства для определения числа клеток, содержаш,их реконбинированнуш ДНК клетки, стойкие к ампициллину, анализируются на стойкость к тетрациклину. Так как введение фрагмента ДНК в участок рассечения фермента Hind III штамма pBR 322 в общем случае дезактивирует ген плазмиды, отвечающий за стойкость к тетрациклину, величина чувствительности к тетрациклину дает число клеток, содержащих рекомбинирова гную ДНК, имеющихся в популяции клеток, Трансформация дает 3,6 х Ю клеток, стойких к ампициллину, на миллиметр и 3,0 X 10 1слеток, стойких к тетрациклину, на миллиметр. Следовательно, примерно 16% клеток чувствительны к тетрациклину, что указывает на содержание в них плазьшд с рекомби- натной ДНК. Пример 3. Выделение колоний E.coli, синтезирующих альфа-ами- лазу. . Приготавливается среда того же состава, что использовавшаяся для выращивания E.coli, за тем исключе- нием, что добавляю1 15 г/л агара плюс ампициллин ( г/мл). Эта с;ре- да помещается на 130 пластинок Петри и на нее прививается разбавленная трансформированная культура Е.со 1i, полученная в примере 2. Эти пластинки дают в среднем 113 колоний на плас1ину. Колонии выращивают до тех пор,, пока они не достигают в диаметр примерно 1-2 мм, а затем копируют на пластинах с крахмальной средой следу ющего состава, г/л: 6; КН2РО 3, NaCl 0,5; 1; экстракт дрожжей 1, пептон 10; агар 15; крахмал Линтнера 10. После выращивания в течение 3 ч . на пластинки, покрытые средой, содержащей крахмал добавляется бактериофаг Т - АТСС № 11303-В4. Для высвобождения всех внутриклеточных ферментов используется примерно 1х. х10 Т на каждую пластинку. После выращивания в течение ночи и лизи- рования на пластинки наносится 2,5%- ный йодный раствор Люголя с целью обнаружения всех прозрачных зон, об- раз.овавшихся под действием активност амилазы. Из примерно 15 000 содержащихся колоний 18 колоний образуют прозрачные зоны, что указывает на присутствие амилазы. Колонии, проявляющие активность амилазы, подвергают копированию на пластинках, -и при этом вновь проявляется активность амилазы однако только после добавления бакте риофага Т4 к лизированным клеткам. Этот факт указывает на то, что амила за получена внутри клеток. Последующие эксперименты показали, что D-цик лосерин является эффективным для получения лизированных клеток, если этот препарат добавляется в среду с концентрацией 600 г/мл. Штамм Е.соИ RRI, содержащий вектор плазмиды pBR 322 с геном амилазы известен как АТСС № 31789. Пример 4. Трансформация плазмид, содержащих гены альфа-амила зы и маркер, стойкий к антибиотику, в штамме Е.соИ С600, АТСС № 23724. Выращивается культура E.coli С600 АТСС №23724, клетки собираются и по готавливаются к трансформации в соот ветствии с примером 2. Выращивается пять различных клонов амилазы, полученных как описано в примере 3, и рекомбинатные плазмид выделяютс:я ггри помощи счлндартной пропроцедуры осветления лизата Клевелла и Хелински. Частично очищенная ЦНК плазмиды суспендируется в смеси 10 мМ грпс -НС1 и 1,0 мМ ЭЛТК с рН 7,5 ггеред перенесением в клетки E.coli, обработанные- СаС, Эту ДНК подвергают анализу, устанавливая, что она стерильна. Таким образом, никаких колоний, синтезирующих амилазу, не может появляться из-за копирования клеток, введенных вместе с ДНК. Трансформирова 1ные клетки выращиваются на среде, содержащей ампициллин с тем, чтобы продолжали расти только клетки, содержащие плазмиды. При проверке колоний на активность амилазы устанавливают 100%-ную корреляцию между присутствием плазмид и активностью амилазы. Это указывает на то, что ДНК плазмиды трансформирует оба штамма E.coli-и превращает их в продуцентов амилазы. Таким образом, это не зависит от штамма, но требует для своего осуществления рекомбинатную плазмиду. Штамм E.coli С600, содержащий вектор плазмиды pBR 322 с геном амилазы, известен как АТСС № 31 788. Пример 5. Термостойкость альфа-ам шазы. Четыре амилазных клона, полученных как описано в примере 3, и одна контрольная культура E.coli RRI выращиваются в 15 мл среды, описанной в примере 2. Клетки растворяются добавлением D-циклосерина, а затем остатки клеток удаляются.центрифугированием. В жидкость, расположенную на поверхности, добавляют ацетат натрия и хлорид кальция с тем, чтобы получить концентрацию в 50 мМ и 2,5 мМ соответственно, рН доводится до 6,0. Растворы фермента помещают в пробирки с завинчивающимися колпачками, соединенными с лентой из тефлона. Рас1воры анализируют на активность аьшлазы, а затем выдерживают при 90 С в течение 45 мин. Активность амилазы определяют скоростью гидролиза крахмала, которая проявляется в скорости снижения способности окрашивать йод, измеряемой спектрофотометрически в соответствии с известной процедурой Б.У. Смита и Дж.Г.Роу. Контрольный штамм E.coli не обладает активностью амилазы. С целью получения стандартов термостой-
K0(,:-il-: Н КС)НТрОЛ1 ПЫЙ ЛИЗЛТ Е . СО 1 1
добаялякпч;я очищенные амилазы из 5ас , ;-. l-oarothermophilus АТСС № 31783 ,, v-MVii, П i г, полученной от г}ирмы Сигма Кемнкэл Ко,, Сент-Луис, Миссури, под наименотзаннем Сигма А6380 и термамил терьюстойкая альфа- амнлачу, полученная из Лабораторий Ново Инк., Уилтон, Конн,
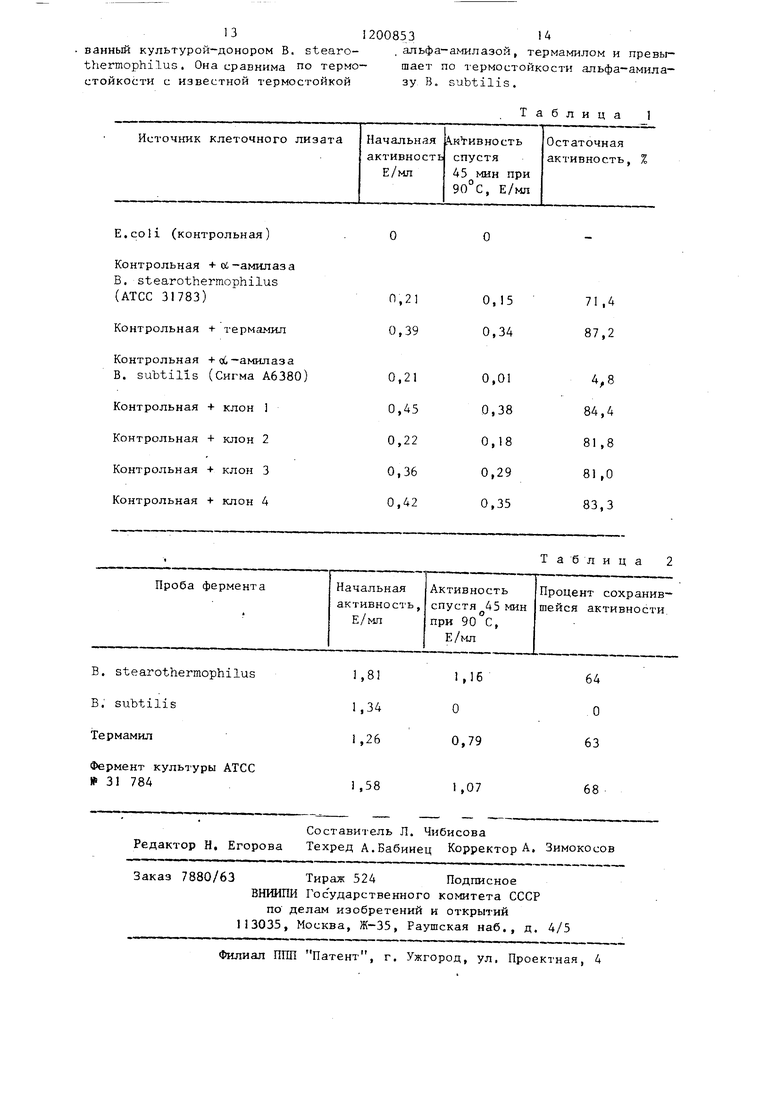
Резу-пьтаты испытаний приведены в i4i6js, .
Амилаза, синтезированная клонами, столь же термостойкая, как и фермент, синтезированный донором В. ste- V 1Г1 Г:;}1кП-1з , Она сравнима по ге.)( t: ныпускаемо про- Mi.iuj.U-HHOc; Ifj-c чермостойкой альфа-ами- .чазоГ) теТрамилом и превосходит по герМ/стойкости ал)зфа-амилазу , котора (мппезируется в промышленных масштабах культурой В. subtilis,
Гидролизаты, полученные в резуль- чате обработки крахмалом каждой из амилаз анализируются при помощи тонкослойной хроматографни с тем, чтобы установить количество сахаров с низким молекулярным весом. Относи- 1 ельное количество сахаров с HHSKHN молекулярным весом, образовавшихся Б результате воздействия амилаз, синтезированных клонаь-ш E.coli, аналогично тем количествам сахаров, которые получены при воздействии извест1й11х альфа-амилаз , использовавшихся в качестве ко трольнь х.
Полученные результаты показывают, что ген термостойкого фермента, по- лучеиньш из крайне термофильных организмов, хорошо копируется в мезо- фильном бактериальном хозяине и дает термостойкий ферментный продукт, Таким образом, установлено, что ген из крайне гермофильных бактерий можно копировать в мезофильных бактериях с использованием методов рекомбина - ных ДИК. Кроме того, синтез активного термостойкого фермента осуществляется при нормальных мезофильных тег-пгературах (приблизительно 20-40 С1
Пример 6. Выделение естественно встречающихся плазмид, содержащих гены альфа-амилазы.
Вся ДНК выделяется из клеток Вас. stearothermohilus АТСС № 31783, как описано в примере 1, ДНК плазмиды отделяется от всей ДНК при помощи ультрацентрифугирования с использованием хлорида цезия, этидийбромкда и
известной проце; 1,у1зы, П 1 д11ожрипой Р. Рэдлос1х}1ом , У.Бау)ром и Л-к . Р/ияо градом.
Тот факт, что ilHlv rvruii гпазмиды содержит Го.н альфа-амилазы, установлен следующим образог-, ЛИК гтлазмиды рассекается при помсмцн ферг- ента рестрикпии i-.itid как и в ре 1 . Тиюны получают путем ,сния этой ДНК в Е, col: агиалогично примерам 1-3. Апа.чиз фепот1-П1а CTOIIKOсти к четрацик.гппгу пшсазал, что 3,3% клеток чувств1 тельиы к- тетрациклину и, следовательно, содержат клонированную ДНК. Поосеиванне клеток отгюсителыю актигзности альфамилазы показало, что 0,42% или примерно одна из ка}:{Д15Гх восьг-и клеток, содержащих клоннронаппую ЛНК, имеет ген амилазы. Рассечение плазмлд) В. Б1еаго1:пеГ1Г;О :)1 Низ при помоки Kind ITT дает )ie фрагменты ДИК, которые разделяются n;.i восемь легко обнар г;клвае1-ых полек: при электрофореза па агаропсь; геле. Частота клонировапия куска а;- илазы (I/B) равна приблизите.плк) ол-атдаемой, если одна из восьья преобладающих полос содержит геп амплазы. Анализ таких полос плазмиды показывает, что о,дпа из полос соста1 ляет примерно 3,6 Мд, т.е. это TITT же размер, что и клонггровапные куски ДНК, которые получень при апа.лизе плазмида примера 1 ,
Этот экспериьепт показьп.иает, что по крайней мере один геп ;и1ьф 1амилазы расположен на естествснпо встречающейся плазмиде в используемом штамме В. stea-rotTiermcTihilns,
Пример 7. Получение и выделение штаммов Е , со 1 i , с:одержаи, различные гибридные плазмиды.
А, Культура производящих амилазу E.coli, выделенная как описано в примере 3, АТСС № 31 789, выращиваеся в течение ночи в среде, используемой в примере 2, ДНК плазмидгл усилвается при noMOiiiii известной процедуры Клевелла Д.Б. с использованием хло)амфеникола на миллиь етр. Для усиления используется следующая среда, г/лТ Ha iiJ-Q,, 6,0; 3,0 NaCl 0,5; . 1 ,0, ,казеиновые аминоки слоты 5,0, глюко з а 2,0, CaClj 2 0,015, -/П 0,246, витамин Б, 0,001.
ДН( плазмиды затем выделяется при помощи сталдартного метода осветления лизата Клевелла и Хелинс- ки. Изолированные плазмиды подвергаются очистке при помощи этидийбро МИДа, CsCl методом примера 6, а затем при. помощи экстрагирования изопропанолом и глубокого диализа в 10 мМтрис -НС1 плюс 1 мМ ЭДТК с рН 7,5..
Культура E.coli RRT, PRC 399, содержащая 3,9 Мд, плазмида рВР 325 выращивается, а ДНК плазмиды усиливается, вьщеляется и подвергается очистке указанным методом.
ДНК двух полученных плазмид рассекаются ферментом рестрикции Hind III. Растворы рассеченных плазмид смешиваются и подвергаются лигации при О С в течение 18 ч с использо- ван.ием общей процедуры примера 1 ,
ДНК после лигации переносится в E.coli RRI при помощи метода, описанного в примере 2. Клетки разбавляются и наносятся на агаровые пластинки, содержащие хлорамфеникол с концентрацией 20шг/мл, В результате этой процедуры получают клетки E.coli, содержащие только плазмиду рВН 325 (с генами, отвечаюк1ими за стойкость к хлорамфениколу). Коло- 1даи клеток, которые при этом получают, просеивают на активность амилазы при помощи метода, описанного в примере 3для растворения клеток используется 1)-циклосерин.
Рекомбинакгная ДНК плазмиды из трех колоний, которые обладают активностью амилазы и проявляют стойкость к хлорамфениколу5 экстрагиру- ется осветлением лиэата, описанным в примере 4, Выделение рекомбинатных плазмид на агаровых гелях показало, что они имеют ожидаемый размер для комбинации плазмиды рВ 325 плюс 3,6 Мд фрагмента, содержащего ген амилазы. Воздействие на плазмиду ферментом Hind TIT дает 3,6 Мд фрагмента и линейную форму плазмиды pBR 325. Это говорит о том, что ген амилазы может повторно копировася на различных векторах, рВН 325, не теряя своей активности по синтез амилазы. Полученный штамм E.coli известен как АТСС № 31 792,
Б. Гибридная плазмида, стойкая хлорамфениколу и ампициллину, полученная в части А, используется в качестве донора фрагмента ДНК, которьш содержит ген альфа-амилазы. Этот фрагмент соединяется с 10 Мд плазмиды вектора BpWL 625 указанным в части А ме/одом. Плазмида pV/L 625 описана У.Гоебелем и др. Она может быть выделена из культуры штамма E.coli АТСС № 31787 при помощи процедуры выделения плазмиды, использованной в части А. Этот вектор наделяют стойкостью к антибиотикам, ампициллину и канамицину. Введение ДНК в pWL 625 в область Hind ITT разрушает стойкость к канамицину.
Клетки E.coli RRI которые трансформированы введением рекомбинатной ДНК, выращиваются на агаровых пластинках, содержащих ампициллин. Те колонии, которые обладают стойкостью к ампициллину, но не обладают стойкостью к хлорамфениколу из-за присутствия pBR 325, и проявляют акт ивност амилазы отбираются для анализа. ДНК плазмиды выделяются из колоний. Анализ на агаровых гелях перед и после воздействия фермента Hind TIT показал, что фрагмент ДНК, содержавш ген амилазы, копируется на плазмиде pWL 625 и дает новую плазмиду. Штамм E.coli, содержащий такую гибридную
плазмиду известен как АТСС № 31791.
%
Пример 8. Трансформация двух различных гибридных плазмид в одном штамме E.coli.
Выращивается ппамм E.coli, синтезирующий амилазу, полученный в примере 7Б; затем он подготавливается для трансформации при помощи-процедуры примера 2. Очищенная плазмида полученная в примере 7А, трансформируется в этих клетках. При выращивании полученных на агаровых пластинах содержащих хлорамфеникол, все колонии проявили активность амилазы. ДНК плазмиды вьщеляют из одной из колоний и анализируют на агаровых гелях. Установлено, что присутствуют обе Гибридных плазмиды, описанные в примере 7А и 7Б. Этот эксперимент показывает, что культура E.coli может продолжать расти и содержать одновременно две различные гибридные плазмиды, содержащие гены альфаамилазы. Стабильность в течение продолжительности времени этой комбинации не определялась. Штамм E.coli, содержащий эти две гибридных плазмиды, известен как АТСС № 31790 I p и м e p 9. Граигформппия r Jia4Nni;i, содерЖгПцих гчиы а ьфа-амилазы и маркер, cTOtiKHX к антибиотику в пггаммо И, ;Г.;11Пт.. Л. Получение донора ДНК, Гибридная нллзмида, полученная в примере 7К, используется в качест донора фрагмента ДНК, который содер жит ген ал,фа-а п1лаяы. Он экстрагируется при помощи процедуры ocBej.-ie ния лизата Клеве.чла и Хелински, ДНК этой плазмиды рассекае1ся ферментом рестрикции Kind TIT. lloлyчeF нь й про дукт смешивается с небольшим коли- чесугвом бромида зтидия и выделяется с использованием известного метода градиента сахарозы, предпожешюго Эл-Гьюли и Хелли} гом, 3,6 Мд фрагмен содбржащий ген альфа-амида;.ы, дважд экстрагируется н-бутиловым спирчом,, осаждается равным объемом изодроцпдового спирта и с успендируется в см си 10 м-М т рис плюс 1 мМ ЭДТК с рН о 7,8, выдерживается при -20 С перед использованием. Б, Получение вектора (nepeHOC4HK Штамм р., subtil.is, полученньй из Генетического центра хранения бацил Факультета микробиологии Университета штата Oraiio под названием штам № 1Е17, содержащий 2,0 Мд цлазмиды рС 9А, который содержит ген, выделяющийся стойкостью и хлорамфеникол наносится полосами на пластину, содержащую триптический соевьш агар Дифко, цодученный из лабораторий Дифко, Детройт, Мичит ан и 50 п г/мл хдорамфеникола. Далее клетки прививаются на 150 мл бульона Пенассея (Дифко) в 1-литровой колбе и выра- щиваются в течение ночи при 37 С пр встряхивании. Клетки гранулируются и вновь суспендируюяся в 10 мл протопластного буфера 25% сахарозы, 0,1 М Nad - 0,05 М трисНС при рН 7,5 и 0,05 М ЭДТК при рН 8,3), 5 мг монтежю белого лизоцима (Сигм Кемикэл Компани) добавляется на 30 мин при 37С, Затем энергично перемешиваются13 мл 2%-ного раствора додецилсульфата натрия в 0,7 М NaCl, а затем 2,5 мл 5 М раствора NaCl, Смесь охлаждается в ледяной воде и центрифугируется с; ускорением 12 1000 X g в течение 20 мин. ДНК осаждается равным объемом изопропилоЕОго спирта. Твердый остаток вьщерживается в ледяной воде в течение 60 ч. чатем с:обирастся цеитрифу ир1)ваннем и суспеггдиругч с.я в раствор, содержащий 0,01 М тоне хлоргидрата и 0,001 М ЭДТК при рП 7,5, ДНК плазмиды выделяется при помощи ул1-трацентрифугироваиия, с использованием бромида эт-идия, CsCl методом Радлоффа и др, 2 Мд плазмиды обрабат 1вается экстрагированием изо- цропиловым спиртом и глубоким диализом в 10 мМ трис плюс 1 мМ ЭДТК при рН 7,5, В. Получение гибридной плазмиды, 2 Мд-вектор части Б рассекается при помощи фермен1-а рестрикции Hind 11 и смешивается с 3,6 Мд фрагмента ДНК части А, Концентрация вектора и донорной ДНК 5 и 17,01 г/мл соответственно, Дигация ос .уще.стпляе ся как и в примере 1, Отсутствие каких-либо линейных 3,6 Мд-фрагментов после лнгации (этот факт устанав::ивается при помощи электрофореза на агаровом геле) указывает на то, что лигадия завершена. Г, Трансформация гибридной плазмиды в В, subtilis. Культура В, subtilis, АТСС № 31735, которая не содержит гена амилазы, выращивается в течение ночи на дластинке, содержащей агар на основе триптоза крови (Дифко и 1 %-ный раствор растворимого крахмала. На пластинку добавляется 2 мл среды для выращивания следующего состава, %: CNH 0,2V К2НР04 1,4; 0,6; цитрат натрия 2Й О 0,1; М) 1-. 0,12; глюкоза 0,5; казеиновые аьшнокислоты (Дифко 0,02 Г,-триптофан 0,005, Примерно 0,1 мл суспензии клеток, полученной таким образом, добавляется в 10 мл той же среды :в 250 мд колбе и инкубируется при 37°С энергичном церемешивании в течение А ч. Затем 1 мл культуры юбавдяется в 9 мл предварительно нагретой среды ддя трансформации при 37 С и инкубирование при встряхивании продолжается в течение 90 мяк. Среда для трансформации является той же, что и среда для роста, за тем исключением, что она содержит 0,01%-ный раствор казеиновых аминокислот и 0,0005%-ный раствор L-трицтофана, В 0,25 мп культуры клеток с плотностью примерно 1х10 кл ток/мл добавляе1ся 5/ц л раствора гибридной плазмиды части В, содержащей 0, плазмиды. Смесь энергично встряхивается при 37°С в течение 30 мин. разбавляется равным объемом бульона Пенассея (Дифко) и встряхивается при еще в течение 90 мин Порция клеток в 0,1 мл наносится на пластинки, содержащие агар на основе ,триптона крови (Дифко , %-ный раствор растворимого крахмала и хлорамфенила, В качестве контрольных проб клетки B.-subtilis без плазмиды и клетки В. subtilis с вектором плаз- МИДЫ рС194 наносятся на ту же среду. Ни одной колонии не было отмечено на пластинках, где клетки не содер- жали добавляемые плазмиды. Три колонии отмечены на пластинках, где клетки содержали плазмиду рС194, но ни одна из колоний не проявила активности амилазы, Одна колония отмечена на пластинках, на которые нанесены клетки, содержащие гибридную плазмиду ДНК част В. Она дала прозрачную зону при воздействии паров йода,Это указывает на то, что клетки синтезируют внеклеточный фрагмент амилазы. Оказалось, что клетки требуют присутствия хлора феникола для стабильности. Эта культура известна под названием АТСС № 31786. Проба ДР1К колонии, содержащей амилазу, вьщеляется при помощи электро™ фореза на агаровом геле. Отмечена полоса плазмиды в примерно 5,6 Мд. Это соответствует размеру гибридной плазмиды из части В. t Очищенную гибридную плазмиду рассекают ферментом рестрикдии Hind III и подвергают электрофорезу на агаровом геле. В результате получают два фрагмента примерно 2,0 и 3,6 Мд, Они соответствуют размерам донорной ДНК части А и ДНК вектора части Б. D. Трансформация гибридной плаз- МИДЫ во втором штамме В. subtilis. Гидридная плазмида, содержащая ген амилазы, выделяется из клеток ко лонии, синтезирующей амилазу, из части В, при помощи процедуры, которая использовалась для выделения плазмир рС194 в части Б, Выделенная гибридна плазмида трансформируется в другом амилаза-oтpицaтeльнo i штамме В. subtilis (штамм № 1А289) , полученном из Генетического центра хранения бацилл, факультета микробиологии, Университета штата Огайо,Трансфор 12 3 мация осуществляется при помощи известного метода слияния фотопласта, предложенного С.Чангом и С.Н,Козном, В результате выращивания клеток на часпластинках методом, описанным в ти Г, зафиксировано примерно х10 кблоний/мл на пластинках, не содержащих хлорамфеникола. Зафиксировано также примерно -1x10 колоний/мл на пластинках, содержапшх хлорамфеникол. При помощи испытания крахмал - йод, установлено, что все эти колонии содержат амилазу. Такие, содержащие амилазу В. subtilis известны под названием АТСС № 31784. Пример 10, Термостойкость альфа-амилазы, синтезированной штаммом В. subtilis, содержащим гибридную плазмиду. Клетки В, subtilis, содержателе гибридную плазмиду, из примера 9Д, АТСС № 31784, выращиваются в 1 л среды в 2,8-литровой колбе Фернбаха с использованием среды следующего состава, %: кукурузный крахмал 9,0, кукурузньп насыщенный ликер 6,OJ ауто- зилат дрожжей (примекс-154, полученный из лабораторий Амбер Джуно Висконсин) О,35; ( 1,0; 0,1; 0,06; МпС,,-4F20 0,05; кукурузное масло 1,0; термамил О.,05 Е/мп. Среда выдерживается в автоклаве в течение 30 мин при температуре , которая разрушает активность термамила, а затем охлаждается до комнатной температуры. Далее, в среду перед прививкой культуры клеток добавляется 0,01 мг хлорамфеникола на миллилитр. Бульон центрифугируется и термостойкость испытывается с использованием разбавленной пробы верхнего слоя жидкости и общей процедуры примера 5, Для сравнения измеряют также термостойкость амилазы культур В. stearothermophilus,В, subtilis, а также известной амилазы термамил в среде для инкубирования, содержащей 50 мМ ацетата натрия и 2,5 мМ CaCJ2(3TO амилазы, использо- вавщиесЯ для сравнения в примере 5, Результаты испытаний приведены в табл. 2, В этом испытании амилазы, синтезированная клоном Б. subtilis АТСС № 31 784, обладает не меньшей термостойкостью, чем фермент, синтезиро-
1312008531
ванный культурой-донором В. stearo-.альфа-амилазой, термамилом и превьгthermophilus. Она сравнима по термо-шает по термостойкости альфа-амиластойкости с известной термостойкой
зу в. subtilis.
Таблица





СПОСОБ КОНСТРУИРОВАНИЯ ГИБРИДНОЙ 1ШАЗМИДЫ, СОДЕРЖАЩЕЙ ГЕНЕТИЧЕСКИЙ КОД ТЕРМОСТОЙКОЙ АЛЬФА-AMfflAЗЫ, включающий гидролиз донорной ДНК эндонуклеазой для получения линейной последовательности ДНК с кодирующим альфа-амилазу геном, гидролиз эндонуклеазой редипиентного вектора для получения второй линейной последовательности ДНК соединение линейных последовательностей ДНК с помощью ДНК-лигазы, причем в качестве донор- ной ДНК Используют природные или гибридные плазмиды из штаммов Bacillus stearothermohilus .АТСС № 31195, 31196, 31197, 31198, 31199, 31783, а в качестве реципиентного вектора используют плазмиду, выбранную из группы плазмид, включаюi ,щих pBR 322, pBR 325, pWL 625, и рС 194, из эндонуклеаз используют (Л эндонуклеазу Hind III, а из ДНК-ли- с: газ - ДНК-лигазу фага Т., ь 
E.coli (контрольная)
Контрольная +oi-амилаз а
В. stearothermophilus
Таблица
| Прибор для записи продолжительности рабочих операций | 1924 |
|
SU1929A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| ГОРЕЛКА ДЛЯ УГОЛЬНОЙ ПЫЛИ | 1925 |
|
SU6694A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
Авторы
Даты
1985-12-23—Публикация
1982-01-14—Подача