11
Изобретение относится к аналитической биохимии, а именно к способам измерения, использующим ферменты, и может быть использовано для определения содержания глюкозы в автоанализаторах, применяемых в микробиологической промышленности и медицинской практике.
Цель изобретения - повьпиение точности определения глюкозы.
Способ осуществляется путем введения в отдельно приготовленные растворы глюкозооксидазы и каталазы в ацетатном буфере порознь окислителя - пеоиодной кислоты или ее солей в массовом соотношении фермент -окислитель 1:(О,1-0,7), затем низкомолекулярные примеси отделяют и растворы .каталазы и глюкозооксидазы в соотно - шении 1:1 по активности смешивают с этанолом.
Согласно предлагаемому способу в реактив вводят отдельно приготовленные растворы окисленной глюкозооксидазы и катализы в эквивалентных по активности количествах в отличие от известных способов, где каталаза в реактиве отсутствует или содержится только в виде примесей. При предварительной обработке каталазы и глюкозооксидазы периодной кислотой или ее солями окисляется углеводный компонент ферментов, что стабилизирует сам фермент. При этом ферментный реактив очищен от низкомолекулярных примесей которые проникают через мембрану в анализируемую среду.
Эти условия получения реактива обеспечивают продолжительность эксплуатации его без снижения точности измерений содержания глюкозы при непрерывной продолжительной работе автоанализатора. Способ иллюстрируется примерам5 конкретного получения реактива и-испытания его в условиях непрерывного автоматического режима.
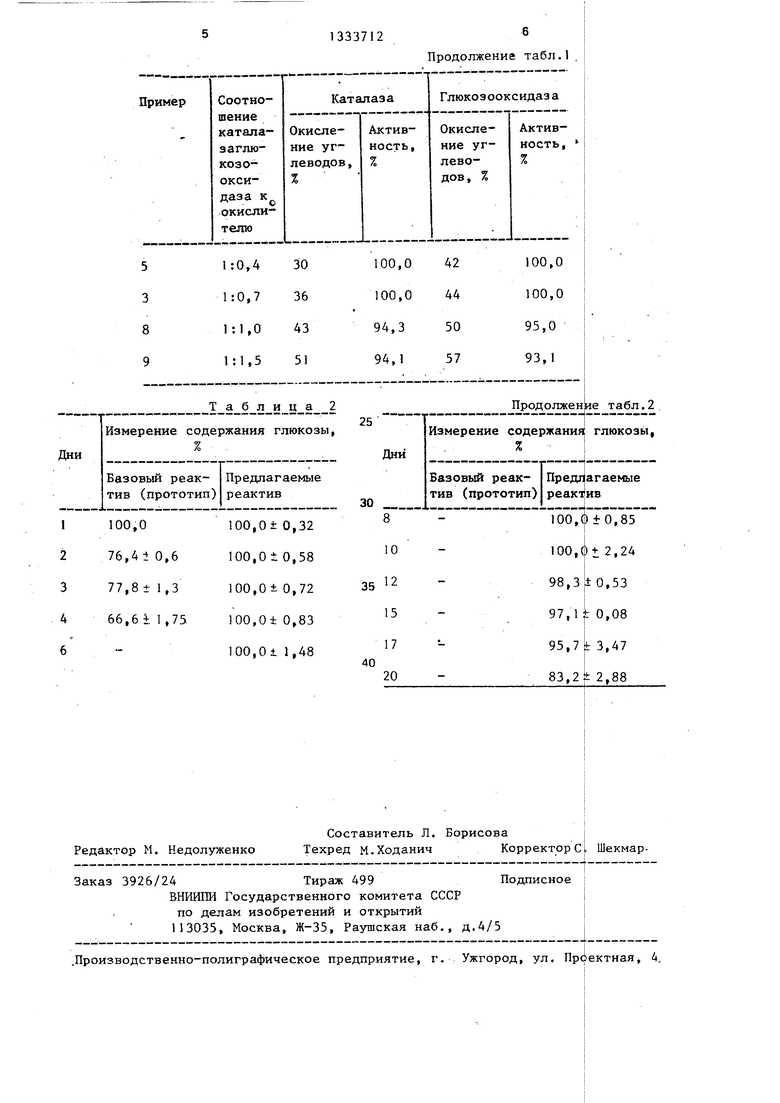
Подбор условий стабилизации ферментов глюкозооксидазыи каталазыпредставлен в табл. 1 , где в примерах 6-9 преставлены запредельные значения соотношений фермент-окислитель.
Пример 1. 400 мг глюкозооксидазы, соответствующих 100000 единиц активности, растворяют в 40 мл 0,05 М ацетатном буферном растворе рН 5,8, добавляют 18,4 мл 0,5%-ного КЛОц (92 мг) (соотношение 1:0,25), смесь перемешивают и инкубируют 3 ч при 4-8 С. Затем прибавляют 0,042 мл
0
5
0
25
37
30
122
этилёнгликоля, 30 мин перет шшивают и диализируют для удаления нйзкомоле- кулярных примесей. 40 мг каталазы, соответствующих 100000 единиц активности, растворяют в 4 мл 0105 М аце- татном буферном растворе рЫ 5,8, добавляют 1,84 мл 0,5%-ного JO (9, 2 мг) при этом соотношение фермент - окислитель равно 1 :0,28, перемешивают и инкубируют 3 ч при 4-8 С. Затем прибавляют 0,004 мл этршенглико.- ля, 30 мин перемешивают и диализируют для удаления низкомолекулярных примесей. Растворы глюкозооксидазы и каталазы в соотношении по активности 1:1 смешивают с этанолом до конечной концентрации этанола 25%. |
П р и М е р 2. 400 мг глюкозооксидазы, соответствующих 100000 единиц активности, растворяют в 5Ш мл 0,05М ацетатном буферном растворе рН 5,8, добавляют 8 мл 0,5%-ной ,0 (.40 мг) (соотношение фермент - окис-, литель 1:0,1) и далее операции повторяют по аналогии с примером 1,40 мг каталазы, соответствующих 100000 единиц активности, раствор |;ют в 5 мл 0,05 М ацетатном буферном {Растворе рН 5,8, добавляют 0,8 мл Oj5%-Horo HJO -2HjO (.4 мг). Последун)щие операции повторяют по аналогии с цриме- ром I .
Пример 3. 400 мг глюкозооксидазы, соответствующих 10ФООО единиц активности, растворяют в 30 мл 0,05 М ацетатном буферном iJiacTBOpe рН 5,8, добавляют 28 мл 1%4ного
NaJO
3H,;,0
(280 мг), соот
ношение фермент-окислитель равно 1:0,7 и далее операции повторяют по аналогии с примером 1. |
40 мг каталазы, соответствующих 100000 единиц активности, 1)астворяют в 3 мл 0,05 М ацетатном буферном растворе .рН 5,8, добавляют 2J8 мл 1%-ного NaJ04-3H20 (28 мг). Последующие операции повторяют по аналогии с примером 1.
При соотношении фермент4 к окислителю 1: (0,1-0, 7) окисдяется около 30% углеводов фермента при | сохранении 100%-ной активности. У1 еньшение соотношения фермент - окис11итель менее 1:0,1 (примеры 6 и 7) Ие обеспечивает достаточного окисления углеводов и, следовательно,необходимой стабильности. С увеличение - количест
1
ва окислителя болбе 1:0,7 (пример 8 и 9) процент окисленных углеводов растет,-НО при этом уменьшается активность фермента. Экспериментально доказано, что дальнейшее увеличение концентрации окислителя не способствует интенсификации окисления углеводов при одновременной потере каталитической активности фермента.
Сравнительные испытания ферментных реактивов, приготовленных по предлагаемому и способу-прототипу, принятому в качестве базового и применяемого на анализаторе Glucose Analizer-2 фирмы Бекман, проводил в автоанализаторе АКГ-01 при измерении концентрации глюкозы в модельном растворе глюкозы 1 г/л с периодичностью 36 мин В течение 20 сут.
Испытания показали, что благодаря использованию предлагаемого реактива значительно увеличивается время непрерывной работы без снижения точност .показаний (табл.2).
Измерения содержания глюкозы на 6-й день и далее по базовому реактиву в связи со значительными погрешностями не проводили.
Как видно из результатов испытаний на 2-е сут точность измерений у базового объекта падает на 24%, а у предлагаемого сохраняется еще на 17 сут (допустимые потери ±5%).
Использование реактива, полученного согласно предлагаемому способу.
1:0,025О
1:0,055
1:0,127
1:0,231.
1:0,2533
0
15
37
о
0
5
5
12
обеспечивает значительное повьш1ение точности измерения содержания глюкозы при непрерывйом проведении анализов благодаря стабилизации реактива, а также возможность использования автоанализаторов глюкозы для контроля в процессах ферментации, продолжительность которых исчисляется несколькими сутками с соблюдением условий герметизации.
Реактив, полученный согласно изобретению, может быть использован в процессе биосинтеза антибиотиков.
Формула изобретения
Способ получения реактива для количественного определения глюкозы в растворе, предусматривающий приготовление ферментного раствора глюкозо- оксидазы и каталазы в ацетатном буфере в заданном соотношении и смешивание с одноатомным спиртом, отличающийся тем, что, с целью повышения точности непрерывного определения глюкозы, одновременно готовят растворы глюкозооксидазы и каталазы в ацетатном буфере, вводят в них пе- риодную кислоту или ее калиевую и натриевую соли в массовых соотношениях фермент - окислитель 1: (0,1-0,7), низкомолекулярные примеси отделяют диализом и полученные растворы, взятые в соотношении 1:1, по активности смешивают с этанолом.
Таблица 1
100,0 100,0 100,0
100,0 100,0
1:0,4 1:0,7 1:1,0 1:1.5
30 36 43 51
100,0 76,41 0,6 77,8± 1,3 66,6i 1,75
100,0± 0,32 100,01 0,58 100,0± 0,72 100,0± 0,83 100,01 1,48
Редактор М. Недолуженко
Составитель Л. Борисова Техред М.Ходанич Корректоре;, ШекмарЗаказ 3926/24Тираж 499Подписное
ВНИИПИ Государственного комитета СССР по делам изобретений и открытий 113035, Москва, Ж-35, Раушская наб., д.4/5
.Производственно-полиграфическое предприятие, г. Ужгород, ул. Проектная, 4.
42 44 50 57
100,0 100,0 95,0 93,1
Продолжение табл.2
20
83,2
2,88
-1,

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения иммобилизованных нуклеофильных соединений | 1983 |
|
SU1690544A3 |
| СПОСОБ ПОЛУЧЕНИЯ КОНЦЕНТРИРОВАННОГО ЖИДКОГО ПИЩЕВОГО ПРОДУКТА | 2012 |
|
RU2580683C2 |
| РЕАКТИВ ДЛЯ ОПРЕДЕЛЕНИЯ ГЛЮКОЗЫ В БИОЛОГИЧЕСКОЙ ЖИДКОСТИ | 1991 |
|
RU2009499C1 |
| СПОСОБ ПРЕДУПРЕЖДЕНИЯ ЖИВОТНЫХ ЖИРОВ ОТ ОКИСЛИТЕЛЬНОЙ ПОРЧИ | 1967 |
|
SU214300A1 |
| Способ получения глюконовой кислоты | 1973 |
|
SU470951A3 |
| СПОСОБ ПИВОВАРЕНИЯ | 2007 |
|
RU2422501C2 |
| Способ определения целлюлолитической активности ферментов | 1977 |
|
SU696377A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ МЕТАБОЛИТОВ В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ, АКТИВНЫЙ ЭЛЕМЕНТ ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1992 |
|
RU2049991C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИБРИДНОГО ПРЕПАРАТА ПАПАИНА И КАРБОКСИМЕТИЛЦЕЛЛЮЛОЗЫ В ВИДЕ ГУСТОГО РАСТВОРА | 2022 |
|
RU2795425C1 |
| СПОСОБ БИОКАТАЛИТИЧЕСКОЙ ФЕРМЕНТАЦИИ | 2014 |
|
RU2641074C2 |
Изобретение относится к аналитической биохимии, а именно к способам измерения, использующим ферменты, и может быть использовано для определения содержания глюкозы в автоанали- заторах, применяемых в микробиологической пррмьшшенности и медицинской практике. Цель изобретения - повышение точности количественного определения глюкозы в растворах. Способ осуществляют путем введения в отдельно приготовленные растворы глюкозоок- сидазы и каталазы в ацетатном буфере порознь окислителя - периодной кислоты или ее натриевой или калиевой соли в массовых соотношениях фермент- окислитель 1:0,1-0,7. Образовавшиеся низкомолекулярные примеси отделяют диализом и полученные растворы в соотношении 1:1 по активности смешивают с этанолом. 2 табл. а S сл :о ее 

Авторы
Даты
1987-08-30—Публикация
1986-03-17—Подача