Изобретение относится к области изыскания новых биологически активных химических соединений, а именно к метиловым эфирам N-ароиламидов малоновой кислоты, которые обладают гипотензивной активностью, что позволяет предполагать возможность их применения в медицине для лечения гипертонической болезни.
Целью изобретения является изыскание в ряду амидов малоновой кислоты новых соединений, обладающих более высокой гипотензивной активностью.
П р и м е р 1. Метиловый эфир N-(n-хлорбензоил)амида малоновой кислоты (соединение I). Смешивают 2 г (0,009 моль) 2-(n-хлорфенил)- 1,3-оксазин-4,6-диона с 10 мл абсолютного метанола и нагревают до полного растворения. Полученный раствор охлаждают, избыток метанола удаляют в вакууме. Выход количественный. После кристаллизации из смеси бензол - гексан (1:1). Т.пл. 137-138оС. Rf 0,63 (этилацетат).
Найдено, %: N 5,70; C 51,90; H 4,15; Cl 14,16.
С11Н10ClNO4.
Вычислено, %: N 5,38; С 51,66; Н 3,91; Cl 13,89.
Спектр ПМР (ДМСО-d6, δ,м.д.): 11,36 (NH); 7,88, 7,50 (С6Н4) 3,78 (СН2); 3,60 (ОСН3). ИК-спектр (крист.) в вазелиновом масле, см-1: NH3260; ν C=0 1730; 1707, 1680.
П р и м е р 2. Метиловый эфир N-(n-толуоил)амида малоновой кислоты (соединение II).
Получают аналогично примеру 1. Выход количественный, т.пл. 122-122,5оС, Rf 0,65 (этилацетат).
Найдено, %: С 61,48; Н 5,46; N 6,02.
С12Н13NO4.
Вычислено, %: C 61,27; H 5,53; N 5,96.
Спектр ПМР (ДМСО-d6, δ , м.д.): 11,32 (NH); 7,92, 7,39 (С6Н4); 3,81 (СН2); 3,63 (ОСН3); 2,35 (СН3). ИК-спектр (крист.) в вазелиновом масле, см-1: νNН 3250; νC=0 1725; 1695; 1660.
Новые соединения являются бесцветными кристаллическими веществами, не имеющими запаха, с относительно невысокой температурой плавления. Они мало растворимы в воде и неполярных растворителях. Хорошо растворимы в спирте.
Изучение влияния новых соединений на уровень артериального давления проводили в острых опытах на кошках под эфиромединаловым наркозом. Артериальное давление регистрировали в общей сонной артерии с помощью ртутного манометра. Соединения вводили внутримышечно в дозе 25 мг/кг. Уровень артериального давления регистрировали через 15, 30, 60, 120, 180, 240 и 300 мин после введения препаратов. Фармакологические анализаторы вводили до и после новых соединений. Результаты приведены в табл.1.
Как видно из таблицы, метиловые эфиры N-ароиламидов малоновой кислоты обладают выраженным гипотензивным действием. Падение артериального давления начинается через 15 мин после введения и достигает максимума через 2-3 ч. Эффект равен 35-36%. Гипотензивное действие продолжается более 5 ч.
В случае известного соединения трет-бутилового эфира N-тиобензоиламида малоновой кислоты падение артериального давления начинается через 30 мин, достигает максимума через 1-2 ч, эффект составляет 30%, продолжительность действия более 5 ч.
Для изучения механизма гипотензивного действия были поставлены эксперименты с фармакологическими анализаторами адреналином (адреномиметик прямого типа действия) и эфедрином (адреномиметик непрямого типа действия). Адреналин вводили в дозе 10 мг/кг, эфедрин - 4 мг/кг. Результаты представлены в табл. 2.
Как видно из таблицы, новые соединения уменьшают прессорную реакцию адреналина на 22% и извращают прессорное действие эфедрина. Подобные эффекты характерны для веществ, обладающих адреноблокирующим действием. Острую токсичность изучали на белых мышах массой 18-21 г при внутрибрюшинном введении препаратов в интервале доз от 1000 до 3400 мг/кг. Наблюдение за животными вели в течение 3 сут. Через 30 мин после введения животные лежали неподвижно, на внешние раздражители не реагировали, дыхание частое поверхностное. Смерть наступила в первые сутки. Установлено: LD50 соединения I составляет 2187 ± 157 мг/кг; соединения II - 2675 ± 83 мг/кг; LD50 трет-бутилового эфира N-тиобензоиламида малоновой кислоты составляет 642 мг/кг.
Таким образом, новые соединения обладают выраженным и длительным гипотензивным действием в эксперименте на животных. Они превосходят известное соединение по силе гипотензивной активности и являются малотоксичными веществами, LD50 метиловых эфиров N-ароиламидов малоновой кислоты в 3,4-4,2 раза ниже, чем у трет-бутиловых эфиров N-тиобензоиламида малоновой кислоты.
| название | год | авторы | номер документа |
|---|---|---|---|
| ТРЕТ-БУТИЛОВЫЕ ЭФИРЫ N-ТИОЗАМЕЩЕННЫХ АМИДОВ МАЛОНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩИЕ ГИПОТЕНЗИВНОЙ АКТИВНОСТЬЮ | 1983 |
|
SU1152211A1 |
| ЛЕКАРСТВЕННОЕ ПРОТИВОШОКОВОЕ СРЕДСТВО | 1996 |
|
RU2142796C1 |
| АНТИГИПОТЕНЗИВНОЕ СРЕДСТВО | 2007 |
|
RU2338538C1 |
| СПОСОБ ПРОФИЛАКТИКИ АРТЕРИАЛЬНОЙ ГИПОТЕНЗИИ ПРИ ПРОВЕДЕНИИ СПИНАЛЬНОЙ АНЕСТЕЗИИ У БЕРЕМЕННЫХ ПРИ КЕСАРЕВОМ СЕЧЕНИИ | 2017 |
|
RU2679587C1 |
| Циклический аналог ангиотензина,обладающий способностью ингибировать прессорное и миотропное действие ангиотензина | 1981 |
|
SU1067796A1 |
| СРЕДСТВО, ВЛИЯЮЩЕЕ НА АРТЕРИАЛЬНОЕ ДАВЛЕНИЕ | 1997 |
|
RU2187309C2 |
| N,N-ДИИЗОБУТИЛ-N`-(П-МЕТИЛОКСИТИОБЕНЗОИЛ)ОКСАЛИЛДИАМИД, ОБЛАДАЮЩИЙ ГИПОТЕНЗИВНОЙ АКТИВНОСТЬЮ | 1989 |
|
SU1614439A1 |
| ГИПОТЕНЗИВНОЕ СРЕДСТВО | 1997 |
|
RU2168987C2 |
| 1-(ИЗОФЛАВОНИЛ-7-ОКСИКАРБОНИЛВИНИЛ)-4-(ИЗОФЛАВОНИЛ-7-ОКСИКАРБОНИЛМЕТИЛЕНОКСИ)БЕНЗОЛ, ОБЛАДАЮЩИЙ ГИПОТЕНЗИВНЫМ И ГИПОЛИПИДЕМИЧЕСКИМ ДЕЙСТВИЕМ | 1988 |
|
SU1531431A1 |
| КАРДИОТОНИЧЕСКОЕ И ГИПЕРТЕНЗИВНОЕ СРЕДСТВО, ДЛИТЕЛЬНО ПОВЫШАЮЩЕЕ ДАВЛЕНИЕ, И ЛЕКАРСТВЕННЫЕ ФОРМЫ НА ЕГО ОСНОВЕ | 1999 |
|
RU2181286C2 |

Изобретение касается производных дикарбоновых кислот, в частности метиловых эфиров N-(n-хлорбензоил или n-толуоил)амида малоновой кислоты, которые обладают гипотензивной активностью и могут быть использованы в медицине. Цель изобретения - создание более активных веществ указанного класса. Их синтез ведут из 2-(n-хлорфенил- или толуоил)-1,3-оксазин-4,6-диона и метанола при нагревании до полного растворения. Выход ~100% , т.пл. 137 - 138°С (C11H10ClNO4) и 122 - 122,5°С (C12H3NO4) . Новые соединения оказывают действие после 15 мин после введения (доза 0,25 мг/кг) и достигают максимума эффекта через 2 - 3 ч. Общее время действия продолжается более 5 ч. Токсичность LD50 в 3,4 - 4,2 раза ниже известного трет-бутилового эфира N-тиобензоиламида малоновой кислоты. 2 табл.
МЕТИЛОВЫЕ ЭФИРЫ N-АРОИЛАМИДОВ МАЛОНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩИЕ ГИПОТЕНЗИВНОЙ АКТИВНОСТЬЮ.
Метиловые эфиры N-ароиламидов малоновой кислоты общей формулы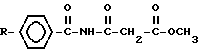
где R=Cl или CH3,
обладающие гипотензивной активностью.
| ТРЕТ-БУТИЛОВЫЕ ЭФИРЫ N-ТИОЗАМЕЩЕННЫХ АМИДОВ МАЛОНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩИЕ ГИПОТЕНЗИВНОЙ АКТИВНОСТЬЮ | 1983 |
|
SU1152211A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1995-03-20—Публикация
1986-01-13—Подача