Изобретение относится к области электрохимических производств, конкретно к электродам для электролиза водных растворов хлоридов щелочных металлов с получением хлора и каустической соды, хлоратов, гипохлоритов,
Известен электрод для электрохимических процессов, содержащий электропроводную основу, например из титана, на которую нанесено активное по крытие из смеси окислов титана, иридия и рутения, причем содержание окислов титана в покрытии является значительным и составляет более 75 мол.%. Например, в известном электроде покрытие имеет следующий состав мол.%: 3,91; ЕиО 7,43 и TiO 88,66 (образец В « образец Д) и Ir0.j 7,25,- RuO 3,8 и TiOj 78,95 (образец С).
Таким образом, в известном электроде ингредиенты взяты в следующих соотношениях, молД: (1г02 + + RuO) 3,8-7,8:1 и .RuO 0,3:1..
Недостатком указанного электрода является Неустойчивость анодного по- ;тенциала при электролизе, низкий выход по току, недостаточная стойкость элрктрод-а. Кроме того, недостатком электрода является неполное срабатывание активной массы - потенциал электрода резко возрастает при наличии еще до.статочного. количества масгы активного покрытия, i Так,при испытаниях образцов В, С и Д в насыщенном растворе NaCl три плотности тока А/см и 65 С Анодный потенциал образца В изменял- Ья в пределах J,53-J,62 В за время Электролиза 2000 ч (83 сут), образца С - в пределах J,35-1,38 В за $ремя электролиза 2300 ч (л,96 сут) и образца Д - в пределах 1,44-1,50 В ja время электролиза 816 ч ( сут). Наиболее близким к изобретению по texничecкoй сущности и достигаемому результату является электрод для Электролиза водных растворов хлоридов щелочных металлов, содержащий основу из вентильного металла с нане сенным на нее покрытием из смеси окислов вентильных металлов, напри- Мер титана, и окислов металлов группы платины, например иридия и рутения, причем содержание окисла вентильного металла в смеси составляет более 50 мол,%. В известном элёктроO
5
0
5
0
5
0
5
0
5
де покрытие может содержать как смесь окислов титана и одного металла группы платины, например рутения, так и смесь окислов титана и нескольких металлов группы платины, например иридия и рутения 2.
Недостатком известного электрода является невысокая стойкость.
Цель изобретения - повышение стойкости электрода.
Поставленная цель достигается тем, что в электроде для электролиза водных растворов хлорида щелочных металлов, содержащем основу из вентильного металла с нанесенным на нее покрытием из смеси окислов титана, иридия и рутения, причем содержание окиси титана в смеси составляет более 50 мол,%, покрытие содержит окислы иридия и рутения при мольном соотношении 0,75-3:J.
Кроме того, в предлагаемом электроде покрытие содержит окислы титана в количестве 50-75 мол.%,
П р и м е р. На титановую основу электрода, предварительно прощедщую пескоструйную обработку, обезжиривание и травление, наносят покров.ный раствор - смешанный водный раствор IrCl,,TiCl4 и RuOHClj,
Покровный раствор готовят из исходных растворов и компонентов: раствора гидрооксихлорида рутения (RuOHCl,) в воде с концентрацией г/л; раствора четыреххлористо- го титана (TiCl) в воде с концентрацией 220+5 г/л (в пересчете на ТгО,); соль треххлористого иридия (IrCl,) добавляют в смешанный раствор RuOHCl.- TiCli, ) в виде кристаллов.
Активное покрытие электрода изготовляют многослойным. Каждый слой наносят по следующей технологии: расход смешанного раствора на J-йспой- 25 мл/м, что соответствует закладке активной массы 1-2 после нанесения каждого слоя электрод сна-, .чала сушат при 150. С, затем обжигают при 350 С в течение 20 мин первые 2-3 слоя, последующие слои прокали - вают при 450-500 0 в течение 20- 40 мин.
Всего было изготовлено 9 электродов. Образцы 1,2,3 и 8 соответствуют по составу известному электроду, образцы 4-7 - .по составу предлагаемо;- му электроду. Образец 9 иллюстрирует электрод с покрытием из смеси окис10
лов титана, иридия и рутения, причем содержание окиси титана в смеси составляет менее 50 мол.%.
Образец 1 соответствует общепринятому в промьшленности окисному ру- тениево-титановому аноду.
Измерения потенциала анода проводят в условиях хлорного электролиза: концентрация раствора хлорида натрия 280 г/л, температура , рН 3,0- 3,5, плотность тока 1000, 2000,4000, 6000 и 10000 А/м, и Б условиях хло- ратного электролиза: 400 г/л NaClO, 100 г/л NaCl, рН 7, плотность тока 1000-3000 температура-80°С,
Стойкость электродов оценивают по - нескольким ускоренным методикам изучения износостойкости электродов по методу переменной полярности и амаль- 20 гамации, при электролизе в растворе NaOH, так и в условиях длительного э шктролиза.
Сущность метода переменной полярности и амальгамации заключается в следующем: испытуемый образец при плотности тока 1 А/см, 60 С в растворе хлорида натрия с концентрацией 300 г/л подвергают переменной анодной и катодной поляризации в течение 40 мин. Затем электрод опускают на 30 с в амальгаму натрия с концентрацией р,2 мас.%. После этих испытаний электрод промывают в дистиллирован- ,ной воде, сушат и определяют потерю веса.
Износостойкость электродов при электролизе растворов NaOH изучают в
веса образца и время до запирания анода.
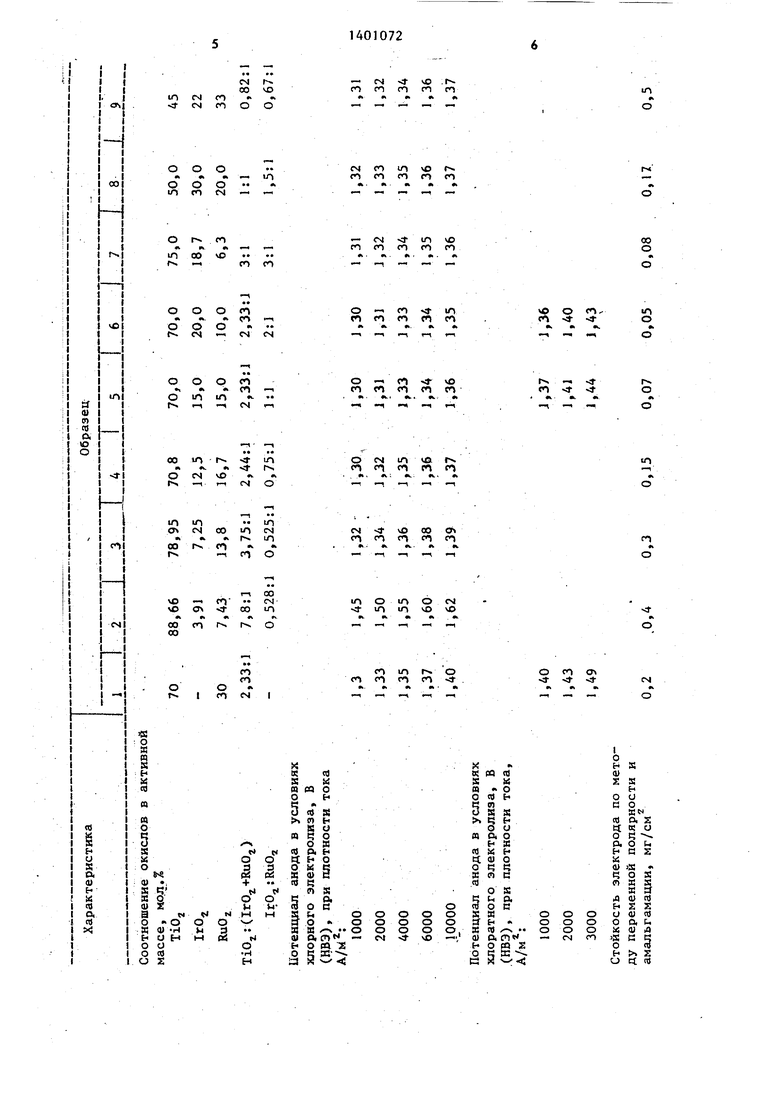
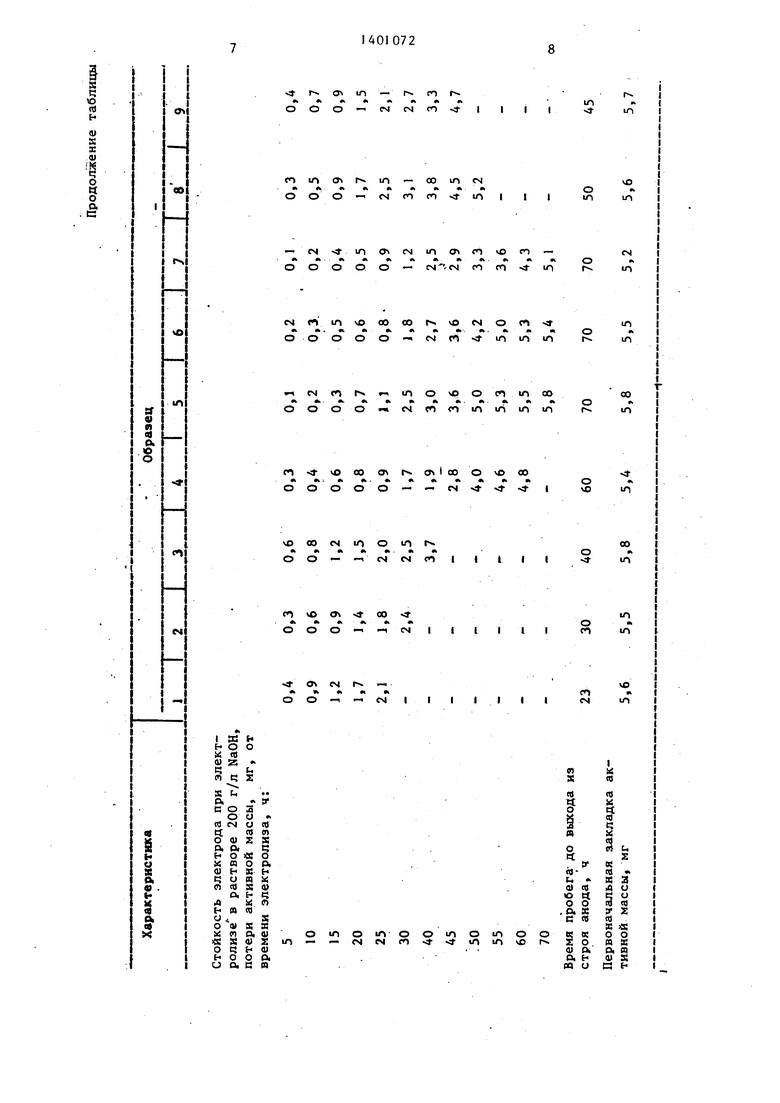
Результаты испытаний приведены в таблице.
Как видно из результатов, прив денных в таблице, предлагаемый э трод (образцы 4-7) не уступает из вестному электроду (образцы J и 8 по величине анодного потенциала в условиях хлорного и хлоратного эл ролиза.
Во всем заявленном интервале м ного соотношения окислов иридия и 15 .рутения в покрытии, а именно 0.75 3:1, стойкость предлагаемого элек рода, оцениваемая по потере актив массы, как при испытаниях по мето переменной полярности и амальгама так в зависимости от продолжитель ности электролиза в жестких услов (200 г/л NaOH), является значител более высокой, чем известного эле рода, примерно в 1,5-2 раза.
При содержании окиси титана в покрытии более 75 мол,% и при мол соотношении окислов иридия и руте вне заявленного интервала стойкос известного электрода ниже, чем у предлагаемого (образцы 2 и 3). Пр содержании окиси титана в покрыти менее 50 мол,% даже в пределах за ленного интервала мольного соотно ния окислов иридия и рутения стой кость электрода является неудовле
25
30
35
рительной (образец 9).
Экономический эффект от исполь вания изобретения составит 182 ты
следующих условиях: 200 г/л раствора
NaOH, температура , плотность то- 40 РУблей из расчета на производство
ка 2 А/см, и определяют потерю
130 тыс.т хлора в год.
веса образца и время до запирания анода.
Результаты испытаний приведены в таблице.
Как видно из результатов, приве- денных в таблице, предлагаемый электрод (образцы 4-7) не уступает известному электроду (образцы J и 8) по величине анодного потенциала в условиях хлорного и хлоратного электролиза.
Во всем заявленном интервале моль- ного соотношения окислов иридия и .рутения в покрытии, а именно 0.75- 3:1, стойкость предлагаемого элект рода, оцениваемая по потере активной массы, как при испытаниях по методу переменной полярности и амальгамации, так в зависимости от продолжительности электролиза в жестких условиях (200 г/л NaOH), является значительно более высокой, чем известного электрода, примерно в 1,5-2 раза.
При содержании окиси титана в покрытии более 75 мол,% и при мольном соотношении окислов иридия и рутения вне заявленного интервала стойкость известного электрода ниже, чем у предлагаемого (образцы 2 и 3). При содержании окиси титана в покрытии менее 50 мол,% даже в пределах заявленного интервала мольного соотношения окислов иридия и рутения стойкость электрода является неудовлетво
рительной (образец 9).
Экономический эффект от использования изобретения составит 182 тыс.
РУблей из расчета на производство
РУблей из расчета на п
130 тыс.т хлора в год.
I I I

| название | год | авторы | номер документа |
|---|---|---|---|
| Электрод для электрохимического получения хлора и щелочи | 1981 |
|
SU1468970A1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ЭЛЕКТРОДА ДЛЯ ЭЛЕКТРОЛИЗА ВОДНЫХ РАСТВОРОВ ХЛОРИДОВ ЩЕЛОЧНЫХ МЕТАЛЛОВ | 2008 |
|
RU2383660C1 |
| Электрод для получения хлора | 1979 |
|
SU1134122A3 |
| Способ изготовления катода | 1985 |
|
SU1326630A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭЛЕКТРОДА, ЭЛЕКТРОД (ВАРИАНТЫ) И ЭЛЕКТРОЛИТИЧЕСКАЯ ЯЧЕЙКА (ВАРИАНТЫ) | 2004 |
|
RU2425176C2 |
| СПОСОБ ЭЛЕКТРОЛИЗА ВОДНЫХ ХЛОРНО-ЩЕЛОЧНЫХ РАСТВОРОВ, ЭЛЕКТРОД ДЛЯ ЭЛЕКТРОЛИЗА ХЛОРНО-ЩЕЛОЧНОГО РАСТВОРА И СПОСОБ ИЗГОТОВЛЕНИЯ ЭЛЕКТРОЛИТНОГО ЭЛЕКТРОДА | 2003 |
|
RU2330124C2 |
| ЭЛЕКТРОД ДЛЯ ЭЛЕКТРОЛИЗА | 2017 |
|
RU2720309C1 |
| Способ гальванического платинирования титана | 1974 |
|
SU514922A1 |
| ВЫСОКОЭФФЕКТИВНОЕ АНОДНОЕ ПОКРЫТИЕ ДЛЯ ПОЛУЧЕНИЯ ГИПОХЛОРИТА | 2005 |
|
RU2379380C2 |
| Электрод для электролиза водного раствора галогенида металла | 1979 |
|
SU1056911A3 |


| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Патент США № 3948751, кл | |||
| Ротационный фильтр-пресс для отжатия торфяной массы, подвергшейся коагулированию, и т.п. работ | 1924 |
|
SU204A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| 0 |
|
SU369923A1 | |
| Видоизменение пишущей машины для тюркско-арабского шрифта | 1923 |
|
SU25A1 |
Авторы
Даты
1988-06-07—Публикация
1981-06-03—Подача