(Л
с

| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ ТЕРЕФТАЛЕВОЙ КИСЛОТЫ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2008 |
|
RU2519254C2 |
| Способ получения фталамида | 1989 |
|
SU1754708A1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ ПИРОКАТЕХИНА, ГИДРОХИНОНА И ПЛАСТИФИКАТОРА БЕТОНА | 1992 |
|
RU2028288C1 |
| Способ выделения пара-терфенила и высокотемпературных органических теплоносителей из кубовых остатков пиролиза бензола | 1988 |
|
SU1655961A1 |
| СПОСОБ ТРАНСАЛКИЛИРОВАНИЯ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ | 2012 |
|
RU2583792C2 |
| Способ переработки высококипящих побочных продуктов процесса получения этриола | 2016 |
|
RU2616004C1 |
| Способ получения фталимида | 1989 |
|
SU1728240A1 |
| СПОСОБ ПОЛУЧЕНИЯ СМЕСЕЙ ИЗОМЕРОВ ЦИПЕРМЕТРИНА | 1990 |
|
RU2045516C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭТИЛОВОГО ЭФИРА α - БРОМИЗОВАЛЕРИАНОВОЙ КИСЛОТЫ | 1993 |
|
RU2080318C1 |
| СПОСОБ ПОЛУЧЕНИЯ р-ИЗОПРОПИЛНАФТАЛИКА | 1972 |
|
SU350774A1 |
Изобретение относится к кето- нам, в частности к получению капро- фенона (КФ), который используется в органическом синтезе. Цель - увели- .чение выхода КФ. Получение его ведут разложением 1-фенилциклогексилгидро- пероксида при 80-15О С в атмосфере инертного газа. Процесс проводят в среде бензола или его метилзамещенных, или кафталина, взятых в количестве 20- 95% мас.% от реакционной массы, с последукяцим вьщелением целевого КФ ректификацией. Способ обеспечивает увеличение выхода КФ на 20%. 1 табл.
4
о
ND
СП
СО 4
Изобретение относится к способу получения алкилароматических кето- нов, в частности капрофенона, который используется как промежуточный продукт при синтезе инсектицидов, третичных ароматических спиртов, аршт- кетоспиртов и других ценных соединений .
Целью изобретения является повы- шение выхода капрофенона.
Для обеспечения условий протекания реакции в жидкой фазе разложение 1-ФЦП1 проводят при давлении 0,1-0,5 МПа, величина которого оп- ределяется температурой киепения используемого растворителя с учетом заданной температуры процесса.
Использование 20-95 мас.% растворителя обусловлено чисто технологи- ческими ограничениями. Так при концентрации растворителя менее 20 мас,% заметно возрастает опасность технологического процесса из-за повьшгения взрывогпасности исходной смеси. При концентрации растворителя вьпяе 95 мас.% затруднено вьзделение целевого продукта из реакционной смеси, возрастают энергозатраты на стадии регенерации растворителя. Оптимальной является концентрация растворителя 60-70 мас.%.
Способ осуществляют следующим образом.
Полученный любым способом 1-ФПГП (чистотой 99,4-100%) подвергают раз- ложению в реакторе барботажного типа в токе инертного газа (аргон, азот, СО) при 80-150 0 (лучше too-120 с), в необходимых случаях под небольшим давлением 0,1-0,5 МПа, в среде органического растворителя - бензола, его метилзамещенных или нафталина. Полно- .ту конверсии 1-ФЦП1 устанавливают методом йод ометрии. В качестве побочных продуктов в реакционной смеси после завершения реакции присутствуют фенил циклогексанол (основной компонент до 30%), низкомолекулярные кислоты, олефины в сумме не более 8-10 мас.%. Полный анализ реакционной смеси осу- ществляют с помощью ГЖХ. Капрофенон из реакционной среды отделяют ректификацией под вакуумом. Отбор ведут п 114-120°(10 мм. рт. ст.). Чистота целевого продукта после выделения не менее 98,5-99,5% т. пл. ,.
Осуществлять процесс при темпера- Tyjie ниже нецелесообразно, по
0
5
скольку не обеспечивается оптимальная производительность реактора из-за низкой скорости реакции. При температуре вьппе 150 С скорость реакции слишком высока, процесс может выйти из под контроля.
Использование в качестве растворителя бензола или его метилзамещенных или нафталина позволяет значительно увеличить выход капрофенона в реакции термического разложения 1-ФЦГП. В промежуточном комплексе ароматический растворитель - алкоксирадикал (комплекс образуется за счет возможности частичной делокализации неспаренного электрона радикальной частицы в развитой Р-электронной системе ароматического ядра) облегчается фрагментация фенидциклогексилрадикала.. Процесс изомеризации и разрыва циклогексиль- ного кольца молекулы 1-ФЦГП приводит к образованию целевого продукта. На все процессы превращения алкоксиради- кала определенное влияние оказывает Как строение, так и геометрия молекулы растворителя.
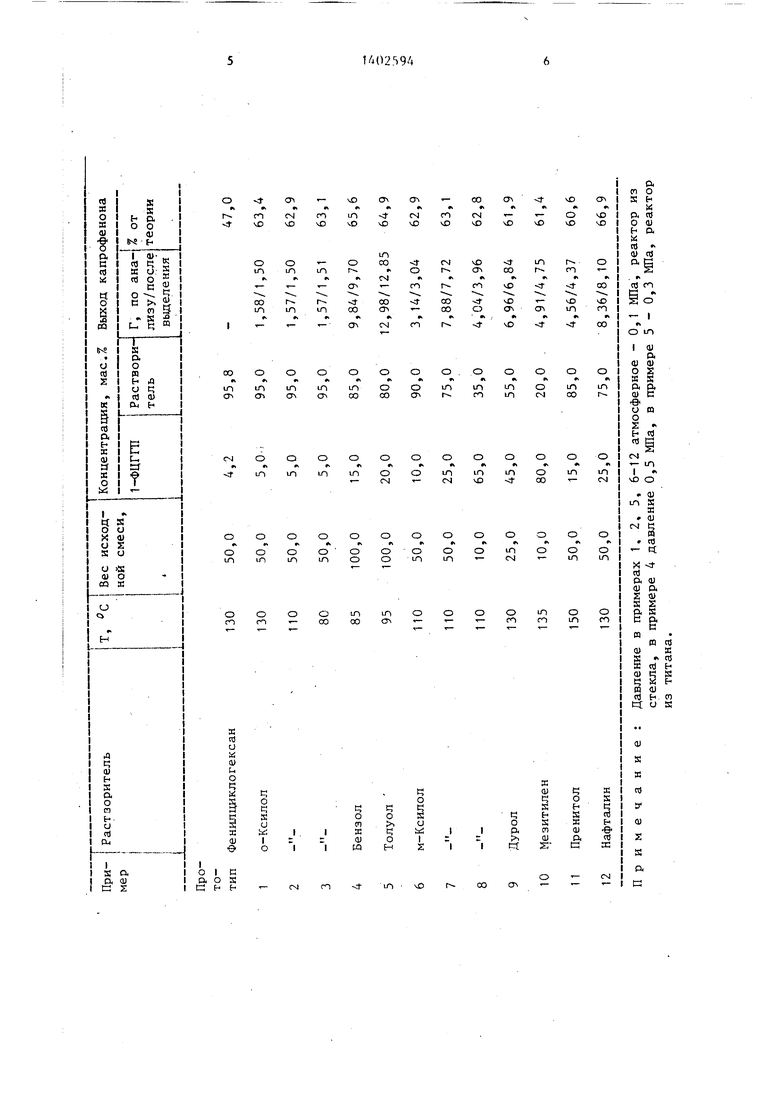
Приме р1. 50 г реакционной смеси, содержащей 5 мас.% 1-ФЦГП и 95 мае,% о-ксилола, помещают в стеклянный реактор барботажного типа. Реакцию разложения осуществляют при в токе аргона 1,2 л/ч. Полноту превращения гидропероксида контролируют методом йодометрии по известной методике. Капрофенон вьщеляют вакуумной ректификацией. Получено 1,5 г кетона. Чистота 99,0%. Выход от теории 63,4%.
П р и м е р 2. Аналогично примеру 1, но температура разложения составляет . Получено 1,5 г капрофенона чистотой 99,1%. Выход от теории 62,9%.
П р и м е р 3. Ту же смесь подвергают разложению в условиях примера 1, но температура разложения составляет . Получено 1,51 г капрофенона чистотой 98,9%. Выход от теории 63,1%.
П р и м е р 4. 100 г реакционной смеси, содержащей Т5 мас.% 1-ФЦГТ1 и 85 мас.% бензола, подвергают разложению в условиях примера 1, но температура разложения составляет 85°С. Получено 9,7 г капрофенона чистотой 99,4%. Выход от теории 65,6%.
Пример5. 100 г реакционной смеси, содержащей 20 мас.% 1-ФЦГП и
- 1А025944
80 мас.% толуола, подвергают разло-пература разложения составляет .
жению в условиях примера 1, но темпе-Получено А,75 г капрофенона чистотой
ратура разложения составляет . По-99,0%. Выход от теории 61,4%. лучено 12,85 г капрофенона чистотой Пример11.50г реакционной .
99,2%. Выход от теории 64,9%. смеси, содержащей 15 мас.% 1-ФЦт и
П римерб. 50 г реакционной мас.% пренитола, подвергают раэлосмеси, содержащей 10 мас.% 1-ФЦГПжению в условиях примера 1, но темпеи 90 мас.% м-ксилола, подвергают раз-ратура разложения составляет 150°С.
ложению в условиях примера 1, но тем- дПолучено 4,37 г капрофенона чистотой
пература разложения составляет .98,8%. Выход от теории 60,6%. Получено 3,0 капрофенона чистотой Пример 12. 50 г реакционной
99,0%. Выход от теории 62,9%.смеси, содержащей 25 мас.% 1-ФЦГП
Пример7, 50 г реакционной 5 мас.% нафталина, подвергают раз- смеси, содержащей 25 мас.% 1-ФЦГП 15ложению в условиях примера 1. Полу- и 75 мас.% м-ксилола, подвергают раз-чено 8,1 г капрофенона чистотой 99,5%. ложению в условиях примера 1, однакоВыход от теории 66,9%. температура разложения составляет Данные опытов сведены в таблицу. 110°С. Получено 7,72 г капрофенона Таким образом, предлагаемый способ чистотой 99,3%. Выход от теории 63,1%.2опо.лучения капрофенона позволяет суП р и м е р В. 10 г реакционнойщественно увеличить на 20% выход цесмеси, содержащей 65 мас.% 1-ФЦГП илевого продукта по сравнению со спо35 мас.% м-ксилола, подвергают разло-собом по прототипу.
жению в условиях примера 1, однакоФормула изобретения температура разложения составляет 25 Способ получения капрофенона путем
110°С. Получено 3,96 к капрофенонаразложения 1-фенилциклогексилгидрочистотой 98,8%. Выход от теории 62,8%.пероксида при нагревании в атмосфере
П р и м е р 8.. 25 г реакционнойинертного газа в среде органического
смеси, содержащей 45 мас.% 1-ФЦГП ирастворителя с последующим вьоделением
55 мас,% дурола, подвергают разложе- зоцелевого продукта ректификацией, о т нию в условиях примера 1. Получено личающийся тем, что, с це6,84 г капрофенона чистотой 99,2%.лью увеличения выхода целевого проВыход от теории 61,9%.дукта, в качестве органического растворителя используют бензол или его
Пример 10, Юг реакционной „метилзамев1енные, или нафталин, взятые
смеси, содержащей 80 мае. % 1-ФЦГПв количестве 20-95 мас.% от реакциони 20 мас.% мизитилена, подвергают раз-ной массы, и процесс проводят при
ложению в условиях примера 1, но тем-80-150 С.
| Велютин Л.П., Потехин В.М | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| - Изв | |||
| вузов СССР | |||
| Сер | |||
| хим | |||
| и хим | |||
| технол., 1980, т | |||
| Прибор для равномерного смешения зерна и одновременного отбирания нескольких одинаковых по объему проб | 1921 |
|
SU23A1 |
| Приспособление для автоматического перевода трамвайных стрелок | 1924 |
|
SU952A1 |
Авторы
Даты
1988-06-15—Публикация
1986-11-27—Подача