Изобретение относится к способу получения смеси энантиомеров (зеркальных изомеров) α-циан-3-феноксибензил-3-(2,2-дихлорвинил)-2,2- диметилциклопропанкарбоксилата (циперметрина) формулы I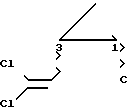 O
O
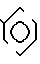 с данным соотношением изомеров, полученных путем асимметричного превращения.
с данным соотношением изомеров, полученных путем асимметричного превращения.
В описании изобретения пространственная конфигурация замещающих атомов, относящихся к хиральному атому углерода (обозначенному в формуле как α) характеризуется символами S и R. Термины "цис" и "транс" используются для обозначения положения атомов, замещающих третий атом углерода циклопропанового кольца, а абсолютная пространственная конфигурация атомов, замещающих первый атом углерода, условно обозначается 1R и 1S. Для обозначения различных энантиомеров и их пар используют следующие сокращения:
1а смесь 1R цис s и 1S цис R;
альфаметрии (Faslac)
1b смесь 1R транс S и 1S транс R
(Transmix)
1с смесь 1R цис R и 1S цис S
1d смесь 1R транс R и 1S транс S
1f 1R цис S
1g 1R транс S
1h 1S цис R
1i 1S транс R
1а + 1b асимметрин (Chinmix) Производные циперметрина являются инсектицидами (ЕР N 215010, ЕР N 208758).
Известен способ получения изомера 1b из циперметрина, содержащего 1b + 1α транс изомеры, путем эпимеризации в присутствии органического или неорганического основания или путем эпимеризации в присутствии такого органического растворителя, как петролейный эфир и 2,6-ди-трет-бутил-4-метифенол в качестве антиоксиданта при 30-60оС (ЕРА 215010).
Известно также, что 1а, 1b и 1а + 1b получают путем взаимодействия суспензии углеводородов исходных изомеров с основанием и катализатором, который в основном растворен в суспензии и выбран из четвертичных соединений аммония и фосфора, а также краунэфира. Суспензию взбалтывают при температуре, эффективной для превращения и получают целевые изомеры. Образование побочного эфира бензоина снижено за счет добавления в суспензию акцептора альдегида в виде метабисульфита и/или катализатора в виде галоидного аммонийтетраалкида, растворимого в апротонном растворителе в виде органического нитрила. В качестве основания используют неорганические основания, например, цианид натрия (РСТ WO 88/10249).
Недостатком данного способа является значительное разложение циперметрина в условиях предложенной реакции, сопровождающееся в равной степени образованием производных бензоина с формулой II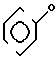

"Молекула-акцептор" предотвращает только образование производных бензоина, но не разложение циперметрина. Дальнейшее препятствие течению процесса создает выделение циана, как побочного продукта разложения. Обработка реакционной смеси, состоящей из нескольких слоев, усложняет в дальнейшем надежное промышленное осуществление данной критической реакции.
В соответствии с известным способом, чистая смесь (1а + 1b) может быть получена путем избирательной кристаллизации циперметрина достаточной чистоты при выборе соответствующих условий, подходящего растворителя, температуры и чистого затравочного кристалла. Процесс длится несколько недель. Таким образом, смесь 1 а + 1b может быть получена с выходом 80% рассчитанным на содержание пары изомера 1а + 1b исходного циперметрина. Недостаток данного способа заключается в том, что другие менее биологически ценные стереоизомеры циперметрина остаются неиспользованными (ЕР N 208758).
Настоящее изобретение позволяет избежать указанных недостатков.
Настоящим способом получают стабильные чистые вещества с хорошим выходом, он прост в осуществлении и экологически чист.
Настоящий способ получения смесей изомеров циперметрина формулы I
 где углеродные атомы, обозначенные 1,3 и α относятся к хиральному атому углерода, а волнистая линия указывает на цис- или транс-конфигурацию относительно циклопропанового кольца, которые из теоретически возможных 8 изомеров циперметрина содержат, по крайней мере, 95% пары изомеров 1R транс S и 1S транс R (1b) или только смесь 1R цис S и 1S цис 1R (1b) и пару изомеров (1b) с соотношением 1а 1b 55 45 25 75, путем асимметричного превращения второго порядка, осуществляемым в присутствии третичного амина и протонного растворителя при температуре от 0 до (+) 25оС из исходной смеси изомеров циперметрина с чистотой минимум 90% которая содержит следующие за парой изомеров (1b) цис- и другие транс-изомеры или пару изомеров 1а + 1b с нежелательным соотношением, заключается в том, что превращение осуществляют непрерывно в 2-7 реакторах, оборудованных холодильником, смесителем, подогревателем, установленных друг за другом с диапазоном указанной темпераутры с максимальной разницей температуры в реакторах 10оС, при этом в первый реактор вводят исходную смесь изомеров формулы 1 с чистотой по крайней мере 90% с добавлением 1 мас.ч. конечного кристаллического циперметрина или смеси изомеров 1а и/или 1b в изопропаноле в количестве 0,4 мас.ч. с добавлением триэтиламина в таком количестве, что его содержание составляет 0,4 мас.ч. смесь перемешивают и часть реакционной смеси переводят во второй реактор, в который, при необходимости, добавляют третичный амин и изопропанол, и затем в последующие реакторы, в которые дополнительно вводят изопропанол, при этом в первый реактор непрерывно или периодически добавляют исходный циперметрин более 0,4 мас.ч. изопропанола и/или третичного амина, реакционная смесь вновь последовательно проходит через все реакторы, проходя указанную обработку, из полученной при этом кристаллической суспензии при необходимости выделяют кристаллы и при необходимости нейтрализуют основание, содержащееся в извлеченной из последнего реактора реакционной смеси или по поверхности кристаллического продукта, и/или рекристаллизуют конечный продукт из растворителя, содержащего кислоту, и/или расплавляют и вываривают суспензию кристаллов при 60-70оС в присутствии кислоты, затем экстрагируют кристаллический продукт при 0-70оС и экстракт промывают водным раствором соли и/или кислоты, при необходимости добавляют альдегид как циансвязующий агент на одной из стадий выделения из кристаллической суспензии. При этом загрузку и выгрузку ведут непрерывно и/или порциями.
где углеродные атомы, обозначенные 1,3 и α относятся к хиральному атому углерода, а волнистая линия указывает на цис- или транс-конфигурацию относительно циклопропанового кольца, которые из теоретически возможных 8 изомеров циперметрина содержат, по крайней мере, 95% пары изомеров 1R транс S и 1S транс R (1b) или только смесь 1R цис S и 1S цис 1R (1b) и пару изомеров (1b) с соотношением 1а 1b 55 45 25 75, путем асимметричного превращения второго порядка, осуществляемым в присутствии третичного амина и протонного растворителя при температуре от 0 до (+) 25оС из исходной смеси изомеров циперметрина с чистотой минимум 90% которая содержит следующие за парой изомеров (1b) цис- и другие транс-изомеры или пару изомеров 1а + 1b с нежелательным соотношением, заключается в том, что превращение осуществляют непрерывно в 2-7 реакторах, оборудованных холодильником, смесителем, подогревателем, установленных друг за другом с диапазоном указанной темпераутры с максимальной разницей температуры в реакторах 10оС, при этом в первый реактор вводят исходную смесь изомеров формулы 1 с чистотой по крайней мере 90% с добавлением 1 мас.ч. конечного кристаллического циперметрина или смеси изомеров 1а и/или 1b в изопропаноле в количестве 0,4 мас.ч. с добавлением триэтиламина в таком количестве, что его содержание составляет 0,4 мас.ч. смесь перемешивают и часть реакционной смеси переводят во второй реактор, в который, при необходимости, добавляют третичный амин и изопропанол, и затем в последующие реакторы, в которые дополнительно вводят изопропанол, при этом в первый реактор непрерывно или периодически добавляют исходный циперметрин более 0,4 мас.ч. изопропанола и/или третичного амина, реакционная смесь вновь последовательно проходит через все реакторы, проходя указанную обработку, из полученной при этом кристаллической суспензии при необходимости выделяют кристаллы и при необходимости нейтрализуют основание, содержащееся в извлеченной из последнего реактора реакционной смеси или по поверхности кристаллического продукта, и/или рекристаллизуют конечный продукт из растворителя, содержащего кислоту, и/или расплавляют и вываривают суспензию кристаллов при 60-70оС в присутствии кислоты, затем экстрагируют кристаллический продукт при 0-70оС и экстракт промывают водным раствором соли и/или кислоты, при необходимости добавляют альдегид как циансвязующий агент на одной из стадий выделения из кристаллической суспензии. При этом загрузку и выгрузку ведут непрерывно и/или порциями.
В процессе используют третичный амин, содержащий один или несколько атомов азота, предпочтительно триэтил.
Предпочтительно процесс ведут таким образом, что кристаллическую суспензию, полученную в конце, фильтруют и для удаления загрязнений из отфильтрованных веществ используют растворитель, выбранный из группы, состоящей из петролейного эфира, гептана, этанола, изопропанола, их смесей с такими кислотами как уксусная, фталевая, малеиновая, фумаровая, малоновая.
Для экстрагирования кристаллической суспензии используют несмешивающийся с водой органический органический растворитель гептан, петролейный эфир, этилацетат, бензол, толуол, ксилол.
Реакционная смесь может быть подкислена или кристаллическая суспензия может быть выварена с целью удаления растворителя с использованием 0,1-5 мас. водного раствора кислоты, предпочтительно хлористоводородной, муравьиной, фталевой, малоновой, фумаровой или алкилированной малоновой или малеиновой кислот, необязательно содержащих циансвязующее вещество.
Для экстракции кристаллической суспензии могут быть использованы водонерастворимые органические растворители, предпочтительно, гексан, циклогексан, петролейный эфир, дихлорметан, дихлорэтан, хлороформ, тетрахлорид углерода, этилацетат, бензол, толуол или ксилол. Целесообразно, экстракт промывать чистой водой или водой, насыщенной хлоридом натрия и/или 0,1 мас. водным раствором минеральных или органических кислот, предпочтительно, растворимыми хлористоводородной, уксусной, фталевой, малоновой, алкилированной малоновой, фумаровой или малеиновой кислот. В качестве циан-связующего использовать формальдегид.
Для рекристаллизации вещества могут быть использованы неполярный и протонный растворители, предпочтительно гексан, гептан, петролейный эфир, метанол, этанол, изопропанол или смесь растворителей с такими кислотами, как уксусная, малеиновая, фумароновая, малоновая или алкилированная малоновая кислоты.
В конце последовательного ряда операций вещество получают в виде кристаллов, расплава или раствора. Вещество содержит изомеры в стабильном соотношении и спустя 12 мес после получения.
В случае, если реакция проходит в безводных условиях, должно быть предотвращено разложение циперметрина, как указано выше. Подавление процесса разложения вызывает также уменьшение содержания циана в реакционной смеси.
Однако в процессе длительной обработки в промышленных условиях может иметь место незначительное разложение реакционной смеси. Поэтому появление свободного циана не вызывает проблем, связанных с безопасностью. Каждый раз, когда происходит процесс образования малых количеств свободного циана в результате подкисления среды, в реакционную смесь добавляют альдегид в качестве стабильного циансвязующего вещества для предотвращения попадания циана в воздух. Предпочтительно, использовать формальдегид. Таким образом полученный нитрил циангликолевой кислоты в остаточной смеси может быть гидролизован до гликолевой кислоты путем простого нагревания. Обработка полученной смеси не представляет собой опасности.
Преимущество данного способа состоит в том, что производительность может быть увеличена за счет нескольких реакторов периодического действия, а также может быть улучшена степень превращения. Образующееся вещество может быть подвергнуто непрерывному процессу обработки, что позволит избежать разложения или агрегации, связанной с остановкой. Желаемая конверсия может быть достигнута за короткий промежуток времени в зависимости от единицы вещества, что уменьшит опасность разложения. Температура оборудования должна сохраняться постоянной во избежание потери энергии.
Изобретение позволяет получить стабильные артроподикальные композиции, содержащие в качестве активного компонента смесь изомеров циперметрина с формулой I, которая содержит, по крайней мере, 95 мас. пару энантиомеров 1R cis S и 1S cis R (1a) и энантиомер 1R trans S и 1S trans R (1b) в соотношении 1а 1b 55 45 25 75 или пару изомеров 1а или 1b и в качестве стабилизатора соединение, содержащее 0,001-0,1 мас. в зависимости от активного компонента, кислоты или смеси кислот, предпочтительно нелетучих карбоксиловых кислот с рК1 1-5, таких как фталевая, янтарная, винная, малеиновая, фумаровая, малоновая или один или несколько раз алкилзамещенные производные этих кислот и/или щавелевой кислоты.
При осуществлении способа в соответствии с изобретением, при непрерывной или периодической подаче целесообразно использовать исходную реакционную смесь следующей концентрации: 50-80 мас. циперметрина, 1-50 мас. пропанола, 10-20 мас. триэтиламина или 0,0002-0,01 мас. DBU или DBN.
Целесообразно также убедиться в том, что концентрации в конечной реакционной смеси после завершения асимметричного превращения будут следующими: 25-45 мас. циперметрина, 45-75 мас. пропанола, 4-14 мас. триэтиламина или 0,0002-0,004 мас. DBN или DBU.
В непрерывном процессе скорость потока реакционной смеси составит 50-150 г/ч/л полезного объема системы реакторов.
Стабилизированные растворы или вещества, содержащие изомеры циперметрина вместе со стабилизированными кислотами, что было определено выше, могут быть использованы в смеси с добавками, используемыми в производстве пестицидов для сельского хозяйства, ветеринарии, в целях охраны здоровья людей и/или гигиены (ЕР 208758). Следует избегать использования добавок, которые могут противодействовать стабилизирующему действию кислот, особенно использования оснований, или принимать в расчет при определении количества используемой кислоты.
Было установлено, что небольшое количество основания в виде примесей, содержащих азот, участвует в эпимеризации конечного продукта. Такая же эпимеризация может быть вызвана присутствием примесей в добавленном растворителе или любым из остаточных реагентов, участвующих в процессе подготовки, или присутствием примесей в веществах, добавляемых при получении препаратов.
Реакционная смесь может быть подкислена или кристаллическая суспензия может быть выварена с использованием 0,1-5 мас. водного раствора кислоты, предпочтительно хлористоводородной, муравьиной, фталевой, малоновой, фумаровой или алкилированной малоновой или малеиновой кислот, необязательно содержащих циансвязующее вещество.
Для экстракции кристаллической суспензии могут быть использованы водонерастворимые органические растворители, предпочтительно в виде гексана, циклогексана, петролейного эфира, дихлорметана, дихлорэтана, хлороформа, тетрахлорида углерода, этилацетата, бензола, толуола или ксилола. Целесообразно, чтобы экстракт был промыт чистой водой или водой, насыщенной хлоридом натрия и/или 0,1 мас. водным раствором минеральных или органических кислот, предпочтительно растворами хлористоводородной, уксусной, фталевой, малоновой, алкилированной малоновой, фумаровой или малеиновой кислот.
Для рекристаллизации вещества могут быть использованы неполярный и протонный растворители предпочтительно гексан, гептан, петролейный эфир, метанол, этанол, изопропанол или смесь растворителей с такими кислотами, как уксусная, малоиновая, фумаровая, малоновая или алкилированная малоновая кислоты.
В конце последовательного ряда операций вещество получают в виде кристаллов, расплава или раствора. Вещество содержит изомеры в стабильном соотношении и спустя 12 мес после получения.
В случае, если реакция проходит в безводных условиях, должно быть предотвращено разложение циперметрина, как указано выше. Подавление процесса разложения вызывает также уменьшение содержания циана в реакционной смеси.
Тем не менее в процессе длительной обработки в промышленных условиях может иметь место незначительное разложение реакционной смеси. Поэтому появление свободного циана не вызовет проблем, связанных с безопасностью. Каждый раз, когда происходит процесс образования малых количеств свободного циана в результате подкисления среды, в реакционную смесь добавляют альдегид в качестве стабильного циансвязующего вещества для предотвращения попадания циана в воздух. Предпочтительно использовать формальдегид. Таким образом полученный нитрил цианогликолевой кислоты в остаточной смеси может быть гидролизован до гликолевой кислоты путем простого нагревания. Обработка полученной смеси не представляет собой опасности.
Асимметричное превращение 2-го порядка является гетерогенной равновесной реакцией, состоящей из двух стадий. Определение кинетики данной реакции возможно только путем эксперимента. В данном случае процесс усложняется в связи с тем, что концентрация, изменяющаяся в процессе кристаллизации, подвергается затем изменению в результате процесса разбавления, и температура реакции эпимеризации может быть увеличена, а затем снижена в ходе процесса. С целью выяснения, позволяет ли кинетика реакции использование цепи реакторов теоретически, был определен порядок реакции. Реакция может быть описана как реакции с кажущейся кинетикой 2-го порядка, что означает возможность возрастания производительности и степени превращения при использовании непрерывной или наполовину непрерывной цепи реакторов, что может быть достигнуто, соответственно за единицу времени.
Способ по изобретению основан на том, что кинетика реакции асимметричного превращения циперметрина 2-го порядка, позволяет осуществлять процесс более благоприятно при использовании непрерывной или наполовину непрерывной цепи реакторов. Реакция может идти непрерывно или квазинепрерывно. В первом случае вещества добавляют или извлекают непрерывно, в то время как во втором случае вещество подают по частям таким образом, чтобы цепь реакторов работала без перерыва. Несколько цепей реакторов могут быть образованы параллельно друг другу. В реакторной цепи предпочтительно использовать транссоединения, так как это способствует рециркуляции и возобнолению процесса. Преимущество метода состоит в том, что производительность может быть увеличена за счет нескольких реакторов периодического действия, а также может быть улучшена степень превращения. Образующееся вещество может быть подвергнуто непрерывному процессу обработки, что позволит избежать разложения или агрегации, связанной с остановкой. Желаемая конверсия может быть достигнута за короткий промежуток времени в зависимости от единицы вещества, что уменьшит опасность разложения. Температура оборудования должна сохраняться постоянной во избежание потери энергии.
Изобретение обеспечивает получение стабильных артро подикальных композиций, содержащих в качестве активного компонента смесь изомеров циперметрина формулы 1, которая содержит по крайней мере 95 мас. пару энантиомеров 1R cis S и 1S cis R (1a) и энантиомер 1R troms S и trous R (1b) в соотношении 1а 1b 55 45 25 75 или пару изомеров 1а или 1b и в качестве стабилизатора соединению, содержащее 0,001-0,1 мас. в зависимости от активного компонента, кислоты или смеси кислот, предпочтительно нелетучих карбоксиловых кислот с рК1 1-5, таких как фталевая, янтарная, винная, малеиновая, фумаровая, малоновая или один или несколько раз алкилзамещенные производные этих кислот и/или щавелевой кислоты.
При осуществлении способа в соответствии с изобретением при непрерывной или периодической подаче целесообразно использовать исходную реакционную смесь следующей концентрации: 50-80 мас. циперметрина, 1-50 мас. пропанола, 10-20 мас. триэтиламина или 0,0002-0,01 мас. DBU или DBN.
Целесообразно также убедиться в том, что концентрации в конечной реакционной смеси после завершения асимметричного превращения будут следующими: 25-45 мас. циперметрина, 45-75 мас. пропанола, 4-14 мас. триэтиламина или 0,0002-0,004 мас. DBN или DBU.
В непрерывном процессе скорость потока реакционной смеси составит 50-150 г/ч/л полезного объема системы реакторов.
Стабилизированные растворы или вещества, содержащие изомеры циперметрина вместе со стабилизированными кислотами, что было определено выше, могут быть использованы в смеси с добавками, используемыми в производстве пестицидов для сельского хозяйства, ветеринарии, в целях охраны здоровья людей и/или гигиены (ЕР 208, 758). Использования добавок, которые могут противодействовать стабилизирующему действию кислот, особенно использования оснований, следует избегать или принимать в расчет при определении количества используемой кислоты. Также должны быть соответствующим образом подобраны растворители.
Дальнейшие подробности описания изобретения проиллюстрированы на следующих примерах.
Анализ используемых выделенных веществ был сделан методом высокоэффективной жидкостной хроматографии. См. "Аналитические методы Регуляторов Роста Растений и Пестицидов": XIII, изд. Цвейг и Шерма, Academic Piess, 1984.
Там, где на это нет специальной ссылки, содержание воды и веществах составляет менее 0,1 мас.
П р и м е р 1. В цепь соединяют 7 реакторов емкостью 750 мл, оборудованных холодильником и мешалкой. Первый реактор охлаждают до 0оС, второй до 8оС и далее последовательно до 14, 15, 10,0 и -10оС. В реакторы добавляют 100 г изомеров 1R cis S и 1S cis R (1a) и 1R trans S и 1S trans R (1b) в соотношении (1а): (1b) 40: 60 и 95% кристаллического α-циан-(m-феноксибензил)-эфира 2,2-диметил-3-(2: 2-дихлорвниил)-циклопропан-карбоксиловой кислоты (циперметрина). В первый и второй реакторы тажке добавляют 30 мл изопропанола и 30 мл триэтиламина и дополнительно в третий реактор 40, в четвертый 80, а пятый 120, в шестой 160 и в седьмой 200 мл изопропанола. Смесь термостатируют при сильном перемешивании. В первый реактор добавляют 100 г масляного циперметрина, содержащего все цис- и трансизомеры в соотношении 41:59, средней чистоты 94% и 30 мл изопропанола. Смесь непрерывно перемеашивают и через 12 ч в первый реактор загружают 30 мл триэтиламина. Половина разбавленной смеси переходит в следующий реактор и процесс добавления циперметрина и изопропанола в первый реактор повторяют снова. Через 12 ч смесь в первом реакторе разбавляют с помощью 30 мл триэтиламина и половина смеси из второго реактора переходит в третий, а половина содержимого первого реактора переходит во второй реактор. Затем 100 г циперметрина и 30 мл изопропилового спирта снова добавляют в первый реактор и после 12 ч перемешивания содержимое первого реактора разбавляют 30 мл триэтиламина, в третий реактор добавляют 40 мл изопропанола, и половина смеси переходит из третьего в четвертый реактор, из второго в третий, а из первого во второй реактор.
Повторив процесс подачи циперметрина и изопропанола после 12-часового перемешивания и прохождения веществ, в первый реактор добавляют 30 мл триэтиламина, а в 3, 4, 5, 6 и 7 реакторы добавляют по 40 мл изопропанола. Половина смеси из одного реактора переходит в следующий, а вещество, полученное в конце реакторной цепи, проходит через фильтр. Полная последовательность операций повторяется каждые 12 ч. Отфильтрованное вещество, содержащее 0,1 мас. формальдегида, промывают изопропанолом, содержащим 0,5% уксусной кислоты и высушивают при комнатной температуре. Каждый раз получают 85 г снежно-белого кристалличесокго вещества.
Соотношение изопропанол циперметрин по реакторам приведено в табл. 1.
Частота: 97 мас. составляет 38,5% для пары изомеров 1а и 58,5% для пары изомеров 1b.
Темпераутра плавле ния 63оС.
Выход относительно исходного вещества 85%
П р и м е р 2. В цепь соединяют 7 реакторов емкостью 750 мл, оборудованные холодильником и мешалкой. Первый реактор охлаждают до 20оС, второй до 25оС, третий до 25оС, четвертый до 20оС, остальные реакторы охлаждают до темпераутры на 5оС ниже температуры предыдущего реактора. В реакторы добавляют 100 г пары изомеров (1b), содержащей по крайней мере 95% кристаллического конечного вещества. В первый и второй реакторы помещают 30 мл триэтиламина и 30 мл изопропанола. Дополнительно в третий реактор добавляют 40, в четвертый 80, в пятый 120, в шестой 180 и в седьмой 200 мл изопропанола. Смесь термостатируют при сильном перемешивании и затем в первый реактор добавляют 100 г масляного циперметрина, содержащего все трансизомеры средней чистоты 94% или расплав циперметрина и 30 мл изопропанола. Через 12 ч после перемешивания в первый реактор добавляют 30 мл триэтиламина. Половина разбавленной смеси переходит в следующий реактор, и процесс добавления циперметрина и изопропанола повторяют. Через 12 ч смесь в первом реакторе разбавляют с помощью 30 мл триэтиламина. Половина смеси из второго реактора переходит в третий, в половина содержимого третьего реактора переходит в четвертый. Затем в первый реактор снова добавляют 100 г циперметрина и 30 мл изопропилового спирта. Через 12 ч после перемешивания в первый реактор добавляют 30 мл триэтиламина, а в третий 40 мл изопропанола. Половина содержимого из третьего реактора переходит в четвертый реактор и из второго реактора в третий, затеем из первого реактора во второй. После повторения процессов добавления циперметрина и изопропанола, через 12 ч после перемешивания в первый реактор добавлют 30 мл триэтиламина, а в 3, 4, 5, 6 и 7 реакторы 40 мл изопропанола. Половина содержимого реактора переходит в следующий реактор и вещество, полученное в конце реакторной цепи, проходит через фильтр. Полная последовательность операций повторяется каждые 12 ч. Отфильтрованное вещество, содержащее 0,5 мас. формальдегида промывают с помощью изопропанола, содержащее 0,5 г фталевой кислоты, и высушивают при комнатной температуре. Каждый раз получают 85 г снежно-белого кристаллического вещества, содержащего 98% пары изомеров 1а.
Соотношение изопропанол циперметрин по реакторами приведены в табл. 2.
Температура плавления 80оС.
П р и м е р 3. Процесс происходит так, как описано в 1 примере за исключением того, что в качестве исходного вещества используют циперметрин, содержащий цис-трансизомеры в соотношении 1:1, а в качестве затравочного кристалла берут кристалл, содержащий изомеры 1а и 1b в соотношении 1:1 концентрацией по крайней мере 95% Получают 85 г снежно-белого кристаллического вещества. Соотношения в реакторах те же, что и в примере 1.
Чистота 97 мас.
Соотношение изомеров 1a 1b 48:49.
Темпераутра плавления 65оС.
П р и м е р 4. Процесс происходит так, как описано в примерах 1-4, за исключением того, что вещество, полученное в конце реакторной цепи, содержащее 0,2 мас. формальдегида, окисляют с помощью 0,2 мас. водного раствора хлористоводородной кислоты, экстрагируют при нагревании до 65оС с использованием 500 мл гептана и промывают горячим способом с помощью 50 мл 1%-ного раствора хлористоводородной кислоты, 100 мл воды и 100 мл раствора хлористоводородной кислоты, 100 мл воды и 100 мл насыщенного раствора хлорида натрия. Смесь кристаллизуют при постоянном охлаждении до -5оС. Осажденное вещество отфильтровывают и высушивают. Каждый раз получают 87 г белого кристаллического продукта. Соотношения изопропанол циперметрин те же, что и в примере 1 и 2.
Чистота 98,5 мас.
Соотношение изомеров 1a 1b 39,0:59,5.
Температура плавления 65,5оС.
П р и м е р 5. Процесс происходит так, как описано в 1 примере, за исключением того, что вещество, полученное в конце цепи реакторов, содержащее 0,3 мас. формальдегида, окисляют с помощью 0,2 мас. хлористоводородной кислоты. Смесь экстрагируют дихлорэтаном, органический слой промывают с помощью 50 мл 1 мас. водного раствора хлористоводородной кислоты и дважды с помощью 100 мл воды выпаривают и растворяют в двойном количестве метанола. Кристаллизация происходит при постепенном охлаждении до -5оС. Каждый раз получают 86 г снежно-белого кристаллического вещества. Соотношения изопропанол: циперметрин те же, что и в примере 1.
Чистота 98 мас.
Соотношение изомеров 1a 1b 39:59.
Температура плавления 63оС.
П р и м е р 6. Процесс происходит так, как описано в 1 примере, за исключением того, что вещество, полученное в конце реакторной цепи, нейтрализуют с помощью 2 мас. хлористоводородной кислоты, экстрагируют этилацетатом и промывают органический слой 5 раз с применением 50 мл 0,5 мас. водного раствора фталевой кислоты, содержащего 0,1 мас. формальдегида. После выпаривания его растворяют в двойном объеме 2 мас. раствора фталевой кислоты и метанола. Кристаллизация происходит при постепенном охлаждении до -5оС. Кристаллы отфильтровывают и высушивают. Получают 86 г снежно-белого кристаллического вещества.
Соотношения изопропанол циперметрин те же, что и в примере 1.
Чистота 98%
Соотношение изомеров 1a 1b 39:59.
Соотношение изомеров остается неизменным по прошествии срока годности через 12 мес.
Температура плавления 63оС.
П р и м е р 7. Процесс происходит так, как описано в 1 примере за исключением того, что после начала процесса в цепь реакторов добавляют кристаллический циперметрин чистоты 99,5% содержащий цис- и трансизомеры в соотношении 4: 6. Каждые 24 ч происходит перенос вещества. В конце цепи реакторов полученную суспензию окисляют водным раствором, содержащим 0,4 мас. формальдегида и 2 мас. хлористоводородной кислоты, экстрагируют с помощью 500 мл (433 г) ксилита и промывают 50 мл 2 мас. водного раствора фталевой кислоты и 100 мл (1% ) раствора малеиновой кислоты. Таким образом получают 535 г раствора Chimuis, содержащего 6,9% пары изомеров 1а, 10,6% пары изомеров 1b, 0,35 пары изомеров 1с и 0,28% пары изомеров 1d.
Соотношение изопропанол циперметрин те же, что и в примере 1.
П р и м е р 8. Процесс происходит так, как описано в 1 примере за исключением того, что полученное в конце реакторной смеси вещество окисляют с помощью водного раствора, содержащего 0,2 мас. хлористоводородной кислоты и 0,4 мас. формальдегида. Смесь экстрагируют с использованием 400 мл петролейного эфира (100-120) при нагревании до 60оС, органический слой промывают водным раствором, содержащим 0,1 мас. формальдегида и 0,1 мас. хлористоводородной кислоты, а затем 50 мл раствора, содержащего 1 мас. хлористоводородной кислоты и 0,1 мас. формалина, 50 мл воды и 50 мл водного раствора, содержащего 5 мас. диэтилмалоновой кислоты. Органический слой отделяют, и раствор кристаллизуют при медленном охлаждении. После фильтрования и высушивания получают 88 г снежно-белой кристаллической смеси изомеров 1а 1b 39,0 59,5.
Соотношения изопропанол циперметрин те же, что и в примере 1.
Чистота 98%
Температура плавления 65оС.
П р и м е р 9. Процесс происходит так, как описано в примере 8, за исключением того, что после промывания раствором малоновой кислоты на последнем этапе работы используют 50 мл воды и отделяют органический слой. В раствор добавляют 0,2 мл пропанола, содержащего 0,04 г малоновой кислоты. Смесь кристаллизуют при медленном охлаждении. После фильтрования и высушивания получают 87 г белого кристаллического вещества, которое представляет собой смесь изомеров 1а 1b 39,0 59,5.
Соотношение изопропанол циперметрин те же, что и в примере 1.
Чистота 98,5%
Температура плавления 64-66оС.
Соотношение изомеров остается неизменным по истечение срока годности через 12 мес.
П р и м е р 10. Испытание на устойчивость. 1 г вещества, полученного способом, описанным в примере 9 растворяют в 2 мл толуола и раствор разбавляют 8 мл безводного этанола, добавляют 10 об. раствора триэтиламина. Растворы выдерживают одну неделю при комнатной температуре и затем исследуют изомерный состав вещества.
Х 1с + 1d
Y 1a + 1b
Данные приведены в табл. 3.
П р и м е р 11. 200 г реакционной смеси, содержащей кристаллическое вещество, полученное способом, приведенным в примере 1, помещают в устройство, оборудованное нагревателем, мешалкой и разгружаемое через дно. Смесь окисляют при постоянном перемешивании водным раствором, содержащим 2 мас. хлористоводородной кислоты и 0,2 мас. формальдегида до рН 2. После перемешивания в течение 15 мин рН раствора проверяют и расплавляют кристаллическую суспензию до эмульсии путем нагревания до 60оС. После 15 мин перемешивания масляный циперметрин осаждают и отделяют. Тепловое вещество добавляют в 150 мл изопропаноле, содержащего 1 мас. малеиновой кислоты, кристаллизуют после медленного охлаждения и вычевают. Выпавшие снежно-белые кристаллы отфильтровывают, промывают 50 мл ледяного изопропанола, содержащего 1 мас. малеиновой кислоты, и высушивают. Таким образом получают 56 г снежно-белого кристаллического вещества.
Температура плавления 62,5-63оС.
Чистота 97%
Соотношение изомеров 1a 1b 38,5:58,5.
Выход относительно количества исходного вещества составляет 88%
П р и м е р 12. Процесс происходит в соответствии с описанием, данным в примере 1, но в 1000 раз большем объеме. Загрузка и выход веществ происходит непрерывно.
Используют следующие потоки веществ, приведенные в табл. 4.
В среднем ежедневно получают 171 кг вещества способом, описанным в примере 1.
П р и м е р 13. Процесс проводят в соответствии с описанием примера 12, но в качестве исходного вещества берут масляный трансциперметрин и в каждый реактор загружают кристаллическое вещество, содержащее 93% изомеров 1b. Смесь выдерживают при температуре в соответствии с данными примера 2. Затем триэтиламин со скоростью потока 1,83 кг/ч переходит во второй реактор, что повышает кристаллообразующую способность вещества в первом реакторе. Таким образом получают 173,2 кг снежно-белого кристаллического вещества, содержащего пару изомеров 1b в 98,1% с температурой плавления 80,5оС.
| название | год | авторы | номер документа |
|---|---|---|---|
| СИНЕРГИТИЧЕСКАЯ ИНСЕКТИЦИДНАЯ КОМПОЗИЦИЯ | 1988 |
|
RU2045183C1 |
| СИНЕРГЕТИЧЕСКАЯ КОМПОЗИЦИЯ ПРОТИВ ЧЛЕНИСТОНОГИХ | 1989 |
|
RU2069058C1 |
| Способ получения изомерной смеси циперметрина | 1986 |
|
SU1579454A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ХИНОЛИНКАРБОНОВЫХ КИСЛОТ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫХ СОЛЕЙ | 1988 |
|
RU2049783C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ АМИДОКСИМА О-(2-ГИДРОКСИ-3-ПИПЕРИДИНО-1-ПРОПИЛ)-НИКОТИНОВОЙ КИСЛОТЫ И ИХ СОЛЕЙ (ВАРИАНТЫ), ЧИСТОЕ КРИСТАЛЛИЧЕСКОЕ ОСНОВАНИЕ АМИДОКСИМА О-(2-ГИДРОКСИ-3-ПИПЕРИДИНО-1-ПРОПИЛ)-НИКОТИНОВОЙ КИСЛОТЫ | 1990 |
|
RU2074854C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ПРОПАРГИЛАММОНИЙХЛОРИДА | 1994 |
|
RU2130450C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ХИНОЛИНКАРБОНОВЫХ КИСЛОТ | 1988 |
|
RU2014331C1 |
| ЭМУЛЬГИРУЮЩИЙСЯ КОНЦЕНТРАТ ДЛЯ ЗАЩИТЫ РАСТЕНИЙ И ЭМУЛЬСИЯ ДЛЯ ОБРАБОТКИ РАСТЕНИЙ | 1989 |
|
RU2086125C1 |
| ИНСЕКТИЦИДНАЯ КОМПОЗИЦИЯ ДЛЯ ЗАЩИТЫ РАСТЕНИЙ ОТ ЧЛЕНИСТОНОГИХ ВРЕДИТЕЛЕЙ ДЛЯ УМО-ПРИМЕНЕНИЯ | 1989 |
|
RU2024225C1 |
| ПРОИЗВОДНЫЕ 3,6-ДИЗАМЕЩЕННОГО 1,2,4,5-ТЕТРАЗИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ЛАРВИЦИДНО- И ОВИЦИДНО-АКТИВНАЯ КОМПОЗИЦИЯ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СПОСОБ УМЕНЬШЕНИЯ КОЛИЧЕСТВА ЛИЧИНОК И ЯИЦ КЛЕЩЕЙ | 1994 |
|
RU2142949C1 |


Использование: в химии циперметрина, в частности в способе получения его изомеров. Сущность изобретения: продукт изомеры циперметрина ф-лы I, где углеродистые атомы, обозначенные 1, 3 и альфа, относятся к хиральному атому углерода, волнистая линия означает цис- или транс-конфигурацию относительно циклопропанового кольца. Продукт из теоретически возможных 8 изомеров циперметрина содержит по крайней мере 95% пара-изомеров 1 R транс S и 1Sтранс R (1b) или только смесь 1R цис S и 1S цис R (1a) и пару изомеров 1В с соотношением 1a: 1b, равным (55:45) (25:75). Реагент 1: смесь изомеров циперметрина (с чистотой минимум 90%), содержащая транс-изомеры или пару изомеров (1b) цис-, а другие транс-изомеры или пару изомеров (1a+1b) с нежелательным соотношением. Условия реакции: асимметричное превращение второго порядка ведут в присутствии амина и протонного растворителя при температуре от нуля до 25°С. Соединение ф-лы I:  8 з. п. ф-лы, 4 табл.
8 з. п. ф-лы, 4 табл.
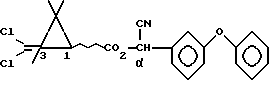
где α углеродные атомы 1,3 относятся к хиральному атому углерода;
волнистая линия указывает на цис- или трансконфигурацию относительно циклопропанового кольца,
которые из теоретически возможных 8 изомеров циперметрина содержат по крайней мере 95% пары изомеров 1R транс S и 1S транс R (1b) или только смесь 1R цис и 1S цис (1a) и пару изомеров (1b) с соотношением 1a 1b 55 45 - 25 75, путем асимметричного превращения второго порядка, осуществляемого в присутствии третичного амина и протонного растворителя при 0 25oС из исходной смеси изомеров циперметрина с чистотой минимум 90% которая содержит следующие за парой изомеров (1b) цис- и другие трансизомеры или пару изомеров 1a 1b с нежелательным соотношением, отличающийся тем, что превращение осуществляют непрерывно в 2 7 реакторах, оборудованных холодильником, смесителем, подогревателем, установленных друг за другом с диапазоном указанной температуры с максимальной разницей температур в реакторах 10oС, при этом в первый реактор вводят исходную смесь изомеров указанной формулы с чистотой по крайней мере 90% с добавлением 1 мас.ч. конечного кристаллического циперметрина или смеси изомеров 1a и/или 1b в изопропаноле в количестве 0,4 мас.ч. с добавлением триэтиламина в таком количестве, что его содержание составляет 0,4 мас.ч. смесь перемешивают и часть реакционной смеси переводят во второй реактор, в который при необходимости добавляют третичный амин и изопропанол, и затем в последующие реакторы, в которые дополнительно вводят изопропанол, при этом в первый реактор непрерывно или периодически добавляют исходный циперметрин, более 0,4 мас.частей изопропанола и/или третичного амина, реакционная смесь вновь последовательно проходит через все реакторы, проходя указанную обработку, из полученной при этом кристаллической суспензии при необходимости выделяют кристаллы и при необходимости нейтрализуют основание, содержащееся в извлеченной из последнего реактора реакционной смеси или по поверхности кристаллического продукта и/или рекристаллизуют конечный продукт из растворителя, содержащего кислоту, и/или расплавляют и вываривают суспензию кристаллов при 60 70oС в присутствии кислоты, затем экстрагируют кристаллический продукт при 0 70oС и экстракт промывают водным раствором соли и/или кислоты, при необходимости добавляют альдегид как циансвязующий агент на одной из стадии выделения из кристаллической суспензии.
гептан, петролейный эфир, этилацетат, бензол, толуол, ксилол.
| Шланговое соединение | 0 |
|
SU88A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1995-10-10—Публикация
1990-01-17—Подача