Изобретение относится к новым химн- Ч65СКИМ соединениям, а именно 7-а1Щл- амидоцефалоспоринам общей формулы
-J™Y
N- COOR,
(I)
где R - водородi натрий, пивалоилок- симетил или 1-пивалоилокси- этил;
, R, - З-хлор-1, 2, 4--триазолил или 5-метил-15 2,354-тетразолиЛэ которые присоединены к экзометиленовой группе в положении 3 дефемового кольца через азотуглеродную связь в виде син-изомеров, проявляющих антибактериальные свойства, или к их гидр охл оридам.
Цель изобретения - поиск новых соединений цефалоспорина, обладающих высокой антибактериальной активностью при низкой токсичности.
И р и м е .р 1 о
1. В -16 мл NsN-диметилацетамида растворяют 3,15 г 2-(2-трет.аминокси- карбоксамидотиазол-4™ил) --М-2-(син)- метоксииминоуксусной кислоты и по Kan .лям при -20°С добавляют 1,69 г окси- хлорида фосфора. Полученную смесь перемешивают при этой текгпературе в течение 1,5 ч, а затем в раствор по каплям добавляют при (-30) (-20)С 3,16 г 7-амино 8 -(З-хлор-ТS2э4-тpи- aзpли.п)мeтш --i32 цефем-4-карбоновой кислоты и 6,1 г ПэО-бис(триметнлеи- лил)ацетамида в 32 мл безводного хло
ристог о метилена. После добавления
по каплям проводят реакцию при этой температуре в течение 1 ч, затем - при 0-10°С в течение 0,5 ч и затем при комнатной температуре в течение 0,5 ч. После завершения реакции отгоняют при понилсенном давлении мети- ленхлорид и полученный остаток вводят в .смесь растворителей ш 80 мл воды и 100 мл этилацетата„ Органический слой затем отделяют и добавляют 80 мл воды. Затем регулируют рН би карбонатом натрия. Водный слой отделяют и добавляют 80 мл эт1- лацетата, после чего рН доводят до 1,5 2н« соляной кислотой при охлаждении льдом Органический слой отделяют, последо- вательно промывают 500 мл воды и 50 насыщенного водного р&створа хлористого натрия и сушат - т, безводным
0
5
g
5
0
5
сульфатом магния. Затем растворитель удаляют перегонкой при пониженном давлении. К остатку добавляют серный эфир.и полученные кристаллы отфильтровывают, получая 5,62 г (выход 91,8%) 7-(25 2 трет„амилоксикарбоксамидоти- )-2-(син)-метоксииминоацет- амидо-8-(3-хлор-1,2,4-триазолил)-4 - цефем-4-карбоновой кислоты с точкой плавления 198-200°С (с разложением).
II.В 30 мл трифторуксусной кислоты растворяют 5,62 г полученной 7-2-(2-трет,амилоксикарбоксамидоти- азол-4-ил)2(син)-метоксиацетамидо- -8-(3-хлор-1, 2,4-триазолил)метил-. - -цефем 4-карбоновой кислоты.Реакцию осуществляют при комнатной температуре
в течение 30 мин. После завершения реак-- ции растворитель отгоняют при понижен- - ном давлении. К остатку добавляют серный эфир и полученные кристаллы отфильтровывают, тщательно промывают серным эфиром и сушат, в результате чего получают 5,23 г (выход 33,1%) трифторуксусно- кислой соли (2-аминотиазол-4- ил)-2-(син)-метоксииминоацетамидо - 3-(3-хлор-1,2,4-триазолил)-метил-Л - цефем-4-карбоновой кислоты с точкой плавления 162 С (с разложением).
ИК-спектр (КВг), см : ) 1715; 1670; 1,630,
III,В 25 мл воды суспензируют 6,13 г трифторуксусной соли (2- аминотиазол-4-ил)-2-(син)-метоксиими- йоацетамида -3-(3-хлор-1,2,4-триазолил) -метил-,/ -цефем-4-карбоновой кислоты и к полученной суспензии добавляют бикарбонат натрия при охлаждении льдом, доводя рН суспензии до 8,0, при которой суспензия превращается
в раствор. Затем рН доводят до 2,5 концентрированной соляной кислотой при указанной температуре, в результате чего выпадают кристаллы. Кристаллы отфильтровывают, тщательно промывают водой, а затем ацетоном и сушат, получая 4,71 г (выход 94,5%) 7-С2-(2-аминотиазол-4- Ш-) -2-(син) - метоксииминоацетамидо -3-(3-хлор- 1,2,4-триазолил)-метил-/ -цефем-4- карбоновой кислоты с точкой плавления по крайней мере .
ИК-спектр (КВг), см : f, M65 , 1660; 1625,
Аналогичным образом получают (2-аминотиазол-4-ил) -2-(син) -мегокси- иминоацетамидо -3- 2-(5-метил-1,2,3, 4-тетразолил)метил -й цефем-5-карбоVc,o 1760;
314
новую кислоту с точкой плавления выше 200°С.
ИК-спектр (КВг), см : V. 1765; 1660; 1625.
IV. Соединение, полученное в II, подвергают обработке 1 н.водным раст- fopoM NaOH при охлаждении льдом, получая (2-аминотиазол-4-ил)-2- (син)-метоксииминоацетамидо7-3-(3- хлор-1,2,4-триазолил)-метил-/9 -цефем- 4-карбоксилатнатрия с точкой плавления 168°С (с разложением).
ИК-спектр (КВг), см 1670; 1605.
Аналогичным образом получают 7-{ 2- (2-аминотиазол-4-ил)-2-(син)-метокси- иминоацетамидо}-3- 2-(5-метил-1,2,3, 4-тетразолил) -метил -/1 -цефем-4-кар- боксилатнатрия с точкой плавления 183-187°С (с разложением).
ИК-спектр (КВг), 1665; 1610.
Соединение, полученное на стадии II, подвергают взаимодействию с концентрированной соляной кислотой в 90%-ном этанольном водном растворе (V/V) с получением гидрохлора (2-аминотиазол-4-ил)-2-(син)-метокси- аминоацетамидо1-3-(3-хлор-1,2,4-три- азолил)-метил -Л -цефем-4-карбоновой ислоты.
ИК-спектр (КВг). см : Vc-c.1770; 1720; 1680; 1620.
Используя описанную методику получают гидрохлорид (-2-аминоти- азол-4-ш1)-2-(син)-метоксииминоацета- мидо (5-метил-1,2,3,4-тетразолил) -метилJ-4 -цефем-4-карбоновой кислоты с tfiA 136-158° С.
Пример 2. К смешанному растворителю из 8 мл безводного хлористого метилена и 2,2 мл Н,К-диметилацет- амида добавляют 3,7 г оксихлорида фосфора при О - 5°С, полученную смесь подвергают реакции при той же температуре в течение 30 мин. Затем реакционную смесь охлаждают до (-15) - , добавляют 2,4 г 2-(2-амино- тиазол-4-ил)-2(син)-метоксииминоук- сусной кислоты и полученную смесь одвергают реакции при той же темпеатуре в течение 20 мин. К реакционной смеси при по каплям добавяют раствор 4,47 г хлоргидрата пива- оиЛоксиметилового эфира 7-амино-З- 2-(5-метш1-1,2,3,4-тетраз олил)-ме тил3-4 -цефем-4-карбоновой кислоты 1,01 г триэтиламина в 20 мл без329
водного хлористого метилена. После закапывания смесь реагирует при -10 С в течение 30 мин, при 0°С - в течение 30 мин, а затем при комнатной температуре - 30 мин. После завершения реакции растворитель отгоняют при пониженном давлении и к остатку добавляют 50 мл воды и 50 мл этилQ ацетата, после чего рН доводят до 7,0 бикарбонатом натрия. Органический слой отделяют, последовательно промывают 30 мл воды и 30 мл насыщенного водного раствора хлорида натрия
5 и сушат над безводным сульфатом магния. Растворитель отгоняют при пониженном давлении и к остатку добавляют серный эфир. Полученные кристаллы собирают фильтрованием и получают
Q 5,1 г (выход 86%) пивалоилоксиметило- вого эфира (2-аминотиазол-4-ил)- 2-(син)-метоксииминоацетамидо}-3- 2- (5-метил-1,2,3,4-тетразолил)-метилJ- 4 -цефем-4-карбоновой кислоты с точ5 кой плавления 127-128°С (с разложением) .
ИК-спектр (КВг), 1780; 1753; 1675.
Аналогично получают следующие соJQ единения:
пивалоилоксиметил-7-| 2-(2-амино- тиазол-4-ил)-2-(син)-метоксиимино- ацетамнно1-3-Е(3-хлор-1,2,4-триазо- . лил)-метил -4 3-цефем-4-карбоксилат с точкой плавления 118-122 С (с разло- жением);
1-пивалоилоксиэтил-7- 2-(2-амино- тиазол-4-ил)-2-(син)-метоксииминоацет- амино -3- 2-(5-метил-1,2,3,4-тетразо-, . лил)-метил -4 -цефем-4-карбоксилат с температ5фой плавления 127-130°С с разложением;
гидрохлорид пивалоилоксиметил-7- Г2-(2-аминотиазол-4-ш1)-2-(син)-меТок - сииминоацетамидо -3- 2-(5-метил-1,2, 3,4-тетразолил)-метип1-л -цефем-4- карбоксилата, имеющего температуру плавления 144-148 С;
гидрохлорид 1-пивалоилоксиэтил-7- 2-(2-аминотиазОЛ-4-ИЛ)-2-(син)-ме- токсииминоацетамидо1-3- 2-(5-метш1- 1, 2,3,4-тетразолил)-метил -/l3-цефем- 4-карбоксилат (перекристаллизация из метанола) с температурой плавления 150 (разложение); хлоргидрат пивалоилоксиметилового эфира (2-аминотиазол-4-ил)-2- (син)-метоксииминоацетамидо -3- 1(3- хлор-1,2,4-триазолил)-метил -Л -це5
фем-4-карбоновой кислоты с точкой плавления 134-136 С (с разложением),
Проводят испытания фармакологического действия полученных соедине
НИИ .
Антибактериальная активность.
В соответствии со стандартным способом культуру, полученную культивированием бактерий в бульоне вытяжки сердца при в течение 20 ч высевают в агар вытяжки сердца и культивируют при 37°С в течение 20 ч, после чего рост бактерий проверяют визуаль
в положении 3 цефемового ядра, именуются Г(3-хлор-1,2,4-триазо- лил)-метилJ- -.
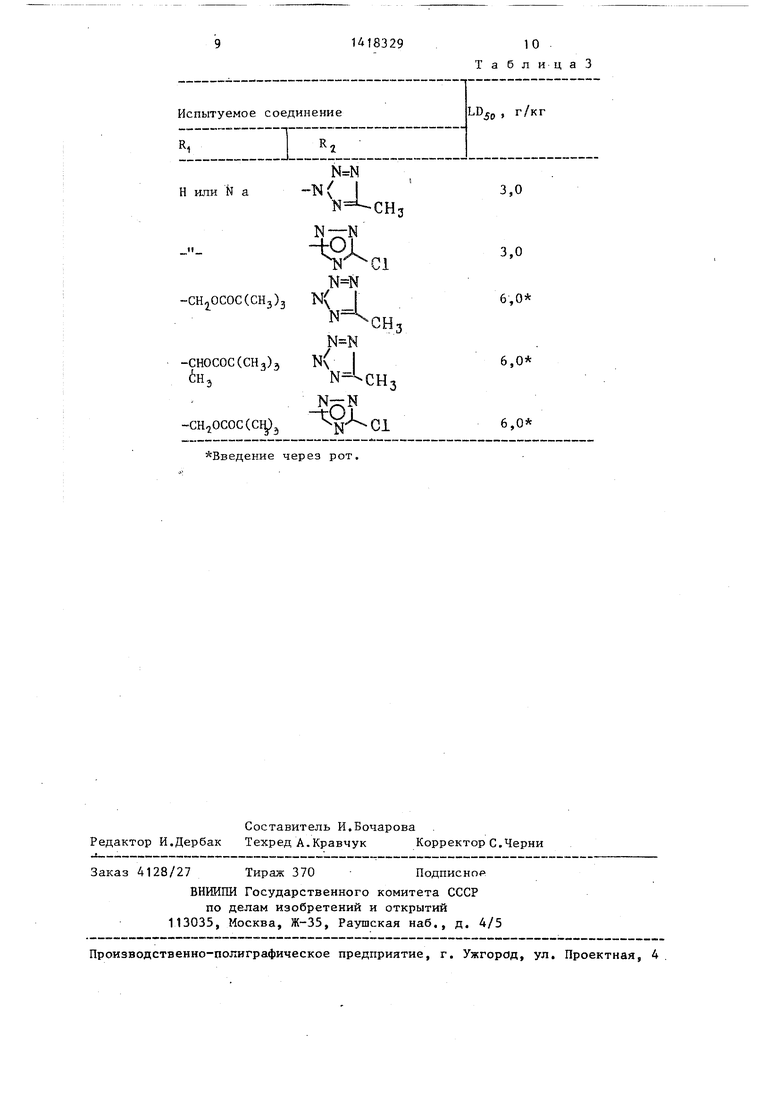
Эксперимент с пероральным введением проводят следующим образом.
Каждое испытуемое соединение вводят через рот мышам (tCP, мужские особи в возрасте 4 нед) при дозировке 2 мг на особь и определяют вьщеле- ние соединения с мочей. Результаты представлены в табл, 2. После всасывания живым организмом все испытуемые соединения легко отщепляют эфир



| название | год | авторы | номер документа |
|---|---|---|---|
| 7-Амино-3-замещенный метил- @ -цефем-4-карбоновая кислота в качестве промежуточных продуктов в синтезе 7-ациламидоцефалоспоринов,проявляющих антибактериальные свойства | 1983 |
|
SU1350166A1 |
| Способ получения производных цефалоспорина или их солей | 1981 |
|
SU1190987A3 |
| Способ получения цефалоспорина или его солей | 1982 |
|
SU1274625A3 |
| Способ получения производных цефалоспорина или их солей | 1982 |
|
SU1318144A3 |
| Цефалоспорины как промежуточные продукты в синтезе цефалоспоринов,обладающих антибактериальными свойствами | 1982 |
|
SU1249017A1 |
| Способ получения цефемовых соединений или их солей | 1989 |
|
SU1831484A3 |
| Способ получения 7-амино-3-замещенной метил- @ -цефем-4-карбоновой кислоты или ее кислотно-аддитивных солей | 1982 |
|
SU1308198A3 |
| СОЕДИНЕНИЕ ЦЕФЕМА ИЛИ ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬ | 1992 |
|
RU2024530C1 |
| СОЕДИНЕНИЯ ЦЕФЕМА И ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ | 1992 |
|
RU2081874C1 |
| Способ получения цефемовых соединений или их приемлемых с физиологической или фармацевтической точки зрения солей | 1986 |
|
SU1482532A3 |
Изобретение касается замещенных гетероциклических соединений, в частности 7-ациламидоцефалоспоринов (ЦС) ,в виде син-изомеров общей формулы ТГ-ТГ-V CONH-T--r 5 оЛ-К-Асн в, ОСНз COOR, Mi где (0) R .Н, Na, пивалоилок-- симетил (или этил); к 3-хлор-1,2,4- триазолил или 5-метил-1,2,3,4-тетра- золил, которые присоединены к экзо- метиленовой группе в положении. 3 це- фемового кольца через азотуглеродную связь. ЦС проявляют антибактериальное действие и могут быть использованы в медицине. Цель - создание более активных веществ указанного класса. Синтез новых ЦС ведут, например, из POClj5 2-(2-трет. аминоксикарбоксами- дотиазол-4-ил))-метоксиимино- уксусной кислоты и 7 амино-8- 3-хлор- 1,2,4-триазолил метил-Л -цефем-4-кар- боновой кислоты в среде и N,N- диметилацетамида сначала при (-20) С 
но. Минимальная ингибирующая концент- ig ную группу, давая соответствующие
рация (МИК, ккг/мп) - концентрацияj при которой подавляется рост бакте рий. Количество инокулированных бактерий 10 клеток, пластина 10 клеток/мл (табл. 1).
Для испытаний берут следующие соединения .
(2 аминотиазол-4-ил-2-(син)- метоксииминоацетамида -3- -2-(5-ме- ТШ1-1,2,3,4-тетразол)-метилЗ- -це- фем-4-карбоновая кислота (А).
(2-аминотиазол-4-ил)-2-(син)- метоксииминоацетамидо -3-(3-хлор-1, 2,4-триазолил)-метш1 J- -цефем-4-кар- боновая кислота (В),
Гидрохлорид 7-С2-(2-аминотиазол- 4-ил)-2-(син)-метоксииминоацетамидо - 3- 2-(5-метил-1,2,3,4-тетразолил)-метил -/ -це фем-4-карбоновой кислоты (С) ,
Гидрохлорид (2-аминотиазол- 4-ил)-2-(син)-метоксииминоацетамидоТ- 3- (З-хлор-1,2,4-триазолил)-метил - дз-цефем-4-карбоновой кислоты (D).
20
свободные карбоновые кислоты. След вательно, количество определяют св бодные карбоновые кислоты, поступа щие в мочу, и их берут как извлече ние из мочи. Способ введения следу щий. Испытуемое соединение суспенз руют в 0,5%-ном CMC растворе и зат вводят перорально.
Способ количественного анализа 25 проводят методом бумажного диска с испытуемыми бактериями, перечислен ными в табл, 2.
Указанные измерения осуществляют с врбодных оснований или их гидрохлор
Проводят испытание на острую токс ность.
Для определения острой токсично ти трех испытуемых соединений мыша вводят внутривенно инъекции.В качес ве подопытных животных берут мышей вида ICP (мужские особи в возрасте 4 нед) или орально крысам (S ДК, в раст 6 нед).Результаты сведены в та бл.
Указанные измерения осуществляю для свободных оснований и их гидро хлоридов. Формула изобретени
30
Положение .связи 1,2,4-триазолил не 40 определяются, поскольку 1,2,А-триазо, ил присоединен к экзометиленовой группе в положений 3 цефемового кольца через связь углерод-азот, но не утверждается, какие из атомов азота 45 1,2,4-триазолильной группы присоединены к экзаметиленовой группе в по- ложении 3 цефемового ядра. Положение заместителя в 1,2,4-триазолильной группе определяется указанием положе- 50 ния заместителя в исходном соединении. То же самое используется и в настоящем описании, когда уже указывается, какой из атомов азота в 1,2,4- триазоле присоединен с экзометилено- 55 вой группе в положении 3 цефемового кольца. Например, соединения, в которых З-хлор-1,2,4-триазол-группа присоединена с экзамети новой группе
20
40 45
50 55
свободные карбоновые кислоты. Следовательно, количество определяют свободные карбоновые кислоты, поступающие в мочу, и их берут как извлечение из мочи. Способ введения следующий. Испытуемое соединение суспензируют в 0,5%-ном CMC растворе и затем вводят перорально.
Способ количественного анализа 25 проводят методом бумажного диска с испытуемыми бактериями, перечисленными в табл, 2.
Указанные измерения осуществляют дл с врбодных оснований или их гидрохлорид
Проводят испытание на острую токсичность.
Для определения острой токсичности трех испытуемых соединений мышам вводят внутривенно инъекции.В качест- ве подопытных животных берут мышей вида ICP (мужские особи в возрасте 4 нед) или орально крысам (S ДК, возраст 6 нед).Результаты сведены в та бл.З .
Указанные измерения осуществляют для свободных оснований и их гидрохлоридов. Формула изобретения
7-Ациламидоцефалоспорины общей формулы
30
.CONH-TГ
-оснз
.B,
XnCH, COOR,
где R - водород, натрий, пивалоилок симетил или 1-пивапоилокси- этил;
R - З-хлор-1,2,4-триазолил или 5-метил-1,2,3,4-тетразолил, которые присоединены к экзометиленовой группе в положении 3 цефемового кольца через азотуглеродную связь, в виде син-изомеров или их гидрохлориды, проявляющие антибактериальные свойства.
E.coli N1HJ
B.coli ТКЗ/Penicillinascing bacteria
Kl.pnucmonia Y-50 Klebsiella spp, Y-72 Kl.pnucmoniae Y-41 Ent.eloacae 11D977 Ser.mareescens 11D 620 Pro.mirabilis T-216 Pro.mirabilis T-111
Pro.vulgaris 76
(бактерия, продуцирующаспориназу)
Al.faccalis В-1 Al.calioaceticus А-6
-N( I N-
N-N
IPJ.
33,1 M. АТ
35,0 To
еднее значение для 5 измерений.
47,0 KI
pn АТ
Таблица 1
1,,,1 0,1 0,1
0,390,39 0,39 0,39
0,,1 0,1 /0,1
0,390,39 0,39 0,39
0,20,78 0,2 0,78
0,,1 0,1 0,1
Таблица2
33,1 M.lutenix АТСС 9341
35,0 To же
47,0 KI
pneumoniae АТСС 10031
Введение через рот.
| Способ получения производных цефалоспорина | 1978 |
|
SU953983A3 |
Авторы
Даты
1988-08-23—Публикация
1982-12-09—Подача