Изобретение относится к медицине, а именно к новым биологически активным соединениям, конкретно к одно- и двухвалентным солям N-(5-гидроксиникотиноил)-L-глутаминовой кислоты, обладающим психотропным (антидепрессивной и анксиолитической), нейропротекторным и противоинсультным действием, которые могут найти применение для лечения депрессии, тревоги, ишемических и геморрагических инсультов, нарушений при старении и других заболеваний, сопровождающихся тревогой, депрессией, снижением когнитивных функций и нейродегенерацией.
Депрессия и тревога являются в настоящее время наиболее распространенными психическими заболеваниями и часто сопровождают другие состояния, в частности старение, инсульты, онкологические заболевания, болезни Альцгеймера и Паркинсона и др.
Инсульт (сосудистое поражение мозга) среди причин смертности занимает второе место в России и третье место в мире. При этом частота развития ишемических инсультов (недостаточность кровоснабжения мозга) составляет 70-80%, а геморрагических (кровоизлияние в мозг) - 20-30%. Эти две формы инсультов различны по патогенезу и требуют разных подходов к их лечению, однако при всех формах инсульта наблюдаются нейродегенеративные процессы. Дифференциальная диагностика этих двух форм инсульта на ранних этапах болезни затруднена, а в более чем 25% и невозможна. В связи с этим целесообразно создание препаратов, которые были бы эффективны при обеих формах инсультов. В настоящее время при инсультах применяются антагонисты кальциевых каналов, но они имеют существенные побочные эффекты и недостатки, одним из которых является наличие сердечно-сосудистых эффектов, приводящих к «обкрадыванию» мозга.
Нарушения когнитивных функций и гипоксические состояния наблюдаются при многих заболеваниях, как у детей, так и при естественном старении, стрессах, заболеваниях, протекающих с нейродегенерацией. Препараты, обладающие противогипоксическим и ноотропным действием, могут применяться для лечения больных, страдающих снижением умственных способностей при старении, при болезни Альцгеймера после мозговой травмы, пренатальной гипоксии, при алкоголизме, вегето-сосудистой дистонии и других заболеваниях. Применяемый для лечения этих состояний препарат пирацетам обладает слабой активностью.
По химической структуре наиболее близким к новым предлагаемым соединениям является нооглютил (основание N-(5-гидроксиникотиноил)-L-глутаминовой кислоты). Однако нооглютил не обладает психотропными эффектами (антидепрессивным и анксиолитическим) и нейропротекторным действием (патент РФ №1368314, опубликован в БИ №3, 1988 г., а также «N-никотиноиламинокислоты, обладающие противогипоксической и антиамнестической активностью»; Воронина Т.А. и соавт. Новое вещество с ноотропной активностью N-(5-оксиникотиноил)-L-глутаминовая кислота. Фармакол. и токсикол., 1990, т.53, №4, с.13-16).
Задачей настоящего изобретения явилось создание новых высокоэффективных и малотоксичных соединений, сочетающих психотропные (анксиолитический, антидепрессивный) эффекты с нейропротекторным, противоинсультным, геропротекторным, противогипоксическим, улучшающим обучение и память действием и имеющих, таким образом, преимущества перед известными средствами.
Эта задача решена путем создания новых соединений, а именно одно- и двухвалентных солей N-(5-гидроксиникотиноил)-L-глутаминовой кислоты (соединения I, II, III) общей формулы:
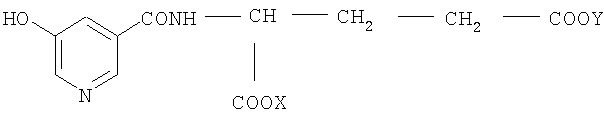 , где
, где
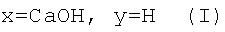 , или
, или
 , или
, или
 ,
,
обладающих антидепрессивной, анксиолитической, нейропротекторной, противоинсультной, геропротекторной, ноотропной, противогипоксической активностями.
Заявляемые соединения принципиально отличаются от нооглютила наличием в спектре фармакологической активности психотропных эффектов (антидепрессивного и анксиолитического) и нейропротекторного действия, а также характеризуются более высокой активностью в отношении психотропных эффектов.
Заявляемые соединения представляют собой белые кристаллические вещества, нерастворимые в метиловом, этиловом и изопропиловом спиртах, практически нерастворимые в бензоле, хлороформе, этилацетате и других органических растворителях. Вещества растворимы в воде, разбавленных растворах кислот и щелочей.
Заявляемые в настоящем патенте соединения являются новыми и в литературе не описаны.
Пример 1.
Суспензию 2,68 г (0,01 моля) N-(5-гидроксиникотиноил)-L-глутаминовой кислоты в 50 мл воды нагревают до 60-70°С и к ней небольшими порциями прибавляют 0,68 г (0,012 моля) окиси кальция. Осадок постепенно растворяется. Нагревают до полного растворения. Водный раствор упаривают до 20 мл. Полученный раствор при перемешивании прибавляют по каплям в 200 мл этилового спирта. Образовавшийся осадок перемешивают 0,5 часа и оставляют на 12 часов при комнатной температуре. Осадок отфильтровывают, промывают спиртом и высушивают при 100°С до постоянного веса (3 часа). Получают Са-соль N-(5-гидроксиникотиноил)-L-глутаминовой кислоты (I), выход 2,7 г (83%), [α]D 20 +11,0° (с 1, вода).
Найдено, %: С 40,80; Н 3,64; N 8,80. С11Н12CaN2О7 или (С11Н10CaN2О6.1H2О для хелата. Уточнить по ПМР).
Вычислено, %: С 40,76; Н 3,70; N 8,64.
ИК-спектр (в KBr), см-1.
УФ-спектр (в воде): λ max.
Спектр ПМР (в D2О), внутренний стандарт (ГМДС).
Пример 2.
Суспензию 0,27 г (0,001 моля) N-(5-гидроксиникотиноил)-L-глутаминовой кислоты в 5 мл воды нагревают до 50-60°С и к ней осторожно прибавляют порциями 0,2 г (0,0024 моля) бикарбоната натрия, нагревают до полного растворения и упаривают в вакууме досуха. В остаток добавляют этиловый спирт и снова упаривают в вакууме. Остаток растирают с сухим эфиром и отфильтровывают осадок. Затем его высушивают при 60°С/1 мм и получают ди-Na-соль N-(5-гидроксиникотиноил)-L-глутаминовой кислоты (II), выход 0,25 г (80,6%).
[α]D 20=+13,7° (с1, вода).
Найдено, %: С 42,51; Н 3,46; N 9,15. С11Н10Na2N2O6.
Вычислено, %: С 42,31; Н 3,23; N 8,97.
ИК-спектр (в KBr), см-1.
УФ-спектр (в воде): λ max.
Спектр ПМР (в D2О), внутренний стандарт (ГМДС).
Пример 3.
Суспензию 0,27 г (0,001 моля) N-(5-гидроксиникотиноил)-L-глутаминовой кислоты в 5 мл воды нагревают до 50-60°С и к ней осторожно прибавляют порциями 0,24 г (0,0024 моля) бикарбоната калия. Нагревают до полного растворения и упаривают в вакууме досуха. В остаток добавляют этиловый спирт и снова упаривают в вакууме. Остаток растирают с сухим эфиром и отфильтровывают осадок, промывают сухим эфиром и высушивают при 60°С/1 мм. Получают ди-К-сольN-(5-гидроксиникотиноил)-L-глутаминовой кислоты (III), гигр., выход 0,27 г (79,4%).
[α]D 20=+10,5° (с1, вода).
Найдено, %: С 38,64; Н 3,15; N 8,35. С11Н10K2N2O6.
Вычислено, %: С 38,36; Н 2,93; N 8,14.
ИК-спектр (в KBr), см-1.
УФ-спектр (в воде): λ max.
Спектр ПМР (в D2О), внутренний стандарт (ГМДС).
Далее приводятся примеры, иллюстрирующие эффективность солей N-никотиноиламинокислот, которые обладают противоинсультным, противогипоксическим, антидепрессивным, анксиолитическим, улучшающим обучение и память действием.
Пример 4. Изучение противогипоксической активности солей N-никотиноиламинокислот.
Противогипоксический эффект исследовался в условиях 2-х методик: гипобарической гипоксии и гипоксии с гиперкапнией в гермообъеме (Воронина Т.А. и соавт. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. М.: Медицина. 2005, с 308-320). Опыты проводили на белых беспородных мышах-самцах массой 22-28 г. Каждую дозу вещества изучали на 10 животных. Контрольным группам животных вводилась дистиллированная вода в эквивалентном объеме. В качестве препарата сравнения использовали нооглютил. Вещества вводили внутрибрюшинно за 40 минут до опыта.
Острую гипобарическую гипоксию моделировали в проточно-вытяжной барокамере. Давление регистрировали высотометром, скорость подъема - вариометром. Животных "поднимали" со скоростью 20 м/с до площадки "высотой" 11000 м. Экспозиция составляла 10 минут. Затем в течение 5 минут животных "спускали" до исходных условий. Гипоксию с гиперкапнией в гермообъеме создавали путем помещения животного в герметично закупоренную стеклянную емкость объемом 200 мл. Регистрировали продолжительность жизни животных в условиях гипоксии. В каждой группе использовали 10 животных.
Установлено, что в условиях гипобарической гипоксии после 10-ти минутной экспозиции в контроле погибали все животные; средняя продолжительность жизни составляла 3,6 минуты. Все изученные вещества 1а-1в обладают способностью увеличивать продолжительность жизни мышей в условиях острой кислородной недостаточности в барокамере, а наибольшей активностью обладает соединение I. Эффект соединения I реализуется в меньших дозах, чем у нооглютила. При использовании одинаковых доз 30 и 60 мг/кг соединение I оказывает более выраженный эффект, чем нооглютил (Таблица 1).
В условиях гипоксии с гиперкапнией в гермообъеме средняя продолжительность жизни контрольных животных составляла 14,3 минуты. Все изученные вещества I-III обладают способностью увеличивать продолжительность жизни мышей в условиях гипоксии с гиперкапнией в гермообъеме, а наибольшей активностью обладает соединение I. Эффект соединения I реализуется в меньших дозах, чем у нооглютила. При использовании одинаковых доз 60 и 120 мг/кг соединение I оказывает более выраженный эффект, чем нооглютил (Таблица 1).
Пример 5. Изучение антиамнестической активности солей N-никотиноиламинокислот.
Исследования проводили на белых беспородных крысах-самцах массой 250-280 г. Каждую дозу вещества изучали на 10 животных. Контрольным группам животных вводилась дистиллированная вода в эквивалентном объеме. В качестве препарата сравнения использовали нооглютил. Вещества вводили внутрибрюшинно за 40 минут до опыта. Исследование проводили на стандартной автоматизированной установке условного рефлекса пассивного избегания (УРПИ) (Passive Avoidance) фирмы Lafayette Instrument Co (США) (Ader R. et al. Retention of a passive avoidance response as a function of the intensity and duration of electric shock. Psychon. Sci. 1972, v.26, p.125-128; Воронина Т.А. и соавт. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. М.: Медицина. 2005, с.253-263 и 308-320). Конструктивно установка состоит из маленькой платформы, расположенной на расстоянии 1 м от пола, освещенной специальной лампой, и соединенной с ней темной камеры с электродным полом. Крысу помещали на освещенную платформу перед входом в темную камеру установки хвостом к входному отверстию, и животное, предпочитая темную камеру, быстро переходит в нее. С целью обучения крыса в темной камере получала однократное болевое раздражение электротоком (0,45 мА) через электродный пол, и животное запоминало, что в темную камеру заходить опасно. Продолжительность раздражения определялась выбеганием животного из темного отсека. Для получения амнезии использовался максимальный электрошок (50 Гц, 0,2 с), который проводили через корнеальные электроды непосредственно после обучения. Электрошок вызывает стирание памятного следа. Тест на воспроизведение УРПИ (на сохранение памятного следа) осуществляли через 24 часа после обучения и электрошока. Животное вновь помещали на освещенную платформу и в течение 2-х минут регистрировали время нахождения животного на освещенной платформе и в опасном темном отсеке (ток на пол при воспроизведении УРПИ не подается).
Контрольные обученные животные при воспроизведении УРПИ без действия электрошока предпочитают находиться на светлой платформе. Стирание обучения при помощи электрошока вызывает у животных амнезию, в результате чего животные с коротким латентным периодом заходят в темную камеру и остаются там значительно большую часть времени, чем животные без амнезии (Таблица 2).
Все изученные соединения обладают выраженной антиамнестической активностью, что выражается в том, что время нахождения животных на безопасной освещенной платформе значительно увеличивается по сравнению с контрольными животными с амнезией. Наибольшей антиамнестической активностью обладает соединение I, которое превосходит по эффективности нооглютил (Таблица 2). Статистически достоверный эффект нооглютила проявляется в дозе 50 мг/кг, а аналогичный по выраженности эффект соединения I - в дозе 25 мг/кг, что свидетельствует о более высокой активности соединения I по сравнению с нооглютилом.
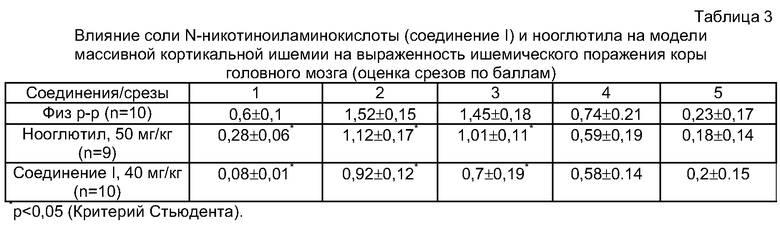
Пример 6. Изучение эффективности соли N-никотиноиламинокислоты (соединение I) и нооглютила на модели массивной кортикальной ишемии.
Эксперименты выполнены на белых беспородных самцах крыс весом 350-450 г, наркотизированных хлоралгидратом (400 мг/кг, в/б). Животным проводили перевязку левой сонной артерии, а затем под микроскопом (увеличение 14,0×3,3) производили окклюзию средней мозговой артерии (ОСМА) проксимальнее места ее бифуркации на фронтальную и париетальную ветви (S.T.Chen et al, Stroke, 1986, v.17, №4, 738-743).
После завершения операции животных случайным образом делили на 3 группы. Животным опытных групп вводили соединение 1а или нооглютил внутрибрюшинно через 30 минут, затем через 2, 24 и 48 часов после операции. Животным контрольной группы в те же сроки вводили физиологический раствор (0,9% хлористый натрий). Через 72 часа после ОСМА животных декапитировали. Из замороженного при -20°С готовили 5 фронтальных срезов толщиной 2,5 мм, которые окрашивали раствором 2,3,5-трифенилтетразолий хлорида (ТФТХ). С помощью морфометрической программы Aucl проводили планиметрию, определяли объем зоны поражения и процент объема зоны поражения относительно объема ипсилатерального полушария. В результате операции создается обширное ишемическое поражение коры головного мозга, локализующееся в пределах фронто-париетальной и дорсо-латеральной зон. Для сравнения выраженности изменений в различных срезах использовалась условная шкала, в которой поражение 75% полушария оценивались как 2,5 балла, 60% - 2 балла, 45% - 1,5 балла, 20% - 1 балл, 5% - 0,5 балла, 0% - 0 баллов.
У контрольных животных, леченых физиологическим раствором, общий объем поражения составляет 20,17±3,12%. Максимальное ишемическое повреждение имеет место на уровне 2-го и 3-го срезов (Таблица 3).
Соединение I в дозе 40 мг/кг, примененное после ишемизирующего воздействия, вызывает достоверное уменьшение объема повреждения на уровне трех первых срезов (Таблица 3). Общая площадь поражения после использования соединения I снижалась до 10,54±1,84% (контроль 20,17±3,12%), и, следовательно, вещество уменьшает общий объем поражения на 47,3% (р<0,05). Нооглютил оказывает эффект в более высокой дозе 50 мг/кг и вызывает менее выраженные изменения (Таблица 3). Общая площадь поражения после введения нооглютила снижалась до 14,31±2,14%.
Таким образом, соединение I, введенное после осуществления ишемизирующего воздействия, достоверно ослабляет выраженность морфологических изменений коры головного мозга, обусловленных перевязкой ипси-латеральной сонной артерии. Эти результаты свидетельствуют о нейропротекторном действии соединения I.
В отдельной серии экспериментов животные обучались в тесте условного рефлекса пассивного избегания (УРПИ), вырабатываемого в аппарате «Lafayette Instrument Co», USA), состоящем из ярко освещенной висячей платформы, присоединенной к темной камере с электрифицированным полом. В силу врожденного норкового рефлекса крыса при обучении заходила в темную камеру, где получала электроболевое раздражение. Оценку памяти проводили через 24 часа после обучения, регистрируя число животных, не зашедших в темную камеру в течение 180 с, а для зашедших- латентное время захода. Как показано ранее в многочисленных контрольных экспериментах на интактных крысах, они обычно не заходят в опасную камеру или заходят в самом конце тестирования (средний латентный период составляет 145±10,1 с). У ишемизированных животных (контроль) латентное время захода в темную камеру снижается и составляет 31,2±8,3 с (большинство животных не помнит о нанесенном накануне раздражении и быстро заходят в опасную камеру). Ишемизированные животные, леченые нооглютилом или соединением I, показывали улучшение памяти, что выражалось в увеличении латентного периода захода в темную опасную камеру: под влиянием нооглютила до 56,2±8,3 с и под влиянием соединения I - до 62,3±7,2 с. Эти эффекты нооглютила и соединения 1а достоверны по сравнению с контролем при р<0,05.
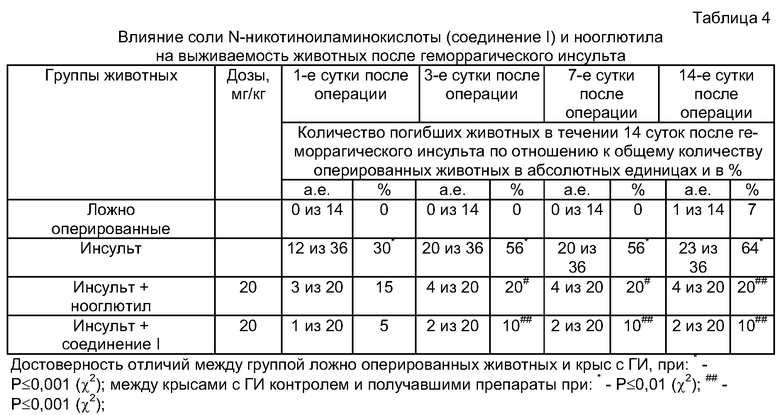
Пример 7. Изучение эффективности соли N-никотиноиламинокислоты (соединение I) и нооглютила на модели интрацеребральной посттравматической гематомы (геморрагического инсульта)
Эксперименты проводились на беспородных белых крысах-самцах весом 200-250 г, содержавшихся в виварии при свободном доступе к пище (стандартный брикетированный корм) и воде, при естественной смене дня и ночи. Моделирование ГИ - локального кровоизлияния в головном мозге проводилось согласно методике А.Н.Макаренко и соавторов (Метод моделирования локального кровоизлияния в различных структурах головного мозга у экспериментальных животных. Ж. высш. нервн. деят., 2002, т.52, №6, стр.765-768). Крысам, наркотизированным нембуталом (40 мг/кг, в/м), при помощи специального устройства (мандреннож) и стереотаксиса осуществляли деструкцию мозговой ткани в области capsule interna с последующим (через 2-3 минуты) введением в место повреждения крови, взятой из-под языка крысы (0,02-0,03 мл). Ложно оперированным животным проводили скальпирование и трепанацию черепа. Животные были разделены на 5 групп: интактные крысы, ложно оперированные, группа животных с ГИ, животные с ГИ, получавшие нооглютил в дозе 20 мг/кг, крысы с ГИ, получавшие соединение 1 в дозе 20 мг/кг. Регистрацию эффектов веществ проводили через 24 часа и 14 суток после операции. Обучение и память крыс исследовали на модели условного рефлекса пассивного избегания (УРПИ, Passive avoidance фирмы Lafayette Instrument Co США). Неврологический дефицит у животных определяли по шкале Stroke-index McGrow в модификации И.В.Ганнушкиной (Функциональная ангиоархитектоника головного мозга, М.: Медицина, 1977, 224 стр.). Тяжесть состояния определялась по сумме соответствующих баллов. Отмечалось количество крыс с легкой симптоматикой до 2,5 баллов по шкале Stroke-index (вялость движений, слабость конечностей, односторонний полуптоз, тремор, манежные движения) и тяжелыми проявлениями неврологических нарушений (от 3 до 10 баллов) - парезы конечностей, паралич нижних конечностей, боковое положение. Нооглютил и соединение I в одинаковых дозах 20 мг/ кг вводили животным внутрибрюшинно однократно через 3-3,5 часов после операции. Контрольным группам животных вводили физиологический раствор. Каждая группа в начале эксперимента состояла из 15-20 животных. Регистрацию гибели крыс проводили в течение всего времени наблюдения (14 дней). Статистическую обработку данных проводили с помощью программы "Биостат" с использованием параметрических и непараметрических методов. В качестве эталона использовался нимодипин (в дозе 0,1 мг/кг) по описанной выше схеме.
При регистрации гибели животных показано, что в группе ложно оперированных крыс к 14-му дню наблюдалась гибель лишь 7% животных, а в группе с геморрагическим инсультом этот показатель составил 64%, при этом в первые трое суток погибло более 56% животных (Таблица 4). Нооглютил обладал сильным протективным действием. Так, в дозе 20 мг/кг препарат почти полностью предупреждал гибель животных на протяжении всего времени наблюдения: погибло 20% (4 из 20) животных. В группе крыс, получавших соединение I, в течение всего времени наблюдения (14 суток) погибло только 10% животных (2 из 20) Под влиянием соединения I отмечалось статистически достоверное уменьшение гибели крыс уже в первые сутки после инсульта, чего не вызывал нооглютил. Полученные результаты свидетельствуют о высокой протективной активности соединения 1a у животных после геморрагического инсульта.
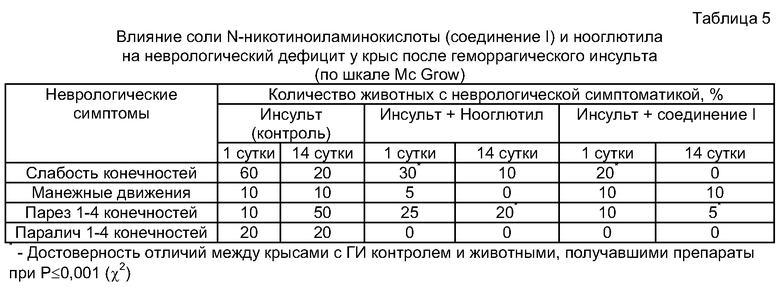
Исследование неврологического статуса выживших животных с использованием шкалы Stroke-index McGrow показало, что в группе животных с ГИ в первый день наблюдения тяжелая симптоматика отмечалась у 20%, а уже к 7-му дню этот показатель составлял 50% (Таблица 5). Нооглютил и соединение I существенно ослабляли у животных неврологический дефицит. Особенно ярко эффект веществ проявлялся на 14-е сутки, когда в контрольной группе крыс с ГИ наблюдалось 60% животных с тяжелыми неврологическими симптомами. Под влиянием нооглютила этот показатель снижался до 25%, а у крыс, получавших соединение I, - до 15%. Таким образом, соединение 1а оказывало выраженный позитивный эффект в отношении динамики развития неврологического дефицита у крыс после ГИ и этот эффект вещества был выражен в большей степени, чем у нооглютила.
Исследование процессов обучения и памяти у животных на модели УРПИ показало, что при воспроизведении рефлекса через 24 часа после обучения поведение ложно оперированных крыс существенно не отличалось от поведения как интактных животных, так и крыс с ГИ, получавших и не получавших нооглютил или соединение I (Таблица 6). 70-80% животных помнили об ударе током в темной камере и не заходили туда. Иные закономерности отмечались при воспроизведении УРПИ на 14 сутки. Так, если у 65% интактных и у 57% ложно оперированных животных отмечалось сохранение памятного следа, то в группе с ГИ об ударе током помнили лишь 8% крыс. Нооглютил в дозе 20 мг/кг увеличивал этот показатель у крыс с ГИ в 5 раз, а соединение I в дозе 20 мг/кг - в 6,5 раза, т.е. способствовало более продолжительному сохранению памятного следа (Таблица 6). Оба препарата статистически достоверно укорачивали латентное время захода в темную опасную камеру. Нимодипин оказывал более слабый эффект на этой модели.
Таким образом, в результате проведенных исследований установлено, что у крыс с ГИ наблюдался выраженный неврологический дефицит, ослабление процессов обучения и памяти, гибель животных. При этом отмечалось углубление патологической симптоматики к 14-му дню наблюдения. Динамика ухудшения состояния и гибели крыс с ГИ может свидетельствовать о скрытой недостаточности компенсаторных реакций организма, нарастающих в определенные критические дни (3, 7, 14 сутки) послеоперационного периода и развитии сопутствующих осложнений (отек, набухание тканей, нарушение интрацеребральной гемодинамики, повышенное внутричерепное давление, ишемия мозга).
Соединение I при введении животным однократно через 3-3,5 часа после создания геморрагического инсульта обладает выраженным противоинсультным действием, предотвращая гибель крыс и существенно ослабляя нарушения неврологического статуса, улучшая память животных с посттравматической гематомой - геморрагическим инсультом. По противоинсультной активности соединение I превосходит нооглютил.
Пример 8. Изучение эффективности соли N-никотиноиламинокислоты (соединение I) и нооглютила на нарушения памяти и неврологический дефицит у старых крыс (24 мес.)
В работе использовали белых беспородных крыс-самцов линии Вистар в половозрелом возрасте 3 мес массой 250-300 г и в старом возрасте 24 мес массой 350-450 г. Нооглютил в дозе 20 мг/кг и соединение I вводили старым крысам внутрибрюшинно в течение 2-х месяцев, а затем оценивали влияние вещества на нарушенные старением обучение и память и неврологический дефицит. Статистическую обработку результатов проводили с использованием метода вариационной статистики по Стьюденту, метода долей вариант, U-теста.
Влияние соединения I на нарушения памяти у старых животных.
Выработка условного рефлекса пассивного избегания (УРПИ) у крыс проводится в установке Passive avoidance фирмы Lafauette Instrument Co (США) (Ader R. et al. Retention of a passive avoidance response as a function of the intensity and duration of electric shock. Psychon. Sci. 1972, v.26, p.125-128; Воронина Т.А. и соавт. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. М.: Медицина. 2005, с.308-320).
Установка состоит из маленькой платформы, расположенной на расстоянии 1 метра от пола, освещенной специальной лампой, и темной камеры с электродным полом. Животное помещают на освещенную платформу перед входом в темную камеру установки хвостом к входному отверстию и в течение трех минут регистрируют латентное время рефлекса, время пребывания крысы в светлом отсеке и количество животных, не зашедших в темный отсек. Животные, предпочитающие светлый отсек, в опыте не используются. Затем в темной камере крыса получает однократное болевое раздражение (0,45 мА), продолжительность раздражения определяется выбеганием животного из темного отсека. Тест на воспроизведение УРПИ осуществляют через 24 часа после обучения и проводят при повторном помещении животных в установку с регистрацией в течение 3 минут латентного периода первого захода крысы в темную экспериментальную камеру и количества животных, не зашедших в нее.
Показано, что контрольные крысы 3-х месячного возраста при воспроизведении рефлекса через 24 часа после обучения в 80% случаев не заходили в темную камеру или заходили с большим латентным временем рефлекса (Таблица 7). В группе старых 24-х месячных крыс условный рефлекс воспроизводили только 30% животных, остальные крысы заходили в темную опасную камеру с коротким латентным временем рефлекса, что свидетельствует о нарушении у крыс памяти. Старые крысы, получавшие соединение I в дозе 20 мг/кг при воспроизведении осуществляли рефлекс в 60% случаев. Таким же отчетливым эффектом обладал нооглютил, значительно улучшая у 60% крыс процесс воспроизведения памятного следа. Соединение I и нооглютил также статистически достоверно увеличивали латентное время захода в темную опасную камеру.
Для оценки у старых животных неврологического дефицита (нарушение координации движений и способности обучаться двигательным реакциям) животных помещали на вращающийся стержень. Регистрировалось количество попыток, необходимых для обучения навыку удерживания на вращающемся стержне в течение 2-х минут. Показано, что 100% молодых животных с первых пяти посадок обучались удерживаться на вращающемся (0,5 об/мин) стержне в течение 2-х минут (Таблица 8). В этих условиях только 25% старых крыс обучались этому навыку и то начиная с 11-й по 14-ю попытки. Это свидетельствует о нарушении неврологического статуса у старых крыс и ослаблении их способности обучаться двигательным реакциям. Старые крысы, получавшие в течение 2-х месяцев нооглютил, к 10 попытке обучились навыку в 60% случаев, а получавшие соединение I - в 66% случаев. Анализ количества попыток, необходимых для обучения 50% животных, показал, что зрелые крысы достигали этого критерия с первой попытки, старые с 17-й, старые животные, получавшие нооглютил, - с 7-й, старые крысы, получавшие соединение 1а, - с 6-й.
Таким образом, нооглютил и соединение I обладают выраженным геропротекторным действием в опытах на старых 24-х месячных крысах, улучшая процессы обучения и памяти и ослабляя неврологический дефицит.
Пример 9. Изучение антидепрессивной активности соли N-никотиноиламинокислоты (соединение I) и в опытах на мышах линии SAM
В исследовании были использованы беспородные мыши и мыши линии SAM Р 10 (Takeda Т. et al. Senescence-Accelerated Mouse (SAM): A novel murine model of accelerated senescence. J. Amer. Geriatr. Soc. 1991, v.39, p.911-919) весом 26-31 г. с ускоренным старением в возрасте 11 месяцев. У животных этой линии генетически детерминирована депрессия и нарушения обучения и памяти, симптоматика, которая активно нарастает начиная с 6 месячного возраста (ускоренное старение) (Miyamoto M. Characteristics of age-related behavioral changes in Senescence-Accelerated Mouse SAMP8 and SAMP10. Exp. Gerontol. 1997, v.32, p.139-148; Shimada A. et al. Age-related deterioration in conditional avoidance task in the SAM-P/10 mouse, an animal model of spontaneous brain atrophy. Brain Res., 1993, v.608, p.266-272). Для оценки депрессивного состояния была использована методика принудительного плавания (Porsolt R.D et al. Behavioral despaire in rats: a new model sensitive to antidepressant treatment. Europ. J.Pharmacol, 1978, V.47, p.370-391). Мышей помещали в цилиндр диаметром - 10 см, высотой - 25 см. Цилиндр наполняли на 1/3 водой (27°С). После неудачных попыток выбраться из воды животные принимают характерную неподвижную позу, которую расценивают как проявление подавленности, «отчаяния». Фиксируют время всех активных попыток животных выбраться из воды в течение первых 6 минут после погружения в воду. Под влиянием антидепрессантов, независимо от механизма их действия, активность животных возрастает и время неподвижности (иммобилизации) уменьшается.
Показано, что мыши линии SAM значительно менее активны, чем беспородные животные, т.е. продолжительность активного плавания этих животных статистически достоверно меньше (Таблица 9). Согласно используемому методу это свидетельствует о более выраженном депрессивноподобном состоянии мышей линии SAM. Соединение I во всех используемых дозах 5, 10, и 20 мг/кг увеличивало время активного поведения мышей. Наиболее ярко этот эффект выявлялся у вещества в дозе 20 мг/кг (Р≤0,03). Полученные результаты свидетельствуют о наличии антидепрессивной активности у соединения I. Эффект соединения 1а сопоставим с действием амитриптилина.
Пример 10. Изучение анксиолитической активности соединение I в опытах на мышах линии SAM P10
В исследовании были использованы беспородные мыши и мыши линии SAM P 10 (Scenecent accelerated mause) весом 26-31 г. с ускоренным старением (Takeda Т. et al. Senescence-Accelerated Mouse(SAM): A novel murine model of accelerated senescence. J. Amer. Geriatr. Soc. 1991, v.39, p.911-919) в возрасте 11 месяцев. У животных этой линии генетически детерминирована депрессия и нарушения обучения и памяти, симптоматика, которая активно нарастает начиная с 6 месячного возраста (ускоренное старение) (Miyamoto M. Characteristics of age-related behavioral changes in Senescence-Accelerated Mouse SAMP8 and SAMP10. Exp. Gerontol. 1997, v.32, p.139-148; Shimada A. et al. Age-related deterioration in conditional avoidance task in the SAM-P/10 mouse, an animal model of spontaneous brain atrophy. Brain Res., 1993, v.608, p.266-272). Оценка уровня тревожности мышей проводилась в условиях методики приподнятого крестообразного лабиринта (ПКЛ) (Pellow S., et al. Validation of open: closed arm entries in elevated plus-maze as a nuasure of anxiety in the rat. Neurosci Meth J. 1985, №14, p.149-167; Воронина Т.А. и соавт. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. M.: Медицина. 2005, с.253-263). Лабиринт представляет собой перекрещенные полоски размером 5×45 см, два противоположных отсека имеют вертикальные стенки высотой 30 см (закрытые, темные рукава), а два других - открытые, светлые рукава. Лабиринт приподнят от пола на 30 см. В месте перекрестка плоскостей находится центральная платформа 50×50 см. Мышей помещали на центральную площадку хвостом к светлому рукаву. Регистрировалось время, проведенное животными в открытых и закрытых рукавах, число заходов в светлые и темные рукава. Общее время наблюдения для каждого животного составляло 5 мин. В качестве критерия анксиолитического эффекта использовали показатель времени, проведенного в открытых рукавах установки.
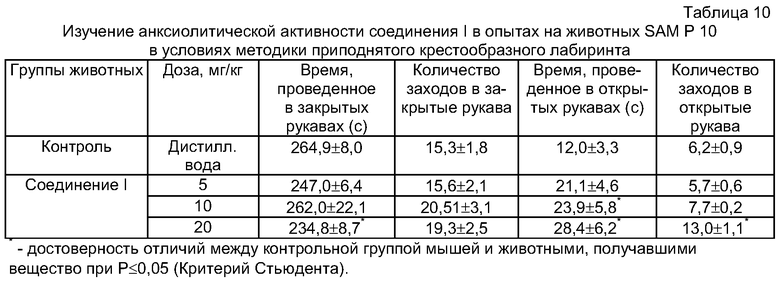
Установлено, что контрольные животные большую часть 5-ти минутного времени наблюдения проводили в закрытых рукавах лабиринта. Соединение I во всех используемых дозах, а именно - 5, 10 и 20 мг/кг, увеличивало основной показатель поведения мышей - время, проведенное в открытых, незащищенных рукавах лабиринта. При этом и эффект вещества в дозах 10 и 20 мг/кг был статистически достоверным (Таблица 10). Особенно эффективно соединение I в дозе 20 мг\кг. Полученные результаты свидетельствуют о наличии у соединения I анксиолитического эффекта на модели приподнятого крестообразного лабиринта.
Пример 11. Изучение острой суточной токсичности соли N-никотиноиламинокислоты (соединение I) и в опытах на мышах
Исследование острой суточной токсичности соединения 1а проводилось в опытах на беспородных мышах-самцах весом 25-28 г, содержащихся в привычных условиях в виварии при свободном доступе к пище и воде. Соединение I вводили однократно внутрибрюшинно. После введения вещества животные наблюдались в течение 2-х суток. При изучении токсичности соединения I были использованы следующие дозы: 800 мг/кг, 1000 мг/кг, 1200 мг/кг, 1500 мг/кг, 1600 мг/кг. Соединение I растворяли в дистиллированной воде и вводили в объеме 0,1 мл на 10 г веса животного при использовании доз 800 мг/кг, 1000 мг/кг и в объеме 0,2 мл на 10 г веса животного при использовании доз 1200 мг/кг, 1500 мг/кг, 1600 мг/кг. Контрольным животным вводили дистиллированную воду в объеме 0,2 мл на 10 г веса.
Число животных в каждой группе составляло 10 особей. Введение контрольным животным дистиллированной воды в объеме 0,2 мл на 10 г веса не вызывает гибели. Результаты исследования с соединением I представлены в таблице 11.
Установлено, что соединение I в дозе 1000 мг/кг вызывает гибель 20% мышей через 48 часов наблюдения, в дозе 1200 мг/кг - 60% мышей, в дозе 1500 мг/кг - 90% мышей и в дозе 1500 мг/кг - 90% мышей. ЛД50 (доза, вызывающая гибель 50% животных) составляет для соединения I -1150 (1110÷1196) мг/кг. Для нооглютила ЛД50 составляет 1200 (1090÷1320) мг/кг. Таким образом, соединение I имеет токсичность, сходную с нооглютилом.
Заключение
Установлено, что соли N-оксиникотиноил глютаминовой кислоты обладают выраженной антиамнестической и противогипоксической активностью. Наиболее эффективным соединением по основным для ноотропов и нейропротекторов проявлениям действия является Соединение I. Его эффект по антиамнестическому и противогипоксическому действию выявляется в диапазоне доз от 5 до 120 мг/кг и превосходит по активности нооглютил.
Соединение I обладает отчетливым противоинсультным действием на экспериментальных моделях ишемического и геморрагического инсультов, предотвращая гибель крыс, ослабляя неврологический дефицит, улучшая процессы обучения и памяти. Противоинсультные свойства соединения I выражены в большей степени и выявляются в меньших дозах, чем у нооглютила. Соединение I эффективно у старых животных: улучшает память и двигательные функции.
Существенным преимуществом соединения I перед нооглютилом является наличие в спектре его фармакологической активности антидепрессивного и анксиолитического эффектов, которые выявляются на модели депрессивноподобного состояния в тесте принудительного плавания и на модели тревожного состояния в тесте приподнятого крестообразного лабиринта. Соединение I обладает также нейропротекторным действием, что выражается в способности вещества восстанавливать пораженные при инсульте участки мозга, и геропротекторным эффектом, который характеризуется ослаблением неврологических дефицитов и улучшением когнитивных функций и физической работоспособности.
60
120
7,68±0,54*
15,2±0,39
16,4±0,53*
60
120
9,17±0,91*
17,8±0,41*
18,1±0,48*
60
120
5,95±0,84*
16,3±0,64
17,8±0,69*
60
120
5,52±0,54*
15,9±0,45
17,4±0,65*
Р≤0,05 (Критерий Стьюдента); # - достоверность отличий
между контрольной группой SAM и опытной, получавшей препараты
при Р≤0,05 (Критерий Стьюдента)

| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИДЕПРЕССАНТНЫМ, АНКСИОЛИТИЧЕСКИМ, НЕЙРОПРОТЕКТОРНЫМ И ИММУНОСТИМУЛИРУЮЩИМ ДЕЙСТВИЕМ | 2010 |
|
RU2429834C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОГИПОКСИЧЕСКИМ, ПРОТИВОИНСУЛЬТНЫМ, УЛУЧШАЮЩИМ ПАМЯТЬ ДЕЙСТВИЕМ | 2007 |
|
RU2326665C1 |
| НЕЙРОТРОПНОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИОКСИДАНТНОЙ, ПРОТИВОГИПОКСИЧЕСКОЙ, НЕЙРОПРОТЕКТОРНОЙ, АНТИАМНЕСТИЧЕСКОЙ И ПРОТИВОУКАЧИВАЮЩЕЙ АКТИВНОСТЬЮ И СПОСОБНОСТЬЮ УЛУЧШАТЬ КОГНИТИВНЫЕ ФУНКЦИИ | 2008 |
|
RU2394816C1 |
| 4-[(4-Ацетоксибензоил)амино]бутират лития, обладающий церебропротективным действием | 2015 |
|
RU2617233C2 |
| СУБЛИНГВАЛЬНАЯ ФОРМА 6-МЕТИЛ-2-ЭТИЛ-3-ГИДРОКСИПИРИДИНА И ЕЕ ПРИМЕНЕНИЕ В КАЧЕСТВЕ СРЕДСТВА, ОБЛАДАЮЩЕГО СТИМУЛИРУЮЩЕЙ, АНОРЕКСИГЕННОЙ, АНТИДЕПРЕССИВНОЙ, АНКСИОЛИТИЧЕСКОЙ, ПРОТИВОГИПОКСИЧЕСКОЙ, АНТИАМНЕСТИЧЕСКОЙ (НООТРОПНОЙ) И АНТИАЛКОГОЛЬНОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2527342C2 |
| ПРОИЗВОДНОЕ ГАММА-АМИНОМАСЛЯНОЙ КИСЛОТЫ, ОБЛАДАЮЩЕЕ НООТРОПНОЙ АКТИВНОСТЬЮ В СОЧЕТАНИИ С ТРАНКВИЛИЗИРУЮЩИМ ДЕЙСТВИЕМ | 2012 |
|
RU2495866C1 |
| ВЕЩЕСТВО, ОБЛАДАЮЩЕЕ НЕЙРОТРОПНОЙ - НЕЙРОМОДУЛЯТОРНОЙ АКТИВНОСТЬЮ | 2006 |
|
RU2329804C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ПРОТИВОГИПОКСИЧЕСКОЙ, НЕЙРОПРОТЕКТОРНОЙ И АНТИАМНЕСТИЧЕСКОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2480233C1 |
| ВОДОРАСТВОРИМОЕ ПРОИЗВОДНОЕ САЛИЦИЛМОРФОЛИДА, ОБЛАДАЮЩЕЕ НООТРОПНОЙ АКТИВНОСТЬЮ В СОЧЕТАНИИ С АНТИДЕПРЕССИВНЫМ ДЕЙСТВИЕМ | 2012 |
|
RU2495032C1 |
| ДИЛИТИЕВАЯ СОЛЬ N-САЛИЦИЛОИЛГЛИЦИНА, ОБЛАДАЮЩАЯ НООТРОПНОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2495867C1 |
Изобретение относится к медицине и касается одно- и двухвалентных солей N-(5-гидроксиникотиноил)-L-глутаминовой кислоты общей формулы
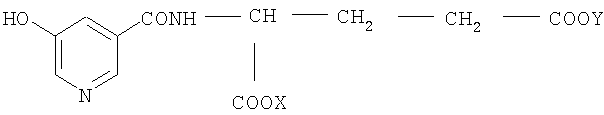
где
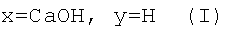
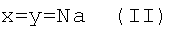 и
и
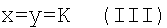 ,
,
которые оказывают антидепрессивное, анксиолитическое, геропротекторное, нейропротекторное, противогипоксическое, противоинсультное, ноотропное действия. От известных препаратов, в том числе ближайшего аналога - основания N(5-гидроксиникотиноил)-L-глутаминовой кислоты (нооглютила), новые соединения отличаются наличием психотропных эффектов, а именно антидепрессивного и анксиолитического, а также нейропротекторного и геропротекторного действия, выражающегося в способности уменьшать очаги поражения при инсультах и улучшать неврологические дефициты, умственную и физическую работоспособность при старении. 11 табл.
Одно- и двухвалентные соли N-(5-гидроксиникотиноил)-L-глутаминовой кислоты общей формулы
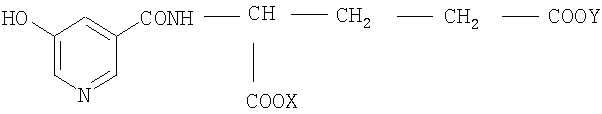 ,
,
где
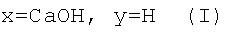
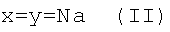
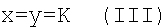 ,
,
обладающие антидепрессивной, анксиолитической, нейропротекторной, противоинсультной, геропротекторной, ноотропной, противогипоксической активностями и отличающиеся от своего ближайшего аналога - основания N-(5-гидроксиникотиноил)-L-глутаминовой кислоты (нооглютила) - наличием психотропных эффектов (антидепрессивного и анксиолитического) и нейропротекторного действия, а также более высокой активностью и широтой терапевтического действия.
| ВОРОНИНА Т.А | |||
| и др | |||
| N-никотиноиламинокислоты, обладающие противогипоксической и антиамнестической активностью | |||
| Фармакология и токсикология | |||
| Способ приготовления консистентных мазей | 1919 |
|
SU1990A1 |
| @ -Никотиноиламинокислоты, обладающие противогипоксической и антиамнестической активностью | 1984 |
|
SU1368314A1 |
| RU 94038232 А1, 27.08.1996 | |||
| СПОСОБ ПОЛУЧЕНИЯ N-АЦЕТИЛ- α -ГЛУТАМИНОВОЙ КИСЛОТЫ | 1992 |
|
RU2068408C1 |
Авторы
Даты
2008-01-10—Публикация
2006-07-31—Подача