Изобретение относится к биотехнологии, в частности к производству ферментов, и может быть применено для получения щелочной фосфатазы с высокой удельной активностью.
Целью изобретения является выявление штамма продуцента щелочной фосфатазы Acinetobacter species ВКПМ В-3905, образующего фермент, обладающий более высокой удельной активностью.
Штамм Acinetobacter species ВКПМ В-3905 (40 МС) выделен по методам общемедицинской микробиологии из целомической жидкости мидии Crenomytilus grayanus, обитающей в бухте Троица залива Петра Великого Японского моря, и отобран по признаку наибольшей удельной фосфатазной активности по р-нитрофенилфосфату из 210 штаммов различных морских микроорганизмов.
Штамм имеет следующие морфологические и физиологические признаки.
Морфологические признаки. Клетки палочковидные, 0,5-0,9 мкм в диаметре и 1,5-2,0 мкм длиной. На стационарной фазе роста клетки укорачиваются. В культуре клетки обычно располагаются парами. Спор не образуют. Грамотрицательные, способны к "дергающемуся" движению. Оксидазная реакция отрицательная, по каталазе положительная. Содержание Г+Ц равно 38,6% На плотных питательных средах образуют круглые, выпуклые, блестящие, слизистые, полупрозрачные колонии. Пигмента не образуют. При росте в жидкой среде вызывают помутнение. Мутность однородная, постоянная, умеренной степени.
Физиологические признаки. Хемоорганотрофы с окислительным метаболизмом. Индол и Н2 не образуют, сахарозу, лактозу, маннит, арабинозу, маннозу не утилизируют. Оптимум температуры роста 28-30оС. Специфических потребностей при росте нет.
Способ, условия и состав сред для размножения: культивируются на среде следующего состава, г/л: пептон 5, дрожжевой экстракт 0,5, глюкоза 1, К2НРО4 0,3, NaCl 25, MgSO4 1, CaCO3 1, оптимум рН 7,5-7,8.
При хранении применяют лиофилизацию, полужидкий агар этой же среды. Сроки пересева не чаще одного раза в год.
П р и м е р 1. Использование штамма при периодическом культивировании. 5 мл бактериальной суспензии (1х1010 клеток в 1 мл воды) 24-часовой культуры Acinetobacter sp. 40 МС, выращенном на мясопептонном агаре, вносят в колбу (объем 500 мл) с 250 мл питьевой среды, содержащей, г/л: пептон 5, глюкоза 1, К2НРО4 0,3, MgSO4 1, дрожжевой экстракт 0,5, NaCl 25, CaCO3 1. Выращивают при 28-30оС при встряхивании на качалке в течение двух суток. Выход бактериальной биомассы в описанных условиях 1,7 г с 250 мл культуральной среды. Продуктивность по белку 155 мг/л.
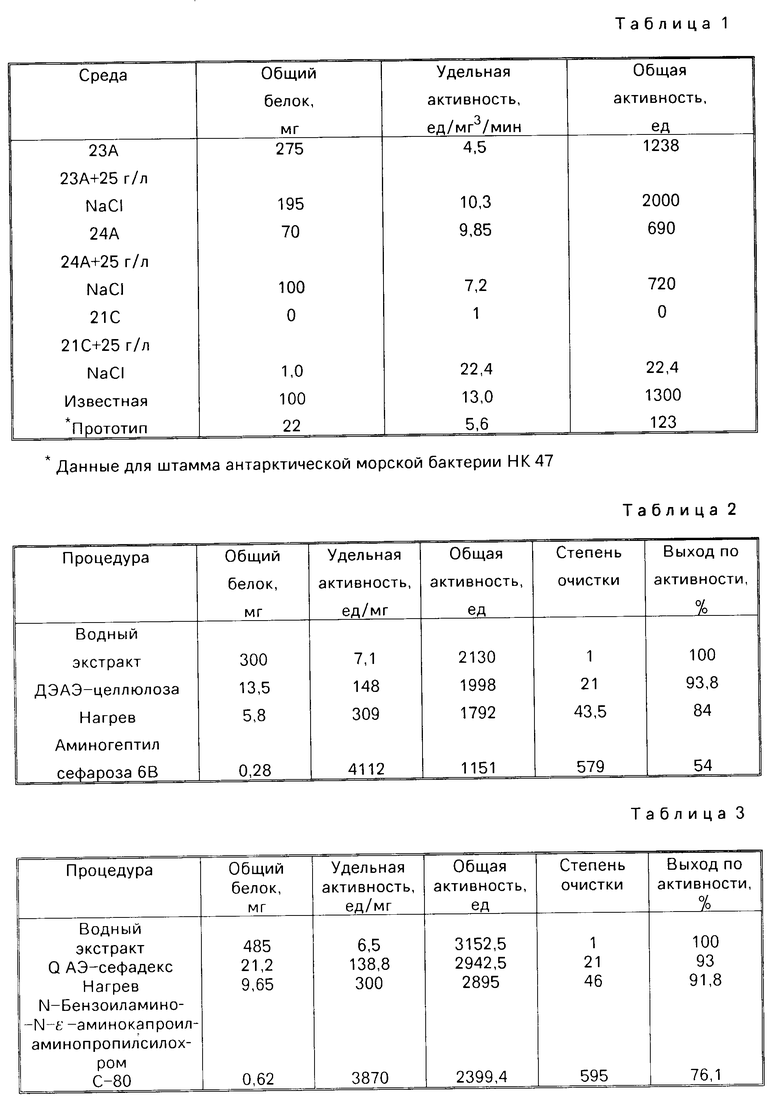
В табл.1 представлены результаты эксперимента, подтверждающего достижение положительного эффекта на известных, общепринятых для данного вида и родственных ему микроорганизмов средах.
В качестве общепринятых сред испытывали комплексные питательные среды, в частности 23А, 23А+25 г/л NaCl 24 A, 24А+25 г/л NaCl и синтетические среды 21 С и 21 С+ +25 г/л NaCl.
Сравнение полученных для предлагаемого штамма Acinetobacter sp. 40 МС данных с характеристиками продукта штамма антарктической морской бактерии НК 47 показывает, что предлагаемый штамм в известных условиях обеспечивает повышение активности и выхода продуцируемой им биомассы.
Эксперимент показал также улучшение указанных характеристик продукта и на общепринятых для данного вида и родственных ему микроорганизмов средах.
Для повышения активности, увеличения выхода целевого продукта и упрощения способ предусматривает использование штамма Acinetobacter sp. ВКПМ В-3905 и применение при хроматографической очистке сочетания ионообменной и гидрофобной хроматографии с обязательной инактивацией примесных активностей сопутствующих ферментов между стадиями.
П р и м е р 2. К 17 г сырой биомассы, полученной из 2,5 л культуральной жидкости по примеру 1, добавляют 85 мл 0,01 М трис-HCl буфера, рН 8,5, содержащего 5 мМ MgCl2, суспензию клеток дезинтегрируют обработкой ультразвуком в течение 3-5 мин, затем центрифугируют при 3000 об/мин в течение 20 мин. Надосадочную жидкость собирают и наносят на колонку с ДЭАЭ-целлюлозой (объем колонки 105 мл), уравновешенную 0,01 М трис-HCl буфером, рН 8,5, содержащим 5 мМ MgCl2 (стартовый буфер).
Фермент элюируют 0,1 М NaCl в стартовом буфере и концентрируют на колонке (объемом 5 мл) с ДЭАЭ-целлюлозой. Концентрированный раствор щелочной фосфатазы (1,5 мг/мл) прогревают в течение 20 мин при 65оС с целью инактивации нуклеазных примесных активностей. От выпавшего в осадок денатурированного балластного белка освобождаются центрифугированием при 5000 об/мин в течение 10 мин.
Надосадочную жидкость, содержащую щелочную фосфатазу, собирают и к ней добавляют сухую соль сульфата аммония до конечной концентрации 2,0 М, после растворения соли раствоp белка наносят на колонку объемом 5 мл с аминогептилсефарозой 6В, уравновешенную 2М сульфатом аммония в стартовом буфере. Щелочную фосфатазу (целевой продукт) элюируют 1,0 М сульфатом аммония в стартовом буфере.
В табл.2 приводятся характеристики продукта в процессе очистки.
П р и м е р 3. 27,5 г сырой биомассы, полученной из 4 л культуральной жидкости, суспендируют в 140 мл стартового буфера. Суспензию клеток обрабатывают ультразвуком в течение 3 мин, образовавшийся экстракт осветляют центрифугированием при 3000 об/мин в течение 20 мин. надосадочную жидкость наносят на колонку объемом 120 мл с Q АЭ-сефадексом, уравновешенную стартовым буфером. Адсорбировавшийся белок элюируют 0,15 М NaCl в стартовом буфере и элюат, содержащий щелочную фосфатазу, концентрируют добавлением к холодному раствору фермента равного объема холодного ацетона. После 1 ч отстаивания при 10оС раствор центрифугируют при 3000 об/мин в течение 20 мин и выпавший осадок белка, содержащий щелочную фосфатазу, растворяют в минимальном 0,01 М трис-HCl буфере, рН 8,5, содержащем 5 мМ МgCl2 и прогревают при 65оС в течение 20 мин. От выпавшего в осадок денатурированного белка освобождаются центрифугированием при 5000 об/мин в течение 10 мин. К надосадочной жидкости, содержащей щелочную фосфатазу, добавляют сухую соль сульфата аммония до конечной концентрации 2 М. Раствор наносят на колонку с N-бензоиламино-N-ε-аминокапроиламинопропилсилохромом С-80 (объем колонки 8 мл), уравновешенную 2 М сульфатом аммония в 0,01 М трис-HCl буфере, рН 8,5, содержащем 5 мм MgCl2. Колонку сначала промывают 1 М сульфатом аммония в стартовом буфере. Фермент элюируют 0,5 М сульфатом аммония в стартовом буфере.
В табл.3 приводятся характеристики продукта в процессе очистки.
П р и м е р 4. 27,5 г сырой биомассы, полученной из 4 л культуры, суспендируют в 140 мл 0,01 М трис-HCl буфера, рН 8,5, содержащего 5 мМА MgCl2. Суспензию клеток обрабатывают ультразвуком в течение 5 мин. Водный экстракт осветляют центрифугированием при 3000 об/мин в течение 20 мин. Надосадочную жидкость наносят на колонку объемом 120 мл с ДАЭА-сефадексом А-50, уравновешенную стартовым буфером. Адсорбировавшийся белок элюируют 0,1 М NaCl в стартовом буфере и элюат, содержащий щелочную фосфатазу, концентрируют ультрафильтрацией до концентрации белка 1,0 мг/мл. Концентрированный раствор фермента прогревают при 65оС в течение 20 мин. Выпавший в осадок денатурированный белок удаляют центрифугированием при 5000 об/мин в течение 10 мин. К надосадочной жидкости, содержащей щелочную фосфатазу, добавляют сухую соль сульфата аммония до конечной концентрации 2 М, после растворения соли ферментный раствор наносят на колонку объемом 8 мл с бензоиламиногептиламиносефарозой 6 В, уравновешенную 2 М сульфатом аммония в стартовом буфере. Щелочную фосфатазу элюируют 1 М сульфатом аммония в стартовом буфере.
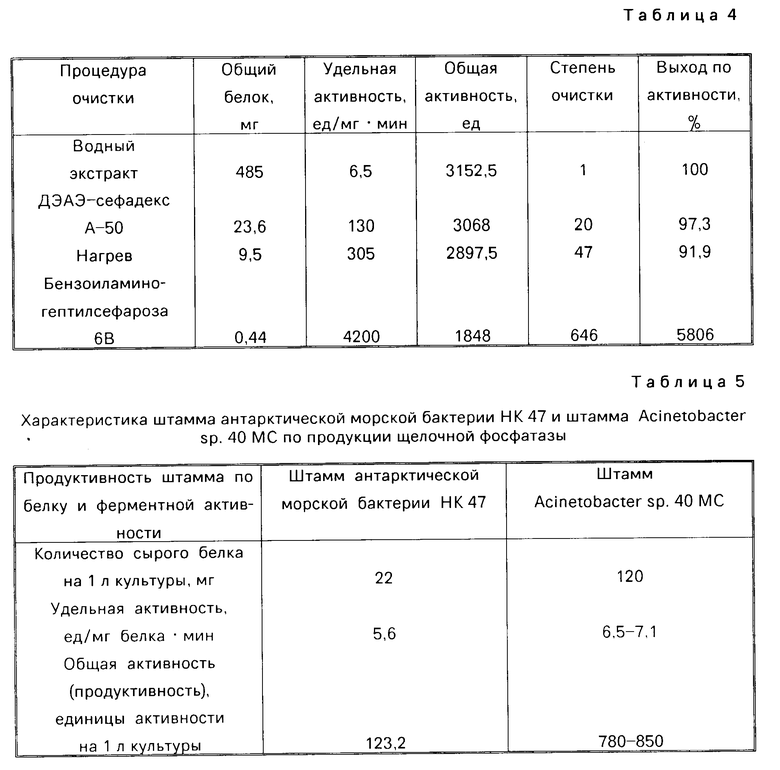
В табл.4 приводятся характеристики продукта в процессе очистки.
Исследование свойств препарата щелочной фосфатазу, продуцируемой штаммом Acinetobacter sp. 40 МС и выделяемой согласно изобретению, показало, что оптимум рН фермента находится в области 8,8-9,6, в то же время фермент проявляет активность в широком интервале рН (7,5-10,5), фермент стабилен в диапазоне рН 6,2-10,5; фермент стабилен в интервале температур 4-65оС, молекулярная масса фермента равна 56000 дальтон, для проявления своей активности фермент требует присутствия в инкубационной среде 5-10 мМ MgCl2, щелочная фосфатаза с высокой скоростью гидролизует р-нитрофенилфосфат, нуклеотидфосфаты и концевой фосфат длинных молекул нуклеиновых кислот и олигонуклеотидов.
Таким образом, применение нового штамма продуцента щелочной фосфатазы и способа получения щелочной фосфатазы позволяет повысить активность щелочной фосфатазы, увеличить выход фермента за счет повышения продуктивности штамма по белку и ферментативной активности (см. табл.5) и за счет использования для выделения и очистки эффективных, емких сорбентов, исключающих потери щелочной фосфатазы, сочетания анионообменной и гидрофобной хроматографии и нагрева, а также упростить способ получения по сравнению с известным способом за счет исключения операции линейной градиентной элюации, требующей строгого контроля.
| название | год | авторы | номер документа |
|---|---|---|---|
| ШТАММ БАКТЕРИИ DELCYA MARINA - ПРОДУЦЕНТ ЩЕЛОЧНОЙ ФОСФАТАЗЫ И СПОСОБ ПОЛУЧЕНИЯ ЩЕЛОЧНОЙ ФОСФАТАЗЫ | 1994 |
|
RU2077577C1 |
| Способ получения щелочной фосфатазы | 1988 |
|
SU1576563A1 |
| Способ очистки щелочной фосфатазы | 1988 |
|
SU1554377A1 |
| СПОСОБ ВЫДЕЛЕНИЯ ЩЕЛОЧНОЙ ФОСФАТАЗЫ ПЛАЦЕНТАРНОГО ТИПА | 2014 |
|
RU2584328C2 |
| Способ получения щелочной фосфатазы | 1985 |
|
SU1287593A1 |
| ПЛАЗМИДА 40Ph, ОПРЕДЕЛЯЮЩАЯ СИНТЕЗ ЩЕЛОЧНОЙ ФОСФАТАЗЫ CmAP, ШТАММ E.coli rosetta(DE3)/40Ph - ПРОДУЦЕНТ ХИМЕРНОГО БЕЛКА, ВКЛЮЧАЮЩЕГО АМИНОКИСЛОТНУЮ ПОСЛЕДОВАТЕЛЬНОСТЬ РЕКОМБИНАНТНОЙ ЩЕЛОЧНОЙ ФОСФАТАЗЫ CmAP, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2010 |
|
RU2447151C1 |
| Способ получения щелочной фосфатазы | 1990 |
|
SU1713265A1 |
| СПОСОБ ПОЛУЧЕНИЯ И ОЧИСТКИ ПЛАЦЕНТАРНОЙ ЩЕЛОЧНОЙ ФОСФАТАЗЫ | 2011 |
|
RU2492868C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЩЕЛОЧНОЙ ФОСФАТАЗЫ | 1991 |
|
RU2016899C1 |
| СПОСОБ ОЧИСТКИ ЩЕЛОЧНОЙ ФОСФАТАЗЫ ИЗ ТОНКОГО КИШЕЧНИКА ТЮЛЕНЯ | 1992 |
|
RU2036236C1 |
Изобретение относится к биотехнологии, в частности к производству ферментов, и может быть использовано для производства щелочной фосфатазы. С целью повышения активности, увеличения выхода целевого продукта и упрощения способа изобретение предусматривает использование в качестве сырьевого источника штамма продуцента Acinetobacter species ВКПМ В-3905 (40 MO). Выделение и очистку фермента осуществляют путем анионообменной и гидрофобной хроматографии с инактивацией примесных активностей между стадиями хроматографии. Штамм Acinetobacter species 40 МС выделен из целомической жидкости мидии Crenomytilus grayanus. Штамм обладает высокой удельной щелочной фосфатазной активностью (6,5 7,1 ед/мг мин) и высокой продуктивностью по белку (155 мг/л культуры). Удельная активность очищенной щелочной фосфатазы 3800 5600 ед/мг мин. 2 с. и 2 з. п. ф-лы, 5 табл.
| Biochemistry, 1968, | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| ПОВОРОТНЫЙ ЭЛЕКТРИЧЕСКИЙ ВЫКЛЮЧАТЕЛЬ | 1925 |
|
SU4336A1 |
| Proccedings of the National Academy of Sciences , 1984, | |||
| Горный компас | 0 |
|
SU81A1 |
| ЭЛЕКТРИЧЕСКИЙ ФОТОМЕТР | 1924 |
|
SU6691A1 |
Авторы
Даты
1995-10-20—Публикация
1987-05-11—Подача