Изобретение относится к области аналитической химии, а именно к способам количественного определения щавелевой кислоты, и может быть использовано при анализе смесей, содержащих щавелевую и серную кислоты, в сульфатцеллюлозном производстве при анализе черного щелока.
Цель изобретения - повьш1ение точности определения.
Пример . Исходная смесь содержит 70 мг серной кислоты и 5,0 мг щавелевой кислоты в 1 мл. В стакан для титрования помещают 0,2 мл анализируемого раствора, приливают 100мл ацетона и 1 мл этиленгликоля. Полученный раствор перемешивают на магнитной мешалке 1 мин и титруют
0,6890 н. раствором едкого кали до первого скачка потенциала. На достижение конечной точки титрования затрачено 0,42 мл щелочи, т.е., на нейтрализацию 14 мг серной кислоты, содержащейся в 0,2 мл анализируемого раствора, идет 0,42 мл 0,6890 н. раствора едкого кали.-Затем в другой стакан помещают 1 мл анализируемой пробы, приливают 100 мл ацетона и 1 мл этиленгликоля. Раствор перемешивают на магнитной мешалке 1 мин и приливают 0, 2,10 мл 0,6890 н. раствора едкого кали, необходимого для нейтрализации 70 мг серной кислоты, при постоянном перемешивании раствора на магнитной мешалке. Объемное процентное соотношение ацетона и
ел
о
Од
со ;о
315
этиленгликоля с учетом объема титран та 97,1:2,9. Полученный раствор фильруют в стакан для титрования, фильтр промывают 30 мл ацетона, приливают 40 мл этиленгликоля и титруют 0,0985 н. раствором едкого кали до первого скачка потенциала. На достижение конечной точки титрования затрачено 0,41 мл КОН. Определено щаве левой кислоты 5,10 мг. Относительная ошибка определения +2,07„. Объемное процентное соотношение ацетона и этиленгликоля (с учетом объема титранта 75,1:24,9.
Пример 2. Исходная смесь содержит 100 мг серной кислоты и 25 мл щавелевой кислоты в 1 мл. В стакан для титрования помещают 0,2 мл анализируемого раствора, добавляют 120 мл ацетона и 1 мл этиленгликоля. Полученный раствор перемешивают на магнитной мешалке I мин и титруют 0,6890 н. раствором едкого кали до первого скачка потенциала. На дости- жение конечной точки титрования затрачено 0,59 мл щелочи, т.е. на нейтрализацию 20 мг серной кислоты, содержащейся в 0,2 мл анализируемого
раствора, идет 0,59 мл 0,6890 н. раст-зо раствора едкого кали при постоянном
не
щавелевой кислоты в условиях анализа составляет 2-3 мг) в смеси с серной кислотой поступают следующим образом Серную кислоту, содержащуюся в анализируемой пробе, нейтрализуют не полностью, а оставляют 1-3 мг ее в титруемом растворе. Эта масса серной кислоты титрованию щавелевой кислоты
мешает.
Пример 3. Исходная смесь содержит 49,0 мг серной кислоты и 2,65 мг щавелевой кислоты в 1 мл. В стакан для титрования помещают 1 мл анализируемого раствора, приливают 80 мл ацетона и 1 мл этиленгликоля. Полученный раствор перемещивают на маг нитной мешалке 1 мин и титруют 0,6890 н, раствором едкого кали до первого скачка потенциала, соответствующего нейтрализации серной кислоты по ступени II диссоциации. На достижение конечной точки титрования затрачено 1,45 мл щелочи. Затем в другой стакан помещают тоже 1 мл анализируемой пробы, приливают 80 мл ацетона и 1 мл этиленгликоля. Раствор перемешивают на магнитной мешалке 1 мин и приливают 1,40 мл 0,6890 н.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ раздельного определения органических кислот в смеси с соляной кислотой | 1985 |
|
SU1314261A1 |
| Способ определения солей органических оксикислот | 1986 |
|
SU1399670A1 |
| Способ определения серной кислоты в присутствии органических кислот | 1985 |
|
SU1280541A1 |
| Способ раздельного определения серной и органической кислот | 1980 |
|
SU940047A1 |
| Способ определения серной кислоты в присутствии органических кислот | 1986 |
|
SU1396051A1 |
| Способ определения муравьиной щавелевой и фосфорной кислот | 1988 |
|
SU1658088A1 |
| Способ определения @ , @ -дихлор- @ -формилакриловой кислоты в водной среде | 1983 |
|
SU1132229A1 |
| Способ количественного определения серной кислоты и сульфокислот при их совместном присутствии в смеси | 1978 |
|
SU746282A1 |
| Способ определения гидроокиси натрия | 1979 |
|
SU833505A1 |
| Способ количественного определения кислот различной степени диссоциации при их совместном присутствии | 1987 |
|
SU1506350A1 |
Изобретение касается аналитической химии , в частности, количественного определения щавелевой кислоты в смеси с серной, может быть использовано в сульфат-целлюлозном производстве при анализе черного щелока. Цель - повышение точности анализа. Последний ведут потенциометрическим титрованием присутствующей в исходной пробе H2SO4 раствором щелочи в среде ацетона и этиленгликоля [объемное соотношение (99-92):(1-8)] с последующим удалением образовавшегося осадка - щелочного сульфата и дальнейшим титрованием щавелевой кислоты при объемном соотношении ацетона и этиленгликоля (85-15):(15-85). Эти условия позволяют анализировать смеси с соотношением серной и щавелевой кислот ≥20:1. Относительная ошибка определения не превышает 2%. 2 табл.
вора едкого кали. Затем в другой стакан помещают 1 мл анализируемой пробы, приливают 120 мл ацетона и 1 мл этиленгликоля. Раствор перемешивают на магнитной мешалке 1 мин и приливают 0,59 5 2,95 мл 0,6890 н. раствора едкого кали, необходимого для нейтрализации 100 мг серной кислоты, при постоянном перемешивании раствора на магнитной мешалке. Объемное процентное соотношение ацетона и этиленгликоля с учетом объема титранта 96,8:3,2. Полученный раствор фильтруют, фильтр промывают ацетоном. Объединенный раствор количественно переносят в мерную колбу емкостью 200 мл, отбирают 1/4 ацетонового раствора и переносят в стакан для титрования. Добавляют 10 мл этиленгликоля и титруют 0,0985 н. раствором едкого кали до первого скачка потенциала. На достижение конечной точки титрования затрачено 0,5 мл титранта. Определено щавелевой кислоты 24,82 мг. Относительная ошибка определения 0,7%. Объемное процентное соотношение ацетон: этиленгликоль 80:20. При определении малых количеств щавелевой кислоты (минимально определяемая масса
5
0
5
0
5
перемешивании раствора на магнитной мешалке (приливают меньший объем ще- . лочи). Объемное процентное соотношение ацетона и этиленгликоля с учетом объема титранта 97,1:2,9. Полученный раствор фильтруют в стакан для титрования, фильтр промывают 30 мл ацетона, приливают 30 мл этиленгликоля и титруют 0,0985 н. раствором едкого кали до второго скачка потенциала. На достижение первого скачка потенциала, соответствующего нейтрализации серной кислоты по ступени I диссоциации, затрачено 0,18 мл 0,0985 н. раствора едкого кали. На достижение второго скачка потенциала, соответствующего нейтрализации серной кислоты по ступени II диссоциации и щавелевой кислоты по ступени I диссоциации, затрачено 0,59 мл раствора щелочи (0,0985 н.), т.е. на нейтрализацию щавелевой кислоты затрачено (0,59-0,18-2) 0,23 мл КОН. Определено щавелевой кислоты 2,85 мг. Относительная ошибка определения ,7%. Объемное процентное соотношение ацетона и этиленгликоля (с учетом объема титранта) 76,9:23,1.
Пример 4. Исходная смесь содержит 107,8 мг серной кислоты и
10
515063496
6,0 мг щавелевой в 1 нп. В стакан для 6,08 мг. Относительная ошибка опре- титрования помещают 0,5 мл анализиру- деления ь1,3%. Объемное процентное емого раствора, приливают 100 мл ацетона и 1 МП этиленгликоля. Полученный раствор перемешивают на магнитной мешалке 1 мин и титруют 0,6890 н. раствором едкого кали до первого скачка потенциала, соответствующего нейтрализации серной кислоты по ступени II диссоциации. На достижение конечной точки титрования затрачено 1,60 мл щелочи. Затем в другой стакан помещают 1 мл анализируемой пробы, приливают 100 МП ацетона и 1 мл этиленгли- 15 способа проанализированы искусственные коля. Раствор перемешивают на магнит- смеси, содержащие серную и щавелевую ной мешалке 1 мин и приливают 3,12 мл 0,6890 н. раствора едкого кали при постоянном перемешивании раствора на магнитной мешалке (приливают меньший 20 объем щелочи с учетом того, что 1-Змг серной кислоты должно остаться в растворе) . Объемное процентное соотношение ацетона и этиленгликоля (с учетом объема титранта) 96,7:3,3. Полу- 25 лоту в 20 раз. Заданные массы щавепе ченный раствор фильтруют в стакан для вой кислоты по предлагаемому способу титрования, фильтр промывают 30 мл ацетона, приливают 35 мл этиленгликоля и титруют 0,0985 н. раствором КОН до второго скачка потенциала. На достижение первого скачка потенциала, соответствующего нейтрализации серной кислоты по ступени I диссоциации, затрачено 0,27 мл 0,0985 н. раствора КОН. На достижение второго скачка потенциала, соответствующего нейтрализации серной кислоты по ступени II диссоциации и щавелевой кислоты по ступени I диссоциации,затрачено 1,03 мл 0,0985 н.раствора КОН.На нейтра-40 рабатывают раствором щелочи в среде лизацию щавелевой кислоты затрачено смеси ацетона и этиленгликоля, взятых (1,03-0,272 1 0,49 нп раствора в объемных процентных соотношениях чи. Определено щавелевой кислоты 99-92:1-8.
Таблица 1
соотношение ацетона и этиленгликоля (с учетом объема титранта) 78,9:21,1.
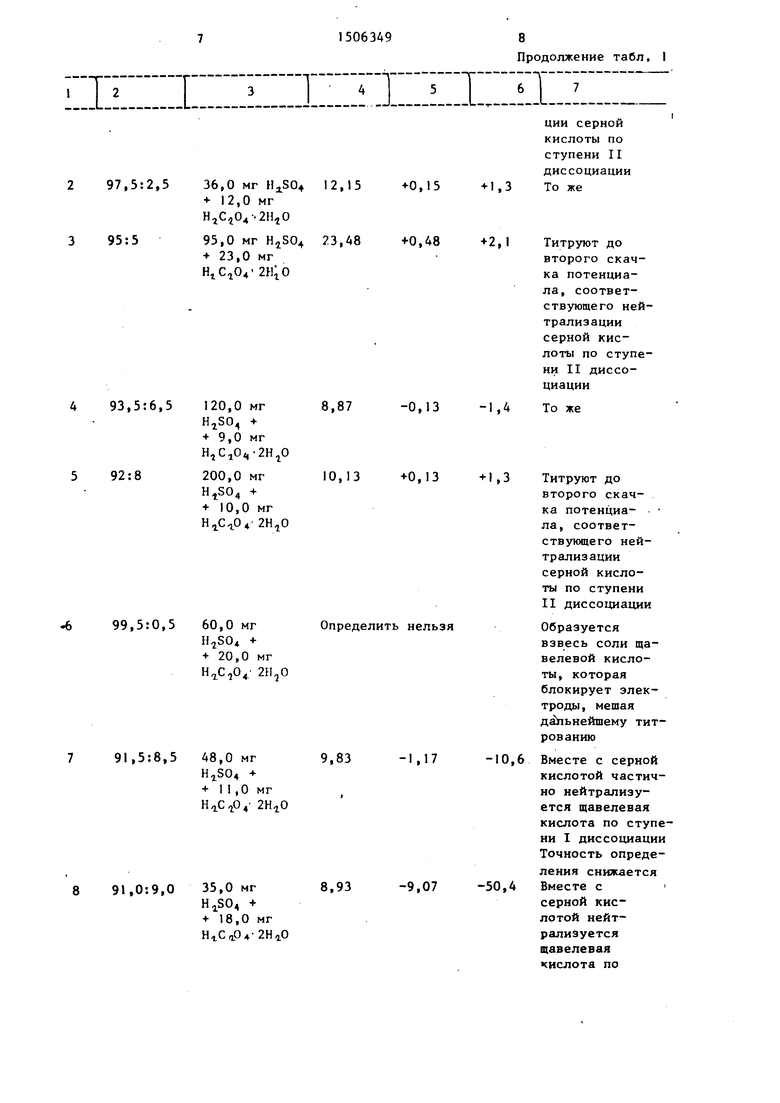
В табл. I приведены примеры, иллюстрирующие предлагаемый способ, а также сравнительные ггримеры проведения анализа в условиях, выходящих за пределы условий предлагаемого способа (6-9), и по известному способу (10).
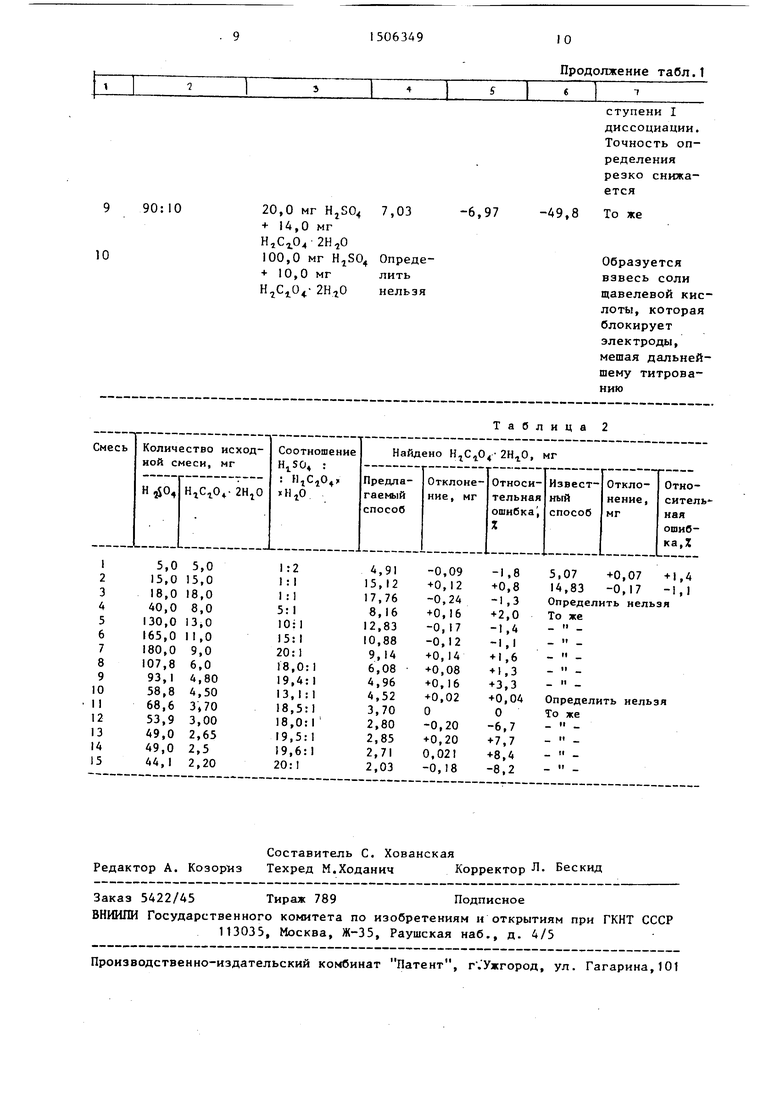
Для оценки точности предлагаемого
кислоты при различном их массовом соотношении предлагаемым и извес ным способами (табл.2).
Приведенные данные свидетельствуют о том, что анализ щавелевой кислоты по предлагаемому способу возможен в смесях, содержащих серную кислоту, по массе превьш1ающую щавелевую кисопределяются с ошибкой, не превьщ1а- ющей 2%.
30 Формула изобретения
Способ количественного определения щавелевой кислоты в присутствии серной кислоты путем потенциометри- 25 ческого титрования раствором щелочи в среде ацетона и этиленгликоля, о т- личающийся тем, что, с целью повышения точности определения, анализируемую пробу предварительно об99:1
25,0 мг HjSO 7,94 I- 8,0 мг
2Н.,0
6,08 мг. Относительная ошибка опре- деления ь1,3%. Объемное процентное способа проанализированы искусственные смеси, содержащие серную и щавелевую лоту в 20 раз. Заданные массы щавепе вой кислоты по предлагаемому способу рабатывают раствором щелочи в среде смеси ацетона и этиленгликоля, взятых в объемных процентных соотношениях 99-92:1-8.
соотношение ацетона и этиленгликоля (с учетом объема титранта) 78,9:21,1.
В табл. I приведены примеры, иллюстрирующие предлагаемый способ, а также сравнительные ггримеры проведения анализа в условиях, выходящих за пределы условий предлагаемого способа (6-9), и по известному способу (10).
Для оценки точности предлагаемого
6,08 мг. Относительная ошибка опре- деления ь1,3%. Объемное процентное способа проанализированы искусственны смеси, содержащие серную и щавелевую лоту в 20 раз. Заданные массы щавепе вой кислоты по предлагаемому способу рабатывают раствором щелочи в среде смеси ацетона и этиленгликоля, взятых в объемных процентных соотношениях 99-92:1-8.
кислоты при различном их массовом соотношении предлагаемым и извес ным способами (табл.2).
Приведенные данные свидетельствуют о том, что анализ щавелевой кислоты по предлагаемому способу возможен в смесях, содержащих серную кислоту, по массе превьш1ающую щавелевую кис6,08 мг. Относительная ошибка опре- деления ь1,3%. Объемное процентное способа проанализированы искусственные смеси, содержащие серную и щавелевую лоту в 20 раз. Заданные массы щавепе вой кислоты по предлагаемому способу рабатывают раствором щелочи в среде смеси ацетона и этиленгликоля, взятых в объемных процентных соотношениях 99-92:1-8.
определяются с ошибкой, не превьщ1а- ющей 2%.
Формула изобретения
Способ количественного определения щавелевой кислоты в присутствии серной кислоты путем потенциометри- ческого титрования раствором щелочи в среде ацетона и этиленгликоля, о т- личающийся тем, что, с целью повышения точности определения, анализируемую пробу предварительно об0,06 -0,8 Титруют до
первого скачка потенциала, соответствующегонейтрализа 12,0 мг H C 04- 2H O
} 95:5 95,0 мг 23,48 +0,48 +2,1 Титруют до
+ 23,0 мгвторого скачК С О 21 0ка потенциала, соответствующего нейтрализациисерной кислоты по ступени II диссоциации
493,5:6,5 120,0 мг 8,87 -0,13 -1,4 То же
, + + 9,0 мг H,C,iOi,
592:8 200,0 мг 10,13 +0,13 +1,3 Титруют до
+второго скач+ 10,0 мгка потенциаH, , соответствующего нейтрализациисерной кислоты по ступени II диссоциации
) 99,5:0,5 60,0 мг Определить нельзя Образуется
+взвесь соли ща+ 20,0 мгвелевой кислоН С 04. , которая
блокирует электроды, мешая дальнейшему титрованию
7 91,5:8,5 48,0 мг 9,83 -1,17 -10,6 Вместе с серной Н, кислотой частич+ 11,0 мг но нейтрализуH C-jp4 2Н Оется щавелевая
кислота по ступени I диссоциации Точность определения снижается 8 91,0:9,0 35,0 мг 8,93 -9,07 -50,4 Вместе с
+серной кис+ 18,0 мглотой нейтHi.Ca04-2Ha.Oрализуется
щавелевая кислота по
Продолжение табл.1
лоты, которая блокирует электроды, мешая дальнейшему титрованию
| Способ определения серной кислоты в присутствии органических кислот | 1986 |
|
SU1396051A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Крешков А.П | |||
| Основы аналитической химии | |||
| М.: Госхимиздат, 1961, с | |||
| ШАХТНАЯ ТОПКА ДЛЯ МНОГОЗОЛЬНОГО ТОРФА | 1922 |
|
SU610A1 |
| Заводская лаборатория, 1983, 10, с | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
Авторы
Даты
1989-09-07—Публикация
1987-08-25—Подача