Изобретение относится к микробиологии и предназначено для ускоренного определения плазмокоагулирующей активности стафилококков при их идентификации.
Цель изобретения - улучшение качества препарата за счет повышения его чувст- вительности, упрощение и ускорение процесса определения, а также увеличение срока годности.
Используемый для определения плазмокоагулирующей активности твердофазный препарат- плазмокарандаш постоянно готов к быстрому применению на стекле, содержит сухую цитратную кроличью плазму и дополнительно полиэтиленгликоль, бычий сывороточный альбумин, сахарозу и глицерин при следующем соотношении ингредиентов, мас.%: Сухая цитратная кроличья плазма36,54- 39,62
Полиэтиленгликоль
с мол. м, 4000 Бычий сывороточный
альбумин
Сахароза
Глицерин
35,85-40,38
3.84-5.66 3,77-5.77 Остальное
Твердый препарат имеет форму карандаша и обладает пишущими свойствами по стеклу, пластмассе, фарфору.
В качестве ингредиентов в препарате используют: сухую цитратную кроличью плазму - порошок белого цвета; полиэтиленгликоль с мол.м. 4000 - кристаллы белого цвета; бычий сывороточный альбумин - ли- офилизированный порошок белого цвета; сахарозу ЧДА - кристаллический порошок белого увета: глицерин чистый - бесцветную прозрачную жидкость.
Сухую цитратную кроличью плазму вводят в препарат в качестве специфического субстрата, полиэтиленгликоль - в качестве
Ё
ON
00
о VI
VI
твердофазного носителя субстрата, консерванта и стабилизатора, обусловливающего форму и пишущие свойства препарата, бычий сывороточный альбумин - в качестве связывающего агента, улучшающего пишу- 5 щие свойства препарата, сахарозу как стабилизатор и связывающий компонент и глицерин как агент, регулирующий консистенцию, пластичность и способствующий сохранению физико-химических свойств 10 препарата.
Препарат получают следующим образом.
В фарфоровую ступку последовательно вносят подиэтиленгликоль, сухую цитрат- 15 ную кроличью плазму, бычий сывороточный альбумин, сахарозу и растирают до гюлуче- ния белой пудры, затем каплями добавляют глицерин и перемешивают до образования однородной массы вязкой консистенции, 20 которую формуют в виде карандаша, используемого впоследствии многократно для определения плазмокоагулирующей активности стафилококков на предметном стекле.25
П р и м е р. В фарфоровую ступку последовательно вносят 2 г полиэтиленгликоля е мол.м. 4000, 2 г сухой цитратной кроличьей плазмы, 0,25 г бычьего сывороточного альбумина, 0,25 г сахарозы и тщательно расти- 30 рают в течение 20 мин до получения мелкой пудры. Затем каплями при постоянном перемешивании добавляют 0,75 мл глицерина до образования однородной массы вязкой консистенции, которой придают форму ка- 35 рандаша. Полученный плазмокарандаш вводят в пластмассовый футляр и хранят в холодильнике при 4°С, По мере надобности плазмокарандаш используют в работе (срок наблюдения 3 года).40
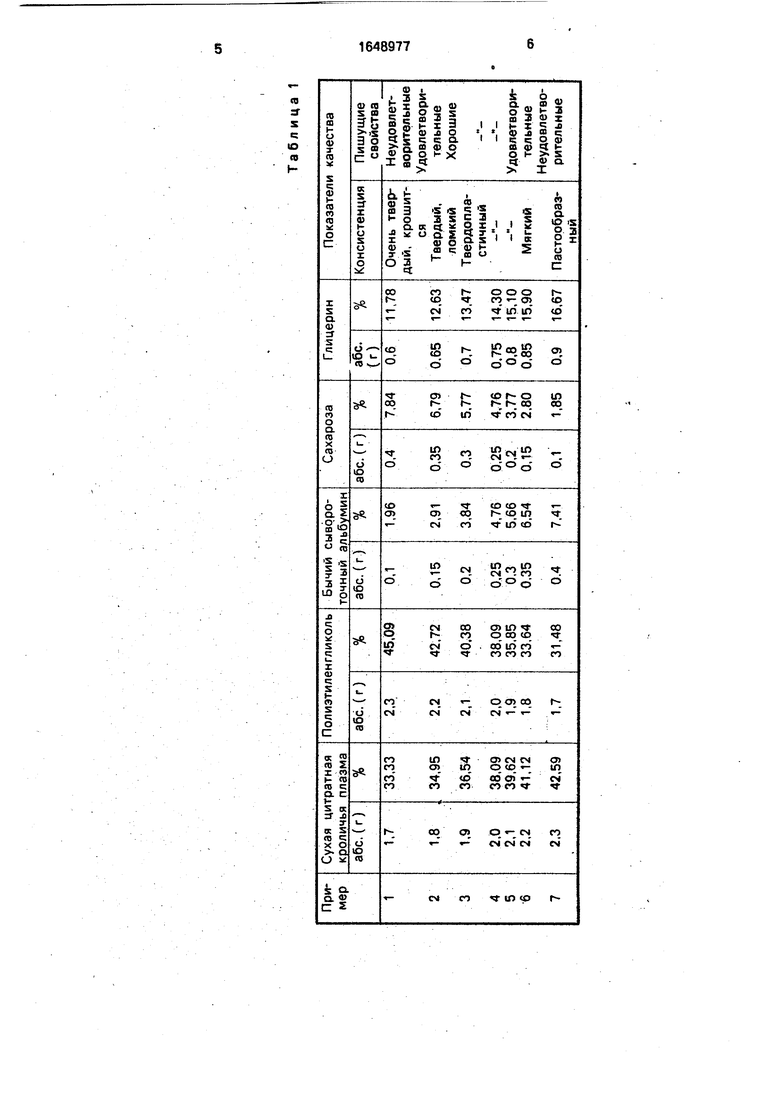
В табл. 1 приведены показатели качества плазмокарандаша в зависимости от содержания ингредиентов; в табл. 2 - оценка экономичности определения плазмокоагулирующей активности стафилококков с по- 45 мощью известного и предлагаемого репаратов; в табл. 3 - оценка скорости определения плазмокоагулирующей активности стафилококков с помощью известного и предлагаемого препаратов.50
Как видно из табл. 1, все плазмокаран- даши, содержащие ингредиенты в пределах граничных значений, обладают хорошими пишущими свойствами, пластичностью и длительной сохранностью.55
Плазмокарандаш применяют следующим образом.
На чистое предметное стекло наносят плазмокарандашом 2-3 пересекающихся
штриха, каждый длиной до 1 см. Затем на штрихи наносят каплю физраствора и в ней тщательно эмульгируют бактериальную петлю 18-24-часовой исследуемой культуры стафилококка. Контролем служат любые ко- агулазоотрицательные микробы. Предметное стекло помещают во влажную камеру и инкубируют в термостате при 37°С. Через каждые 15 мин учитывают результаты.
В опытной капле через 30-40 мин наступает частичная, а через 60-90 мин полная коагуляция плазмы. Окончательный результат можно учитывать через 2 ч. Контрольная капля через 2 ч остается жидкой.
Применение плазмокарандаша в качестве препарата для определения плазмокоагулирующей активности стафилококков является более экономичным, чем применение сухой цитратной плазмы, так как позволяет использовать минимальное количество сухой цитратной плазмы и других реагентов без потерь, что снижает себестоимость препарата (табл. 2).
Кроме того, применение плазмокарандаша по сравнению с использованиемюухой цитратной плазмы позволяет ускорить выдачу окончательного ответа о плазмокоагулирующей активности исследуемой культуры в среднем в 5 раз (табл. 3).
Таким образом, технико-экономическая эффективность предлагаемого препарата состоит в уменьшении себестоимости препарата, увеличении срока его годности, упрощении и ускорении определения плазмокоагулирующей активности стафилококков.
Формула изобретения
Препарат для определения плазмокоагулирующей активности стафилококков, содержащий сухую цитратную кроличью плазму, отличающийся тем, что, с целью улучшения качества препарата за счет повышения его чувствительности, упрощения и ускорения процесса определения, а также увеличения срока годности, он дополнительно содержит полиэтиленгли- коль с мол.м. 4000, бычий сывороточный альбумин, сахарозу и глицерин при следующем соотношении компонентов, мас.%: Сухая цитратная
кроличья плазма36,54-39,62
Полиэтиленгликоль
с мол. м. 4000 35,85-40,38
бычий сывороточный альбумин3,84-5,66
Сахароза3,77-5,77
Глицерин Остальное
Таблица 2

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения фосфатазной активности микроорганизмов | 1990 |
|
SU1726516A1 |
| СТАБИЛИЗИРОВАННЫЙ ВОДНЫЙ РАСТВОР ЭРИТРОПОЭТИНА | 1998 |
|
RU2128517C1 |
| НАБОР ДЛЯ ВЫЯВЛЕНИЯ ХЛАМИДИЙНОЙ ИНФЕКЦИИ | 1992 |
|
RU2042360C1 |
| СТАБИЛИЗИРУЮЩИЙ СОСТАВ ДЛЯ ПОЛУЧЕНИЯ РЕФЕРЕНС-СЫВОРОТОК, СОДЕРЖАЩИХ IGM-АНТИТЕЛА | 1997 |
|
RU2136313C1 |
| Способ иммуногистохимического выявления антигенов в препаратах органов продуктивных и непродуктивных животных длительного хранения в фиксаторах | 2016 |
|
RU2627448C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИОФИЛИЗИРОВАННОГО ПРЕПАРАТА КРОВЬ ГЕМОЛИЗИРОВАННАЯ | 2011 |
|
RU2455014C1 |
| Штамм гибридных культивируемых клеток животных MUS мUSсULUS L.-продуцент моноклонального антитела к гликопротеиду миелина головного мозга, угнетающего активность естественных киллеров человека | 1990 |
|
SU1721092A1 |
| Способ постановки реакции микроагглютинации | 1983 |
|
SU1147353A1 |
| СПОСОБ ДИАГНОСТИКИ АКТИВНОСТИ ИНФЕКЦИОННОГО ЭНДОКАРДИТА | 1997 |
|
RU2146824C1 |
| Штамм гибридных культивируемых клеток животных MUS мUSсULUS, используемый для получения моноклональных антител к @ - тимозину | 1988 |
|
SU1527260A1 |
Изобретение относится к микробиологии и предназначено для определения коагулирующей активности: стафилококков при их идентификации. Цель изобретения - улучшение качества препарата за счет повышения его чувствительности, упрощение и ускорение процесса определения, а также увеличение срока годности. Используемый препарат содержит сухую цитратную кроличью плазму, полиэтиленгликоль с мол.м. 4000, бычий сывороточный альбумин, сахарозу и глицерин при следующем соотношении компонентов, мас.%: сухая цитратная кроличья плазма 36,54-39,62; полиэтиленгликоль 4000 35,85-40.38; бычий сывороточный альбумин 3,84-5,66: сахароза 3,77-5,77: глицерин остальное. 3 табл.
Критерии экономичности
Сухая цитратная кроличья плазма
2-3
Пробирки, пипетки
Растворение сухой плазмы,
ее разведение и разливка
в пробирки
До 25-30
2
После открытия ампулы 3-4 дня
Исследуемая культура
Золотистый стафилококк 209
243
Кован-Г Королев Иванов
12600 Смит
Эпидермальный стафилококк
Сапрофитовый стафилококк
Микрококк лизодейктикус
Кишечная палочка (0-55)
Плазмокарандаш
2-3
25-30
Предметные стекла
Нанесение штрихов на
стекло
До 3-5
Таблица 3
Время получения рез
льтата. f мин )
Сухая цитратная кроличья плазма (прототип)
Плазмокарандаш
62 48 66 74 74 82 85
| Никитин В.М | |||
| Справочник методов биохимической экспресс-индикации микробов.- Кишинев: Картя молдовеняска, 1986, с | |||
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
Авторы
Даты
1991-05-15—Публикация
1989-05-31—Подача