Ё

| название | год | авторы | номер документа |
|---|---|---|---|
| ОБЪЕДИНЕННОЕ ЭКСТРАГИРОВАНИЕ АММИАЧНЫМ РАСТВОРИТЕЛЕМ И ВОССТАНОВЛЕНИЕ НИКЕЛЯ ВОДОРОДОМ | 2002 |
|
RU2287598C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОЧИСТОГО КАРБОНАТА КАДМИЯ | 2013 |
|
RU2522007C1 |
| Способ получения аммиаката меди | 1984 |
|
SU1248956A1 |
| КРИСТАЛЛИЧЕСКИЙ ФОСФАТ АКВААММИНКОБАЛЬТА (II) И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1991 |
|
RU2032615C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОСНОВНЫХ УГЛЕКИСЛЫХ СОЛЕЙ МЕДИ, ЦИНКА, НИКЕЛЯ И КОБАЛЬТА И ИХ ОКСИДОВ | 1991 |
|
RU2043301C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ ПОЛУЧЕНИЯ МЕТАНОЛА | 1990 |
|
RU1774556C |
| РЕГЕНЕРАЦИОННАЯ СИСТЕМА И СПОСОБ ОБРАБОТКИ ГАЗОВОГО ПОТОКА ИЗ КРИСТАЛЛИЗАЦИОННОГО БЛОКА КАРБАМИДНОЙ УСТАНОВКИ | 2015 |
|
RU2683086C2 |
| СПОСОБ И УСТРОЙСТВО ДЛЯ ПОЛУЧЕНИЯ ГИДРАЗОДИКАРБОНАМИДА С ИСПОЛЬЗОВАНИЕМ МОЧЕВИНЫ В КАЧЕСТВЕ ИСХОДНОГО ПРОДУКТА | 2001 |
|
RU2292335C2 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ МОЧЕВИНЫ И МЕЛАМИНА | 1973 |
|
SU370774A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКОВ МЕТАЛЛОВ W, MO, RE, CU, NI, CO И ИX CПЛABOB | 1993 |
|
RU2048279C1 |
Изобретение относится к неорганической химии vi может быть использовано для получения аммиакатов меди, применяемых в аналитической практике и в производстве печатных плат. Цель изобретения - получение устойчивых аммиакатов меди повышенной чистоты.Аммиакаты меди получают путем смешивания порошка металлической меди и кристаллической соли аммония, взятых в эквивалентных количествах, увлажнения смеси концентрированным водным раствором аммиака при молярном соотношении аммиака и меди (0,24-0,66): 1 и взаимодействии реагентов при перемешивании. Процесс проводят в воздушно-аммиачной атмосфере или полученные аммиакаты меди дополнительно обрабатывают газообразным аммиаком. 1 табл.
Изобретение относится к неорганической химии и может быть использовано для получения аммиакатов меди, которые находят применение при производстве солей меди, катализаторов, используются в аналитической практике и в технологии печатных плат для приготовления медно-аммиачных растворов травления и беспалладиевой металлизации диэлектриков.
Цель изобретения - получение устойчивых аммиакатов меди повышенной чистоты. . Аммиакаты меди получают путем смешения порошка металлической меди и кристаллической соли аммония, взятых в эквивалентных количествах, увлажнения смеси концентрированным водным раствором аммиака при молярном соотношении аммиака и меди (0,24-0,66): 1 и взаимодействии реагентов при перемешивании. Процесс проводят в воздушно-аммиачной
атмосфере или полученные аммиакаты меди дополнительно обрабатывают газообразным аммиаком.
Оптимальные параметры процесса получения аммиакатов меди выбраны по следующим причинам. Только изоэквивалентные количества меди и соли аммония обеспечивают достижение требуемой чистоты продукта, не загрязненного макроколичествами непрореагировавшего избытка одного из компонентов реакционной смеси. Оптимум количества вводимого в реакцию концентрированного водного раствора аммиака установлен экспериментально и обусловлен тем обстоятельством, что химическая реакция между металлической медью и солью аммония протекает с максимальной скоростью в слабо увлажненной сыпучей реакционной смеси. Как при снижении влажности смеси, так и при ее переувлажнении скорост ь
VI
О
о
Ч)
о ел
реакции образования аммиакатов меди резко снижается вплоть до полного прекращения взаимодействия компонентов в реальном масштабе времени. Экспериментально установлено, что в зависимости от дисперсности металлической меди, молекулярной массы соли аммония и ее плотности (насыпной массы) оптимальная влажность реакционной смеси достигается при введении концентрированного ( 25%-ного водного раствора аммиака в количестве 0,24-0,66 молей МНз на 1 моль Си.
Время взаимодействия реагентов зависит от величины загрузки и состава реакционной смеси и колеблется от 5 до 25-30 мин при получении от единицы до сотен граммов аммиакатов меди за цикл.
Реакция между медью и солью аммония сопровождается выделением тепла и разогревом смеси. Окончание реакции определяют визуально по образованию интенсивно окрашенного продукта - от ярко-голубого до темно-фиолетового цвета, не содержащего частиц непрореагировавшей металлической меди.
Идентификацию полученных аммиакатов меди проводят методами химического и рентгенофазового анализа. Продукты реакции представляют собой аммиакаты соответствующих солей меди состава Cu(NH3Jx An, где 2 х 4, с примесями непрореагировавших исходных реагентов - металлической меди и соли аммония. Выход целевого продукта - аммиаката меди составляет 95-99% от теоретического по меди. Как правило, получаемые аммиакаты меди лишь частично растворимы в воде, однако после дополнительной обработки продукта реакции газообразным аммиаком или при проведении синтеза в воздушно-аммиачной атмосфере образуются устойчивые аммиакаты, полностью растворяющиеся в воде без гидролиза. Дополнительную обработку получаемого продукта аммиаком осуществляют либо пропусканием тока газообразного аммиака над продуктом или через его слой, либо выдерживанием продукта в атмосфере аммиака до насыщения продукта аммиаком и образования устойчивого аммиаката медис молярным соотношением МНзгСи 4,0.
Синтез в воздушно-аммиачной атмосфере проводится при получении аммиакатов меди в аппаратах с механическим перемешиванием реакционной смеси, например в шнековых смесителях. В этом случае в зону реакции одновременно подаются воздух и газообразный аммиак или воздух, насыщенный аммиаком при бэрботировании воздуха через концентрированный водный раствор аммиака. При этом насыщение продукта аммиаком происходит непосредственно в процессе синтеза, по окончании
которого образующийся продукт представляет собой тетрааммиакат соответствую- щей соли меди.
П р и м е р. В фарфоровой чашке смешивают при комнатной температуре 20 г мед0 ного порошка марки ПМС-2 и 33, 7 г аммония хлористого (ЧДА), смесь увлажняют 10 мл концентрированного (220 г МНз на 1 л воды) раствора аммиака. Соотношение эквивалентов Cu:NH4CI 1:1, молярное соот5 ношение МНз:Си 0,41:1. Смесь перемешивают фарфоровым шпателем до окончания реакции, определяемому по отсутствию в реакционной смеси визуально различных розовых частиц металлической меди. Время
0 от начала перемешивания до завершения реакции составляет 10 мин. В процессе синтеза реакционная смесь разогревается. Полученный продукт, масса которого после охлаждения составляет 56,9 г, по данным
5 химического анализа представляет собой аммиакат дихлорида меди с молярным соотношением МНз:Си 2,2 и содержит около 1 % непрореагировавшей металлической меди от ее исходного количества. Аммиакат дих0 лорида меди частично растворим в воде с образованием раствора синего цвета и ярко-голубого осадка.
Продукт выдерживают в течение 1 ч в эксикаторе над концентрированным рас5 твором аммиака. При этом цвет аммиаката переходит от голубого в интенсивно-синий. продукт растворяется в воде без осадка, а содержание в нем аммиаката возрастает до молярного соотношения МНз:Сш4,051.0.10.
0 По данным рентгеиофазного анализа полученный продукт идентичен тетрааммизка- ту дихлорида меди, синтезированному взаимодействием дигидрата меди с сухим газообразным аммиаком и высушенному
5 над едким кали.
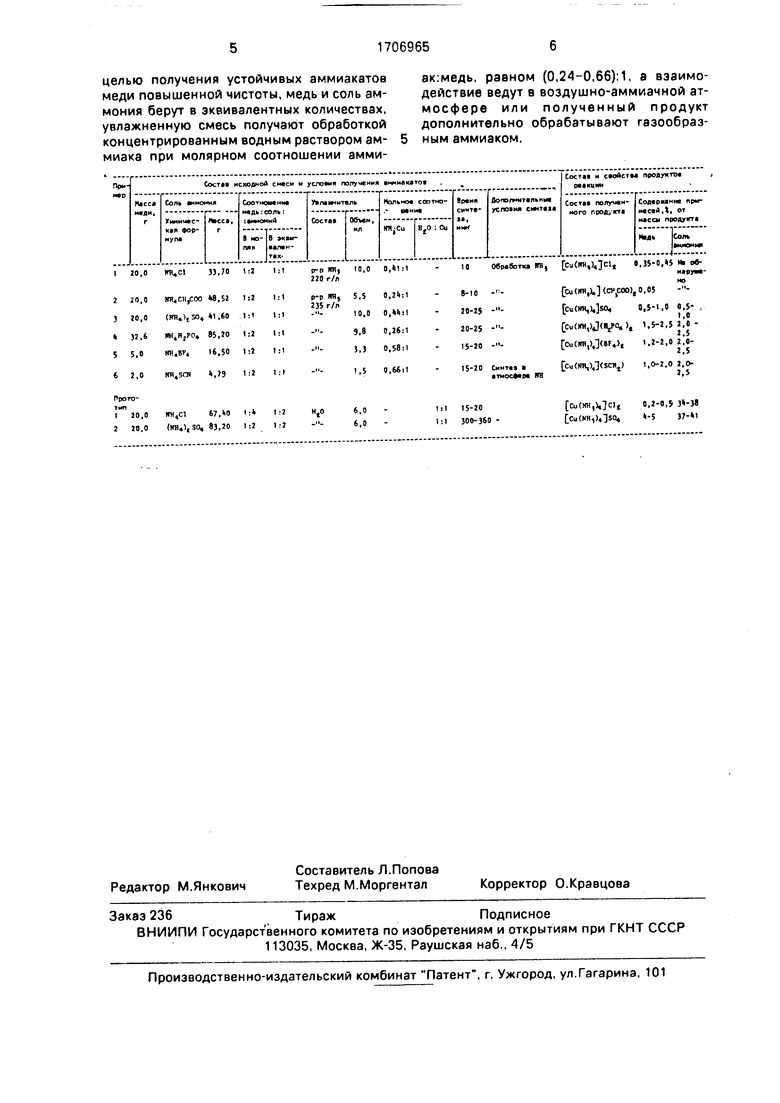
Примеры осуществления предлагаемого способа, а также его сопоставление с прототипом представлены в таблице.
Предлагаемый сопособ позволяет пол0 учить более широкий ассортимент аммиака тов меди, при этом чистота получаемых веществ повышается, а время их синтеза уменьшается в 1,5-15 раз по сравнению с прототипом.
5Формула изобретения
Способ получения аммиакатов меди включающий взаимодействие при перемешивании увлажненной смеси металлической меди с кристаллической солью аммония, отличающийся тем. что. с
целью получения устойчивых аммиакатов меди повышенной чистоты, медь и соль аммония берут в эквивалентных количествах, увлажненную смесь получают обработкой концентрированным водным раствором ам- миака при молярном соотношении амми
20,0 KH,CI
20,0
20,0
2,°
КН«С)1,СОО W.521:2I
, 41,60.1:1I
KH,HjPOf 85,01:21
НН.БГ, 16.501:2I
NH.SCH «,791:21
р-0 РШ| 10,0 0,111:1 22 г/л
р-р ЯН, 5,5 0,2Ы 2 35 г/л
,0 0,Mil
,8 0,26:1 3,3 0,58:1
,5 0,66it
mt.cl
67,«О l:k
(ХЯ),30, 83,20 1:2 1:2
ным аммиаком,
ак:медь, равном (0,24-0,66):1, а взаимодействие ведут в воздушно-аммиачной атмосфере или полученный продукт дополнительно обрабатывают газообраз10 06(6oTic И, СиСтфЛс, в.35-0,5 I о«и«рум
фер NB
CudtH lCCHjCOO), 0,05 CuOlH,),,
0.5-1,0 О
1 (() 1,5-2,52
2
1,0-г.о 2
Cu(«H,)J(f«.,
cu(tm,)4l sciit)
1:1 15-20 1:1 300-360
Cu(KK,,clt0.2-0,5 Jll-38 Cu(KH,),3SQ4 -5 
| Способ получения аммиаката меди | 1984 |
|
SU1248956A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1992-01-23—Публикация
1989-02-28—Подача