Изобретение относится к новым производным ряда бензофурана, а конкретно к гидрохлоридам 2-метил-3-ацил-4-диалкиламинометил-5-оксибензофурана общей формулы I где R1 = R2 = H, R3 = Br, R4 = R5 = CH3 (Ia);
где R1 = R2 = H, R3 = Br, R4 = R5 = CH3 (Ia);
R1 = R2 = H, R3 = F, R4 = R5 = CH3 (Iб);
R1 = R2 = H, R3 = OCH3, R4 = R5 = -(CH2)5- (Iв);
R1 = R3 = OCH3, R2 = H, R4 = R5 = CH3 (Iг);
R1 = R3 = OCH3, R2 = H, R4 = R5 = C2H5 (Iд);
R1 = H, R2 = R3 = OCH3, R4 = R5 = CH3 (Iе);
R1 = H, R2 = R3 = OCH3, R4 = R5 = C2H5 (Iж) или
R1 = R2 = R3 = OCH3, R4 = R5 = CH3 (Iз), обладающим местноанестезирующей активностью.
Известны соединения, близкие одновременно и по структуре, и по фармакологическому действию соединениям I. Так, слабая местноанестезирующея активность при терминальном и инфильтрационном методах исследования обнаружена у ряда производных 3-ацил-5-оксибензофурана, не содержащих 2-метильной группы.
Известно соединение бензофуранового ряда - тартрат 2-метил-3-карбэтокси-4-хлор-5-окси-6-диметиламинометилбензо- фурана (бензофурокаин), которое обладает местноанестезирующей и анальгетической активностью.
Как по структуре, так и по фармакологическосу действию бензофурокаин является одним из ближайших аналогов соединений I.
Следует отметить, что бензофурокаин имеет относительно низкую местноанестезирующую активность. При инфильтрационной анестезии он превосходит новокаин по глубине и продолжительности только в 2-3 раза, а при проводниковой - в 2-4 раза. С современными эффективными анестетиками (маркаин, лидокаин) сравнение не проводилось. Существенным недостатком бензофурокаина является также плохая растворимость в воде и органических растворителях.
Известен также 2-(3'-бром-4'-метоксифенил)-3-карбэтокси-4-диметиламиноме- тил-5-оксибензофуран (А), обладающий местноанестезирующей активностью.
Целью изобретения являются новые производные в ряду бензофурана, обладающие более высокими местноанестезирующей активностью и растворимостью.
Поставленная цель достигается химической структурой новых соединений общей формулы I.
Способ их получения основан на реакции аминометилирования 3-ацил-5-оксибензофуранов.
Соединения I представляют собой кристаллические вещества белого цвета, растворимые в воде и спиртах. Их растворимость в воде обеспечивает возможность использования в виде растворов в необходимых для медицинского применения дозировках.
П р и м е р. Получение гидрохлорида 2-метил-3-(4-бромбензолил)-4-диметилами-нометил-5-оксибензофурана (Ia).
Смесь 3,3 г (0,01 моль) 2-метил-3-(4-бромбензоил)-5-оксибензофурана и 1,5 мл (0,011 моль) бисдиметиламинометана в 20 мл диоксана кипятят до исчезновения исходного бензофурана. Процесс контролируется хроматографически на пластинке "Silufol UV254"в системе бензол:ацетон (9:1). Для окончания реакции обычно требуется 7 ч. Растворитель отгоняют в вакууме. К остатку прибавляют 100 мл воды. Выпавшие кристаллы отфильтровывают, промывают на фильтре водой и сушат. Сухой кристаллический осадок растворяют в 100 мл абсолютного эфира и прибавляют к нему эфирный раствор хлористого водорода до pH 1-2. Образовавшийся осадок отфильтровывают, промывают на фильтре абсолютным эфиром.
Получают 3,1 г (73,1%) гидрохлорида 2-метил-3(4-бромбензоил)-4-диметиламино- метил-5-оксибензофурана, т.пл. 230-232оС (из изопропилового спирта).
Найдено, %: C 53,45; Н 4,87; Cl 7,95; Br 18,37; N 2,86.
С19H19BrClNO3.
Вычислено, %: С 53,73; Н 4,51; Сl 8,35; Br 18,82; N 3,30.
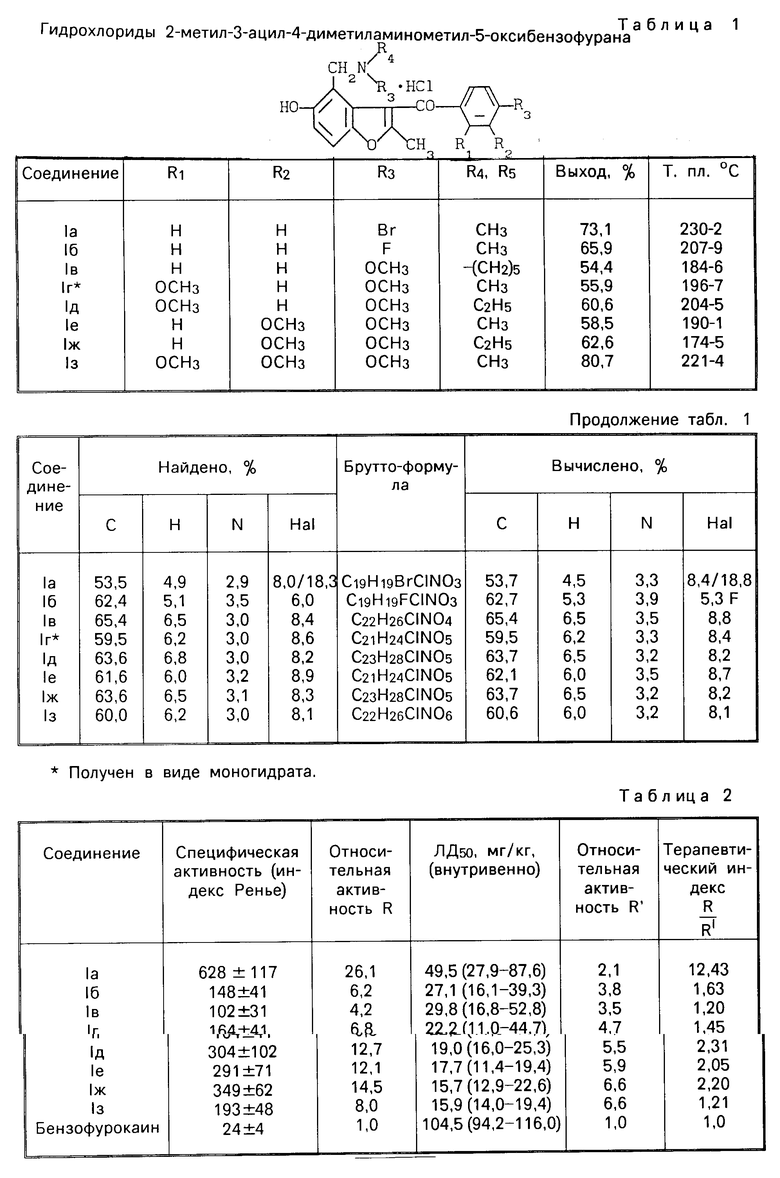
В условиях, аналогичных примеру 1, из 2-метил-3-(4-фторбензоил)-, 2-метил-3-(4-метоксибензоил)-, 2-метил-3-(2,4-диме- токсибензоил)-, 2-метил-3-(3,4-диметоксибензоил)-, 2-метил-3-(2,3,4-триметоксибензоил)-5-оксибензофуранов получают соответствующие соединения Iб-з. Физико-химические характеристики последних и данные элементного анализа представлены в табл.1.
Острую токсичность соединений Iа-з определяли на белых беспородных мышах-самцах массой 18-20 г при однократном внутривенном введении в виде 0,1% -ного раствора в дозах 10-60 мг/кг. Значения токсичности (ЛД50мг/кг) соединений Iа-з представлены в табл.2.
Местноанестезирующую активность соединений Iа-з изучали в сравнении с производным бензофурокаина. Исследования проводили по стандартной скрининговой экспериментальной модели - метод Ренье на глазах кроликов-самцов массой 2,0-2,5 кг. Соединения исследовались в виде 0,05%-ных растворов на восьми животных каждое. Об активности соединений судили по индексу анестезии и по рассчитанному статистически терапевтическому индексу - отношению относительной активности к относительной токсичности 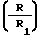 . Статистическая обработка результатов проводилась с использованием t-критерия Стьюдента.
. Статистическая обработка результатов проводилась с использованием t-критерия Стьюдента.
Сравнение местноанестезирующей активности соединений Ia-з с бензофурокаином (см. табл. 2) показало, что все исследуемые вещества превосходят препарат сравнения как по индексу анестезии (более чем в четыре раза), так и по терапевтическому индексу, причем соединение Ia - в 12 раз.
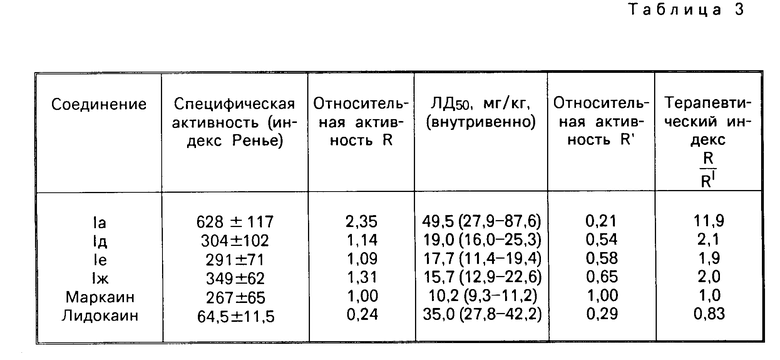
Для соединений Ia, д-ж, имеющих наибольшие значения терапевтического индекса, дополнительно изучалась местноанестезирующая активность в сравнении с наиболее эффективными современными местными анестетиками - маркаином и лидокаином.
Активность соединений I также оценивали по индексу анестезии и терапевтическому индексу.
Установлено (см. табл. 3), что соединения Ia,д-ж превосходят специфическую активность как лидокаина, так и маркаина в два раза, а соединение 1а - в 12 раз.
Что касается другого аналога по структуре и действию - соединения А, то согласно известным данным исследований этого соединения следует, что эффект достигался при использовании растворов весьма высокой концентрации (0,25 и 0,5% ), в то время как предлагаемые соединения применялись в разбавленных растворах с концентрацией 0,05%. Уже исходя из дозозависимого эффекта соединений этого типа видно, что соединения I являются более активными местными анестетиками.
Тем не менее, эксперименты с 0,25%-ными растворами наиболее и наименее активных соединений Ia и Iе показали следующие результаты по специфической активности: Соединения Специфическая
активность
(индекс Ренье)
(0,25%-ные
растворы) Ia 1110 ± 109 Iе 905 ± 48 A 850 ± 83,5
При сопоставлении токсичности соединений (A) и Iа при внутрибрюшном введении ЛД50 соединения (A) 131,25 мг/кг, для соединения Iв - 185,71 мг/кг.
Таким образом, в результате проведенного исследования обнаружен новый ряд производных бензофурана, доступных в синтетическом отношении и обладающих высокой биологической активностью, существенно превосходящих препарат сравнения (аналог по структуре и действию) - бензофурокаин как по местноанестезирующему действию, так и по терапевтическому индексу. Некоторые из этих соединений имеют заметное преимущество и перед современными, наиболее активными местноанестезирующими лекарственными препаратами. Обнаруженный ряд соединений расширит арсенал применяемых в настоящее время лекарственных средств и обеспечит новые возможности для медицинского применения и поиска новых эффективных лекарственных средств в ряду замещенных бензофуранов с целью их широкого использования как анестетиков.
Изобретение касается замещенных бензофурана, в частности гидрохлоридов 2-метил-3-ацил-4-диалкиламинометил-5-оксибензофурана общей формулы  , где X=-CH2-NR4R5·HCl: a)R1=R2=H;R3=Br.F; R4=R5=CH3;b)R1=R2=H;R3=OCH3;R4 c R5=-(CH2)5-; c)R1=R3=OCH3;R2=H;R4=R5=CH3;C2H5;d)R1=H; R2=R3=OCH3;R4=R5=CH3;C2H5; e)R1=R 2=R3=OCH3;R4=R5=CH3. обладающих местноанестезирующей активностью, что может быть использовано в медицине. Цель - создание новых более активных веществ указанного класса. Синтез ведут реакцией аминометилирования 3-ацил-5-оксибензофуранов. Выход.%: т.пл. °С, брутто - формула: а) 73,1; 230 - 232, C19H19BrClNO3; б) 65,9; 207 - 209, C19H19FClNO3 , в) 54,4 184-186, C22H26ClNO4 , г)55,9; 196 - 197, C21H24ClNO5 (моногидрат); д) 60,6; 204 - 205, C23H28ClNO5 , е) 58,5; 190 - 101; C21H24ClNO5 , ж) 62,6; 174 - 175, C23H28ClNO5 , з) 80,7 221 - 224, C22H26ClNO6 . Новые вещества активнее маркаина и лидокаина более чем в два раза по терапевтическому индексу. 3 табл.
, где X=-CH2-NR4R5·HCl: a)R1=R2=H;R3=Br.F; R4=R5=CH3;b)R1=R2=H;R3=OCH3;R4 c R5=-(CH2)5-; c)R1=R3=OCH3;R2=H;R4=R5=CH3;C2H5;d)R1=H; R2=R3=OCH3;R4=R5=CH3;C2H5; e)R1=R 2=R3=OCH3;R4=R5=CH3. обладающих местноанестезирующей активностью, что может быть использовано в медицине. Цель - создание новых более активных веществ указанного класса. Синтез ведут реакцией аминометилирования 3-ацил-5-оксибензофуранов. Выход.%: т.пл. °С, брутто - формула: а) 73,1; 230 - 232, C19H19BrClNO3; б) 65,9; 207 - 209, C19H19FClNO3 , в) 54,4 184-186, C22H26ClNO4 , г)55,9; 196 - 197, C21H24ClNO5 (моногидрат); д) 60,6; 204 - 205, C23H28ClNO5 , е) 58,5; 190 - 101; C21H24ClNO5 , ж) 62,6; 174 - 175, C23H28ClNO5 , з) 80,7 221 - 224, C22H26ClNO6 . Новые вещества активнее маркаина и лидокаина более чем в два раза по терапевтическому индексу. 3 табл.
ГИДРОХЛОРИДЫ 2-МЕТИЛ-3-АЦИЛ-4-ДИАЛКИЛАМИНОМЕТИЛ-5-ОКСИБЕНЗОФУРАНА общей формулы 1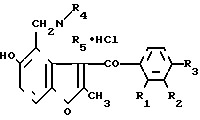
где R1 = R2 = H1R3 = Br, R4 = R5 = CH3;
R1 = R2 = H1R3 = F1R4 = R5 = CH3;
R1 = R2 = H1R3 = OCH3, R4R5 = -(CH2)5-;
R1 = R3 = OCH3R2 = H1R4 = R5 = CH3;
R1 = R3OCH3R2 = H1R4 = R5 = C2H5;
R1 = H1R2 = R3 = OCH3R4 = R5 = CH3;
R1 = H1R2 = R3 = OCH3R4 = R5 = C2H5;
или
R1 = R2 = R3 = OCH3R4 = R5 = CH3,
обладающие местноанестезирующей активностью.
| J.J | |||
| Savarese, B.G | |||
| Приспособление для изготовления в грунте бетонных свай с употреблением обсадных труб | 1915 |
|
SU1981A1 |
Авторы
Даты
1994-10-15—Публикация
1990-03-29—Подача