Изобретение относится к неописанным ранее 7-алкокси-8,9-дигидроксантилиевым солям общей формулы (I)
где R1 C1-C6 алкил;
R2 и R3 C1-C6 алкил;
R4 R5 R7 атом водорода;
R6 атом водорода или галогена, C1-C6 алкил, C1-C6 алкокси- или нитрогруппа;
R8 атом водорода или аллил;
X ClO4,
которые проявляют флуоресцентные свойства и могут быть использованы как флуоресцентные красители для крашения текстильных и нетекстильных материалов, а также в производстве чернил, карандашей, косметических препаратов, сигнальных красок, синтонов для производства флуоресцентных красителей и способу их получения.
Наиболее близкими по структуре являются производные ксантилия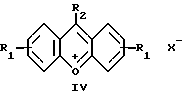
(соли дибензопирилия) общей формулы (IV) (Венкатараман К. Химия синтетических красителей, Л. т. 2, с. 820 860).
Соединения (IV) устойчивы в растворах сильных кислот, в воде гидролизуются до ксантгидролов (9-оксиксантенов) и ввиду неустойчивости не могут быть используемы как люминофоры.
Способ получения соединений (IV) заключается в пиролизе фениловых эфиров салициловой кислоты (салолов) общей формулы (V), действии на образующийся ксантон (ксантен-9-кетон)(IV) магнийорганических производных, с последующим гидролизом продуктов реакции (VII) и превращением образующихся ксантгидролов (9-оксиксантенов) (VIII) в соли ксантлия (IV).
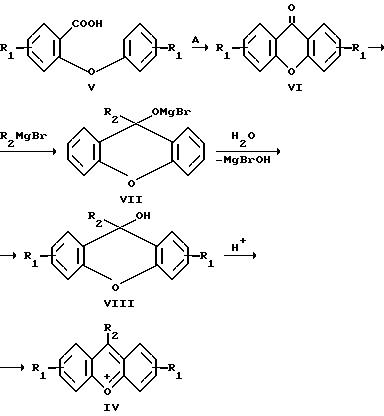
Однако данный способ многостадиен, трудоемок и не позволяет получить соединения общей формулы (I).
Техническим результатом изобретения являются новые производные в ряду 8,9-дигидроксантилиевых солей общей формулы (I), проявляющие флуоресцентные свойства (новое свойство для данного ряда), устойчивые в кислых и нейтральных средах, а также способ их получения.
Технический результат достигается соединениями формулы (I) и способом их получения.
Способ получения формулы (I) заключается в том, что соли 5,5-R2,R3-1,3-диалкокси-1-R4-циклогексения общей формулы (II) (Олехнович Е.П. Коробка И.В. //ЖОрХ. 1990, т. 26. Вып. 1. с.213 214.), где R1 R4 имеют вышеприведенные значения, вводят во взаимодействие с о-гидроксиаральдегидами общей формулы (III), где R5 - R8 имеют вышеприведенные значения в присутствии триалкилортоформиата. Последний используется в избытке, достаточном для поглощения воды, выделяющейся в результате реакции, и одновременно как растворитель для проведения реакции в гомогенной среде.

Соединения (I), а также способ их получения обладают изобретательским уровнем, так как наличие высоких флуоресцентных характеристик у соединений (I), их новизна, а также возможность их получения в присутствии триалкилортоформиатов в столь мягких условиях являются неочевидными.
Ранее не было изучено действие салициловых альдегидов (III) на соли 5,5-R2, R3-1,3-диалкокси-1-R4-циклогексения (II) в среде триалкилортоформиатов.
Известно, что при действии на салициловые альдегиды (III) 4,6-диметил-2H-1,3,2-оксаоксониоборатов (IX) в 1,2-дихлорэтане с последующей обработкой хлорной кислотой в уксусной кислоте образуются перхлораты 2-[(2H-1-бензопиран-2-илиден)-метил] -1-бензопирилия (XI) (DD. P. 265622 (1987), TH Merseburg, Erf. R.Dusi u H.Hartman; C.A. 111. 214390 (1989)).

Действие салициловых альдегидов (III) на 1,3,2-оксаоксониабораты циклических 1,3-дикетонов неизвестно.
Изучено действие натриевых солей салициловых альдегидов (XII) на натриевые соли 2-метилдимедонов (XIII) в гексамтаполе, и последующей обработке продуктов реакции хлорной кислотой с образованием 6,13,13-триметилл-13Н-(дибензо[b; e] пирано)-[3,2-b] -1-бензопирилиевых перхлоратов (XIV) (DOS 2942931 (1980), BASF, Erf. R.Schmidt u V.Koch; C.A. 95. 117065 (1980)).

Взаимодействие соединений (XII) и (XIII) в триалкилортоформинатах неизвестно.
Известно, что при действии салициловых альдегидов (III) на ациклические 1,3-дикетоны (например ацетилацетон (XV) в присутствии смеси хлорной и соляной кислот образуются перхлораты 3-ацетил-2-метил-1-бензопирилия (XVI), а при избытке салициловых альдегидов (III) образуются перхлораты 3-ацетил-2-[2-(2-гидроксифенил)-этинил] -1-бензопирилия (XVII) (A.Lowenbein u W.Katz, Ber. Dtsch. Chem. Ges. 59. 1377 (1926).

Действие салициловых альдегидов (III) на 1,3-дикетоны в присутствии триалкилортоформиатов неизвестно.
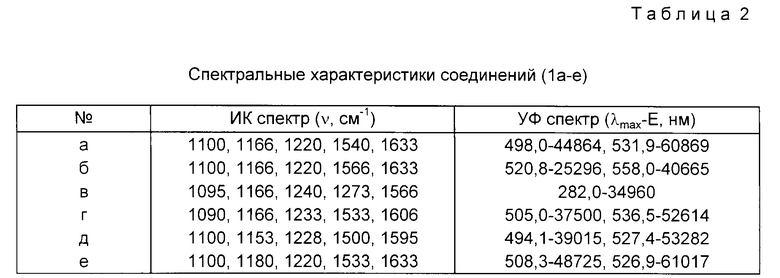
Ниже приведены примеры получения соединений (Ia-e), их константы (R1-R8, выходы, температуры плавления, элементный анализ и спектральные характеристики приведены в табл. 1,2. УФ спектры соединений измерены на спектрофотометре Specord M-40 в ацетонитриле, ИК спектры соединений получены на спектрометре Specord IR-71 в вазелиновом масле, а ПМР спектры соединений получены на спектрометре Varian VXR-300 (300 МГц) в дейтероацетонитриле.
Пример 1. Получение перхлората 7-этокси-9,9-диметил-8,9-дигидроксантилия (Ia).
2,96 г (0,01 моль) перхлората 5,5-диметил-1,3-диэтокси-1-циклогексения (II) и 1,25 г (0,01 моль) салицилового альдегида (III) в 20 мл триэтилортоформиата нагревают до начала кипения (70 80oC) и кипятят 5 мин. Охлаждают, выделившиеся кристаллы отфильтровывают, промывают этилацетатом (2 раза по 10 мл) и эфиром (2 раза по 10 мл) и перекристаллизовывают из уксусной кислоты.
Выход: 62,8% т.пл. 207 210oC.
Пример 2. Получение перхлората 2-метокси-7-этокси-9,9-диметил-8-9-дигидроксантилия (Iб).
2,96 г (0,01 моль) перхлората 5,5-диметил-1,3-диэтокси-1-циклогексения (II) и 1,25 г (0,01 моль) п-метоксисалицилового альдегида (IIIб) в 20 мл триэтилортоформиата нагревают до начала кипения (70 80oC) и кипятят 5 мин. Охлаждают, выделившиеся кристаллы отфильтровывают, промывают этилацетатом (2 раза по 10 мл) и эфиром (2 раза по 10 мл) и перекристаллизовывают из уксусной кислоты.
Выход: 2,7 г (69,5%), т.пл. 194 195oC.
ИК спектр (v, см): 1100, 1166, 1220, 1246, 1566, 1633.
Спектр ПМР (δ м. д. ): 1.50т(9H), 2.78c(2H), 3.92c(3H), 4.40к(2H), 6.41c(1H), 7.38д(1Н), 7.58с(1Н), 7.70д(1Н), 8.72с(1Н).
Найдено, C 56.11; H 5.43; Cl 9.30. СHCl10. Вычислено, C 56.18; H 5.50; Cl 9.21.
Растворы соединений (Ia,б) в полярных и неполярных растворителях обладают интенсивной красной флуоресценцией и фотохимически стабилны.
Пример 3. Получение перхлората 4-аллил-7-этокси-9,9-диметил-8,9-дигидроксантилия (Iв).
2,96 г (0,01 моль) соединения (II) и 1,6 г (0,01 моль) о-аллилсалицилового альдегида (IIIв) в 20 мл триэтилортоформиата перемешивают при температуре 18 25oC 1,5 ч. Желтые кристаллы отфильтровывают, промывают эфиром. Очищают переосаждением из нитрометана эфиром.
Выход: 2,25 г (57,1%), т.пл. 108 110oC.
Соединение гигроскопично, для длительного хранения помещают в эксикатор над пятиокисью фосфора.
Раствор соединения (Iв) в полярных и неполярных растворителях обладает интенсивной фиолетовой флуоресценцией и фотохимически стабилен.
Пример 4. Получение перхлората 2-бром-7-этокси-9,9-диметил-8,9-дигидроксантилия (Iб).
2,96 г (0,01 моль) перхлората 5,5-диметил-1,3-диэтокси-1-циклогексения (II) и 2,0 г (0,01 моль) п-бромсалицилового альдегида (III) в 20 мл триэтилортоформиата нагревают до начала кипения (70 80oC) и кипятят 5 мин. Охлаждают, выделившиеся кристаллы отфильтровывают, промывают этилацетатом (2 раза по 10 мл) и эфиром (2 раза по 10 мл) и перекристаллизовывают из уксусной кислоты.
Выход: 64,0% т.пл. 238 240oC.
Представленные в табл. I соединения (Iд,е) получены аналогично соединениям (Ia-г). (Примеры 1 -4).
Все описанные соединения (Ia-е) устойчивы, получены одностадийно и с высоким (55 70%) выходом. Они растворимы в спирте, водном спирте, хлороформе, нитрометане, ацетонитриле и других растворителях. Растворы соединений (Iа, б,г-е) обладают интенсивной оранжево-красной флуоресценцией, а растворы соединения (Iв) фиолетовой флуоресценцией.
Ниже приведен пример использования 7-алкокси-8,9-дигидроксантилиевых солей (I) в качестве синтонов при простом одностадийном синтезе труднодоступного ранее перхлората 2,10-диметокси-6Н-13,13-диметил(дибензо[b, e]пирано)[3,2-b]-1- бензопирилия (XXa, R H) представителя нового класса высокоперспективных флуоресцентных красителей (DOS 2942931, 1980, BASF, Erf. R.Schmidt, V.Koch; C.A. 95, 117065 (1980)) (Пример 5).

Пример 5. Получение перхлората 2,10-диметокси-6Н-13,13-диметил(дибензо[b;e]пирано)[3,2-b]-1- бензопирилия (XXa).
Реакционную смесь в соотношении 3,84 г (0,01 моль) перхлората 2-метокси-7-этокси-9,9-диметил-8,9-дигидроксантилия (Ia), 20 мл триэтилортоформиата и 1,5 г (0,01 моль) п-метоксисалицилового альдегида нагревают до начала кипения (60oC) и кипятят 1 ч. Охлаждают, выделившиеся кристаллы отфильтровывают, промывают на фильтре этилацетатом (2 раза по 5 мл) и эфиром (2 раза по 5 мл).
Выход: 2,75 г (58,5%), т.пл. 303 305oС (из лед. CH3COOH).
ИК спектр ( ν см-1): 1100, 1166, 1240, 1500, 1620;
Спектр ПМР ( d м. д. ): 1.90c(6H), 3.98c(6H), 6.79c(1H), 7.45к(4Н), 7.73д(2Н), 8.52с(2Н).
Найдено, C 60.91; H 4.40; Cl 7.64. C24H21ClO8. Вычислено, C 60.96; H 4.48; Cl 7.50.
Таким образом соединения (I) являются новыми производными в ряду солей 8,9-дигидроксантилия, получаются из доступных исходных веществ простым, одностадийным, предлагаемым способом, могут быть использованы как синтоны в органическом синтезе и? в частности в синтезе флуоресцентных красителей. Соединения (I) стабильны и обладают достаточно высокими флуоресцентными характеристиками, достаточными для возможности самостоятельного использования этих соединений в качестве флуоресцентных красителей и люминофоров. Данные люминофоры обладают высокой фотохимической стабильностью и могут использоваться в качестве красителей для пластмасс и синтетических волокон (поливинилхлорида, поливенилендихлорида, полиакрилонитриала). Растворы люминофоров в ацетонитриле могут быть применены как активные среды в жидкостных лазерах при различных способах возбуждения. Соединение (Iв), являясь аллильным производным, способно к фото- и электрополимеризации и сополимеризации, что делает возможным синтез на его основе полимерных люминофоров.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДИБЕНЗО (В,Е)ПИРАНО(3,2-В)-1-БЕНЗОПИРИЛИЕВЫХ СОЛЕЙ | 1995 |
|
RU2082715C1 |
| ДИБЕНЗО(В,Е) ПИРАНО(3,2-В)-1-БЕНЗОПИРИЛИЕВЫЕ СОЛИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1995 |
|
RU2084455C1 |
| ПРОИЗВОДНЫЕ 8,9-ДИГИДРОКСАНТЕНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1996 |
|
RU2106350C1 |
| ПЕРХЛОРАТЫ ДИФЕНИЛЭТОКСИПОЛИМЕТИНЦИАНИНОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1995 |
|
RU2087459C1 |
| 2,8-ДИМЕТИЛ-3,7-ДИАЛКОКСИ-5-R -ФУРО [C,B] ТРОПИЛИЕВЫЕ СОЛИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1996 |
|
RU2103267C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОЛЕЙ 1,3-ДИМЕТИЛ-4,8-ДИАЛКОКСИ-6-R-ПИРРОЛО-(ТИЕНО)-[C] ТРОПИЛИЯ | 1997 |
|
RU2131871C1 |
| ДИГИДРОХЛОРИД 1-(2-ТРЕТ-БУТИЛАМИНОЭТИЛ)-2-ТРЕТ-БУТИЛИМИДАЗО [1,2-А]-БЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЙ МЕСТНОАНЕСТЕЗИРУЮЩИМ ДЕЙСТВИЕМ | 2000 |
|
RU2160263C1 |
| 3-ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ 3Н-2,3-БЕНЗОДИАЗЕПИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2146678C1 |
| Перхлораты 2,4-дифенил-8-(4 @ -нитро-3 @ -R-фениламинометилиден)-5,6,7,8-тетрагидрохромилия в качестве реагента для обнаружения анионных синтетических поверхностно-активных веществ в водах | 1988 |
|
SU1565840A1 |
| ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1987 |
|
RU2062778C1 |

Изобретение относится к соединению общей формулы (I) ,
,
где R1 - C1-C6 алкил; R2 и R3 - C1-C6 алкил; R4 = R5 = R7 = атом водорода; R6 - атом водорода или галогена, C1-C6 алкил, C1-C6 алкокси- или нитрогруппа; R8 - атом водорода или аллил; X = ClO4, обладают высокими спектральными характеристиками, высокой фотохимической стабильностью, устойчивы в полярных и неполярных растворителях и могут быть использованы как флуоресцентные красители для крашения различных текстильных и нетекстильных материалов в производстве чернил, карандашей, косметических препаратов, сигнальных красок, синтонов для производства флуоресцентных красителей, как активные среды в жидкостных лазерах при различных способах возбуждения и др. Способ получения соединений (I) заключается в том, что соли 5,5-R2, R3-1,3-диалкокси-1-R4 -циклогексения вводят во взаимодействие с о-гидроксиаральдегидами в присутствии триалкилортоформиатов. Даны: N, R1, R2, R3, R4, R5, R6, R7, R8, выход (%), т.пл.(oС), УФ спектр ( λmax- E, нм): Ia,C2H5,CH3, CH3, H,H,H,H,H,62.8, 207 - 208,498.0-44864,531.9-60869; Iб,C2H5,CH3,CH3,H,H, CH3O, H, H, 69.5,194-195,520.8-25296,558.0-40665; Iв, C2H5,CH3,CH3,H,H,H,H, CH2CH= CH2,57.1,108-110,282.0-34960; Iг,C2H5,CH3,CH3,H,H,Br,H,H, 64.0,238-240,505.0-37500,536.5-52614; Iд, C2H5, CH3, CH3, H, H, NO2,H,H, 73.5,247-245,494.1-39015,527.4-53282; Iе, C2H5, CH3, CH3, H, H, CH3,H,H, 65.0,201-203,508.3-48725,526.9-61017. 2 с. п.ф-лы, 2 табл.

где R1 C1 C6-алкил;
R2 и R3 C1 C6-алкил;
R4 R5 R7 водород;
R6 водород или галоген, С1 С6-алкил, С1 - С6-алкокси- или нитрогруппа;
R8 водород или аллил;
X ClO4.
где R1 C1 C6-алкил;
R2 и R3 C1 C6-алкил;
R4 R5 R7 водород;
R6 водород или галоген, С1 С6-алкил, С1 - С6-алкокси- или нитрогруппа;
R8 водород или аллил;
X ClO4,
отличающийся тем, что соли 5,5-R2, R3-1,3-диалкокси-1-R4-циклогексения общей формулы II
вводят во взаимодействие с о-гидроксиаральдегидами общей формулы III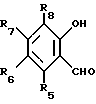
где R1 R8 имеют указанные значения,
в присутствии триалкилортоформиатов.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Олехнович Е.П | |||
| и др., ЖОрХ, 1990, т | |||
| Прибор для получения стереоскопических впечатлений от двух изображений различного масштаба | 1917 |
|
SU26A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Кулиса для фотографических трансформаторов и увеличительных аппаратов | 1921 |
|
SU213A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| DE, патент, 2942931, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| A | |||
| Lowenbein et al, Ber | |||
| Stsch., 1926, 59 | |||
| v | |||
| Способ переработки сложных природных солей щелочных металлов | 1924 |
|
SU1377A1 |
Авторы
Даты
1997-12-27—Публикация
1996-01-16—Подача