Изобретение относится к способам сорбционного извлечения цветных металлов и может быть использовано при сорбционном извлечении их из растворов сложного состава с различным солесодержанием, например морской воды и рассолов.
Известные способы извлечения цветных металлов из солевого раствора (морской воды) осуществляют путем сорбции их на ионитах различного класса: катионитах, анионитах, амфолитах, хелатных сорбентах. Наиболее перспективными для извлечения цветных металлов из морской воды являются полиамфолиты и хелатные сорбенты, коэффициенты распределения их на этих сорбентах достигают величины выше 105.
Однако трудность десорбции цветных металлов с них и отсутствие промышленного выпуска ограничивает применение этих сорбентов в рамках концентрирования цветных металлов с помощью аналитического определения. Селективные катиониты не нашли широкого применения для извлечения цветных металлов из морской воды.
Наиболее близким техническим решением к предлагаемому является способ сорбционного извлечения цветных металлов из солевых растворов сложного состава, заключающийся в пропускании исходного раствора через низкоосновный анионит АН- 31с последующей десорбцией цветных металлов разбавленным 0,5 М раствором соляной кислоты.
VJ
со
00
VI ел о
Способ позволяет извлекать цветные и другие ценные металлы из морской воды на установках различного типа. Способ позволяет достигнуть степени концентрирования а ( а является отношением концентрации металла в регенерационном растворе к его содержанию в исходной воде) по меди, никелю и цинку, равных соответственно 10 , 4- 102, 1,5- 102. Величина коэффициента распределения по меди составляет 3,6 10 мл/г.
Недостатком известного способа являются низкие величины сорбированных металлов и низкая концентрация их в регенерационном растворе. Так, концентрация меди в ионите равна 4,9 мг/л, а в регенерационном растворе - 0,4 мг/л. Таким образом, несмотря на достаточно высокую селективность ионита и степень концентрирования металлов, метод практически неприменим к задаче извлечения цветных металлов, требуется дальнейшее концентрирование.
Целью изобретения является повышение степени извлечения цветных металлов.
Указанная цель достигается тем, что согласно способу сорбционного извлечения цветных металлов из солевых раствор сложного состава, заключащемуся в пропускании исходного раствора через низкоосновный анионит с последующей десорбцией цветных металлов разбавленным раствором кислоты, в качестве низкоосновного анионита используют анионит эпокси- аминного типа, с периодической обработкой последнего раствором щелочи 0,1-1,0 М в объеме 3-10 уд.об.. Причем, обработку анионита проводят после насыщения его бором.
Использование концентрации щелочи ниже 0,1 М неэффективно, так как это приводит к увеличению времени перевода сорбента в гидроксил ьную форму, необходимую для дальнейшего проведения процесса сорбции цветных металлов, а кроме того, затруднена десорбция бора.
Применение раствора щелочи концентрации выше 1 М приводит к необоснованным затратам реагента.
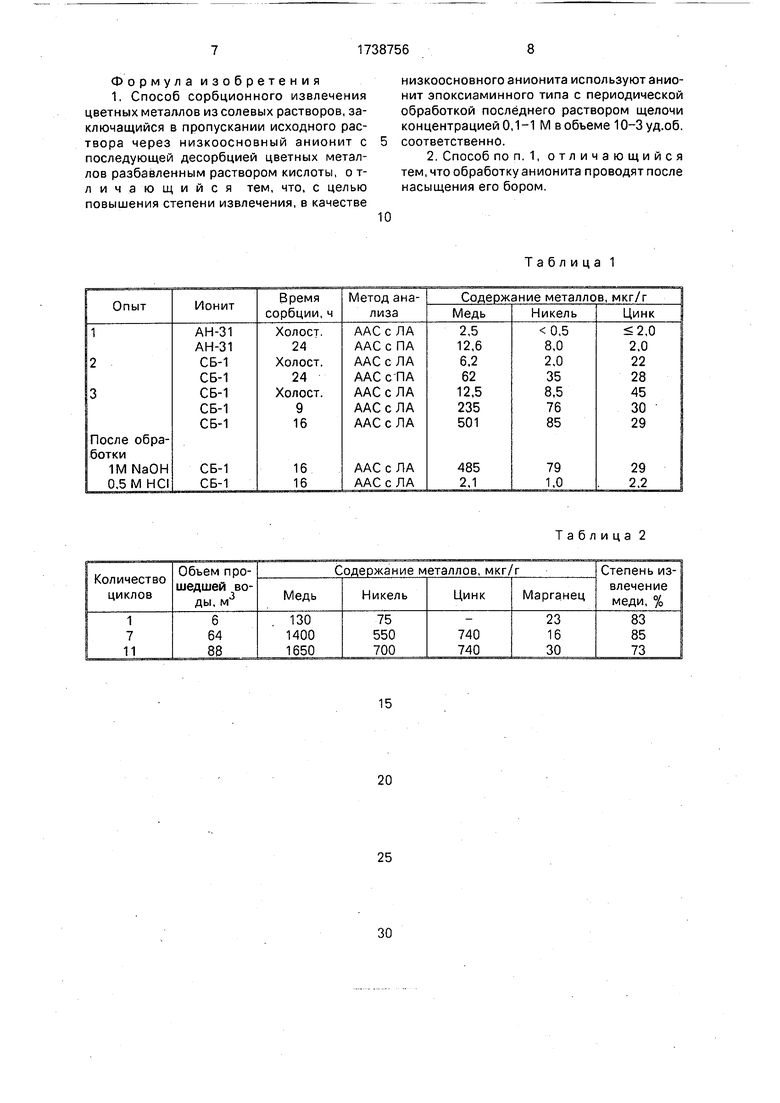
На фиг. 1 представлена зависимость сорбированного количества металла от пропущенного объема воды (а - сорбция, мкг/г; V - объем воды, м ; - медь; х - никель); на фиг. 2 - зависимость рН воды на выходе из колонны от времени сорбции, т; на фиг. 3 - кривые десорбции металлов с анионита СБ- 1 0,5 М раствором соляной кислоты (с - концентрация, мг/л, q - удельный объем соляной кислоты;-- медь; ч - никель).
Анионит СБ-1 синтезирован в форме сферических частиц гелевой структуры, обладающих удовлетворительной термической устойчивостью и химической
стойкостью. Анионит содержит аминогруппы всех основностей, а кроме того, он содержит аминооксиэтильные группировки, селективные к бору (ранее анионит СБ-1 использовался для извлечения бора из мор0 с кой воды).
При изучении сорбционных свойств СБ- 1 обнаружено, что попутно с бором происходит сорбция цветных металлов, причем от цикла к циклу происходит их накопление.
5 Так, за один цикл сорбируется 130, а за одинадцать- 1650 мкг/г меди, что составляет соответственно 0,06 и 0,7% от величины полной обменнной емкости анионита. Накопление за 11 циклов количество меди
0 (1650 мкг/г) соответствует величине коэффициента распределения, равной 2,4- 10 мл/г при концентрации меди в морской воде 7 мкг/л и, (фиг. 1) не является предельным: зависимость сорбционного количества
5 от объема пропущенной воды представляет прямую линию. Эта величина сопоставима с коэффициентами распределения меди, полученными для высокоселективтных волокнистых ионитов Полиоргс XII и Мтилон-Т.
0 Однако десорбция цветных металлов с этих сорбентов затруднена.
Большие количества меди, сорбируемые анионитом в указанном режиме с периодической обработкой гидроксидом натрия,
5 обусловлены спецификой процесса сорбции цветных металлов в щелочных средах. После десорбции бора 0,1 М раствором NaOH рН воды на выходе из колонны повышается до 8,5 и превышает рН морской во0 ды, равный 8,25, в течение всего цикла сорбции бора (фиг. 2). В указанных условиях сорбция металлов осуществляется преимущественно за счет образования в фазе сорбента гидроксокомплексов типа (Cu(NH2)
5 (ОНз) и гидроксидов металлов.
Полная десорбция цветных металлов с СБ-1 осуществляется раствором 0,5 М соляной кислоты. При обработке ионита 0,1-1,0 М раствором NaOH в раствор переходит не
0 более 5% сорбированных цветных металлов.
Предлагаемый способ извлечения цветных металлов анионитом СБ-1 в гидроксиль- ной форме может быть осуществлен как в
5 статических, так и динамических условиях, Пример 1. Опыт по сорбции проводят в статических условиях из модельного раствора морской воды с концентрацией меди 15 мг/л и рН исходного раствора, равным 6. Сорбцию меди проводят при постоянном
перемешивании 0,1 г измельченного ионита с 200 мл раствора в течение 24 ч. Затем сорбент отделяют от раствора, промывают 10 мл 0,1 М раствора гидроксида натрия (элюирование бора), 5 мл дистиллированной воды. В следующем цикле сорбции ионит заливают новой порцией раствора. Процесс сорбции с последующей обработкой ионита раствором NaOH повторяют многократно. В контрольном опыте после сорбции ионит СБ-1 гидроксидом натрия не обрабатывают. Содержание меди в растворе определяют методом атомно-абсорбционной спектрометрии с пламенной атомизацией (ААС с ПА). Содержание меди в ионите рассчитывают по разности концентраций меди в исходном и равновесном растворах. После пяти циклов сорбции содержание меди в ионите составляет 148 мг/г (64% полной обменной емкости). При периодической обработке анионита 0,1 М раствором гидроксида натрия происходит полное извлечение меди анионитом из модельного раствора морской воды. После трех циклов сорбции содержание меди в ионите в контрольном опыте 70 мг/г (30% полной обменной емкости), после четвертого цикла 72 мг/г, т.е. после трех циклов емкость ионита увеличивается незначительно.
Пример 2. Опыты по сорбции цветных металлов из натурной морской воды проводят в динамических условиях на колонне сечением 63 см (навеска 25-50 г, высота слоя 1,5-2 см, расход морской воды 0,5 м3/ч).
Условия проведения опытов и результаты сорбции цветных металлолов приведены в табл. 1: в опытах 1 и 2, проведенных на имитате морской воды, приготовленном разбавлением рапы, сорбцию осуществляют на анионитах СБ-1 и АН-31; в опыте 3 сорбция металлов осуществлялась анионитом СБ-1 из океанской воды. Содержание металлов в ионите определяют методом атомно-абсорбционной спектрометрии с лазерной атомизацией ААС с ЛА, а также рассчитывали по данным десорбции металлов 0,5 н.раствором соляной кислоты с использованием метода ААС с ПА.
Из данных табл. 1 видно, что на аниони- те СБ-1 получена более высокая концентрация цветных металлов, чем на АН-31, при идентичных условиях проведения опыта. Особенно высокие содержания цветных металлов получены в пробах СБ-1, отработанных на океанской воде (опыт 3), что связано с более высокой концентрацией цветных металлов, в частности меди, в воде 7,3 мкг/л, по сравнению с концентрацией в воде Черного моря 2 мкг/л. Степень извлечения меди в опыте 3 составляет 40%.
Из табл. 1 видно, что при обработке отработанного ионита 1 М раствором NaOH
концентрация цветных металлов в ионите уменьшается не более чем на 5%, а при обработке той же пробы ионита 0,5 М раствором соляной кислоты происходит десорбция цветных металлов до уровня
содержания их в холостой пробе.
Пример 3. Сорбцию цветных металлов из океанской воды проводят на колонне сечением 120 см2 (объем ионита 1,35 л, высота слоя 11 см, расход морской воды 0,5
м3/ч, время сорбции 8-10 ч). После сорбции ионит промывают 2 л водопроводной воды, затем обрабатывают для десорбции бора 15 л 0,1 М раствора гидроксида натрия. При этом анионит переходит в гидроксильную
форму (контроль осуществляется титрованием раствора щелочи). Перед каждым новым циклом сорбции ионит отмывают от взвеси и взрыхляют противотоком морской воды. После нескольких циклов отбирают с
помощью противотока пробу ионита для анализа. Содержание металлов в сорбенте определяют методом ААС с ЛА. Результаты приведены в табл. 2 (масса ионита 280 г).
Как видно из табл. 2, проведение процесса извлечения металлов в динамических условиях с промежуточной обработкой анионита 0,1 М раствором гидроксида натрия способствует накоплению цветных метал-.
лов в ионите. С увеличением числа циклов растет количество сорбированных металлов, степень извлечения меди при этом составляет 85-73%. В тоже время накопления марганца практически не происходит. Такое
различие в сорбции металлов можно объяснить другим механизмом сорбции марганца, для которого рН осаждения гидроокиси (рН 9) значительно выше, чем цветных металлов (рН 5-7,5). Десорбцию цветных металлов с анионита осуществляют 12 л 0,5 М раствора соляной кислоты, при скорости ее течения 3 л/ч. После 8 циклов концентрация никеля и меди в элюате достигает соответственно 30 и 60 мг/л (фиг. 3). Степень концентрирования меди при этом составляет 8,5- 103.
Таким образом, предлагаемый способ позволяет получить высокие величины емкости цветных металлов при извлечении их
из растворов типа морской воды за счет применения анионита СБ-1 в гидроксиль- ной форме с обработкой его 0,1 М раствором гидроксида натрия между сорбционными циклами.
Формула изобретения 1. Способ сорбционного извлечения цветных металлов из солевых растворов, за- ключащийся в пропускании исходного раствора через низкоосновный анионит с последующей десорбцией цветных металлов разбавленным раствором кислоты, о т- личающийся тем, что, с целью повышения степени извлечения, в качестве
низкоосновного анионита используют анионит эпоксиаминного типа с периодической обработкой последнего раствором щелочи концентрацией 0,1-1 М в объеме 10-Зуд.об. соответственно.
2. Способ по п. 1, отличающийся тем, что обработку анионита проводят после насыщения его бором.


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВЫДЕЛЕНИЯ ИОНОВ $$$ ИЗ ТЕХНОЛОГИЧЕСКИХ РАСТВОРОВ | 2004 |
|
RU2259952C1 |
| СПОСОБ РАЗДЕЛЕНИЯ ПЛАТИНЫ (II, IV), МЕДИ (II) И ЦИНКА (II) В СОЛЯНОКИСЛЫХ РАСТВОРАХ | 2016 |
|
RU2637547C1 |
| СПОСОБ ОТДЕЛЕНИЯ ПЛАТИНЫ (II, IV) И ПАЛЛАДИЯ (II) ОТ СЕРЕБРА (I), ЖЕЛЕЗА (III) И МЕДИ (II) В СОЛЯНОКИСЛЫХ РАСТВОРАХ | 2019 |
|
RU2694855C1 |
| Способ очистки растворов электролитов от серной кислоты | 1981 |
|
SU982784A1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ БЛАГОРОДНЫХ МЕТАЛЛОВ | 1992 |
|
RU2006506C1 |
| СПОСОБ РАЗДЕЛЕНИЯ ПЛАТИНЫ (II, IV) И ЖЕЛЕЗА (III) В СОЛЯНОКИСЛЫХ РАСТВОРАХ | 2015 |
|
RU2610185C2 |
| СПОСОБ ОЧИСТКИ РАСТВОРОВ ЭЛЕКТРОЛИТОВ ОТ СЕРНОЙ КИСЛОТЫ | 1999 |
|
RU2152256C1 |
| СПОСОБ РАЗДЕЛЕНИЯ РЕНИЯ И МОЛИБДЕНА ПРИ ПОМОЩИ НИЗКООСНОВНОГО АНИОНИТА ПОРИСТОЙ СТРУКТУРЫ | 1996 |
|
RU2096333C1 |
| СПОСОБ ПЕРЕРАБОТКИ СКАНДИЙСОДЕРЖАЩИХ РАСТВОРОВ | 2001 |
|
RU2196184C2 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ГАЛЛИЯ ИЗ ЩЕЛОЧНЫХ РАСТВОРОВ | 1991 |
|
RU2051113C1 |
Изобретение относится к способам сорбционного извлечения цветных металлов из растворов сложного состава с различным солесодержанием, например морской воды и рассолов, и позволяет повысить степень извлечения. Способ сорбционного извлечения цветных металлов из солевых растворов сложного состава заключается в пропускании исходного раствора через низкоосновный анионит с последующей десорбцией цветных металлов разбавленным раствором кислоты, при этом в качестве низкоосновного анионита используют анионит эпоксиаминного типа, с периодической обработкой последнего раствором щелочи 0,1-1 М в объеме 10-3 уд об. соответственно. Обработку анионита проводят после насыщения его бором. 1 з п. ф-лы, 3 ил., 2 табл. СО с
Таблица 1
Таблица 2
о. ttt
ISM
30
в
10 Фиг. 2
t 20
С ВО
ЬО 20
х/
1I
50
245 В #
Фиг.З
| Сенявин М | |||
| М., Сорочан А | |||
| М | |||
| Бордов- ский О | |||
| К | |||
| и др | |||
| Методы сорбционного извлечения металлов из океанских вод | |||
| - В кн | |||
| Биогидрохимия Северо-Западной части Индийского океана | |||
| - М : Наука, 1981, с | |||
| Способ образования азокрасителей на волокнах | 1918 |
|
SU152A1 |
Авторы
Даты
1992-06-07—Публикация
1990-08-31—Подача