Изобретение относится к способу управления процессом твердофазного . синтеза биополимеров на нежестких полимерных носителях и может найти широкое применение в химических, биологических, медицинских исследованиях, а также в промышленном производстве биологически активных веществ.
Целью изобретения является повьг шение производительности процесса.
Способ управления процессом твердофазного синтеза биополимеров основан на свойстве полимера носителя изменять свой объем (набухать) в процессе протекания операций синтеза. В зависимости от физико-химических свойств носителя, характеризующихся его прирог
дои, числовым порядком операций и стадий, химическим составом растущей биополимерной цепи, объем носителя изменяется в 1,05-9 и более раз
Способ управления процессом твердофазного синтеза биополимеров поясняется с помощью фиг. 1 и 2.
Нэ фиг. 1 показаны: кривая а - график изменения объема полимера носителя - хлорметилирова иного полиъти рола с 2&-ной сшивкой дивинилбензола на отдельных операциях синтеза - промывках хлористым метиленом, метанолом, ди мет илф орма мидом;
кривая б - определение приращения объема носителя, например, путем диф/г
kj
Ј 4
О 00
sj
ференцированил информационного сигнала (кривой а);
кривая в - задержка выполнения следующей операции на время, необходимое для завершения текущей (выработка сигнала задержки операции);
кривая г - переход к выполнению следующей операции или выработка сиг.Ьок Val 0(p) в ДМФА
50% CF СООН в CHtCb
нала завершения предыдущей операции и начала следующей.
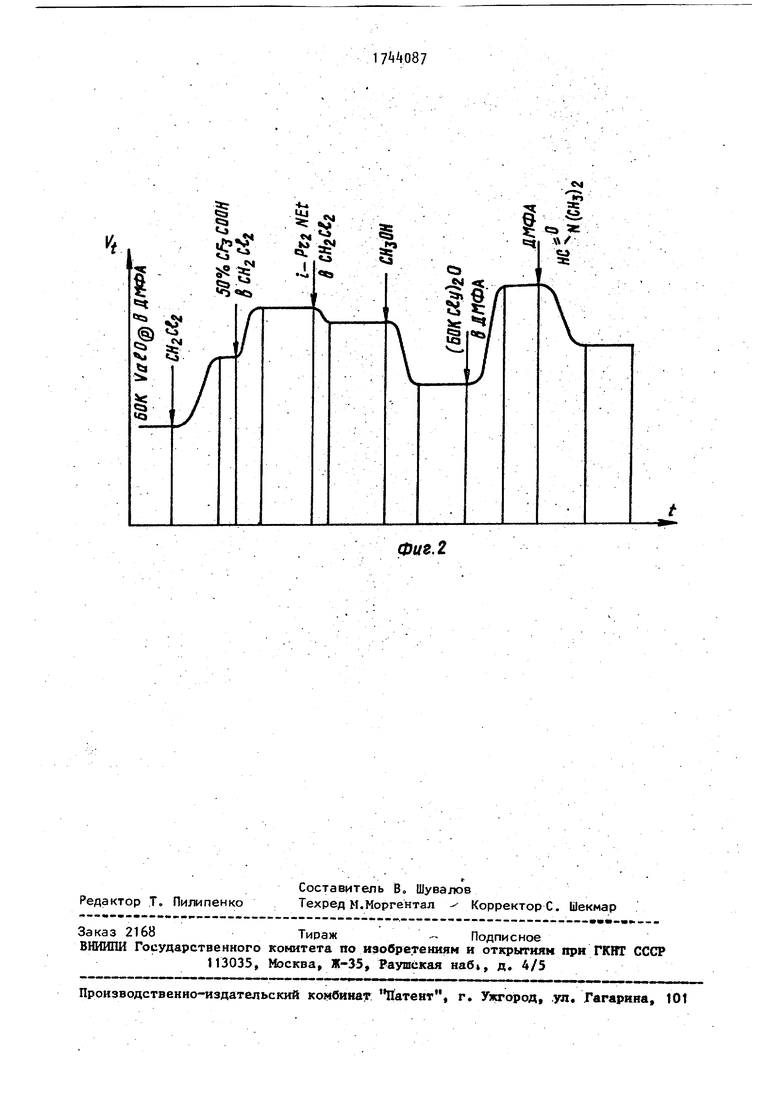
На фиг. 2 показано изменение объема носителя, которое характеризует динамику наращивания пептидной цепи на полимере носителе полистироле с 1% дивинилбензола (реакция сигнала пептида
Val-Qg) 10% JPr-aNEt CF3COOeв СН2С12



| название | год | авторы | номер документа |
|---|---|---|---|
| Синтезатор биополимеров | 1989 |
|
SU1787988A1 |
| Проточный реактор для твердофазного синтеза биополимеров | 1986 |
|
SU1650240A1 |
| Синтезатор биополимеров | 1989 |
|
SU1787989A1 |
| ДЕКАПЕПТИД, ОБЛАДАЮЩИЙ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 1993 |
|
RU2084458C1 |
| СПОСОБ СИНТЕЗА ТЕРАПЕВТИЧЕСКИХ ПЕПТИДОВ | 2012 |
|
RU2625793C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕПТИДА ЭКСЕНАТИДА | 2011 |
|
RU2458066C1 |
| АВТОМАТИЗИРОВАННАЯ РЕАКТОРНАЯ СИСТЕМА ДЛЯ СИНТЕЗА С КОНТУРОМ РЕЦИРКУЛЯЦИИ | 2018 |
|
RU2771746C1 |
| СПОСОБ НАПРАВЛЕННОГО ТРАНСПОРТА ФАРМАКОЛОГИЧЕСКИХ ПРЕПАРАТОВ ПУТЕМ ИХ КОНЪЮГАЦИИ С АРГИНИЛ-ГЛИЦИЛ-АСПАРТИЛ (RGD) СОДЕРЖАЩИМИ ПЕПТИДАМИ | 1996 |
|
RU2119354C1 |
| Способ определения содержания свободных аминогрупп в пептидил-полимере при твердофазном синтезе пептидов | 1981 |
|
SU1084271A1 |
| НЕУПОРЯДОЧЕННАЯ БИБЛИОТЕКА ПЕПТИДОВ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СПОСОБ ИДЕНТИФИКАЦИИ ПЕПТИДА, СИНТЕЗИРОВАННОГО ТВЕРДОФАЗНЫМ СИНТЕЗОМ | 1991 |
|
RU2145233C1 |
Изобретение относится к способу управления процессом твердофазного синтеза биополимеров на Нежестких полимерных носителях и может быть использовано в производстве биологически активных веществ. Оно позволит увеличить производительность процесса не менее чем в два раза. Способ заключается в том, что на каждой операции в процессе твердофазного синтеза непрерывно измеряют объем носителя, определяют его приращение и при значении приращения равном нулю задерживают выполнение следующей операции на заданное время, после чего переходят к выполнению следующей операции. 2 ил. 1 табл. (Л
,
(Ьок Gly)20 в ДМФА
Координаты графиков: по оси ординат VI- объем носителя; м - масса носителя; i, u - сила тока и напряжения;, по оси абсцис t время.
Способ управления осуществляется следующим образом. В реактор в необходимой последовательности подают компоненты синтеза. При их поступлении изменяется объем носителя в зависимости от конкретной операции и это изменение непрерывно регистрируют на каждой операции синтеза,- как показано на фиг. 1а, 2.
Изменение объема носителя при операциях синтеза - промывка (фиг,1а):
I- хлористым метиленом
IIи IV - метанолом СНзОН;
III- диметилформамидом HCON(CH)2
Изменение объема носителя при операциях наращивания пептидной цепи (фиг, 2):
I- промывка хлористым метиленом;
II-деблокирование 50Ј трифторук- сусной кислотой CF3COOH в хлористом метилене;
III- нейтрализация этилдиизопро- пиламином i-Pr2N t)
IV- промывка метанолом CHjOH;
V- конденсация трет-бутилоксикар- бонилглицина (Бок Gly)20 в диметил- формадмде (ДМФА) HCON(CH3)25
IV - промывка диметилформамидом
На участках графика (фиг. 1а) показано: 1-2 - сухой носитель; 2-3, 6-7 увеличение объема носителя; , 8-9 уменьшение объема носителя.
На участках графика (фиг. 1 а) показано: 1-2 - сухой носитель; 2-3, 6-7 - увеличение объема носителя; 4-5, 8-9 - уменьшение объема носителя
На участках графика (фиг. 2) показано: 1-2 - присутствие в реакторе frpeT-бутилоксикарбонилвалина Ьок Valp
0|
5
на полимере - носителе; 2-3, 4-5, ь-7, 8-9, 10-11, 11-12 - течение операций (по изменению объема носителя).
Зная изменение объема носителя, непрерывно определяют его приращение, например, дифференцированием сигнала (фиг. 1 б), характеризующего изменение объема (фиг. 1а) и при значении
сигнала величины приращения, полученного с определенной погрешностью, характеризующего нулевое приращение объема, задерживают выполнение следующей операции для гарантированного
0 обеспечения удаления избытков реагентов и продуктов (фиг. 1в),
Учас1жи кривых З 1, 5-6, -8v 9-Ю, 11-12, 13-Й - задержки времени выполнения следующих операций II-IV и II-VI.
После истечения времени задержки переходят к выполнению следующей one рации путем подачи управляющего CHI- нала (фиг. 1г).
о Пример.В проточном реакторе, представляющем камеру переменной емкости, заполненную полимерным нежестким носителем бензгидриламин с 2%-ной сшивкой дивинилбензолом (PRF Япония)
был синтезирован пептид ТучРчОРЬе NH , Температура реагентов и растворителей - комнатная 20 , атмосферное давление 100+ МПа.
В качестве защитных групп в синте0 зе были использованы Вес-группы. Активированные эфиры аминокислот приготовляли ДСС/НОВ методом. Для подготовки полимера к конденсации каждой аминокислоты использовался М-метилпир- ролидон (МНР); для промывки и сжатия полимера после конденсации пользовались изопропиловым спиртом (1-РчОН), Изменение объема носителя регистрировалось с помощью датчика, сигналы
которого передавались на самописец. Реагенты и растворители, подавались в камеру мини-насосом, скорость протока, 1,2 и 4 мл/мин.
Перед началом синтеза загруженный в реактор полимерный носитель был пеВое PhrO,Bt
- NH-FheBoc
(gbNH3Cl
50% TFA/CHCls „„ „u ,,,t nnL ф NH-phe-NHjCF5COO
5% TEA/CHCl3-(gHlH-P +- 50% TEA/CHCls
l-PheMI,CF3COO - J5% TEA/CHC13
BocTy402Bt
I-PhepMoNH,-NH
(pVNHPhe Рчо Туч Вое-r,u о о
-РЬеРчоВ
50% TFA/CHClg (g-NH-Phe Рчо Туч NH3CF3COO
Ґ Ь% ТЕА/СНС1 N2H РпеРчо ТучШ , ТЕА/тианизол p NHphe РчоТуч NH
Условные обозначения: TEA -три- этиламин; TFA - трифторуксусная кислота .
На диаграммной ленте самописца непрерывно регистрируют изменение объема носителя и определяют его приращение; при значении приращения объема, равном нулю, (фиг. 1 и 2) задерживают выполнение следующей операции на время, необходимое для завершения текущей операции (1-10 мин), после чего переходят к выполнению следующей операции.
Для. связывания непрореагировавших аминогрупп после каждой конденсации в реактор вводят раствор 2 мл 0,05 М DMF/CH2C12; 1 мл 5% TEA в толуоле; 7 мл толуола.
В связи с тем, что предлагаемый способ предусматривает непрерывный контроль и управление процессом синтеза, методика синтеза существенно отличается от существующих стандартных методик, что в свою очередь, не позволяет проводить формальное сравнение по всем операциям синтеза. Возможно сравнение лишь по отдельным операциям. Такое сравнение приводится в таблице.
После полного синтеза пептида на полимере для контроля полноты проте кания синтеза была проведена стандартная проверка пикриновой кислотой.
а,
17ОД087
реведен из хлоргидрата в свободную аминоформу- 5% триэтиламином в хлороформе, а затем сжат изопропиловым спиртом. При этом на каждой операции в процессе синтеза происходит
- NH-FheBoc
3-(gHlH-PR-NH2
-NH
-r,u о о BocP40 Bt
-РЬеРчоВос S
(pVNHPhe Рчо Туч Вое
I
Прирост массы пептидил-полимера
составляет Э9,1% от теоретически рассчитанного значения прироста. Снятый с полимера пептид проверялся на хрома- тографическую гомогенность. Чистота равна 96%.
Способ управления процессом твердофазного синтеза биополимеров на
нежестких носителях по изменению объема носителя позволяет повысить не менее чем в два раза производительность синтеза за счет полной автоматизации
процесса путем регистрации изменений объема носителя и преобразования этих изменений в информационные и управляющие сигналы; снижает расход дорогостоящих и дефицитных реагентов в
несколько раз за счет своевременного завершения каждой операции по сигналу, информирующему о прекращении изменения объема носителя,
Эффективность синтеза повышается
за счет уменьшения побочных продуктов реакций вследствие уменьшенного объема реагентов, повышенной их концентрации, что, в конечном итоге, приводит к повышению качества синтезируемых биополимеров.
Формула изобретения
Способ управления процессом твердофазного синтеза биополимеров на не717И0878
жестком полимерном носителе в зависи-теля, определяют его приращение и при
мости от физико-химических свойствзначении приращения объема, равном ну/лю,
носителя, отличающийся тем, что, с целью повышения производительности процесса, на каждой операции в процессе синтеза измеряют объем носи5
задерживают выполнение следующей операции на заданное время, после че-/ го переходят к выполнению следующей операции.
л
Дано полное время на все операции, включая контроль окончания реакции конденсации.
дано чистое время нахождения реагентов и растворителей в реакторе. Время на заполнение реактора и слив из реактора, которое значительно превышает время операций синтеза, не приводится. Не учтено также время, необходимое на контроль окончания реакции конденсации, которое составляет 90-210 мин.
/лю,
задерживают выполнение следующей операции на заданное время, после че-/ го переходят к выполнению следующей операции.
СН3ОН
Фиг.2
| Старт Д | |||
| и Янг Д | |||
| Твердофазный синтез пептидов, М.: Мир, 1971, с | |||
| Шланговое соединение | 0 |
|
SU88A1 |
| Реакции на полимерных подложках при органическом синтезе | |||
| М.: Мир, 1983, с | |||
| Автоматический прибор для регистрирования числа замыканий | 1922 |
|
SU454A1 |
Авторы
Даты
1992-06-30—Публикация
1986-09-10—Подача