Изобретение относится к пищевой промышленности, сельскому хозяйству и может быть использовано для определения количества антоцианинов в различных частях растений, пищевых продуктах, пищевых красителях, в сельскохозяйственном сырье, а также для оценки Р-витаминной активности некоторых плодово-ягодных культур и их селекции по этому признаку.
Цель изобретения - повышение точности.
При осуществлении данного способа экстракцию антоцианинов из растительного материала проводят двухфазной системой растворителей петанол-1 - концентрированная соляная кислота - вода в соотношении 10-12:10-12:2-4 в течение 10-25 мин при 100-110°С, охлаждают экстракт, отделяют органическую фазу. Затем отбирают аликво- ту органической фазы и измеряют оптическую плотность при длинах волн 530 и 655 нм относительно пентанола-1. После этого к аликвоте добавляют смесь метанола и 30%- ного пероксида водорода в соотношении 2,5-2,0:1,5-2,0 так, чтобы на 1 объемную часть аликвоты приходилось 1,5-4,0 объемных частей смеси, и через 20-25 мин вновь измеряют оптическую плотность на тех же длинах волн. Суммарную концентрацию антоцианинов рассчитывают по разности оптических плотностей.
Для увеличения экстракционной способности экстрагента используется равновесная двухфазная система растворителей пентанол-1 - концентрированная соляная кислота в смеси с водой. В водном слое, представляющем собой раствор соляной кислоты в воде, экстрагируемые из растительного материала антоцианины при нагревании гидролизуются до единой
VI
О
VI
агликонной формы, Наличие в слое небольших количеств пентанола-1 понижает полярность водной фазы, что улучшает экстракцию антоцианинов. Образующиеся агликоны, хорошо растворимые в пентано- ле, накапливаются в спиртовой фазе. Таким образом, спиртовый слой играет роль фазы- коллектора, который, поглощая антоциани- ны в агликонной форме, постоянно поддерживает водный слой в ненасыщен- ном состоянии, способствуя более глубокой экстракции и гидролизу антоцианинов.
Высокая температура (100-110°С) и высокая концентрация соляной кислоты обеспечивают полный гидролиз антоцианинов до единой агликонной формы.
Для предотвращения мешающего влияния компонентов (флавоны, флавонолы и халконы) проводят измерение оптической плотности при длине волны 530 нм до и после обработки смесью 30%-ного перокси- да водорода и метанола (1,5-2,0:2,5-2,0) в течение 20-25 мин. При действии этой окислительной системы из всего разнообразия флавоноидных соединений разрушаются лишь антоцианины, поэтому при вычитании оптической плотности раствора до и после окисления величины, соответствующие поглощению мешающих флавонолов, становятся равными нулю.
Влияние хлорофиллов, также мешающих определению антоцианинов, учитывается дополнительным измерением оптической плотности при длине волны 655 нм,
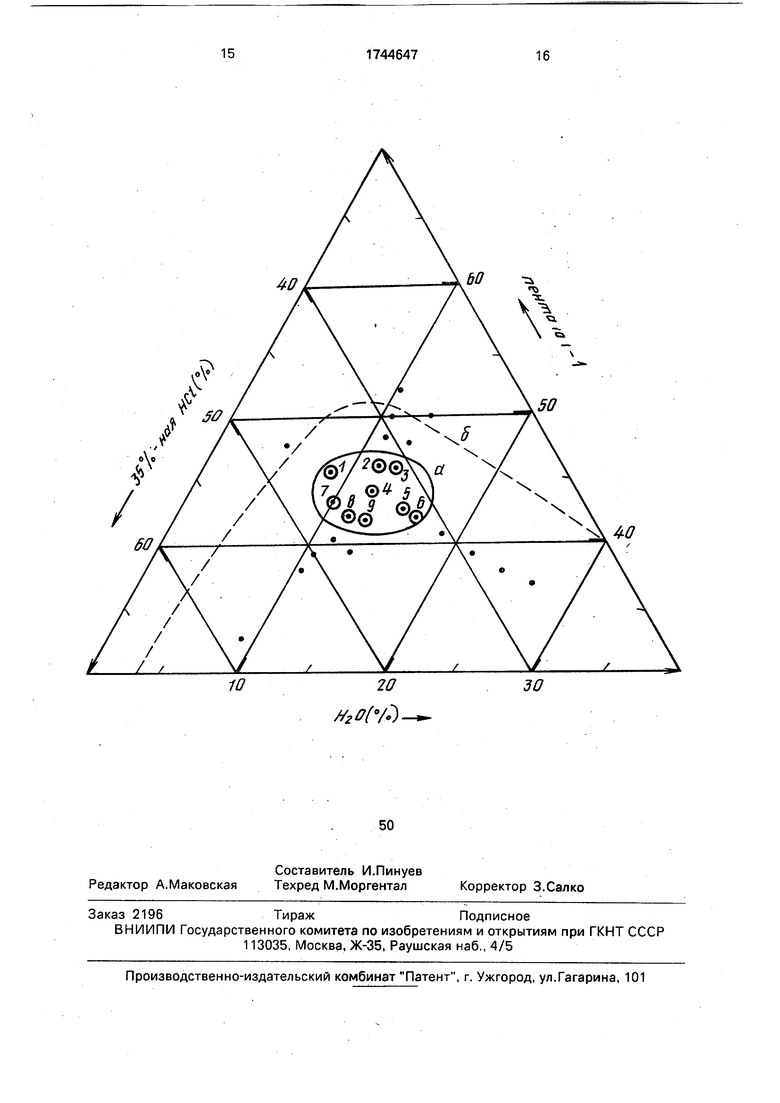
На чертеже показана треугольная диаграмма Гиббса-Розебома зависимости выхода суммы антоцианинов от соотношения компонентов экстрагирующей смеси.
Пример 1. Плод, очищенный от косточек, гомогенизируют, отбирают 0,10- 0,25 г гомогената, помещают его в колбу емкостью 50-70 мл, заливают смесью 11 мл концентрированной соляной кислоты и 11 мл пентанола-1. Затем добавляют 3 мл воды и нагревают смесь с обратным холодильником на глицериновой или масляной бане при 100-110°С, изредка встряхивая содержимое колбы.
Спустя 20 мин нагревание прекращают, колбу охлаждают, ее содержимое переносят в делительную воронку. Стенки колбы омывают 1-2 порциями пентанола-1 (по 5 мл), который затем также переносят в делитель- ную воронку. Органический (верхний) слой сливают в мерную колбу емкостью 50 мл. Водную фазу после разделения взбалтывают с 5-10 мл пентанола-1, отделяют его в воронке и объединяют с остальной органической фазой. Объем последней доводят пентанолом до 50 мл, отбирают аликвоту 3 мл и определяют ее оптическую плотность на длинах волн 530 и 655 нм. Если плоды особенно богаты антоцианинами и одной экстракции недостаточно для полного их извлечения, операцию экстрагирования проводят дважды, используя мерную колбу на 100 мл. Для проб, содержащих малые количества антоцианинов, отбор аликвоты следует проводить прямо из органического слоя экстрагента. Аналогичного эффекта можно достигнуть, используя для анализа соответственно меньшие или большие исходные навески гомогената.
К взятой аликвоте добавляют 6 мл метанола, 6 мл 30%-ного пероксида водорода, раствор перемешивают и через 25 мин снова спектрофотометрируют. Расчет суммарной концентрации антоцианинов проводят по формуле
Q +
V М ант
9 Е ант . А 530 - Г Д 530 - X ( А 655 - Г А 655 )
1 - ха
где Q - содержание суммы антоцианинов в пробе, мг/г или мг/мл;
V - общий объем органической фазы (мерной колбы), мл;
Мант- молекулярная масса стандартного антоцианина, на который ведут пересчет всех остальных веществ этой группы, г/моль;
Еант - молярный коэффициент погашения стандартного антоцианина, л/моль см;
г - разведение аликвоты (в примере к аликвоте добавляют 6 мл метанола и 6 мл Н202. Объем аликвоты до разбавления - 3 мл, после разбавления - 15 мл. Таким образом, );
g - масса или объем пробы, г или мл;
Абзо и Аб55 - оптические плотности аликвоты на длинах волн 530 и 655 нм до добавления метанола и Н20а;
ASSO и Дб55 - оптические плотности раствора спустя 20-25 мин после добавления метанола и НаОа;
х и а - соотношения коэффициентов погашения хлорофиллов (смеси хлорофиллов или стандартного хлорофилла и стандартного антоцианина на длинах волн 655 и 530 нм).
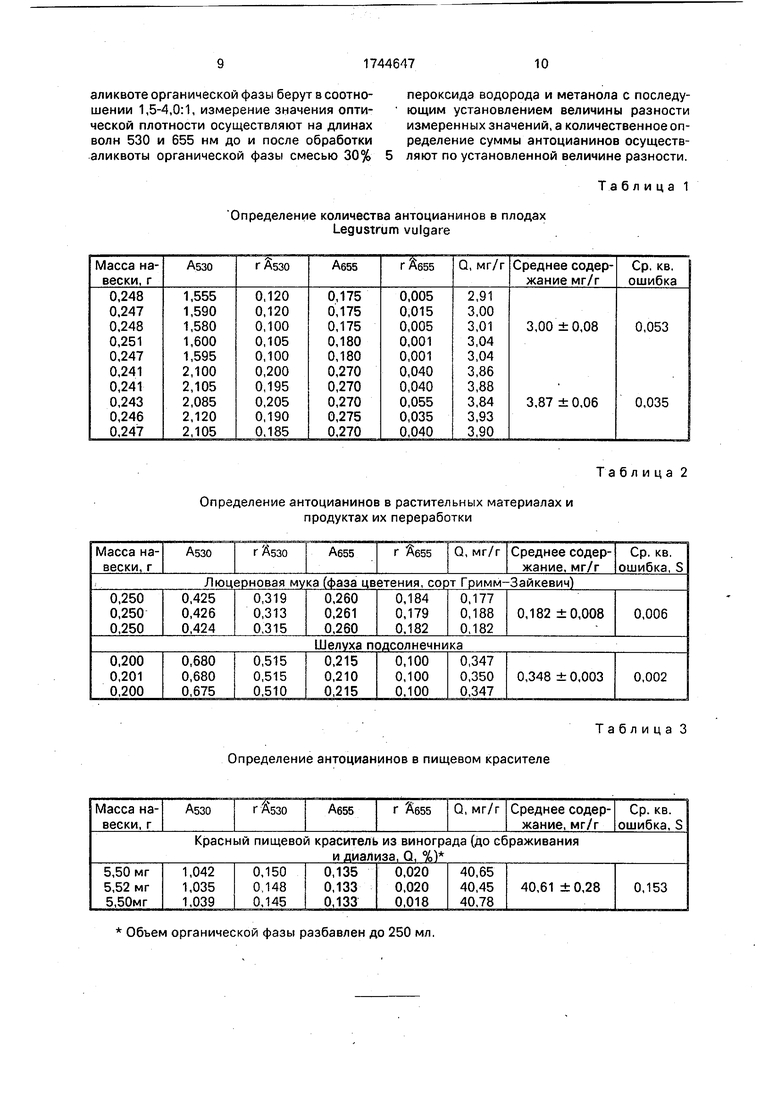
Результаты анализа количества суммы антоцианинов в плодах Legustrum vulgare приведены в табл.1. В качестве стандартного антоцианина и внутреннего стандарта для проверки способа использован пеллар- гонидин. Выход внутреннего стандарта 97,8%, среднеквадратическая ошибка - 0,06-0,08, ошибка среднего - 1,6-2,7%.
Внутренний стандарт - 0,89 мг/г.
Выход внутреннего стандарта - 0,87 мг/г (97,8%).
Пример 2. 0,25 г травяной муки, полученной из люцерны, скошенной в фазе цветения (используют для кормления сельскохозяйственных животных) или 0,2 г измельченных лушпаек подсолнечника (используют как сырье для получения красного пищевого красителя) тщательно перемешивают с раствором HCI и пентанолом-1, затем добавляют 3 мл воды и анализируют, как в примере 1. Полученный гидролизат имеет интенсивный желто-коричневый цвет из-за большого количества сопутствующих фенольных соединений. Если аликвота слишком сильно поглощает на длине волны 530 нм, ее разбавляют пентанолом в 2-3 раза, а полученную оптическую плотность умножают на величину разведения. Результаты определения приведены в табл.2.
Пример 3. 5,5 мг (5, г) неочищенного (до сбраживания и диализа) пищевого красителя заливают 11 мл пентанола-1, слегка нагревают и перемешивают до полного растворения, затем добавляют остальные компоненты смеси и проводят анализ, как в примере 1. Во время нагревания экс- трагент каждые 2-3 мин тщательно перемешивают или встряхивают. Это необходимо для более полного контакта антоцианиновс раствором HCI (более полного гидролиза). При слишком сильном поглощении антоци- анинов либо разводят аликвоту, как в примере 2, либо повторяют весь анализ с меньшей навеской пигмента. Результаты измерения см. в табл.3.
Пример 4. К 22 мл смеси пентанола-1 и концентрированного раствора HCI (11:11) приливают 3 мл виноградного напитка. Далее анализ проводят, как в примере 1. По мере гидролиза антоцианины переходят из водного слоя в органический. Время гидролиза - 10 мин. Количество антоцианинов в виноградном напитке приведено в табл.4.
Пример 5. 0,2 г лепестков астры красноцветковой однолетней (Aster amellus) экстрагируют системами растворителей, содержащих различные соотношения пентанола-1, концентрированной соляной кислоты и воды, в течение 10 мин. Далее анализ проводят, как в примере 1. Количество пентанола и соляной кислоты варьируют от 36 до 52%, воды - от 4,5 до 25%. Максимальная концентрация антоцианинов (1,26 мг/г) получена при соотношении спирта, кислоты и воды 10-12:10-12:2-4.
Результаты подбора соотношения компонентов экстрагирующей системы растворителей приведены на треугольной диаграмме состава Гиббса-Розебома (см
чертеж). Изолинией а ограничена область состава смеси, при которой достигается извлечение более 85% антоцианинов (точки 1 - 86,0%; 2,3 - 88,4%; 4 - 100,0%; 5 - 88,6% 6 - 85,3% 7 - 89,1 %; 8 - 95,3%; 9 - 90,7%)
Линия б отделяет область составов, npt которых двухфазная система неустойчиво или не существует. Из диаграммы, изобра женной на чертеже следует, что при увеличении количества спирта, соляной кислоты
и при уменьшении количества воды разделение фаз ухудшается. Уменьшение в системе доли соляной кислоты или увеличение объема воды приводит к понижению общего содержания HCI, что замедляет экстракцию
и ухудшает условия гидролиза. При уменьшении количества спирта соответственно уменьшается объем органической фазы, что вызывает снижение эффективной емкости экстрагента. Таким образом, оптимальным
является соотношение компонентов пента- нол-1 - конц. соляная кислота - вода - 10- 12:10-12:2-4. Отклонения от данного соотношения либо ухудшают условия экстракции, либо понижают устойчивость двухфазной системы.
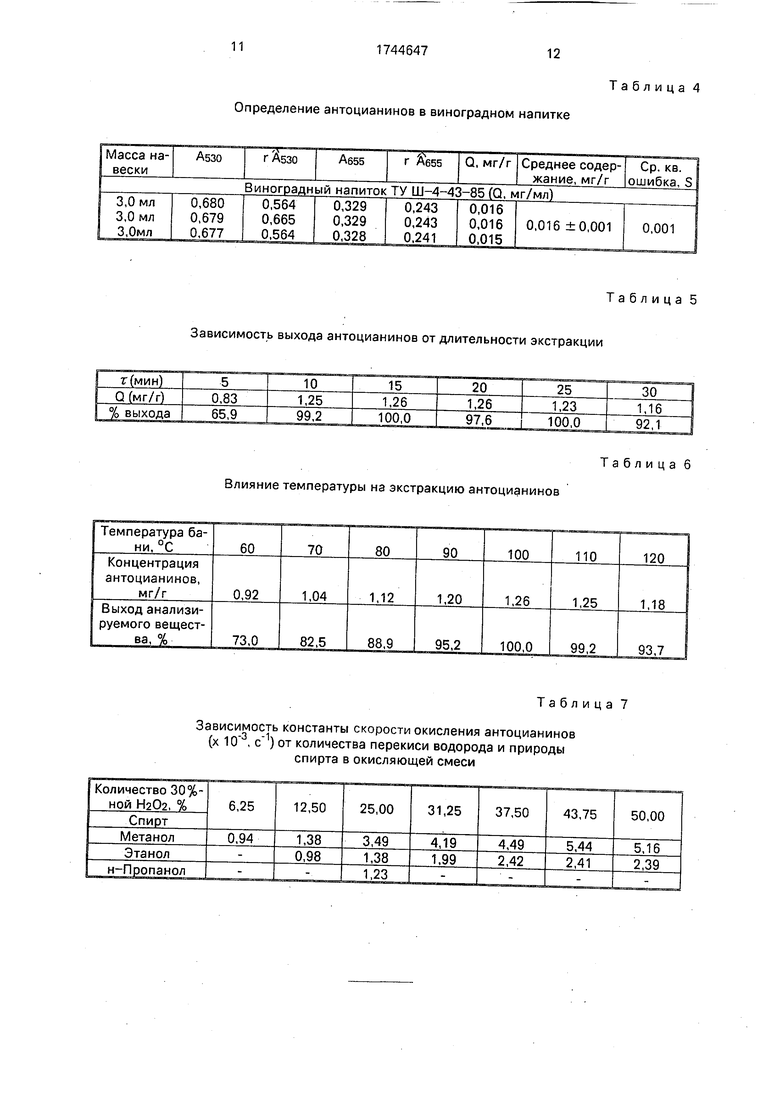
Пример 6. 0,2 г лепестков астры экстрагируют системой растворителей пен- танол-1 - конц. соляная кислота - вода (11:11:3) в течение 5-35 мин. Результаты определения суммарного количества антоцианинов приведены в табл.5. Максимальное извлечение наблюдается при продолжительности экстракции 10-25 мин. Большее время экстракции приводит к уменьшению
количества антоцианинов, по-видимому, из- за реакции окислительной полимеризации, характерной для антоцианинов и протекающей в жестких условиях.
Пример 7. 0,2 г лепестков астры
однолетней заливают экстрагентом состава пентанол-1 - конц.соляная кислота - вода (11:11:3) и нагревают на термостатируемой бане в течение 15 мин при температурах 60-120°С. Отсчет времени начинают, когда
показания термометра, помещенного в экс- трагент, достигают заданной температуры (60-100°С) или когда экстрагент начинает кипеть (110-120°С). Результаты, приведенные в табл.6, показывают, что максимальное количество антоцианинов извлекается при температуре среды 100-110°С. При 60-90°С скорость гидролиза и извлечение антоцианинов уменьшаются, при 120°С начинается полимеризация антоцианинов, поэтому
концентрация анализируемых веществ в экстракте понижается.
Пример 8. К 1 мл раствора пелларго- нидина в пентаноле-1 (,6х10-5 М) приливают 4 мл смеси спирта и 30%-ного пероксида водорода. Количество раствора Н202 в смеси варьируют от 6,25 до 50 объемных процентов. Добавление больших объемов Н2Р2 приводит к помутнению пробы за счет разделения фаз и образования эмульсии. Измерение оптической плотности проводят на автоматическом спектрофотометре каждые 100 с. Константу скорости реакции определяют методом наименьших квадратов по формуле
пАг пА0-К т,
где АО - начальная оптическая плотность раствора (530 нм);
К- константа скорости реакции, с-1; т- время протекания реакции, с;
А г оптическая плотность в данный момент времени.
Зависимость скорости реакции от соотношения 30%-ного пероксида водорода и спирта, а также от химического строения последнего приведены в табл.7. Наибольшая скорость окисления наблюдается при добавлении к раствору антоцианинов смеси 30%-ной и метанола в соотношении 1,5-2,0:2,5-2,0.
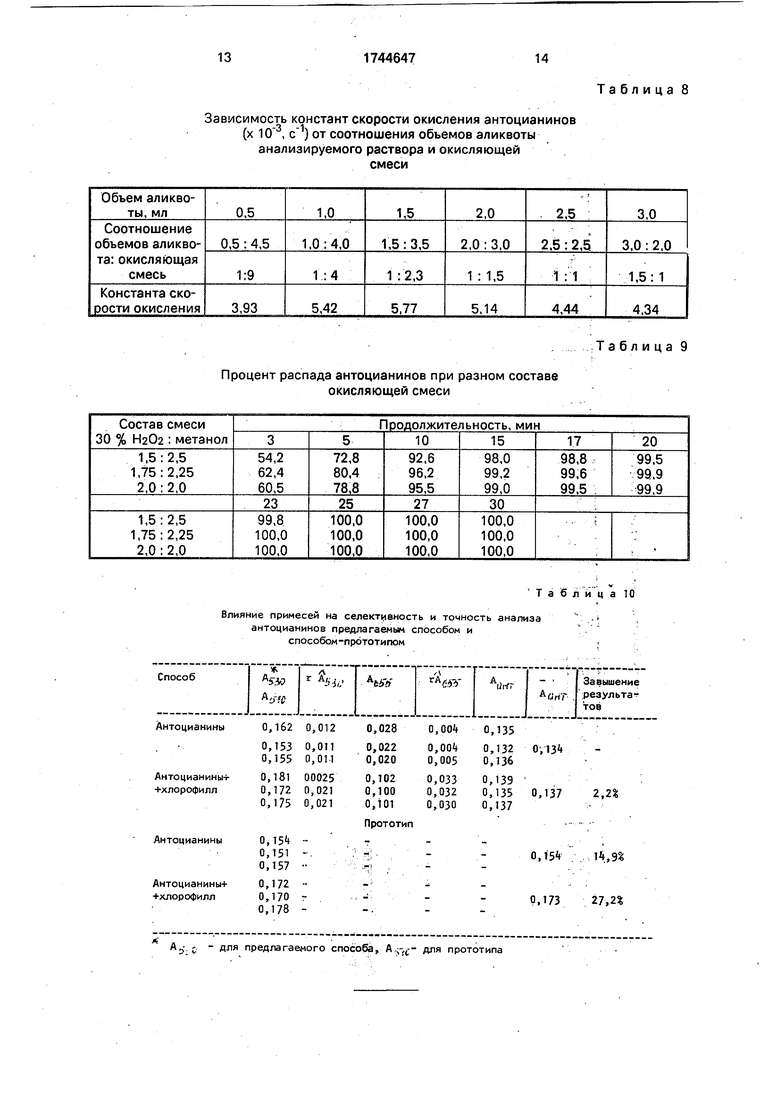
Пример 9. Аликвоты 0,5; 1,0; 1,5; 2,0; 2,5; 3,0 мл раствора пелларгонидина (,2х ) в пентаноле-1 смешивают с окисляющей смесью 30%-ная Н202 - метанол (2:2) так, чтобы общий объем полученного раствора был равен 5 мл. Константы скорости реакции определяют, как в примере 2. Полученные результаты (табл.8) показывают, что наибольшая скорость окисления (распада) наблюдается при соотношении объемов аликвоты и окисляющей смеси 1:4-1:1,5.
Пример 10. К растворам пелларгонидина объемом 1 мл добавляют по 4 мл смеси 30%-ной Н20а и метанола в соотношении 1,50:2,50; 1,75:1,25; 2,00:2,00, Измерения оптической плотности проводят каждые 3-5 мин, затем рассчитывают процент распада антоцианина. Результаты, приведенные в табл.9, показывают что распад более чем 99,0% антоцианинов достигается при продолжительности реакции более 20 мин. В целях сокращения времени аналитического определения верхний предел продолжительности реакции взят равным 25 мин. За 5 мин пробу подготавливают к спектрофото- метрированию и определяют ее оптическую плотность при 530 и 655 нм.
Пример 11. Навески смеси феноль- ных соединений, выделенной из лепестков хризантемы корейской и содержащей фла- вонолы и антоцианины, растворяют в рав- ных объемах 1 %-ного водного раствора HCI и пентанола-1. Определение оптической плотности проводят согласно предлагаемому способу и способу-прототипу. Затем к аналогичным растворам добавляют хрома0 тографически очищенный спиртовый экстракт хлорофилла А в количестве 0,1 мл на 3 мл раствора антоцианинов и снова проводят анализ. Из полученных сравнительных данных, приведенных в табл. 10, следует, что
5 как флавоноиды, так и хлорофиллу значительно ухудшают точность и селективность способа-прототипа. В предлагаемом способе мешающее влияние этих примесей практически полностью компенсируется.
0 Следовательно, предлагаемый способ более селективен и позволяет получить большую точность анализа.
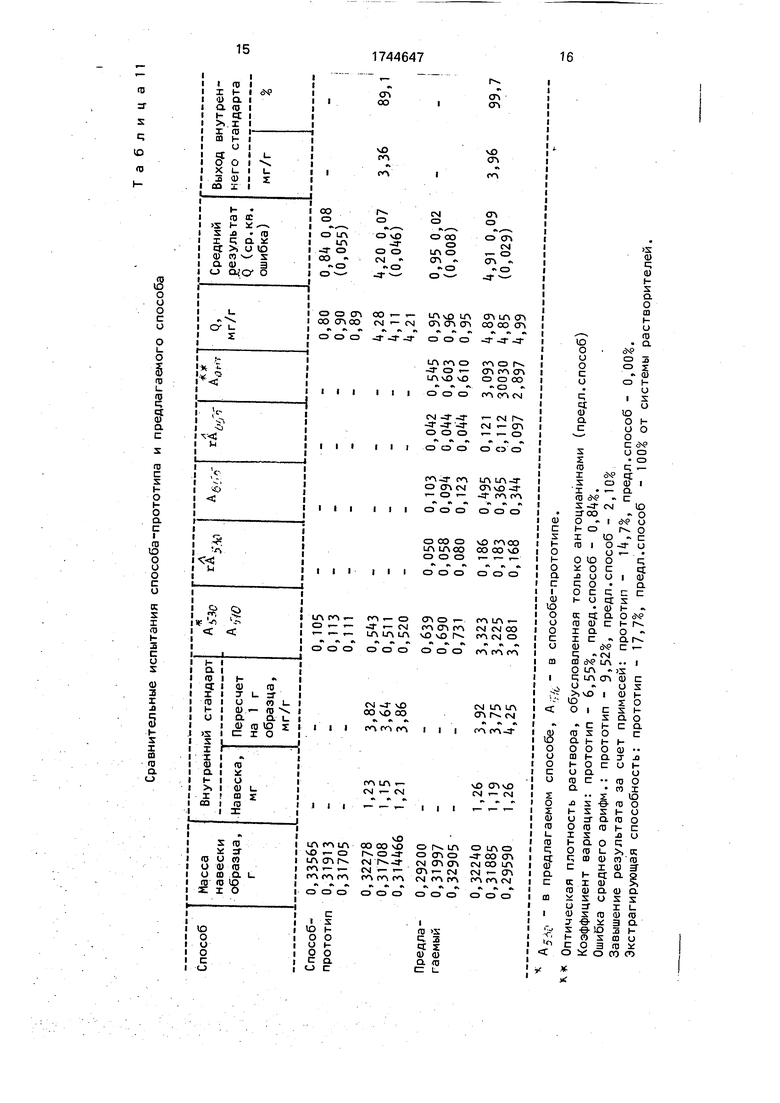
Пример 12 (сравнительное испытание прототипа и предлагаемого способа). Наве5 ски 0,29-0,33 г лепестков хризантемы корейской Бекон анализируют на содержание суммы антоцианинов предлагаемым способом и способом-прототипом в трех повтор- ностях. Параллельно проводят аналогичные
0 аналитические определения в присутствии внутреннего стандарта - 1,15-1,26 мг пелларгонидина.
Сравнительным испытанием установлено, что предлагаемый способ имеет боль5 шие чувствительность, точность, лучший выход внутреннего стандарта. Резкое отличие между полученными результатами в предлагаемом способе и способе-прототипе объясняется низкими экстрагирующими
0 свойствами системы растворителей прототипа. Результаты сравнительных испытаний приведены в табл.11.
Формула изобретения Способ количественного определения
5 суммы антоцианинов, предусматривающий их экстракцию из растительного материала в присутствии соляной кислоты и измерение значения оптической плотности полученного экстракта, отличающийся тем, что,
0 с целью повышения точности, экстракцию антоцианинов проводят двухфазной системой растворителей пентанол-1 .-концентрированная соляная кислота:вода в соотношении 10-12:10-12:2-4 в течение 105 25 мин при 100-110°С, из полученного экстракта осуществляют отбор аликвоты органической фазы и обработку аликвоты в течение 20-25 мин смесью 30% пероксида водорода и метанола, взятых в соотношении 1,5-2,0:2,5:2,0, причем смесь последних к
аликвоте органической фазы берут в соотношении 1,5-4,0:1, измерение значения оптической плотности осуществляют на длинах волн 530 и 655 нм до и после обработки аликвоты органической фазы смесью 30%
пероксида водорода и метанола с последующим установлением величины разности измеренных значений, а количественное определение суммы антоцианинов осуществляют по установленной величине разности.



| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ТРИСНАТРИЕВОЙ СОЛИ ХЛОРИНА Е6 | 2019 |
|
RU2705199C1 |
| Способ определения мышьяка (III) | 1990 |
|
SU1734009A1 |
| ФОТОСЕНСИБИЛИЗАТОР И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2001 |
|
RU2183956C1 |
| Экстракционно-фотометрический способОпРЕдЕлЕНия СуРьМы B бРОНзАХ | 1979 |
|
SU833491A1 |
| Способ определения германия | 1990 |
|
SU1734010A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ВОДОРАСТВОРИМЫХ ВИТАМИНОВ | 2005 |
|
RU2318216C2 |
| ФОТОСЕНСИБИЛИЗАТОР И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2014 |
|
RU2568597C1 |
| Способ фотометрического определения ванадия | 1991 |
|
SU1797050A1 |
| Способ количественного определения хлордиазепоксида в биологических объектах | 1978 |
|
SU792116A1 |
| Способ определения хрома (yI) | 1980 |
|
SU975579A1 |
Изобретение относится к пищевой промышленности, сельскому хозяйству и может быть использовано для определения количества антоцианинов в различных частях растений, пищевых продуктах, пищевых красителях, в сельскохозяйственном сырье, а также для оценки Р-витаминной активности некоторых плодово-ягодных культур и их селекции по этому признаку. Экстракцию антоцианинов из растительного материала проводят двухфазной системой растворителей пентанол-1 - концентрированная соляная кислота - вода в соотношении 10-12:10-12:2-4 при температуре 100-110°С в течение 10-25 мин. Суммарное количество антоцианинов вычисляют по разности оптических плотностей при длинах волн 530 и 655 нм до и после обработки органической фазы экстрагента смесью 30%-ного перок- сида водорода и метанола. 1 ил., 11 табл.
Определение количества антоцианинов в плодах Legustrum vulgare
Определение антоцианинов в растительных материалах и продуктах их переработки
Определение антоцианинов в пищевом красителе
Объем органической фазы разбавлен до 250 мл.
Таблица 1
Таблица 2
Таблица 3
Определение антоцианинов в виноградном напитке
Зависимость выхода антоцианинов от длительности экстракции
Влияние температуры на экстракцию антоцианинов
Зависимость константы скорости окисления антоцианинов
(х , ) от количества перекиси водорода и природы
спирта в окисляющей смеси
Таблица 4
Таблица 5
Таблица 6
Таблица 7
Зависимость констант скорости окисления антоцианинов
(х , ) от соотношения объемов аликвоты
анализируемого раствора и окисляющей
смеси
Процент распада антоцианинов при разном составе окисляющей смеси
Влияние примесей на селективность и точность анализа антоцианинов предлагаемым способом и способом-прототипом
АЭ с - для предлагаемого способа, A ,-ft- для прототипа
Таблица 8
Таблица 9
Таблица 10
Сравнительные испытания способа-прототипа и предлагаемого способа
&5 - в предлагаемом способе, А, в способе-прототипе.
Оптическая плотность раствора, обусловленная только антоцианинами (предл.способ) Коэффициент вариации: прототип - 6,55%, пред.способ - 0,84%. Ошибка среднего арифм.: прототип - 9,52%, предл.способ - 2,10% Завышение результата за счет примесей: прототип - 14,7%, предл.способ - 0,00%. Экстрагирующая способность: прототип - 17,7%, предл.способ - 100% от системы растворителей.
Г
X
л
ъ
| Муравьева Д.А., Бубенчикова В.Н., Беликов Н.В | |||
| Спектрофотометрическое определение суммы антоцианинов в цветах василька синего | |||
| - Фармакология, 1987, т | |||
| Коридорная многокамерная вагонеточная углевыжигательная печь | 1921 |
|
SU36A1 |
| Видоизменение прибора с двумя приемами для рассматривания проекционные увеличенных и удаленных от зрителя стереограмм | 1919 |
|
SU28A1 |
Авторы
Даты
1992-06-30—Публикация
1989-01-24—Подача