iio;i xpop.iaTory ielxin; длительность (до 2-х суток), невысокая чувствительность (граница обнаружения 0,2 мг в 100 г оОъекта). Целью изобретения является упрощ ние способа и повышение чувствитель ности определения. Поставленная цель достигается описываемым способом количественног определения хлордиазепоксида в биологических объектах путем гидролиза непосредственно анализируемой пробы раствором соляной кислоты при 100110°С с последующей экстракцией пол ченного гидролизата органическим растворителем и хроматографировании полученного экстракта в тонком слое сорбента, элюирования бензофенонов и проведения азосочетания с М-о(.-наф тилэтилендиамином и дигидрохлоридом и спектрофотометрирования полученного при этом окрашенного раствора. Отличительным признаком способа является то, что гидролизу подверга ется непосредственно анализируемая проба при 100-110°С. Примеры иллюстрируют предлагаемый способ. Пример 1. К 25 г гомогенизата отдельного органа (печень, желудок с содержимым, кишечник, почки) в круглодонной колбе с притертой пробкой емкостью 140-200 прибавляют lio 100 мл 6н раствора со ляной кислоты и гидролизуют в течение 2 ч при 100-110 С на глицериновой бане с обратным холодильником. По окончании гидролиза обратные холодильники промывают 3-5 мл 2н раст вора соляной кислоты, присоединяя промывные воды к гидролизату, который фильтруют через, ватмановский (бумажный) фильтр (белая лента} в делительную воронку. Фильтрат нейтрализуют, добавляя гранулированный едкий натр, и доводят рН раствора до 10 по универсаль ному индикатору. 2-ами1-;о-5-хлорбензофенон, полученный в результате гидролиза, экстрагируют и-гептаном трижды порциями 20, 15, 15. Гептановые извлечени после расслоения фаз переносят в мерную колбу на 50 мл, пропуская через воронку с безводным сульфатом натрия (1-1,5 г). В случае образова ния эмульсии, с целью расслоения фаз, проводят центрифугирование в течение 5-10 мин. при 5000 об/мин. Объем раствора в мерной колбе на 50 мл доводят гептаном до метки и тщательно перемешивают. Хроматографическое определение бензофенона хлордиазепоксида от бен зофенонов других производных 1,4бензодиазпенина и их обнаружение. По 10, мл полученных гептановых извлеченийвыпаривают при комнатной температуре или на роторном испарителе в выпаривательных колбах до объема 0,5-1 мл, остатки наносят на стартовую линию хроматографической пластинки с тонким слоем силикагеля КСК (0,62 на 1 см, от 250 меш.), закрепленного гипсом (5% от веса силикагеля) в виде 2-х полос (в каждой 10 мл выпаренного экстракта) длиной в 1 см на расстоянии 2 см друг от друга. Рядом на ту же стартовую линию наносят пятно метчика, состоящего из смеси 0,1% этаноловых растворов бензофенонов производных 1,4-бензодиавенина (диазепама, нитразепама, хлордиазепоксида) в количестве 10-15 мкг каждого бензофенона. Хроматографируют в системе бензола. Пробег фронта растворителя 10 см. Время хром.тографирования 20-25 мин. С хроматограммы удаляют органический растворитель под током теплого воздуха (феном) 5 мин . Часть хроматограммы, соответствующую первой полосе исследуемого раствора, предназначенной для элюирова- ния, закрывают сте лянной пластинкой. Ва открытой части хроматограммы с пятном метчика и 2-ой полосой исследуемого раствора проводят реакцию образования азокрасителя. С этой целью хроматограмму опрыскивают последовательно 2н-ым раствором соляной кислоты, 0,1%-ым раствором нитрата натрия, через 5 мин избыток нитрита натрия удаляют обработкой пластинки 0,5% раствором сульфамата аммония и через 1-2 минуты полученную соль диазония сочетают с 0,1%-ым раствором N-ot-нафтилэтилендиамина. В случае присутствия 2-амино-5хлорбензофенона (продукта гидролиза хлордиазепоксида) на хроматограмме через 15 мин образования пятно сиреневого цвета (бензофенон нитразепама дает пятно разового цвета с Rr 0,16) сравнивают величину R метчика хлордиазепоксида (0,27-0,3) и исследуемого раствора. Реакцией удается обнаружить 1 мкг хлордиазепоксида в пятне. Из закрытой части пластинки зону селикагеля, соответствующую расположению иятна метчика, собирают на стеклянный фильтр № 4 и элюируют двумя порциями этанола по 5 мл в мерную пробирку. Элюат доводят этанолом до 10 мл. Снимают спектр 2-, амино-5-хлорбензофенона в УФ области (от 200-400 нм) в кювете с толщиной рабочей поверхности 1 см на СФ-16. Наличие характерных максимумов поглощения в области 238 нм и 390 нм подтверждает п рисутствие соединения в исследуемом растворе ( 980). Этаноловый раствор бензофенона после снятия спектра количественно переносят в стеклянный бокс, тула же присоединяют раствор, оставшийсч в мерной пробирке. Этанол упаривают под током теплого воздуха, а остаток растворяют в 5 мл 2н-ой соляной кислоты при постоянном помешивании в течение 10-15 мин. В зависимости от концентрации в полученном растворе 2.-амино-5-хлорбензофенона, которую ориентировочно рассчитывают после снятия спектра в УФ, на реакцию образования азокрасителя берут 0,5,1,0 или 3 мл и доводят (если это необходимо) до 3 мл 2 н-ым раствором соляной кислоты. Далее последовательно добавляют 0,5 мл 0,1% раствора нитрата натрия, через 5 минут - 0,5 мл 0,5% раствора сульфамата аммония. Азокраситель сиреневого цвета образуется через 15 мин после добавления 1 мл 0,1%-го раствора N-o -нафтилэтилендиамида дигидрохлорида. Окраска устойчива в течение cyToi:. Оптическую плотность окраииенного раствора измеряют на спектрофотометре СФ-16 при 550 нм в кювете с рабочей длиной поверхности 1 см. В качет стве раствора сравнения используют контроль реактивов. Концентрацию хлордиазепоксида в органах определя от по формуле: D У/- Уд -. 100 с -v. EVcA V; где X - содержание хлордиазепокс да, мг в 25 г органа; D - оптическая плотность изм ряемого раствора; V, - объем разведенного гидро лизата (50 мл); V - количество аликвоты гепт нового экстракта, взятог для нанесения на хромато графическую пластинку (10 мл); Vg- количество 2 н-го раствора соляной кислоты, взятого на растворение сухого остатка; количество аликвоты, взятой на реакцию солянокисл, лого раствора; Е /е/1/ удельный показ.атель поглощения;С - навеска исследуемого органа. Количество хлордиазепоксида, выделяемого из 25 г органов, представлено в таблице. Методика: Из стандартного раство-, ра хлордиазепоксида в этаноле (1000 мкг/мп) готовили серию растворов в мерных колбах на 25 мл, содержащих 20,50,100,150,200 мкг/мп. К 0,5 мл этих растворов, помещенных в колбу для гидролиза, добавляют по 3,0 мл 2 н-го раствора соляной кислоты и гидролизуют 20-25 минут при 100110°С на глицериновой бане с обратным холодильником. Охлажденный гидролизах доводят в мерной пробирке до 5 мл. 2 н-ым раствором соляной кислоты и 1 мл из этого раствора берут на реакцию образования азокрасителя (реакция Браттои-Маршалла), описанную выше. После определения плотности окрашенного раствора на спектрофотометре СФ-16 при 550 нм вычисляют удельный коэффициент поглощения по формуле: Е где D - оптическая плотность; С - концентрация раствора, вес % ; t - толщина поглощающего слоя, Способ позволяет упростить процесс и повысить чувствительность определения с 0,2 мг в 100 г объекта до 0,05 мг в 100 г объекта.
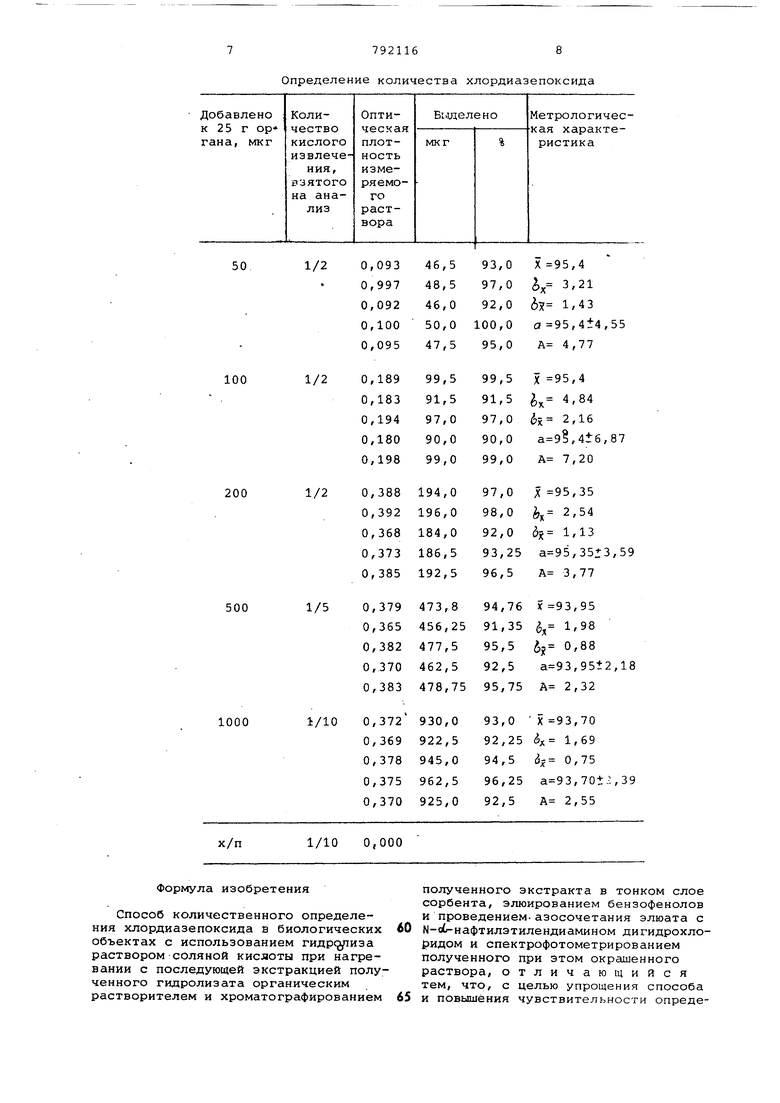
Определение количества хлордиазепоксида
7921168



| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ГИДАНТОИНА, 1-АМИНОГИДАНТОИНА, ФУРАДОНИНА, ФУРАГИНА | 1991 |
|
RU2009483C1 |
| Способ определения фоксима в секционном материале | 1984 |
|
SU1196772A1 |
| Способ количественного определения хлорхолинхлорида | 1978 |
|
SU767639A1 |
| Способ количественного определения сапонина в воде | 1983 |
|
SU1105809A1 |
| АНТИГИПОКСИЧЕСКОЕ И ГИПОЛИДЕМИЧЕСКОЕ ФАРМАЦЕВТИЧЕСКОЕ СРЕДСТВО, УЛУЧШАЮЩЕЕ КОРОНАРНЫЙ И МОЗГОВОЙ КРОВОТОК | 2013 |
|
RU2536275C1 |
| Способ определения уксусного ангидрида | 1981 |
|
SU1012128A1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ЦИКДОМЕТИАЗИДА | 1994 |
|
RU2090866C1 |
| Способ определения патулина в пищевых продуктах | 1988 |
|
SU1585754A1 |
| Способ определения @ -Токоферола | 1986 |
|
SU1332223A1 |
| Способ определения простых сахаров в тонком слое сорбента | 2016 |
|
RU2642264C2 |

1/2
50
1/2
100
1/2
200
1/5
500
1/10 0,372930,0
1/10 0,000
х/п
Формула изобретения
Способ количественного опрелеления хлордиазепоксида в биологических объектах с использованием гидрс иза раствором соляной кислоты при нагревании с последующей экстракцией полученного гидролизата органическим растворителем и хроматографированием
,4
1 3,21
6;; 1,43
,4i4,55
А 4,77
,4
4,84
6х 2,16
,4Jr6,87
А 7,20
;(95,35
2,54
Зх 1,13 ,,59 А 3,77
473,894,76i(93,95
456,2591,35 1,98
477,595,5Jjj 0,88
462,592,,95l2,18
478,7595,75А 2,32
93,0 X 93,70 92,25 &к 1,69
0,369922,5 94,5 (3jf 0,75
0,378945,0 96,25 ,70j:- 39
0,375962,5 92,5 А 2,55
0,370925,0
полученного экстракта в тонком слое сорбента, элюированием бензофенолов и проведением-азосочетания элюата с N-cir-нафтилэтилендиамином дигидрохлоридом и спектрофотометрированием полученного при этом окрашенного раствора, отличающийся тем, что, с целью упрощения способа и повышения чувствительности опреде979211610
1ения, гидролизу подвергают непос-fluorometric Micro Method Analytical эедственно анализируемую пробу приBiochemistry. 1963, № 5, р.195-207. температуре 100-110 С.2. Сборник Определение физиолоИсточники информации,болитов в биологических объектах тринятые во внимание при экспертизев °Д редакцией А.И. Тенцовой и
)Arconte. Determination of Chlor-.. ..Изотов Б.Н. и др. Изолирование
liazepoxide and of а Metabolite ofхлордиазепоксида из внутренних орга.actam Character in Plasma of Humans,,нов трупа, 1977, с. 20-24 (прото)ogs and Rats by a specific spectro-тип). гически активных веществ и их мета
Авторы
Даты
1980-12-30—Публикация
1978-09-25—Подача