Изобретение относится к способам получения новых соединений общей формулы М eri3(NCS)2 ANCS, где М - Си. Zn, Cd; A - Na, К, NH4, которые обладают биологической активностью и могут найти применение в медицине, биотехнологии и сельском хозяйстве.
Цель изобретения - способ получения нового класса веществ
Поставленная цель достигается тем, что для получения соединения М епз(МС5)2х , где М - Zn, Cd, окисид цинка или оксид кадмия, подвергают взаимодействию с тиоцианатом аммония и этилендиамином при молярном соотношении оксид металла: тиоцианат аммония; этилендимамин, равной 1:3-3,2:3-3,2, в среде ацетонитрила. А для получения соединения М en3(NCS)2X
xANCS, где M-Zn, Cd; А- К, Na, оксид цинка или оксид кадмия, подвергают взаимодействию с тиоцианатом аммония, этилендиамином и тиоцианатом калия или натрия при молярном соотношении оксид металла: тио- цизнат аммония: этпендиамин: тиоцианат калия или натрия, равном 1:2-2,2:3-3,2:1,2, в среде ацетонитрила или метанола.$
Для получения соединения Си епз(МС5)2 xANCS где А - К, Na, металлическую медь подвергают взаимодействию с тиоцианатом аммония, этилендиамином и тиоцианатом калия или натрия при молярном соотношении медь: тиоцианат аммония: этилендиамин; тиоцианат калия или натрия, равном 1:2-2,2:3-3,2: 1-1,2, а ацетонитриле.
Получение целевого продукта предлагаемым способом в лабораторных условиях
Х|
ГО
XI со ел
проводят, как правило, в реакторе, снабженном мешалкой и нагревателем. В реактор вносят порошок металла или оксида металла, тиоцианат калия (натрия) и/или аммония и приливают раствор этилендиа- мина в метаноле или ацетонитриле и нагревают при постоянном перемешивании до полного превращения металла или оксида металла. Температуру процесса выбирают с учетом температуры кипения растворителя, Целевой продукт выделяют из реакционной смеси известными методами.
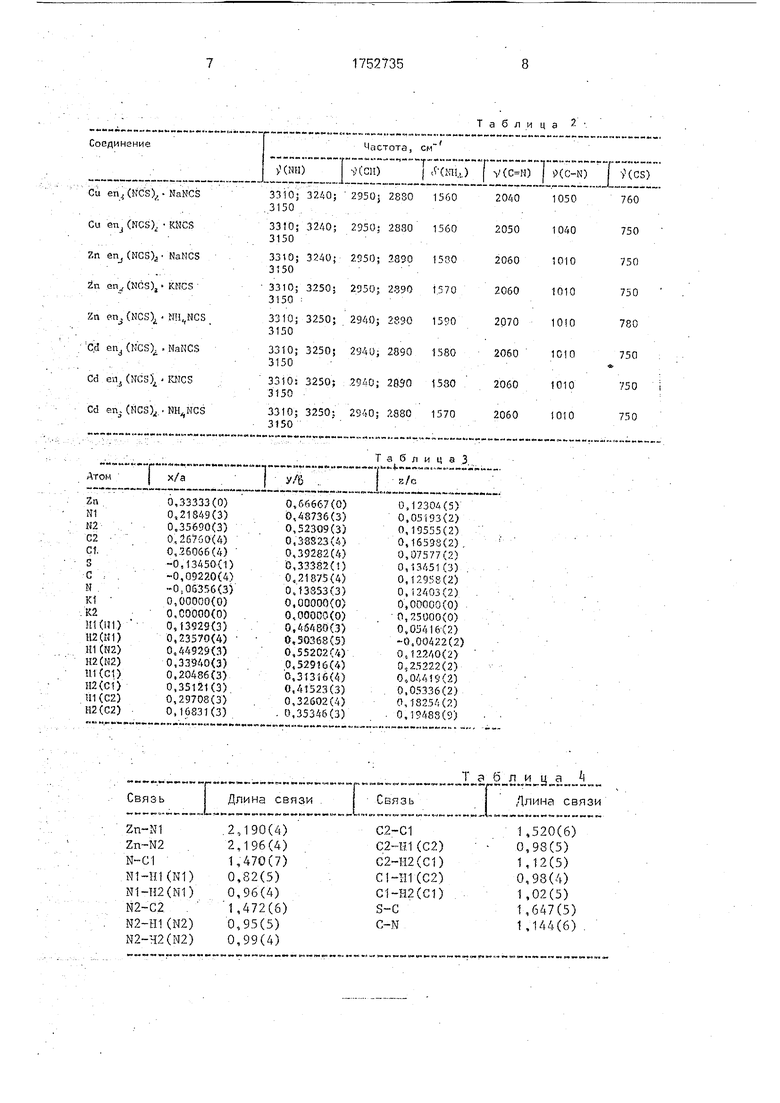
На фиг.1 - 3 приведены структуры соединений.
П р и м е р. В реактор вносят 0,81 г оксида цинка, 2,28 г тиоцианата аммония, приливают 20 мл аиетонитрила, 2.1 мл эти- лендиэмина (молярное соотношение исходных компонентов 1:3:3) и нагревают при температуре 50°С и перемешивании в течение 10 мин. Выход целевого продукта-3,99 г (91%).
Найдено, %: Zn 1-1,7; SCN 38,9; N 32,0; С 24,8, Н 6,2.
Вычислено, %: Zn 14,93: SCN 39,87; N 31,97; С 24,66; Н 6,39.
Результаты анализа и И К спектральные характеристики остальных соединений представлены в табл.1 и 2. Указанные соединения выделены впервые.
По данным рентгенаструктуриого ana лиза(табл.3-8ифиг 1 -3) синтезированные соединения обладают неизвестным ранее строением
Основу структуры Zn ens(NCS)2 KNCS составляют непрерывные колонки К(МСЗ)з11Х,,в которых два сорта ионов калия находятся в октаэдрических окружениях, образованных атомами азота тиоцианатных групп, Октаэдры ассоциированы по граням (фиг.1). Расстояние К1 - «2 равно 4,199 A, ar(K1 - N) и r(K2 - N) составляют 2,949 и 2,972 А соответственно Между колонками находятся катионы Zn , связанные с SCN-rpyn- памй/ЫН.,,5СЫ-водородными связями. Кристалл высокосимметричен:лишь одна SCN-rpynna независима кристаллографически.
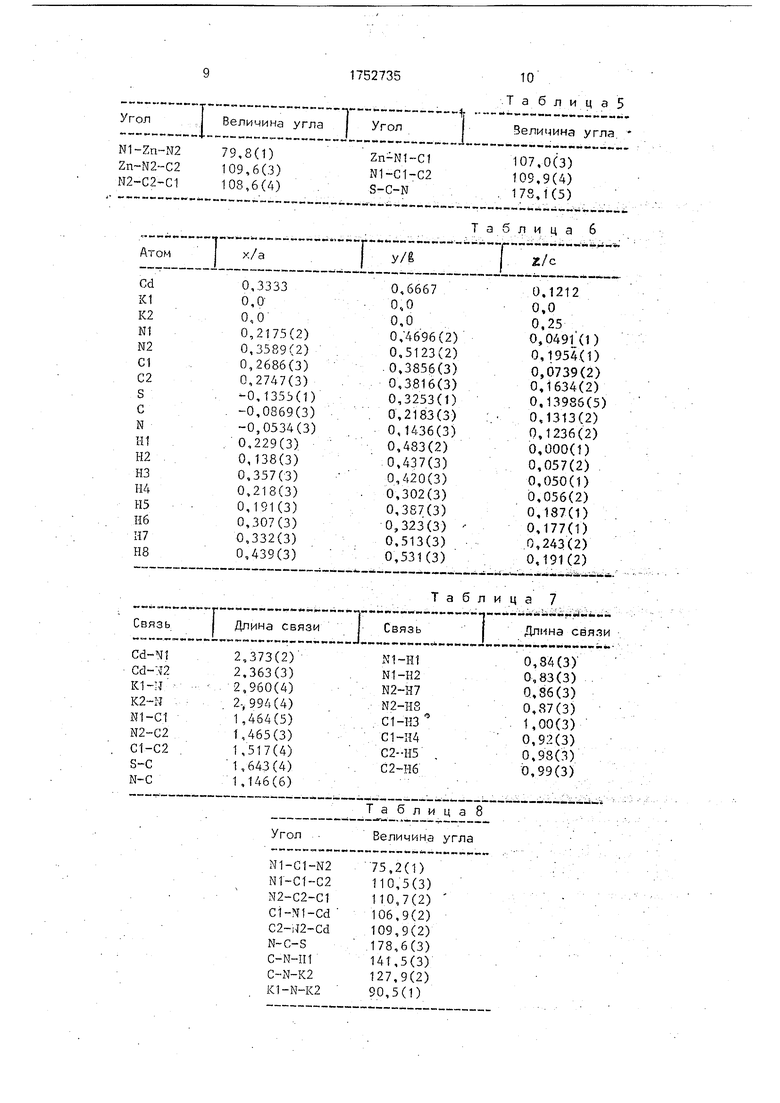
Координационный полиэдр иона цинка образован шестью атомами азога трех би- дентатных молекул этилендиамина (фиг.2). Расстояние в среднем составляет 2,19 А и является характерным для обычно наблюдаемого в октаэдрическмх комплексах цинка с этилендиамином.
Координированная молекула этилендиамина имеет гош-конфигурацига; атомы С1 и С2 отклоняются от плоскости металлоцик- ла Zn en на 0,466 и -0,236 А соответственно, т.е., в среднем на 0,35 А, что не противоречит ранее полученным результатам (0,30 - 0,34 А для координированного гош-зтилен- диамина).
Средние величины длин связей в метал- лоцикле Zn en составляют: r(NC) 1,47 А и г(СС) 1,52 А.
Величины r(NC) и г(СС) соответствуют
общепринятым представлениям о длинах
одинарных связей между указанными атомами, а величины валентных углов у атома
углерода и азота близки к тетраэдрическим.
Тиоцианат практически линеен: угол NCS равен «178°; межатомные расстояния углерод - азот и углерод - сера обычны для тиоцианат-иона.
Структура характеризуется разветвленной системой водородных связей На фиг.З показаны водородные связи, реализующие- ся в элементарной ячейке кристалла. Приводим параметры NH...S - : N1 - Н ,.S (1 + Y, 1 - X -i Y, -Z); r(N1H,..S) 3,459 А, г (N1-H) Л,96 A; r(H.,.S) 2,60 A; Z.N1 - Н - S 149°, N24...S (1 + X - Y, 1 - Y, 1 /2 - Z), r(N2H...S) 3,418 A, r(N2 - Н) 0,99 A, r(H. .S) 2,75 А; N2-Н-5 125°.
Основными структурными элементами
Со1 епз(МС5)2 KNCS являются комплексы
Cd и колонки объединенных через
общую грань октаэдров К(МСЗ)б (фиг.1 и 2).
Координационное число кадмия в комплексном катионе равно шести. Атомы азота трех бидентатных молекул этилендиамина образуют искаженный октаэдр. Атом кадмия занимает частную позицию на тройной оси,
Этилендиэминные циклы имеют гош- конфигурацию.
Атомы калия занимают две кристалло- графически неэквивалентные позиции. Каж- дый из атомов координирует шесть тиоцианатныхгрупп.
Координационные полиэдры представляют собой искаженные октаэдры, вытяну- тые вдоль оси третьего порядка. Расстояние KN несколько отличается для атомов К1 и К2, Чередуясь друг с другом, октаэдры KNe через общую грань объединяются в бесконечные колонки, ориенти- рованные вдоль (001).
Атомы серы имеют несколько контактов с атомами водорода аминогрупп, которые можно рассматривать как водородные свя- зи. Система таких связей объединяет катионы в трехмерный каркас (фиг.З) Таким образом, тиоцианатные группы являются бидентатномостиковыми,
По данным рентгенофазового анализа строение остальных соединений аналогично.
Синтезированные соединения обладают биологической активностью (табл 9- 12),
«. Таким образом, предлагаемый способ получения новых координационных соединений позволяет синтезировать биологически активные вещества
В табл. 1 даны результаты химического анализа синтезированных соединений.
Данные ИК-спектроскопических исследований синтезированных соединений приведены в табл 2,
Координаты атомов в структуре Zn ens(NCS)2 KNCS даны в табл 3.
В табл, 4 и 5 приведены межатомные расстояния (А) и валентные углы (град) в структуре Zn епз(МС5)2 КМС5 соответствен- но,
В табл, 6 приведены координаты атомов в структуре Cd ens(NCS)2 KNCS,
В табл. 7 и 8 даны межатомные рассто- яния (А) и.валентные углы (град) соответственно в структуре Cd ena(NCS)2 KNCS.
В табл. 9 дана бактерицидная и фунги- цидиая активность 1%-ного раствора координационных соединений цинка.
Бактерицидное и фунгицид юе действие соединений оценивали методом диффузии его 0,1%-ного или 1%-ного раствора в агаре по величине зон ингибирования роста микроорганизмов.
В табл 10 приведены данные, характеризующие нематоцидную активность соединений
Токсичность соединения Си епз(МС5)2 KNCS против рисовогоафеленхоида, стеблевой немато ды картофеля и свекловичной цистообразующей нематоды характеризуется данными табг.11.
Биологическая эффективность спедине ния Си ens(NCS) KNCS против галловых «е- матод в почве характеризуется данными табл.12.
Формула изобретения
Способ получения координационных соединений общей формулы М епз(МС5) xNCS, где М - Си, Zn, Cd; A - К, Na, en - этилендиэмин, заключающийся в том, что тиоцианат аммония, этилендиамин и тиоци- анат общей формулы ANCS. где А имеет указанное значение, подвергают взаимо действию с оксидом цинка или кадмия в среде метилового спирта или ацетонитрил при получении соединений, где М - Zn или Cd, или подвергают взаимодействию с медным порошком в среде ацетонитрила при получении соединений, где М - Си.




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения аминотиоционата или аминогалогенида металла | 1983 |
|
SU1186571A1 |
| Способ получения аминотиоцианата или аминогалогенида кобальта или никеля | 1983 |
|
SU1175873A1 |
| Способ определения тиоцианата аммония в присутствии тиомочевины | 1984 |
|
SU1318838A1 |
| Способ получения дитиоцианатодииодидокадмата калия | 1985 |
|
SU1386568A1 |
| СПОСОБ ПОЛУЧЕНИЯ СУЛЬФИДА МЕТАЛЛА | 2000 |
|
RU2189944C2 |
| Способ получения аминотиоцианата или аминохлорида или аминобромида меди ( @ ) | 1983 |
|
SU1181998A1 |
| Хелатные комплексы гетарилформазанов, обладающие положительной и отрицательной термохромией | 1977 |
|
SU658155A1 |
| Способ получения аминотиоцианата меди или этилендиаминхлорида,этилендиаминбромида,этилендиаминиодида или пиридинтиоцианата цинка,или пиридинтиоцианата,или этилендиаминтиоцианата кадмия | 1984 |
|
SU1263631A1 |
| Комплексы цинка и кадмия N-[2-(алкилиминометил)фенил]-4-метилбензолсульфамидов, обладающие люминесцентной активностью | 2017 |
|
RU2650529C1 |
| ЛИТИЕВАЯ ВТОРИЧНАЯ БАТАРЕЯ С ЭЛЕКТРОЛИТОМ, СОДЕРЖАЩИМ СОЕДИНЕНИЯ АММОНИЯ | 2006 |
|
RU2335044C1 |
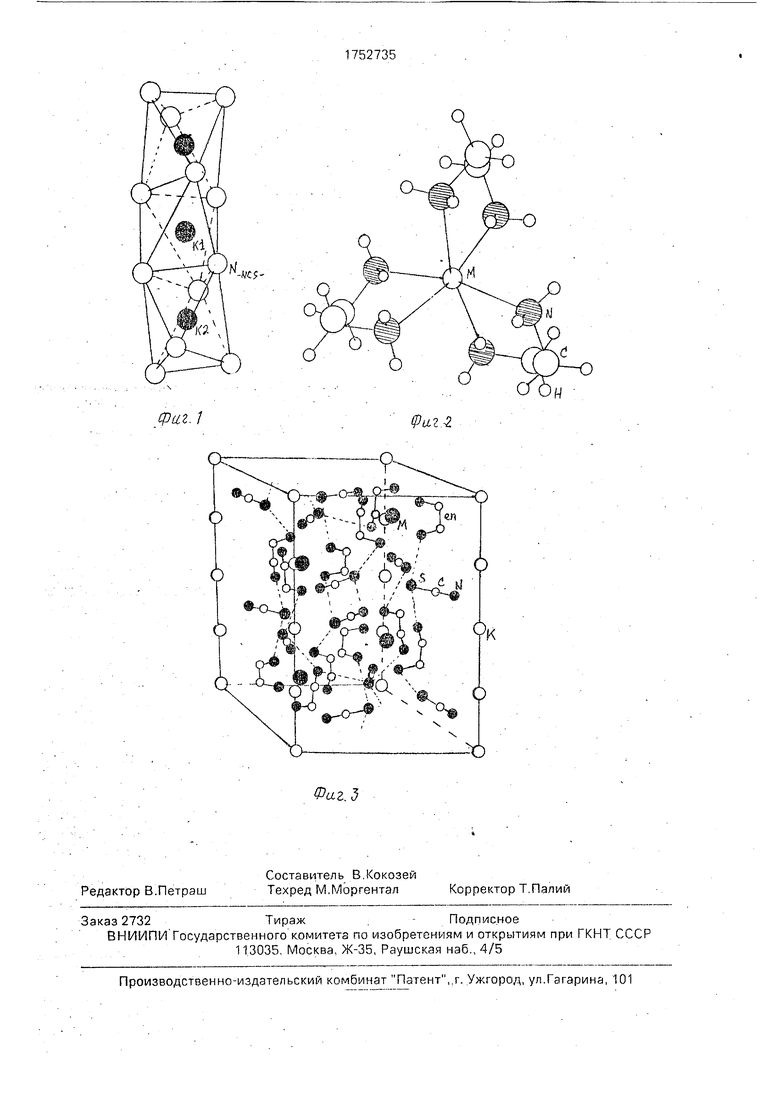
Изобретение относится к способам получения новых координационных соединений, которые обладают биологической активностью и могут найти применение в медицине, биотехнологии и сельском хозяйстве. Цель изобретения - новый способ получения нового класса веществ. Для получения координационных соединений общей формулы М )2 ANCS, где М - Си, Zn, Cd; A - К, №. МЩ; en этилендиамин, металлосодержащий реагент подвергают взаимодействию с тиоциа- натом аммония, этилендиамином и тиоцианатом общей формулы ANCS , где значение А указано выше, в среде растворителя. В случае получения соединения М ens(NCS)2 ANCS, где М - Zn и Cd, в качестве металлсодержащего реагента используют оксид металла и реакцию проводят в среде метилового спирта или ацетонитрила. В случае получения соединения Cuens(NCS)2 ANCS в качестве металлсодержащего реагента берут медный порошок и реакцию проводят в среде ацетонитрила. Доказана бактерицидная и фун- гацидчая активность полученных координационных соединений цинка, а также нематоцидная активность соединений меди. 3 ил. 12 табл.
.,.
Таблица
Примечание. 1 Staphytococcus aureus 209; 2 - Staphylococcus aureus cowan 1;
3 - Staphylococcus aureus smith; A - Staphylococcus аигеич wood-46; 5 - Staphylococc-js auraus 3272r 6 - Esecherihia call; 7 - rseudomoiws aeruginosa HO; 8 - t5i.crococcus albus; 9 - Micrococeus lysodeicticus; 10 - Bacillus sublilis; 11 - Bacillus mesentericus,
Предлагаемое:
Cu en,(NCS), NsNCS
Си en, (NCS),, Ю-ТС5
Известное:
гетерофос
карбатион
дазомет
Контроль (без добавки соединения)
Примечание,
Таблица 10
О О
ч
87Л
100
66,1 галл/ /раит. (100%)
Нематоцидная активность соединений изучалась в лабораторных опытах против сапрозойной нематоды в концентрации 0,0025% и в вегетационных опытах против галловых нематод в норме расхода 0,08 г/кг почвы.
вестное:
СКИ Этафос
СК.
0,000)
0,0033
0,004 0,00036 0,000|2
0,00038
Контроль (без добавки соединения)
Таблица 11
0,00052
0,0033 0,0011 0,00036 0,00012
0,00023
31,5 62,8 5,3 27,0
Таблица12
1,1 г/раст. 6,5 галл/раст.
(100%)
(100%)
-WCJФаг /
Фаг 2
Авторы
Даты
1992-08-07—Публикация
1989-07-21—Подача