Изобретение относится к области органического синтеза, а конкретно к синтезу смеси алифатических диеновых углеводородов - 2-метилпента-1,3-диена (I) и 4-метил- пента-1,3-диена(II),причем
2-метилпента-1,3-диен является исходным соединением в синтезе ряда ценных душистых веществ, получаемых конденсацией Дильса-Альдера.
Способ получения смеси диенов I и II основан на дегидратации 2-метилпентан- 2.4-диола (III) по следующей схеме
ГГОН ОН
пш
+
(I)
(И)
Известен способ получения диенов I и II дегидратацией диола III в присутствии бромгидрата анилина в качестве катализатора. Выход диеновой фракции примерно 50%, тогда как остальная часть продукта представляет собой смесь спиртов 1,
Недостатки данного способа - низкий выход и наличие большого количества примесей.
Наиболее близким к изобретению является способ получения смеси 2-метилпента- 1,3-диена и 4-метилпента-1,3-диена (I и II) дегидратацией 2-метилпентан-2,4-диола (lit) при 90-200°С в присутствии кислотного катализатора, например 5%-ной водной серной или фосфорной кислот. В качестве
XJ
СП
о
00
ю ел
растворителя используют гликоли или эфи- ры гликолей общей формулы RiO- CHR(CH2), где R, Ri и Ra-H или Ci-C -алкилы; m 1-3; n 1-4, например диэтиленгликоль, пропиленгликоль, монобутиловые эфиры этиленгликоля и диэти- ленгликоля, дибутиловый эфир диэтиленгликоля.
Растворитель используется в большом избытке (200-500% от массы диола). Продукт дегидратации содержит 56-62,8% смеси диенов I и II; 22,5-25,6% смеси непредельных спиртов; 4,8-6,2% других кислородсодержащих продуктов: 9,3- 11,8% смеси низкокипящих продуктов деструкции гликоля III (изобутилен, ацетальдегид), а также 0,5-0,7% продуктов уплотнения. Сведения об общем выходе продукта дегидратации или диеновой фракции отсутствуют. Не указано также соотно- шение 2-метилпента-1,3-диена (I) и 4-мет илпента-1,3-диена (II) в диеновой фракции 2.
Недостатками указанного способа являются низкий выход смеси диенов I и II, низкая селективность процесса по 2-метил- пента-1,3-диену и значительное образование побочных продуктов.
Цель изобретения - повышение выхода целевой смеси и селективности процесса по 2-метилпента-1,3-диену и снижение образования побочных продуктов.
Цель достигается способом получения смеси 2-метил- и 4-метилпента-1,3-диенов дегидратацией 2-метилпентан-2,4-диола при нагревании в присутствии кислотного катализатора с одновременной отгонкой продукта дегидратации из реакционной смеси, отличительная особенность которого состоит в том, что в качестве кислотного катализатора используют каталитическую систему, полученную путем растворения гидроксида калия в гликоле - этиленглико- ле, или диэтиленгликоле, или триэтиленгли- коле при 20 -85°С с последующим взаимодействием полученного раствора с концентрированной серной кислотой, причем указанные компоненты берут из расчетамолярногосоотношения2-метилпентан-2,4 диол:гидроксид ка- лия:серная кислота.тликоль, равного 1 :(0.10-0,25):(0,10-0.25):(0.2-1,0), и дегидратацию ведут в присутствии гидрохинона. Предпочтительно после отгонки продуктов дегидратации от оставшейся смеси отгоняют фракцию, содержащую воду, гликоль и высококипящие побочные продукты, и полученный при этом кубовый остаток повторно используют в качестве кислотного катализатора.
Изобретение иллюстрируется приведенными ниже примерами.
Приме р-с равнение 1 (прототип). В колбу загружают 60 г диэтиленгликоля и 10 г 5%-ной серной кислоты. Смесь нагревают на масляной бане до 120°С и постепенно при перемешивании прибавляют 20 г 2-метилпентан-2,4-диола (III), одновременно отгоняя воду и смеси продуктов
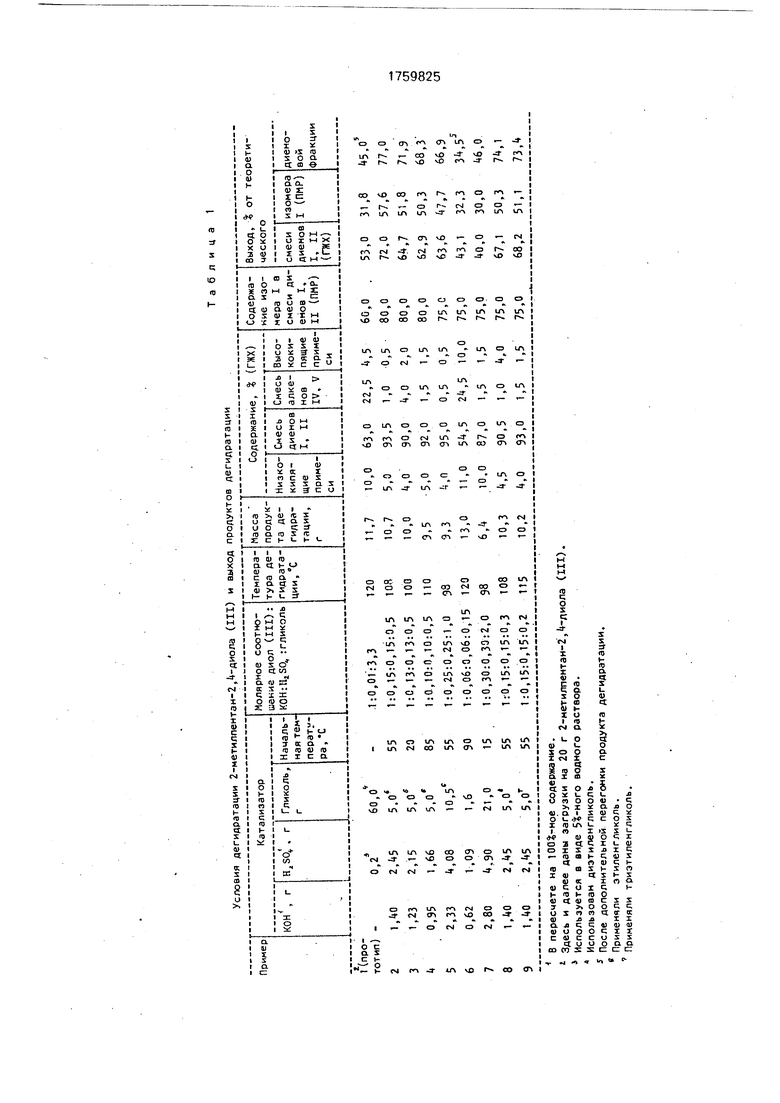
дегидратации с т.кип. 58-94°С (11,7 г). По данным ГЖХ-анализа (см. пример 1, табл.1) продукт содержит 63% смеси диенов I и II; аналитический выход смеси диенов I и I составляет 53,0% от теоретического.
В полученной смеси диенов I и II соотношение изомеров I и II определяли методом ПМР-спектроскопии. В спектрах смесей диенов I и II, полученных на спектрометре Varlan НА-100Д в растворе ССЦ с
ГМДС в качестве внутреннего стандарта выделены следующие характеристичные сигналы (д, от ТМС):
Для изомера : 6,12уш.д(1Н, Н-С3), 5,62 дк. (1Н, Н-С4). 4,80 уш.с. (Н2С1).
Для изомера II: 5,00 уш.д. и 4,90 уш.д.
(всего 2Н, Н2С1, 6,49 дт (1Н, Н-С2), 5,80 уш.д. (1Н, Н-С3).
30
к1
3Ч
I
Соотношение изомеров 1:11 определяли по интегральным интенсивностям протонов Н-С3 в изомере I и Н-С2 в изомере II.
По данным ПМР-спектроскопии содержание изомера I в смеси диенов I и 11 состав- ляет 60%; таким образом, выход 2-метилпента-1,3-диена (I) составляет 31,8% от теоретического.
После дополнительной перегонки продукта дегидратации с эффективным дефлег- матором (10-12 см) получают 6,3 г диеновой фракции с т.кип. 73-79°С (выход 45,3% от теоретического).
При попытке повторного использования раствора серной кислоты в диэтиленг- ликоле, оставшегося после отгонки продукта дегидратации, выход смеси диенов I и II снижается.
Пример 2. В четырехгорлую колбу, снабженную механической мешалкой, ка- пельной воронкой, небольшим дефлегматором с нисходящим холодильником и термометрами для измер ения температуры в жидкости и в парах, загружают 5 г этилен- гликоля, нагревают его до 55°С и прибавляют 1,69 г 83%-ного(1,40 г 100%-ного) твердого гидроксида калия, перемешивают 10 мин до полного растворения, постепенно прибавляют 2.63 г 93%-ной (2,45 г 100%- ной) серной кислоты, что сопровождается повышением температуры смеси до 60- 65°С. Прибавляют 20 г диола III, 0,1 г гидрохинона и нагревают смесь до 100°С, отгоняя продукт дегидратации с т.кип. (10,7 г). По данным ГЖХ-анализа (см. пример 2, табл.1) продукт содержит 98,5% смеси диенов I и II; аналитический выход смеси диенов I и II составляет 72% от теоретического.
По данным ПМР-спектроскопии содержание изомера I в смеси диенов I и II составляет 80%: выход 2-метилпента-1,3-диена (I) составляет 57,6% от теоретического.
Примеры 3-9. Представлены в табл.1.
Пример 10. Процесс осуществляют по примеру 2, за тем исключением, что кубовый остаток после отгонки диеновой фракции продолжают нагревать до 110- 130°С, собирая фракцию (2,5-3,0 г) с т.кип. 90-110°С, содержащую воду, этиленгликоль и высококипящие побочные продукты, и 5,5-6 мл воды. Кубовый остаток охлаждают до 100°С, прибавляют 2-метилпентан-2.4- диол (10 г), содержащий 0.1 г гидрохинона, и нагревают, отгоняя диеновую фракцию (5.35 г) с т.кип. 70-80°С. По данным ГЖХ- анализа содержание смеси диенов I и II составляет 93%. По данным ПМР-спектроскопии выход 2-метилпента-1,3-диена (I) составляет 57,3%.
Вновь отгоняют от кубового остатка фракцию(1,2-1,5 г)с т.кип. 90-110°С и 2,5-3 мл воды, загружают 10 г диола III и проводят дегидратацию, как описано выше. Кубовый остаток может быть использован не менее четырех раз.
Пример-сравнение 11.
Процесс осуществляют по примеру 1. за тем исключением, что реакцию проводят в присутствии 5 г диэтиленгликоля. Результаты приведены в табл.2.
Пример-сравнение 12.
Процесс осуществляют по примеру 11, за тем исключением, что реакцию проводят, применяя концентрированную серную кислоту. Результаты приведены в табл.2.
Пример-сравнение 13.
Процесс осуществляют по примеру 3, за тем исключением, что реакцию проводят,
применяя монофениловый эфир этиленгли- коля. Результаты приведены в табл.2.
Таким образом, в отличие от прототипа, где применяют водные растворы серной кислоты в большом избытке гликоля или
простого эфира гликоля, применение глико- лей в тех количествах, что указаны в изобре- тении, или применение вместо разбавленной серной кислоты концентрированной кислоты, или применение монофенилового эфира этиленгликоля в условиях изобретения не дают положительного эффекта, что подтверждает различие двух каталитических систем - в прототипе и в данном изобретении.
Проведение дегидратации диола III согласно предлагаемому способу позволяет повысить выход смеси диенов с 53 до 62,9- 72% от теоретического: повысить селективность процесса по 2-метилпента-1,3-диену,
в результате чего его содержание в смеси диенов увеличивается с 60 до 75-80%; снизить образование побочных продуктов с 22,5 до 4%.
Формула изобретения
1.Способ получения смеси 2-метил и 4метилпента-1.3-диенов дегидратацией 2- метилпентан-2,4-диола при нагревании в присутствии кислотного катализатора с одновременной отгонкой продукта дегидратации из реакционной смеси, отличающий- с я тем, что. с целью повышения выхода целевой смеси и селективности процесса по 2-метилпента-1,3-диену и снижения образования побочных продуктов, в качестве кислотного катализатора используют каталитическую систему, полученную путем растворения гидроксида калия в гликоле- этиленгликоле, или диэтиленгликоле, или триэтиленгликоле при 20-85°С с последующим взаимодействием полученного раствора с концентрированной серной кислотой, причем указанные компоненты берут из расчета молярного соотношения 2-метил- пентан-2,4-диол:гидроксид калия;серная
кислота, гликоль, равного 1:(0,10- 0,25):(0,10-0,25):(0,2-1,0), и дегидратацию ведут в присутствии гидрохинона.
2.Способ по п. 1,отличающийся тем, что после отгонки продуктов дегидрата0 ции от оставшейся смеси отгоняют фракцию, содержащую воду, гликоль и высококипящие побочные продукты, и полученный при этом кубовый остаток повторно используют в качестве кислотного
5 катализатора.
Условия дегидратации 2-метилпентан-2,4-диола (III) и выход продуктОв дегидратации


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКООКТАНОВЫХ КИСЛОРОДСОДЕРЖАЩИХ КОМПОНЕНТОВ БЕНЗИНОВ | 1996 |
|
RU2116998C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕРЕФТАЛАТНОГО И БЕНЗОАТНОГО ПЛАСТИФИКАТОРОВ ИЗ ПОБОЧНЫХ ПРОДУКТОВ | 2019 |
|
RU2708641C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИЕНОВЫХ УГЛЕВОДОРОДОВ | 1971 |
|
SU425384A3 |
| СМЕСЬ 2,4-ДИМЕТИЛ-6-ВТОР-АЛКИЛФЕНОЛОВ, ОБЛАДАЮЩАЯ СТАБИЛИЗИРУЮЩИМ ДЕЙСТВИЕМ | 1992 |
|
RU2067972C1 |
| КОМПОЗИЦИЯ ДЛЯ ИЗДЕЛИЙ И ПОКРЫТИЙ | 2002 |
|
RU2286361C2 |
| БОЛЕЕ ЭНЕРГОЭФФЕКТИВНЫЙ СПОСОБ ГИДРОГЕНИЗАЦИИ С5 | 2013 |
|
RU2627657C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКООКТАНОВЫХ КИСЛОРОДСОДЕРЖАЩИХ КОМПОНЕНТОВ БЕНЗИНОВ | 1996 |
|
RU2121476C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОСТЫХ ПОЛИЭФИРОВ СЛОЖНЫХ ЭФИРПОЛИОЛОВ И ИХ ПРИМЕНЕНИЕ ДЛЯ ПОЛУЧЕНИЯ ПОЛИУРЕТАНОВ | 2007 |
|
RU2478661C2 |
| Способ получения винилоксиалкилметакрилатов | 1978 |
|
SU771084A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ АНТРАХИНОНОВ И ИХ ПРИМЕНЕНИЕ ДЛЯ ПОЛУЧЕНИЯ РЕИНОВ | 1998 |
|
RU2202535C2 |
Использование: исходные соединения в синтезе душистых веществ, получаемых конденсацией Дильса-Альдера. Сущность изобретения: продукт - смесь 2-метил-() и 4-метилпента-1,3-диенов (II), БФ СбНд, выход смеси 62,9-72,0% от теории, содержание I в смеси 75-80%. Реагент 1: 2-метилпентан-2,4-диол. Условия: кипение реакционной смеси в присутствии гидрохинона и катализатора с отгонкой продуктов дегидратации. Катализатор:каталитическая система, полученная растворением гидро- ксида калия в гликоле - этиленгликоле, или диэтиленгликоле, или триэтиленгликоле при 20-85°С с последующим взаимодействием полученного раствора с концентрированной серной кислотой. Молярное соотношение 2-метилпентан-2,4-диол:гидроксид калия:серная кислотэ:гликоль 1:(0,10- 0.25):(0.10-0,25):(0.2-1.0).Кубовый остаток после дегидратации может быть повторно использован как катализатор. 1 з.п.ф-лы. 2 табл.
В пересчете на 100%-ное содержание.
Здесь и далее даны загрузки на 20 г 2-метилпентан-2,1 -лиола (III). Используется а виде 5%-ного водного раствора. Использован диэтиленгликоль.
После дополнительной перегонки продукта дегидратации. Применяли зтиленгликоль. Применяли триэтияенгликоль.
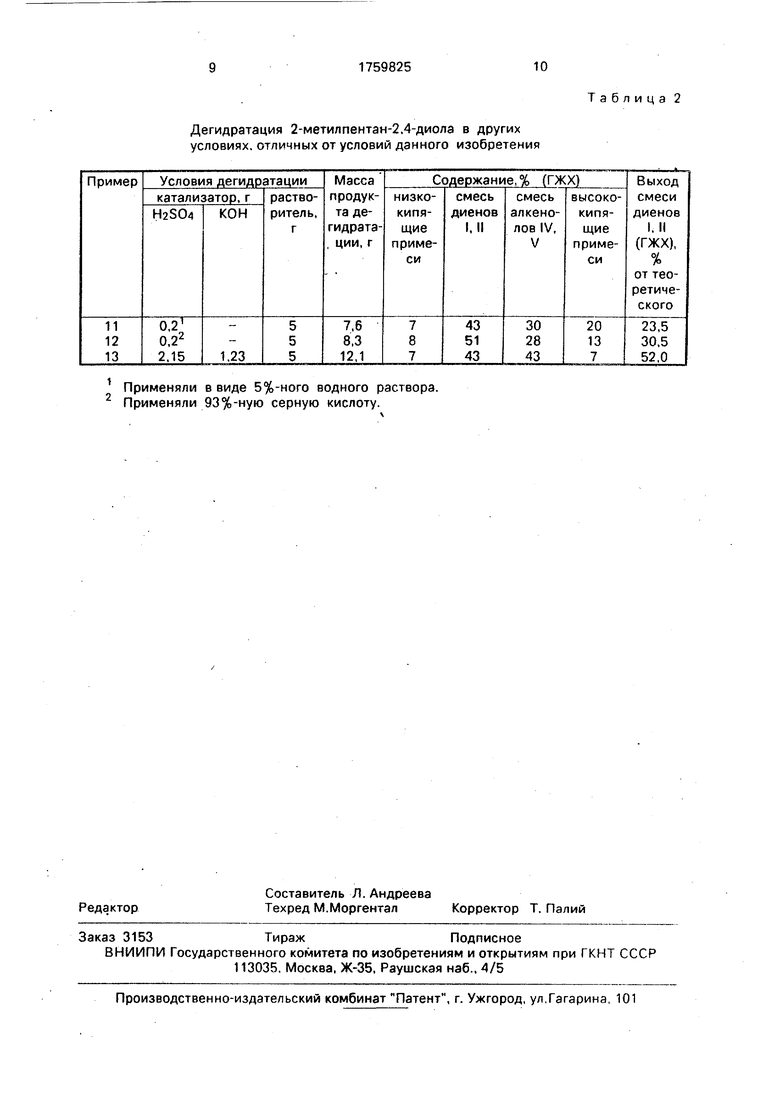
Дегидратация 2-метилпентан-2,4-диола в других условиях, отличных от условий данного изобретения
1Применяли в виде 5%-ного водного раствора.
2Применяли 93%-ную серную кислоту.
Таблица 2
| LKyriakides L.P | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| III | |||
| Catalytic dehydration of hydroxy- compoupo s | |||
| Part I | |||
| Dehydration of ditertiary glycols, JACS, 36, 1914, p.980 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1992-09-07—Публикация
1990-07-26—Подача