Изобретение относится к области аналитической химии, а именно к способам количественного определения новокаинамида. Новокаинамид относится к противо- аритмическим средствам (ПАС). Кроме того в эту группу входят хинидин, аймолин, этмо- зин. Предлагаемый способ позволяет определять повокаинамид в присутствии других ПАС на серийной отечественной аппаратуре.
Известен способ определения новокаинамида путем взаимодействия его с бром- феноловым синим с последующим
фотометрированием полученного окрашенного соединения 1.
Недостатком способа является его невысокая чувствительность (2 мг/мл).
Известен способ определения новокаинамида с использованием в качестве реагента лактата этакридина 2.
Недостатком способа является его сложность, связанная с необходимостью экстракции, а также недостаточно высокая чувствительность - 27 мг/мл.
Наиболее близким к изобретению является способ определения новокаинамида.
ч О О 4 СО 00
основанный на обработке реагентом тропе- олином 00 3.
Недостатком способа является необходимость экстракции, что приводит к сложности епособа, а также его невысокая чувствительность (11 мг/мл).
Цель изобретения - упрощение способа, повышение чувствительности и селективности определения.
Цель достигается тем, что определение новокаинамида проводят путем обработки пробы спиртовым раствором п-диметила- минокоричного альдегида (п-ДМАКА) в присутствии сульфонола с концентрацией в реакционной смеси 4,0 ,0 М при рН 2,0-5,0 с последующим фотометри- рованием полученного раствора.
Эксперимент показал, что растворы, содержащие новокаинамид и органический реагент п-ДМАКА, окрашены в желтый цвет. Спектры поглощения двойных систем в среде цитратных буферных растворов с рН 1,25-6,0 представлены двумя полосами поглощения С Ямакс 265-280 НМ И Амакс 400
нм. Введение третьего компонента - раствора сульфонола приводит к возникновению ярко-малиновой окраски раствора системы.
Спектры поглощения тройных систем новокаинамид-п-ДМАКА-сульфонол пред- ставлены при всех значениях рН тремя полосами поглощения Амакс 280нм , Лмакс 370-400 нм, Лмакс 570нм,АА составляет 170 нм.
Установлены оптимальные условия определения новокаинамида с п-ДМАКА и сульфонолом.
Изучение зависимости светопоглоще- ния систем новокаинамид-п-ДМАКА-сульфонол от рН среды показало, что оптимальной средой являются нитратные буферные растворы с рН 2,0-5,0; 2,,0.
Исследовано влияние СДМАКА на правильность получаемых результатов определения новокаинамида.
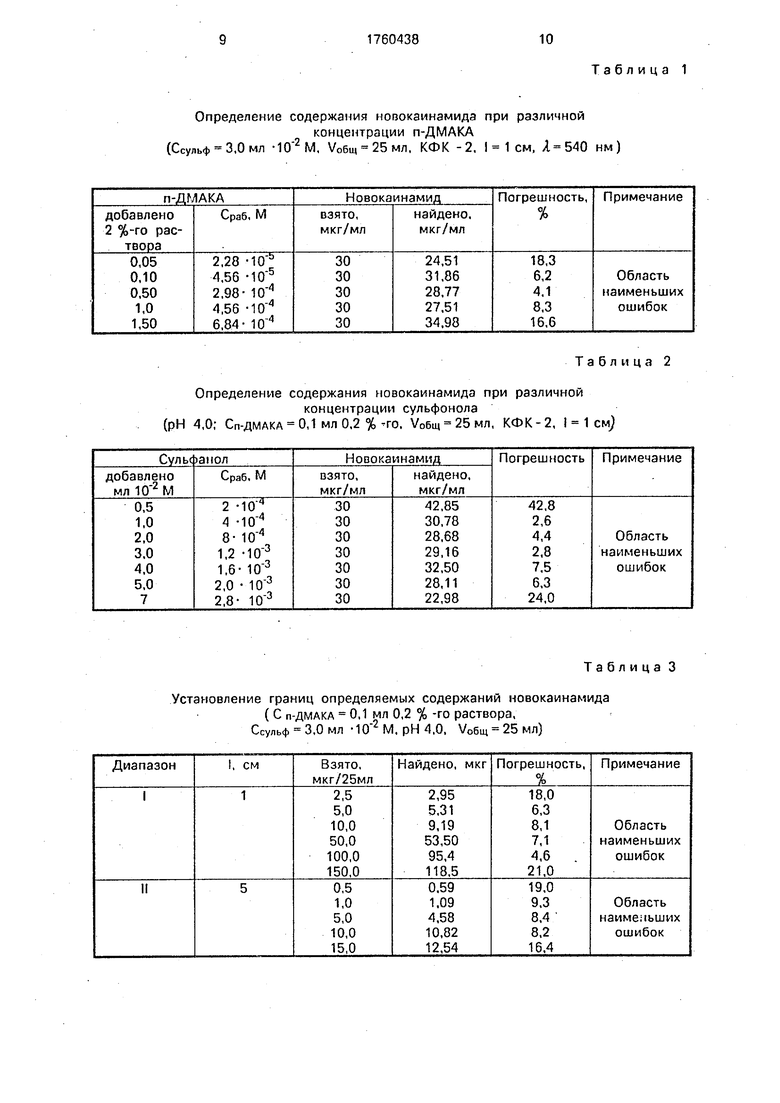
Как следует из данных, представленных в табл.1, наименьшие ошибки определения новокаинамида наблюдаются в интервале концентраций 0,1-1,0 мл 0,2%-ного раствора п-ДМАКА (4,5 М СП-ДМАКА 4,5 10 М).
Установлена оптимальная концентрация сульфонола в реакционной системе. Для этого исследовано п систем, содержащих постоянную концентрацию п-ДМАКА (0,1 мл 0,2%-ного раствора), рН растворов была постоянной, равной 4,0.
Установлено, что концентрация сульфонола в различной смеси должна составлять 4,0- 2,0- М, что достигается при добавлении сульфонола в количестве
1-5 мл М.
Все дальнейшие исследования проводили с растворами следующих концентраций: 0,1 мл 0,2%-ного раствора п-ДМАКА; 3 мл М сульфонола, У0бщ 25 мл.
0 Изучена подчинимость системы новокэ- инамид-п-ДМАКА-сульфоиол закону Бугера- Ламберта-Бера, размах варьирования концентраций составлял 1-100 мкг/25 мл. Установлено, что по предлагаемому способу
5 определения новокаинамида можно находить как большие, так и маленькие концентрации противоаритмического средства. Установлено два определяемых диапазона концентраций новокаинамида.
0 I (большие количества) 5-100мкг/25мл, или 0,2-4,0мкг/мл,
II (маленькие количества) 1- 10мкг/25мл, или 0,04-0,4мкг/мл, 5см Доказательство существования диапа5 зона определяемых содержаний новокаинамида приведено в табл.3.
Анализ данных, представленных в табл.З, показал, что ошибки определения соответствуют фотометрическому методу и
0 не прееышают 10% в интервале 5,0- 100,0мкг/25мл при I 1 см, 1.0- 10,0мкг/25мл при I 5 см.
Нижняя граница диапазона определяемых содержаний новокаинамида - 1
5 мкг/15мл, или 0,04мкг/мл - следовательно, это и может быть принято за предел обнаружения.
В литературе 1 указано, что предел обнаружения по методу-прототипу составляет
0 11мкг/мл, следовательно по предлагаемому способу удалось снизить предел обнаружения в 250 раз.
Изучена зависимость предела обнаружения новокаинамида от рН среды и кон5 центрации реагента, з также третьего компонента (табл.4-6).
Анализ данных, представленных в табл.4-6, показал, что ошибка определения предела обнаружения новокаинамида ми0 нимальна при концентрации п-ДМАКА 4.56Х х 105-4,56 . концентрации сульфонола 4 .0 . рН2-4.
Исследован широкий круг лекарственных препаратов, которые могут быть назна5 чены больным совместно с новокаинамидом.
Соотношение новокаинамида к мешающему компоненту было выбрано 1:1 согласно прописываемой рецептуре в медучреждениях. Как видно из данных.
представленных в табл.7, препараты из груг.п антиаритмические средства (№№ 27- 29), противотуберкулезные средства (№ 12,19-23); антибиотики (№ 25 и 26) и другие препараты широкого спектра деист- вия не оказывают мешающего действия на результаты определения новокаинамида предлагаемым способом. Чрезвычайно важно, что возможно определение новокаинамида в присутствии других антиаритмических средств.
Изобретение иллюстрируется примерами конкретного выполнения.
П р и м е р 1. Построение градуировоч- ной характеристики для количественного фотометрического определения больших количеств новокаинамида.
Точную навеску субстанции сухого препарата новокаинамида (0,0250 г) помещают в мерную колбу вместимостью 25 мл и рас- творяют в дистиллированной воде. Стандартный раствор содержит 1 мг/мл новокаинамида, рабочий раствор содержит 100мкг/мл новокаинамида. Для построения градуировочной характеристики в мерные колбы вместимостью 25 мл помещают по 10-15 мл буферного раствора рН 4,0, затем 0,1 мл (Юмкг), 0,3мл (ЗОмкг), 0,5мл (50мкг), 0,7мл (70мкг), 1,0мл (100мкг) рабочего раствора новокаинамида с С 100мкг/мл, при- бавляют в каждую колбу 0,1мл 0,2%-ного раствора п-ДМАКА и 3 мл М раствора сульфонола и доводят до метки буферным раствором рН 4,0.
Оптические плотности указанных рас- творов измеряли на КФК-2-УХЛ 4,2 в кюветах с толщиной поглощающего слоя I 1 см при А 540 им относительно холостого раствора, в состав которого входят цитратный буферный раствор рН 4,0, 0,1 мл 0,2%-ного раствора п-ДМАКА (4,56-10 5 М) и 3 мл М раствора сульфонола (1.2 М), У0бщ 25 мл.
По полученным значениям оптической плотностью строят зависимость А f(C). За- кон Бугера-Ламбертз-Бера выполняется при концентрации новокаинамида 5-100 мкг/25 мл. или 0,2-4,0 мкг/мл при I 1 см.
П р и м е р 2. Построение градиуропоч- ной характеристики для количественного фотометрического определения малых количеств новокаинамида.
Точную навеску субстанции сухого препарата новокаинамида (0,0250 г) помещают в мерную колбу вместимостью 25 мл и рас- творяют в дистиллированной воде. Стандартный раствор содержит 1 мг/мл новокаинамида, рабочий раствор содержит 10 мкг/мл новокаинамида.
Для построения градуировочной характеристики для малых количеств новокаинамида в колбы на 25 мл вносят по 7-10 мл буферного цитратного раствора рН 4,0, затем 0,1 мл (2 мкг), 0,3 мл(3 мкг), 0.5 мл (5 мкг), 0,7 мл (7 мкг), 1,0мл (10 мкг) раствора новокаинамида с концентрацией 10 мкг/мл. Добавляют по 0,1 мл 0,2%-ного раствора п-ДМАКА и по 3 мл М раствора сульфонола и доводят объем в каждой колбе до метки цитратным буферным раствором рН 4,0. Оптические плотности полученных растворов измеряют на КФК-2-УХЛ4,2 в кюветах с толщиной поглощающего слоя I 5 см при Я 540 нм. Раствор сравнения готовят как в примере 1. По полученным данным оптических плотностей строят зависимость А f(C). Градуировочная характеристика прямолинейна в интервале концентраций 1-10мкг/25мл, или 0,04-0,4 мкг/мл новока- инамидз. Предел обнаружения - 0,04 мкг/мл новокаинамида.
П р и м е р 3. Определение содержания новокаинамида в таблетках.
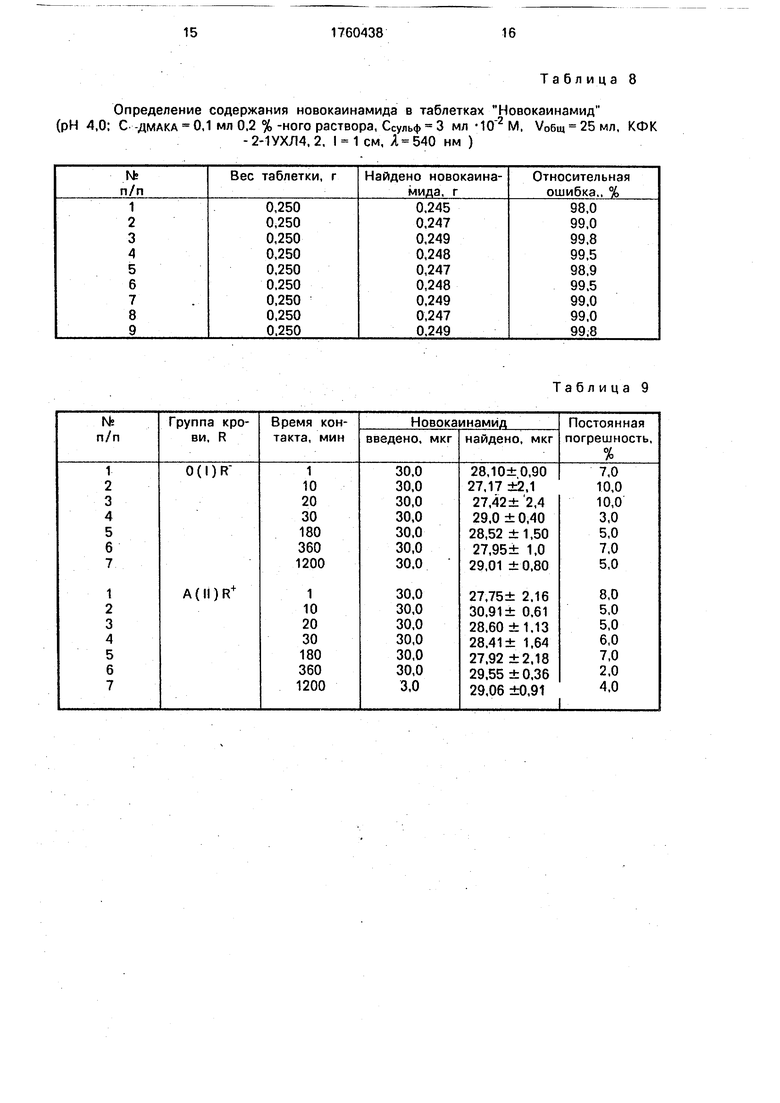
Анализируемые таблетки лекарственных форм тщательно растирают в фарфоровой ступке. Точные навески 0,5000 г количественно переносят в мерные колбы и растворяют в дистиллированной воде. Алик- воты полученных растворов переносят в колбы на 25 мл и далее проводят определение новокаинамида, как в примере 1. Полученные результаты приведены в табл.8,
Анализ данных, представленных в табл.8, позволяет заключить, что предлагаемый способ определения новокаинамида отличается хорошей воспроизводимостью и правильностью.
П р и м е р 4. Определение содержания новокзинамида в донорской крови.
При подготовке крови к анализу белки крови осаждают трихлоруксусной кислотой,
В пробирки вносят по 2 мл крови доноров, добавляют 30 мкг новокаинамида, тщательно перемешивают. Время контакта препарата с кровью варьировали от 1 мин до20ч. После фиксированного времени контакта осаждают белки 2 мл 30%-ной трихлоруксусной кислоты. Смесь перемешивают стеклянной палочкой и центрифугируют 5- 10 мин на центрифуге при скорости 3000 об/мин. Фильтрат сливают в мерные колбы на 25 мл, добавляют к фильтрату 8-10 мл буферного раствора рН 4,0, 0,1 мл 2%-ного раствора п-ДМАКА, 3 мл 10 М раствора сульфонола и доводят до метки буферным раствором. Полученные смеси фотометри- руют по примеру 1. Содержание новокаинамида определяют по градуировочной характеристике. Результаты определения
новокаинамида в донорской крови приведены в табл.9.
Анализ результатов определения новокаинамида в донорской крови позволяет сделать следующие выводы:
Вне зависимости от групповой принадлежности крови и ее резус-фактора возможно определение новокаинамида предлагаемым способом.
Время контакта новокаинамида может быть достаточно длительным, это не влияет на результаты анализа.
По методу введено-найдено показано, что результаты отличаются правильностью и хорошей воспроизводимостью.
П р и м е р 5. Определение содержания новокаинамида в слюне.
При подготовке слюны к анализу белки, входящие в ее состав, осаждают 96%-ным спиртом-ректификатором.
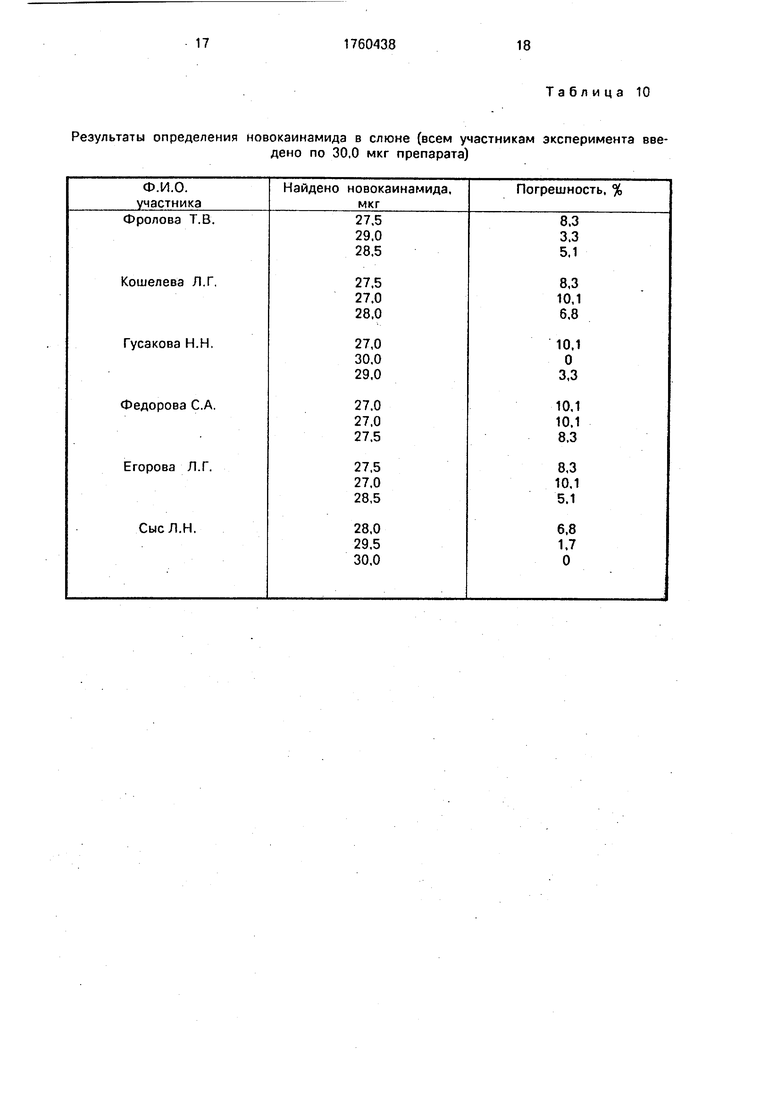
В мерные пробирки собирают слюну испытуемого, центрифугируют в течение 15 мин при скорости 4000 об/мин (для осаждб- ния твердых остатков слюны). Затем добавляют 2 мл осадителл и центрифугируют еще 7-10 мин. Фильтрат переносят количественно в мерные колбы на 25 мл и добавляют к каждому фильтрату по 10-12 мл буферного раствора рН 4,0 по 0,1 мл 0,2%-ного раствора п-ДМАКА и по 3 мл 10J2 М растворах сульфонола. Смеси доводят до метки буфер ным раствором и фотометрируют как указано в примере 1. Результаты определения новокаинамида у случайно выбранных сотрудников приведены в табл. 10. Как следует из представленных данных, ошибка определения новокаинамида не превышает 10%. Определение новокаинамида в слюне является очень перспективным, так как позволяет легко произвести забор анализируемой биологической жидкости, особенно по сравнению с кровью.
Существенным отличием нового способа определения новокаинаммда является проведение реакции новокаинамид-п-ДМА- КА в присутствии сульфонола в среде цит- ратного буферного раствора рН 2-5. Эти два серьезных изменения привели к тому, что удалось, во-первых, снизить значительно предел обнаружения: в 250 раз по сравнению с прототипом; во-вторых, изменить селективность реакции. Новый способ позволяет определять новокаинамид в присутствии других антиаритмических
средств, что особенно важно, а также в присутствии противотуберкулезных препаратов и антибиотиков широкого спектра действия. В-третьих, расширен диапазон определяемых содержаний новокаинамида
(0,04-0,4 мкг/мл; I 5 см; 0,2-4,0 мкг/мл. I 1 см). Предлагаемый способ впервые позволяет определять малые количества новокаинамида (0,04-4 мкг/мл). Кроме того впервые показана возможность определения новокаинамида в крови и слюне, что чрезвычайно важно для определения наилучшего терапевтического эффекта с учетом индивидуальной чувствительности больного и своевременного поддержания эффективной
лечебной концентрации препарата в организме. Данным способом можно определять и большие количества новокаинамида, что может быть использовано в фармацевтическом контроле. Предлагаемый способ
анализа новокаинамида экспрессен, прост, выполняется на серийной отечественной аппаратуре с использованием выпускаемых в СССР органических реагентов и может быть доступен для выполнения в клинических и биохимических лабораториях лечебных учреждений.
В табл.11 приведено сравнение предлагаемого способа с прототипом и базовым объектом.
Формула изобретения Способ количественного определения новокаинамида путем обработки анализируемой пробы органическим реагентом в
кислой среде с последующим фотометриро- ванием раствора, отличающийся тем. что, с целью упрощения способа, повышения чувствительности и селективности определения, в качестве реагента используют
спиртовой раствор п-диметиламиноко- ричного альдегида о количестве 4,5 -4,5 М и обработку ведут в присутствии сульфонола с концентрацией в реакционной
1-3
смеси 4,0 -10-4,0-10 М при рН 2,0-5,0.
Таблица 1






| название | год | авторы | номер документа |
|---|---|---|---|
| Способ количественного определения 0-, м-, п-фенилендиаминов | 1991 |
|
SU1800331A1 |
| Способ количественного определения сульфаниламидных препаратов | 1991 |
|
SU1817008A1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БЕНЗИДИНА И 3,3-ДИМЕТОКСИБЕНЗИДИНА | 1992 |
|
RU2009471C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ О-, М- ИЛИ N-АМИНОБЕНЗОЙНОЙ КИСЛОТЫ | 1991 |
|
RU2011969C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АНИЛИНА И ЕГО МОНОНИТРОПРОИЗВОДНЫХ | 1991 |
|
RU2011968C1 |
| Способ количественного определения п-аминосалициловой кислоты | 1989 |
|
SU1668924A1 |
| Способ количественного определения новокаина | 1987 |
|
SU1529086A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НОВОКАИНАМИДА В ОБЪЕКТАХ БИОЛОГИЧЕСКОГО ПРОИСХОЖДЕНИЯ | 1990 |
|
RU2018113C1 |
| Способ определения спазмолитина | 1986 |
|
SU1352330A1 |
| Способ определения бора | 1990 |
|
SU1797022A1 |
Сущность изобретения: анализируемую пробу обрабатывают спиртовым раствором п-диметиламинокоричного альдегида в количестве 4,5 .5 10 М в присутствии сульфонола с -.-2 концентрацией 4,0 ,0 М при рН 2,0-5,0 с последующим фотометрированием полученного раствора. 11 табл. сл с
Определение содержания новокаинамида при различной
концентрации п-ДМАКА (Ссульф 3,0 мл М, У0бщ 25мл, КФК -2. , нм )
Определение содержания новокаинамида при различной
концентрации сульфонола (рН 4,0; Сп-дМАКА 0,1 мл 0.2 % -го. Уобщ 25мл, КФК-2, I 1 см)
Установление границ определяемых содержаний новокаинамида
( С П-ДМАКА 0,1 мл 0,2 % -го раствора, Ссульф 3,0 мл -10 М. рН 4,0, У0бщ 25мл)
Таблица 2
Таблица 3
Зависимость значения предела обнаружения от концентрации п-ДМАКА ( рН 4,0, ССульф 3 мл -10 М, У0бщ 25мл, I 5 см)
Зависимость значения предела обнаружения новокаинамида от концентрации сульфонола
( СП-ДМАКА 4,56 М ( 0,1 мл 0,2 %-ный раствор). V06in 25 мл. 1 5 см)
Таблица 6
Зависимость значения предела обнаружения новокаинамида
от рН среды (СП-ДМАКА 0,1 мл 0,2%-го раствора), ССульф 3 мл -ЮМ, /общ 25мл, 5см)
Таблица 4
Таблица 5
дминивии Knwiui iv)- орфали/к1ропмлк п) фенотиазина гилрохпоОпределение содержания новокаинэмидз в таблетках (рН 4,0; С -ДМАКА 0,1 мл 0,2 % -ного раствора, Ссульф 3 мл
- 2-1УХЛ4, 2. I 1 см, Я 540 нм )
1
Таблица 8
Новокаинамид
Vo6m 25 мл, КФК
М.
Таблица 9
Результаты определения новокаинамида в слюне (всем участникам эксперимента введено по 30,0 мкг препарата)
Таблица 10
жения
деляемых
реагент
Фотометрический
0,04 мкг/мл, 1 - 5 см
0,,4 мкг/мл, см 0,2-4,0 мкг/мл, см
Цитратный буфер,- рН 2,0-5,0
Не мешают определению другие антиаритмические средства (см. табл. 7)
0,1 мл 0,2%-ного раствора п-диметиламиноко ричного альдегида - 4,5- , сульфонол - 4,0- Ю 2,
Титриметрический
0,1-0,3 г/80 мл Разбавленная UC1
Тропеолии 00 с метиленовым синим
| Буга И.А., Бабилев Ф.В | |||
| Экстракционно- фотометрическое определение новокаина и новокаинамида | |||
| - Фармация, 1973, с.22, М 4, с.42-46 | |||
| Ивахненко П.Н., Чигаренко Л.С., Киля- кова Г.М | |||
| Фотометрическое определение новокаина и новокаинамида | |||
| - Фармация, 1977, с.26 | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Рыжков Ю.Д., Базова Р.П., Пшеничная Д.П | |||
| Экстракционно-фотометрический метод определения новокаинамида | |||
| Методы аналитического контроля окружающей среды, материалы семинара | |||
| М., 1980 | |||
| Рогульчатое веретено | 1922 |
|
SU142A1 |
Авторы
Даты
1992-09-07—Публикация
1990-12-25—Подача