1
(21)4717325/26
(22) 06.07.89
(46)15.10.92. Бюл. №38
(71) Институт катализа СО АН СССР
(72)Л. И. Кузнецова, М. А. Федотов, Э.Н.Юрченко, Л. Г. Детушева и Т. П. Лазаренко
(56)РЖ Химия, 1984, реферат № 18И557П.
(54) СПОСОБ УЛАВЛИВАНИЯ МОНООКСИДА АЗОТА ИЗ ГАЗОВЫХ СМЕСЕЙ
(57)Изобретение относится к технологии мокрого улавливания N0 из газовых смесей, применяемой в химической промышленности и позволяющей повысить эффективность процесса за счет увеличения поглотительной способности раствора и его
стабильности. Газовую смесь, содержащую N0 контактируют с водным раствором комплексного соединения Fe (II). В качестве комплексного соединения используют фер- рито (II) - гетерополивольфраматы натрия, содержащие в качестве гетероатома Р или Si. Концентрация комплекса в растворе 0,01 - 0,25 мол/л, рН раствора 1,45 - 8,6, температура 15 - 80°С. Образуются нитро- зильные комплексы. В присутствии 02 при рН ниже 6 в растворах не образуется осадок Fe (III). Поглотительная способность растворов, содержащих Na5PWiiFe(H20)039, NaaP2Wi7Fe(H20)039, NaeSiWnFe(H20)039, Nai2(PWg034)2 (FeOH2)s, составляет 0,80 - 0,99 мол No/мол Fe при 22°С. 4 табл.

| название | год | авторы | номер документа |
|---|---|---|---|
| Метод количественного определения монооксида азота в газе | 1990 |
|
SU1774250A1 |
| Способ получения смеси ацетатов этиленгликоля | 1977 |
|
SU789506A1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-МЕТИЛ-1,4-НАФТОХИНОНА | 1992 |
|
RU2061669C1 |
| Способ получения акваионов благородных металлов | 1990 |
|
SU1784034A3 |
| Способ получения раствора сульфата титана | 1990 |
|
SU1768516A1 |
| Катализатор для нитрозирования дифениламина в N-нитрозодифениламин | 1990 |
|
SU1695976A1 |
| Способ приготовления катализатора для превращения метанола в диметиловый эфир | 1989 |
|
SU1703172A1 |
| Применение нитрозильного комплекса железа с N,N-диэтилтиомочевиной в качестве нового NO-донорного противоопухолевого средства | 2016 |
|
RU2687269C2 |
| БИЯДЕРНЫЕ НИТРОЗИЛЬНЫЕ КОМПЛЕКСЫ ЖЕЛЕЗА С БЕНЗАЗАГЕТЕРОЦИКЛИЧЕСКИМИ ПРОИЗВОДНЫМИ, СПОСОБ ИХ ПОЛУЧЕНИЯ | 2007 |
|
RU2441872C2 |
| Гомогенный катализатор для окисления окиси углерода | 1981 |
|
SU1027880A1 |

Изобретение относится к способам улавливания N0 из газовых смесей и может найти применение в химической промышленности.
Цель изобретения - повышение эффективности процесса за счет увеличения поглотительной способности раствора и его стабильности.
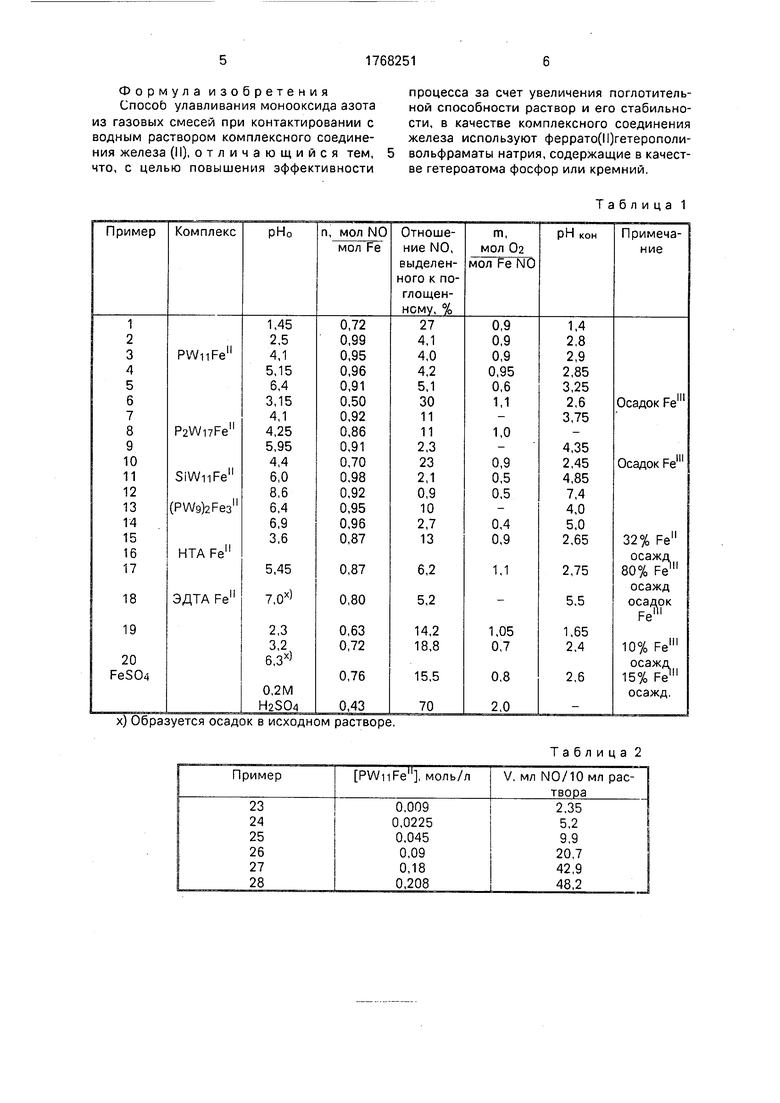
Пример 1.10 мл раствора, содержащего 0,1 М l lasPWiiFe(H20)039 (условное обозначение PWnFe (II)) и эквимолярное количество Na2S04 с начальным значением рНо-1,45 помещают в термостатируемый при 22° реактор типа утка, общий объем которого 80 мл. Систему продувают чистым N0, насыщенным парами воды при той же температуре, герметизируют, затем реактор встряхивают с частотой 400 качаний в минуту. По бюретке измеряют объем поглощенного N0. Поглощение газа завершается за 10 - 15 сек и составляет 17,2 мл. Затем реактор останавливают, удаляют N0 из гасл
С
зовой фазы током аргона, насыщенным парами воды при 22°, вновь герметизируют систему и при встряхивании измеряют объем выделившегося N0. он равен 4 6 мл. Окисление полученного нитрозильного комплекса кислородом проводят в тех же условиях, после продувки системы чистым 02, реакция завершается за 30 мин. при этом образуются НМОз и PWnFe . После завершения реакции конечный рН раствора равен 1.4, осадка нет
Примеры 2-5. Аналогичны примеру 1, но рНо раствора равен 2,5, 4,1; 5 15 6,4, соответственно Полученные характеристики поглотителя приведены в табл 1 Осадки не образуются.
Пример 6. 10 мл раствора, содержащего 0,1 М геторополикомплекса (ГПК) состава NasP2Wi7Fe (Н20)0б1 (P2Wi7Fefl) и Na2S04 с рН0 3,15 испытывают аналогично примеру 1. Результаты даны в табл 1 После реакции с кислородом рН . 6 и из
раствора выпадает осадок, содержащий Fe(lll).
Примеры 7-9. Аналогичны примеру 6, но рН0 растворов равен 4,1; 4,25; 6,4, соответственно. Результаты испытаний даны в табл. 1. Осадки не образуются.
Примеры 10-12, 10 мл раствора, содержащего 0,1 м ГПК состава NaeSiWn Ре(Н20)Озэ (SiWtjFe) с рН . 4,4; 6,0 и 8,6, соответственно, помещают в реактор и испытывают аналогично примеру 1. Полученные результаты даны в табл 1, Осадок Fe(lll) образуется только при рН0 4,4 (пример 10).
Пример 13. 10 мл раствора, содержащего0,05М
Nai2(PWg034)2(FeOH2)3/PWg)2Fe3), через 5 мин после приготовления ГПК по методике 9 помещают в реактор и испытывают аналогично примеру 1. Полученные результаты даны в табл. 1.
Пример 14, 10 мл раствора, содержащего 0,05 М (, через 1 час после приготовления ГПК испытывают аналогично примеру 1. Результаты даны в табл. 1. Осадков нет.
Примеры 15-17. Для сравнения, аналогично примеру 1, испытаны 0,1 М растворы комплекса нитрилотриуксусной кислоты (НТА) с Fe(ll) с рНо 3,5; 5,45 и 7, соответственно. Результаты даны в табл. 1. После взаимодействия с 02 выпадают осадки, содержащие Fe(lll). При рН0 7 (пример 15) образуется осадок в исходном растворе.
Примеры 18- 20. Аналогично примеру 1 испытаны 0,1 М растворы комплекса этилендиаминтетраацетата (ЭДТА) с Fe(ll) с рН0 2,3; 3,2 и 6,3, соответственно. Результаты даны в табл. 1. При рН0 3,2 и 6,3 (примеры 19 и 20) выпадают осадки, содержащие Fe(lll). При рНо 6,3 (пример 20) образуется осадок и в исходном растворе.
Пример 21. 10 мл раствора FeS04, содержащего 0,2 М H2S04, испытаны аналогично примеру 1. Результаты даны в табл. 1.
Пример 22. 10 мл 0,23 М раствора PWnFe 1 с рНо 3, аналогично примеру 1, помещают в реактор, напускают 100% N0, систему герметизируют, встряхивают реактор. Поглощения N0 не наблюдается.
Примеры 23- 28. Растворы с концентрацией ГПК PWnFe, равной 0,009; 0,0225; 0,045; 0,09; 0,18 и 0,208 моль/л, соответственно, и N32S04 с рН0 3 помещают в реактор и аналогично примеру 1 измеряют поглощение N0. Полученные при 25°С результаты даны в табл. 2, где V - объем N0, поглощенный 10 мл раствора.
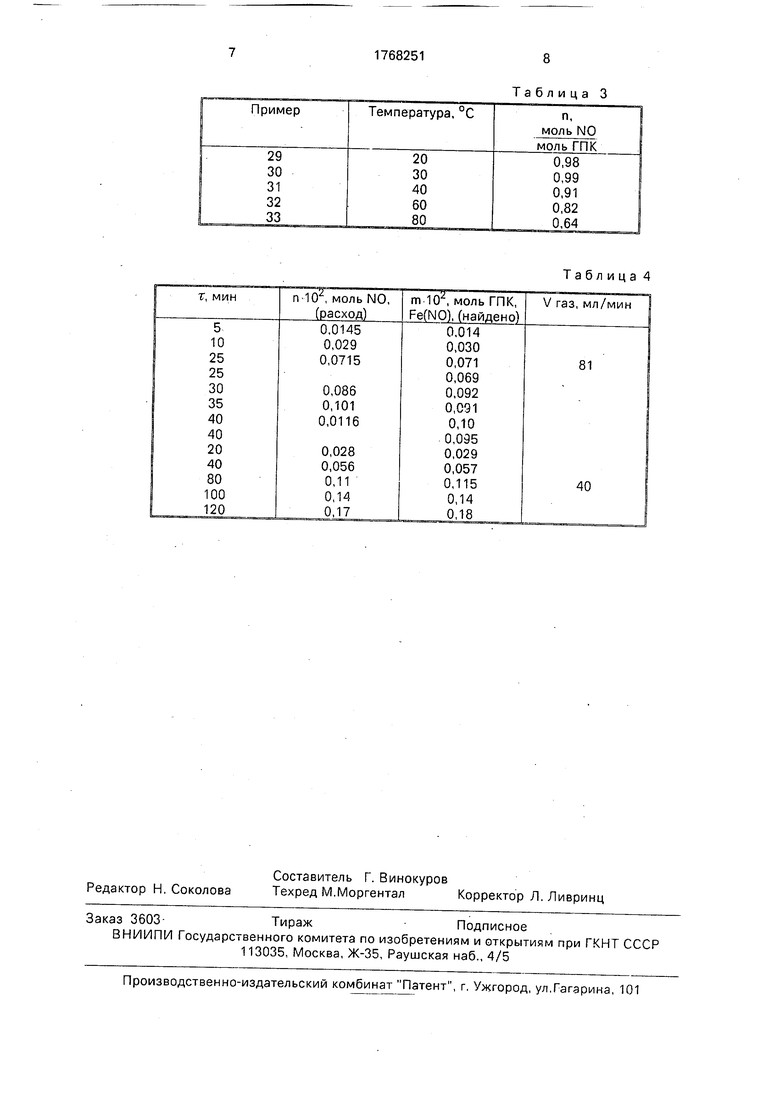
Примеры 29 - 33. По 10 мл 0,08 М PWnFe и №2504 с рН0 2,7 помещают в реактор и аналогично примеру 1 измеряют
количество поглощенного N0 при разных температурах. Результаты измерений даны в табл. 3.
Пример 34. По 10 мл раствора 0,25 М
PWnFe и N32S04 с рН0 4 помещают в реактор объемом 80 мл и встряхивают при 22° с частотой 500 качаний в минуту при пропускании газовой смеси 0,85% N0 + аргон со скоростью 4,85 л/ч в течение 5, 10, 25
и т. д. мин (табл. 4). Количество N0, поглощенное каждой порцией раствора, определяют по концентрации образующегося нитрозильного комплекса спектрофотомет- рически при v 27000 см и сравнивают с
количеством пропущенного через раствор N0. Наблюдается полное поглощение МОдо концентрации образующегося нитрозильного комплекса 0,1 моль/л (табл. 4). Окисление растворов, содержащих
нитрозильный комплекс, кислородом воздуха проходит за 60 мин.
Пример 35. В опытах, аналогичных примеру 34, газовую смесь 0,85% N0 + аргон пропускали со скоростью 2,4 л/ч. При
этом достигается полное поглощение NO до концентрации нитрозильного комплекса 0,2 моль/л (см. табл. 4).
Опыты по взаимодействию ГПК железа (II) с N02 показали, что данный поглотитель
может быть использован и для поглощения N02 в смеси с N0. При этом часть Fe(ll) окисляется в Fe(ll) и протекают следующие реакции:
ГПКРе(П) + N02 + 2H+ -
rnKFe(ll) + NO + H20,
ГПК Fe(ll) + NOit:rnK-Fe(ll)(NO) Поглощенный N0 окисляется кислородом до HN02 и НМОз, Fe(ll) до Fe(lll).
Окисленные растворы ГПК Fe(lll) восста на вливаются действием HiS до исходных комплексов ГПК Fe(ll) с .образованием 5°, чем достигается регенерация поглотителя. Реакция ГПК Fe(lll) с H2S протекает до полного расходования H2S при его напуске
в раствор поглотителя в стехиометрическом отношении Fe(lll) 2. Скорость реакции соизмерима со скоростью растворения
H2S.
Как следует из табл. 1, поглотительная способность растворов при 22°С с использованием ГПК возрастает до 0,80 - 0,99 мол NO/мол Fe против 0,76 мол NO/мол Fe в известном способе с использованием ЭДТА. Fe(ll). При рН растворов ниже 6 в заяв- ленном способе в отличие от известного в области устойчивости лиганда ГПК в присутствии кислорода не образуется осадок, что указывает на повышение стабильности раствора.
Формула изобретения Способ улавливания монооксида азота из газовых смесей при контактировании с водным раствором комплексного соединения железа (II), отличающийся тем, что, с целью повышения эффективности
х) Образуется осадок в исходном растворе.
процесса за счет увеличения поглотительной способности раствор и его стабильности, в качестве комплексного соединения железа используют феррато(П)гетерополи- вольфраматы натрия, содержащие в качестве гетероатома фосфор или кремний.
Таблица 1
Таблица 2
Таблица 3
Таблица 4
Авторы
Даты
1992-10-15—Публикация
1989-07-06—Подача