Изобретение гпногмгсп к области органической химии, в частности к способу получения вещества, обладающего урстротонической активностью на примереспнтетичсского аналога 11-дезо;сси-ПГЕ 3-циг 9-оксо-13-трапс-15- а- окси-Г/ 2-фурил)- 18,19,20-гриьор ПГЕт,
Основным недостатком простатапди- нопых препаратов ййТртся быстрый метаболизм вжйвй/тканях, что ограничивает их
применение в медицине.
СКе лью повышения устойчивости проста гла ди к5вых препаратов их модифицируют, получая различные синтетические аналоги или применяют в виде Ьолее устойчивых лекарственных форм, в чы.гг.оспч, комплексов включения с циклодекстрпнэми
(ЦД).
Применение синтетических модифицированных аналогов ограничивается их высокой токсичностью и нерастворимостью в водных средах, а также малой стабильностью.
Ограничения второго пути использования простагландинов в медицине путем клатратообразования с циклодскстринэми связаны с высокой токсичностью последних, вследствие чего возможно только оральное, ректальное и наружное применение комплексов включения ЦД, Комплексо- образование с ЦД не приводит к повышению биологической активности простагландинов, способ не дает возможность снизить эффективную дозу простагланди- новых препаратов.
Целью изобретения является изыска- ние нового способа повышения устойчивости Тт ростягландиновых препаратов с одновременным повышением утеротопиче- ской активности и снижением эффективной дозы.
Цель достигается тем, что аналог простаг- лан дМна в растворе этанола обрабатывают сапонином мыльного корня (Acamhophyllum дурзорЫ о с е5Рд1(а1 антофиллозид)вд ,1ме- тилсульфоксиде при массовом соотношении 1;4 и комнатной температуре.
Сущность способа заключается в том, что используемый аналог Л Г, 3-цис-9-оксо-13- транс-15 ч -окси-17(2-фурил 18,19,20-три- нор-ПГЕ1 в растворе этанола обрабатывают сапонином из мыльного корня, растворенным в диметилсульфоксиде, при весовом соотношении реагентов 1:4 при комнатной температуре, получая новую лекарственную форму ПГ в виде комплексных соединений с акантофил- лозидом.
Для достижения рабочей концентрации ПГ смесь разбавляется фосфатным буфером.
Получение сапонина (акантофиллозида) из мыльного корил (Acanthophylium gypsophlloides Rgl.).
1,0 кг воздушно-сухих измельченных корней заливают 3,5 л метанола м экстрагируют 2 часа при 70°С. Делают 10 сливов. Сапонин, выпавший из экстракта при осты- пании, отделяют фильтрованием на воронке Бю/нера или Шотта, маточник убирают, а осадок промывают ацетоном {100 мл х 2) и высушивают при комнатной температуре. Маточник концентрируют на роторном испарителе при 40°С до 1/2 объема, выпавший осадок обрабатывают аналогично. Вторичный маточник снова упаривают в тех же условиях до 1 /2-1/3 объема и повторяют операцию обработки осадка,
Биологические испытания ПГ в виде комплексов с сапонином из мыльного корня были проведены в лаборатории новых лекарственных средств Института химии БНЦ УрО АН СССР Обнаружен эффект повышения утеротропной активности исходного ПГ при использовании его в виде новой лекар- стпенпой формы с сапонином из мыльного корня. О
IIГО„Н
2п
ОН (П
Утеротоническую активность 111 (I) в виде новой лекарственной формы изучали по методу Магнуса (in vitro) на изолированной матке крыс и морских свинок в концентрации 1. г/мл, а также методом in situ на наркотизированных-беременных и небеременных морских свинках при внутривенном введении в дозах 10, 50 и 100 мкг/кг. Об утеротонической активности судили по изменению амплитуды и тонуса маточных сокращений в процентах к исходной амплитуде,
В качестве референс-препаратов использовали синтетический ПГ (I) в фосфатном буфере (Na - соль) и известный утеростимулирующий препарат - просте- нон (ПГЕг, Таллинн), применяемый в аку- шерско-гинекологической практике для родостимулирования, а также комплекс ПГ (I) с Р -глицирризиновой кислотой.
Острую токсичность определяли по Лит- чфильду и Уилкоксону на белых беспородных мышах при внутривенном введении.
В результате изучения утеротонической активности ПГ () в комплексе с сапонином и ПГ в буфере методами in vitro и In situ было выявлено, что сапонин повышает утеростимулирующий эффект простагландина, Так, в опытах на изолированной матке крыс и морских свинок ПГ (I) в буфере увеличивает амплитуду сокращений на 76,8-85%, а в комплексе с сапонином тот же ПГ вызывает инотропный эффект на 128-150%, т.е. сапонин увеличивает инотропный эффект ПГ{) в 1,5-2 раза. Простенон в том же разведении повышает СДМ крыс и морских свинок на 55,8-83,8%, соответственно (табл. 1).
Как видно из данных табл. 1, синтетический простагландин (I) в виде комплекса с сапонином из мыльного корня обладает более выраженной утеротропной активностью (изменение амплитуды и тонуса матки) In vitro как на крысах, так и на морских свинках при равной концентрации (1x10 г/мл). Ток- сичность комплексов одинакова.
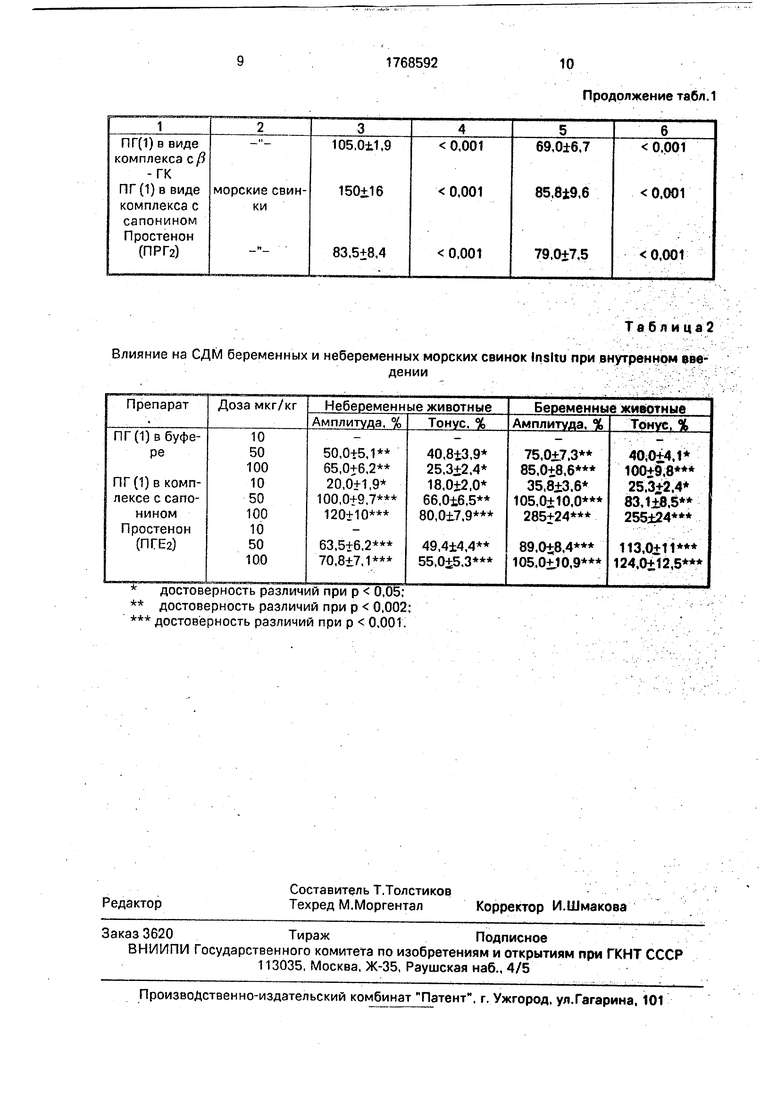
В опытах in situ при внутривенном введении наркотизированным небеременным морским свинкам в дозах 10,50 и 100мкг/кг ПГ в буфере увеличивал амплитуду маточ- ных сокращений на 50-65% в дозах 50 и 100 мкг/кг, а в комплексе с сапонином ПГ проявлял утеротропный эффект в дозе 10 мкг/кг - на 20,0 + 1,9%, в дозах 50 и 100 мкг/кг- на 100% соответственно. Простенон вызывал инотропный эффект в дозах 50 и 100 мкг/кг на 63,5-70,8% (табл. 2). ЕДбО ПГ в буфере составила 50 (60-41,8) мг/кг, ЕДбо комплекса ПГ с сапонином - 23 (27,6-19,9) мг/кг.
В опытах in situ на беременных морских свинках ПГ в буфере увеличивал амплитуду маточных сокращений на 75-85%, а в комплексе с сапонином - на 105-285%. Простенон вызывал инотропный эффект в тех же дозах 50 и 100 мкг/кг на 89,0-105,0%, соответственно.
Токсичность ПГ () не меняется При использовании его в виде новой лекарственной формы - комплекса с сапонином из мыльного корня, LDso ПГ (I) в буфере и в комплексе с сапонином составила 240 (264- 218) мг/кг, LDso простенона 40 (36.7-44,0) мг/кг. ПГ в виде комплекса с сапонином обладает в 2-3 раза более высокой утерото- нической активностью, чем известный уте- ростимулирующий препарат Простенон (ПГЕ2)(табл. 1 и 2).
Таким образом, комплексообразование С акантофиллозидом (сапонином из корней Acanthophyllum gyp.) позволяет, не изменяя токсичности, повысить инотропный эффект простагландина в опытах in vitro в 1,5-2,0 раза, а опытах in situ - в 2-4 раза, а также снизить эффективную дозу (ЕДво) ПГ в сравнении с ПГ в буфере в 2 раза.
Одновременно повышается устойчивость простагландина, поскольку раствор ПГ в присутствии сапонина можно хранить
при комнатной температуре продолжительное время без потери активности (-v 6 мес.).
Сущность изобретения демонстрируется следующими примерами.
Пример 1. Получение простагландина (I) с сапонином из мыльного корня.
К раствору 10мг простагландина в 10 мл этанола добавляют раствор 10-40 мг сапонина (акантофиллозида) из мыльного корня (Acanthophyllum gypsophiloides) в 40 мл перегнанного диметилсульфоксида и смесь перемешивали 1 час. Полученный раствор комплексов ПГ разбавляли фосфатным буфером до необходимой концентрации ПГ.
Для приготовления фосфатного буфера растворяют 8 г NaCI, 800 мг NaH2P04.H20. 12 г NaaHP04.7H20 в 1 л бидистиллята.
Пример 2. Методика исследования утеротонической активности веществ методом in vitro.
Утеротоническую активность синтетичегжг - го аналога 11-дезокси-ПГЕ 1 3-цис-9-оксо-13- транс-15 -а-окси-17(2-фурил)-18,19,20-тринор- -а-простеновой кислоты (I) в буфере и в комплексе с сапонином изучали в оптимальном разведении г/мл на изолированном по Магнусу отрезке рога матки небеременных крыс и морских свинок. Рог матки помещали в аэрируемый термостатируемый раствор Рингер-Локка (состав: NaCI - 9 г, KCI - 400 мг, CaCh - 240 мг, №НСОз 150 мг, глюкоза- 1 г, дистиллированная вода - до 1 л; ). Об утеротонической активности судили по проценту изменения тонуса (тонотропный эффект) и амплитуды (инотроп- ный эффект) маточного сокращения. Эффективность аналога ПГ в буфере и в комплексе с сапонином сравнивали с утерот- ропным эффектом простенона (ПГЕ2 Таллинн), применяемого в акушерско-гине- кологической практике в качестве средству для родостимуляции.
В результате изучения утеротонической активности ПГ в комплексе с сапонином и ПГ в буфере методом in vitro было выявлено, что сапонин повышает утеростимулирую- щий эффект ПГ. Так ПГ в буфере увеличивает амплитуду сокращений матки крыс и морских свинок на 76,8-85,0%, а тонус - на 35,9-50,0%, соответственно. Аналогичный утеротропный эффект вызывает простенон, увеличивая амплитуду сокращений матки крыс и морских свинок на 55,8-83,8%, соответственно. Синтетический аналог 11-де- зокси-ПГЕч в комплексе с сапонином вызывал инотропный эффект на 128-150%, т.е. в 1,5-2 раза больший (табл, 1),
Пример 3. Методика изучения утеротонической активности препаратов In situ.
Утсротрбпаую актийно сть синтетического а i аи о га 11 -де зо ксм:П Г Е t (I) в; буфере и в комплексе с сапонином изучали методом In situ на беременных и нё бё ре мё Шых морских свинках, У лабораторных животных, находящихся под уретгэновым наркозом (1 г/кг, внутрмбрюшинно),.послойно вскрывали брЮшйую полости, выводили петлю рога матки в стаканчик с нагретым физиологичен ским раствором (0,9% р-р NaCI, т-37°С) и фикб й ровали лигатурой k подвижной системе датчика механотрона 6Мх1С. Выходной сигнал мехзнотрона подавали на вход уси- л ителя В Э В С -. А М, выход усилителя сое ди- н ял и; со сходом осциллографа С1-68, регистрацию сократительной деятельности матки осуществляли с помощью потенциометра КСП-4. Об утеротоническойi активности ПГ в буфере и е комплексе с сапонином судили по увеличению амплитуды и тонуса сокращений матки в % к исходной амплитуде. Эффективность ПГ в комплексе с сапонином сравнивали с утеротропной активностью простенона. Препараты вводили внутривенно в дозах 10, 50 и 100 мкг/кг, . В опытах in situ на небеременных морских свинках синтетический аналог ПГ (I) в буфере У оёдим ивал амплитуду маточных со- кращений на 50-65% в дозах 50 и 100 мкг/кг (табл. 2), в комплексе с сапонином ПГ (I) прбйв Ил утёротонические свойства и в дозе 100 мкг/кг- на 20,0 ± 1,9%, а в Дозах 50 И 1Ш мкг/кг -1 и 120%, соотвШтетвЩНо.: ЕДбо ПГ в буфере составила 50(60-41,8) мг/кг/ЁДет ПТ в комплексе с сапонином - 23(27;б-19,9)мг/кг. В опытах in situ на беременных морских свинках ПГ (I) в буфере увеличивал ЗмплИту- ду сокращений матки на 75-85%, а ё комплексе с сапонином - на, 105-285%. Просте- нон в тех же дозах 50 и 100 мкг/к - вызывал инотропный эффект на 89,0-105%, соответственно. Следовательно, комплексообра зование ПГ (Т)с акантофилпозидом - сапонином из мыльного корня увеличивает утеротропный эффект ПГ на небеременных животных в 1,5-2 раза, на беременных - в 3-4 раза.
П р и м е р .4, Методика определения острой токсичности.J
Острую токсичность препаратов опре деляли на беспородных белых мыша х весом
15-18 г при внутривенном вйеденим. Параметры токсичности оценивали по Пйтчфиль- ду и Уилкокрону. ЛДбо nf1 в буфере составила 240(264-218) мкг/кг. Токсичность ПГ (I) в комплексе с сапонином была аналогична ЛДбо ПГ в буфере. ЛДво простенона
составила 40 (36,7-44,0) мг/кг.
Формула изобретения Способ получения; вещества, обладающего у теротоническим действием путем обработки аналога проЬтагландйна
3-цис-9-оксо-13-транс-15 -«-окси-17(2-фурил)-18,19,20-тринор- -«-гомопростеновой
кислоты химическим реагентом, о т л и Ч а.. ю щ и и с я teM, что, с целью повышения
устойчивости вещестйа и активности снижении эффективной дозы аналог про- стагландина обрабатывают бапонином мыльного корня Acanthophyllum Gypsophiloldes Rgl при массовом соотношекии 4:1, причем раствор сапонина И дйме- тилсупьфоксиде добавляют к раствору аналога простагландина в этанйле и перемешивают при комнатной температуре.




| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОСТАГЛАНДИНСОДЕРЖАЩИЙ ПРЕПАРАТ ВЕТЕРИНАРНОГО НАЗНАЧЕНИЯ "КЛАТИРАМ" | 1997 |
|
RU2123336C1 |
| ПРИМЕНЕНИЕ ДОНОРОВ ОКСИДА АЗОТА ИЛИ ИНГИБИТОРОВ ОКСИДА АЗОТА ДЛЯ РЕГУЛИРОВАНИЯ РАСКРЫТИЯ И РАСТЯЖЕНИЯ ШЕЙКИ МАТКИ | 1996 |
|
RU2199346C2 |
| Комплекс глицирризиновой кислоты с 9-оксо-11 @ , 15 @ -дигидрокси-13Е-простеновой кислотой или N-метан-сульфонамидом-16-фенокси-17,18,19,20-тетранорпростагландина Е @ , проявляющий утеротоническую активность | 1988 |
|
SU1566697A1 |
| СПОСОБ СТИМУЛЯЦИИ РАСКРЫТИЯ ШЕЙКИ МАТКИ | 1992 |
|
RU2134588C1 |
| СРЕДСТВО, ПРЕДСТАВЛЯЮЩЕЕ СОБОЙ ЭТИЛОВЫЙ ЭФИР (±)-11,15-ДИДЕЗОКСИ-16-МЕТИЛ-16-ГИДРОКСИПРОСТАГЛАНДИНА E, ПРОЯВЛЯЮЩЕЕ УТЕРОТОНИЧЕСКУЮ АКТИВНОСТЬ | 2009 |
|
RU2394814C1 |
| Средство, представляющее собой этиловый эфир (±)-11,15-дидезокси-16-метил-16-гидроксипростагландина E, проявляющее абортивную активность, оптимально, в сочетании с мифепристоном | 2015 |
|
RU2612005C2 |
| БИОЛОГИЧЕСКИ АКТИВНЫЙ КОМПЛЕКС, ОБЛАДАЮЩИЙ ПРОТИВОАЛЛЕРГИЧЕСКИМ ДЕЙСТВИЕМ | 2012 |
|
RU2493861C1 |
| Способ получения производных 16-амино-18,19,20-тринор-простагландина или их кислотно-аддитивных солей | 1981 |
|
SU1093244A3 |
| СРЕДСТВА, ОБЛАДАЮЩИЕ АНТИАЛЛЕРГИЧЕСКОЙ И ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ ПРИ ПОРАЖЕНИИ КОЖИ НЕМИКРОБНОГО ГЕНЕЗА | 1991 |
|
RU2060731C1 |
| СПОСОБ ПРЕДУПРЕЖДЕНИЯ АНАФИЛАКСИИ У КОРОВ ПРИ ПРИМЕНЕНИИ НАТИВНОЙ СЖК | 1995 |
|
RU2098104C1 |
Изобретение касается простагландин- содержащих вещее гв, в частности вещества на основе 3-цис-9-оксо13-транс-15-о:-окси- 17 (2-фурил)-18,19,20-тринор-а -гомопросте- новой кислоты, обработанной сапониномо мыльного корня Acanthophyilum Gypsophiloides Rgl, обладающей утеротони- ческой активностью. Цель - повышение активности и устойчивости вещества. Синтез ведут обработкой раствора простагландина в этаноле раствором сапонина мыльного корня Acanthophylium Gypsophiloides Rgl в диметил- сульфока.де при массовом соотношении 4:1, перемешивании при комнатной температуре. Соединение проявляет изотопный эффект в 1.5-2 раза выше, чем указанная кислота при эффективной дозе 23 мг/кг, что в 2 раза ниже, чем у кислоты. 2 табл. XI О 00 О1 ю ю
Влияние препаратов на СДМ небеременных крыс и морских свинок в концентрации 1 10
;-7- .: -..- г/мл .-, Г.,.
,Т&б л и ц-а
..... : и ;si «,
,7
Табл и ца2
Влияние на СДМ беременных и небеременных морских свинок Insltu при внутреннем введении
достоверность различий при р 0,05; достоверность различий при р 0,002; достоверность различий при р 0,001.
Продолжение табл.1
| Roberts S.M., Scheinman F | |||
| Chemistry, Biochemistry and Pharmacological Activity of Prostanoids | |||
| New York, Permagon Press, 1979 | |||
| Атжихин И.С | |||
| Простагландины | |||
| M.: Медицина, 1978,415с | |||
| Srantay С., Nova R.L, Synthesis of Prostaglandins | |||
| Bydapest | |||
| Akademia Kiado, 1978 | |||
| Bender M., Komijama | |||
| Cyclodextrin Chemistry | |||
| Speinger - Verlag Berlin, Heidelberg, New York, 1978 | |||
| Szejtei J | |||
| Cyclodextrin and their Inclusion Complexes | |||
| Akademia Ktado, Budapest, 1982 | |||
| Inclusion Compounds | |||
| V | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Physical Properties and Applications Ed | |||
| Atwood J.L, Davis J.E.D., MacNicpl D.D | |||
| Academic Press, London, Orlando, New York, 1984 | |||
| Путиева Ж.М., Мжельская Л.Г„ Кондратенко Е.С | |||
| Абубакиров Н.К | |||
| Тритерпеновые гликозиды Acanthophyilum Gypsophilodies.- Хим | |||
| Прир | |||
| соед | |||
| Кинематографический аппарат | 1923 |
|
SU1970A1 |
| Прибор для автоматического контроля скорости поездов | 1923 |
|
SU486A1 |
| Путиева Ж.М., Мжельская Л.Г., Горобиц Т.Т., Кондратенко Е.С | |||
| Тритерпеновые гликозиды Acanthophyilum gypsophiloides | |||
| III | |||
| Строение 0-гликозидной углеводной цепи акантофиллозидов В и С.- Хим | |||
| прир | |||
| соед | |||
| Сплав для отливки колец для сальниковых набивок | 1922 |
|
SU1975A1 |
| Кулисный парораспределительный механизм | 1920 |
|
SU177A1 |
| Тритерпеновые гликозиды Acanthophyilum Gypsophiloides | |||
| IV | |||
| Строение акантофиллозидов В и С.- Хим | |||
| прир | |||
| соед | |||
| Сплав для отливки колец для сальниковых набивок | 1922 |
|
SU1975A1 |
| ПРИБОР ДЛЯ СОЖИГАНИЯ НЕФТИ | 1922 |
|
SU728A1 |
| Путиева Ж.М., Мжельская Л.Г., Горобиц ТТ., Кондратенко Е.С., Абубакиров Н.К | |||
| Тритерпеновые гликозиды Acanthophylium Gypsophiloides V | |||
| Д - хиновоза в акантофил- лозидах В и С | |||
| - хим | |||
| прир | |||
| соед | |||
| Шеститрубный элемент пароперегревателя в жаровых трубках | 1918 |
|
SU1977A1 |
| Водоподъемный аппарат | 1923 |
|
SU806A1 |
| Путиева Ж.М., Горобиц Т.Т., Кондратенко Е.С., Абубакиров Н.К | |||
| Тритерпеновые гликозиды Acanthophylium Gypsophiloides | |||
| VI | |||
| Строение акантофиллозида Д.-Хим | |||
| прир | |||
| соед., 1979, № 2, с | |||
| Приспособление для удаления таянием снега с железнодорожных путей | 1920 |
|
SU176A1 |
| Авторское свидетельство СССР № 1702642, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1992-10-15—Публикация
1990-02-05—Подача