Изобретение относится к области химии комплексных соединений и может быть использовано для синтеза гидридотрис(три- фенилфосфин)карбонилродия(1)
НРЬ(РРЬз)з(СО), обладающего высокой каталитической активностью в реакциях гидроформилирования, гидросилилирования, гидрирования и изомеризации олефинов.
Известен способ получения HRtyPPhaMCO) взаимодействием трихлори- да родия с водным формальдегидом и бор- гидридом натрия в присутствии избытка трифенилфосфита (РРпз) в среде этанола п ри температуре его кипения. После окончания реакции смесь охлаждается до комнатной температуры, осадок отделяется фильтрованием, промывается этанолом и водой. Высушивается в вакууме. Выход: 96%.
Известен способ получения НКп(РРЬз)з(СО) взаимодействием трихлори- да родия с водным раствором формальдегида и гидроксидом калия в присутствии избытка трифенилфосфина в среде этанола при температуре его кипения. После окончания реакции смесь охлаждается до комнатной температуры, осадок отделяется фильтрованием, промывается этанолом и водой, высушивается в вакууме. Выход: 93%.
Известен способ получения ННН(РРпз)з(СО) взаимодействием трихлори- да родия с оксидом углерода, гидроксидом калия и водородом в присутствии избытка трифенилфосфина в среде алифатического спирта при температуре его кипения в атмосфере оксида углерода с последующей заменой его на водород в течение 3-4 ч.
VI VI 00
00
После окончания реакции горячий раствор профильтровывается, осадок промывается этанолом, водой, высушивается в вакууме. Выход: 90%.
Известен способ получения (РРЬз)з(СО) взаимодействием карбонил- содержащего соединения родия - Rh(PPh3)a(CO)CI с бутанолом и гидроксидом калия в присутствии избытка трифенилфос- фина в среде бутанола при температуре его кипения (116°С) в атмосфере оксида углерода. После окончания реакции раствор охлаждается, добавляется вода для растворения образовавшегося неидентифицированного белого осадка, продукт отфильтровывается, промывается метанолом и высушивается в вакууме. Выход: 90%.
Наиболее близким техническим решением, выбранным в качестве прототипа, является способ получения НРЬ(РРпз)з(СО) взаимодействием карбонилсодержащего соединения родия - Rh(PPh3)2(CO)CI с бор- гидридом натрия в присутствии избытка трифенилфосфина в среде алифатического спирта в атмосфере оксида углерода в течение 1-10 ч. После окончания реакции реакционная смесь охлаждается в атмосфере оксида углерода до 25°С. Осадок отфильтровывается, промывается этанолом и водой, высушивается в вакууме. Выходг99%.
Недостатки способа:
1.Все операции проводятся в атмосфере токсичного оксида углерода. В присутствии СО, как известно, (D.Evans, G.Vaqupsky, G.WIIklnson, J.Chem. Soc. (A), 2660, 1968) комплекс НЯп(РРпз)з(СО) превращается в Rh(PPh3)2(CO) и HRr,(PPh3)3(CO)2. При удалении СО первый из них превращается в Рл(РРпз)з(СО)2, что приводит к загрязнению целевого продукта. Кроме того, в HRh(PPh3)3(CO),полученном из Rh(PPhs)2(CO)CI, присутствует исходный комплекс,
2.Так как процесс идет при температуре кипения спирта, реакционную смесь необходимо охлаждать перед фильтрованием, что усложняет процесс и увеличивает его продолжительность.
Целью предполагаемого изобретения является повышение качества целевого продукта и упрощение способа.
Поставленная цель достигается тем, что в известном способе получения HRh(PPhs)3(CO) взаимодействием карбонилсодержащего соединения родия с бор- гидридом натрия в присутствии трифенилфосфина в инертной атмосфере в среде алифатического спирта при нагревании, отмывкой полученного продукта последовательно алифатическим спиртом и водой
и сушкой его в качестве карбонилсодержащего соединения родия используют ацети- лацетонатотрифенилфосфинкарбонил родий (1), RhAcac(PPh3KCO)J, или ацетилацетонатодикарбонилродий (1), RhAcac(CO)2, и процесс ведут при температуре 35-45°С.
Сущность предлагаемого способа состоит в следующем. К раствору трифенилфосфина (PPrts) в алифатическом спирте
(этаноле, бутаноле, метаноле) добавляются ацетилацетонатные карбонильные комплексы родия, RhAcac(PPh3)(CO) или RhAcac(CO)2 (ТУ 6-09-05-74-74) при мольном отношении PPh3:Rh от 3:1 до 6:1, реакционная смесь перемешивается, к ней добавляется раствор боргидрида натрия (NaBH/i) в алифатическом спирте в мольном отношении NaBH4 : Rh от 5:1 до 6:1. Смесь перемешивается 30 - 60 мин при температуре
35-45°С. Осадок отделяется фильтрованием, промывается этанолом и водой, высушивается в вакууме, Все операции проводятся в атмосфере аргона.
Чистота продукта контролируется элемечтным анализом и измерением ИК и 31Р ЯМР спектров. ИК спектры растворов комплексов в толуоле измерялись на спектрометре Specord кюветы из CaF2, толщина поглощающего слоя 0,01 см; 31Р
ЯМР спектры растворов комплексов в толуоле измерялись на спектрометре Bruker AM 500 при частоте 202,46 Гц в импульсном режиме. Величину химических сдвигов отсчитывали от сигнала внутреннего стандарта - трибутилфосфата (0,45 м.д. относительно 85% НзРО/j).
П р и м е р 1. Получение HRh(PPh3b(CO) осуществляют в атмосфере аргона. К раствору 4,1 г (15,6 ммоль) трифенилфосфина в
150 мл этанола добавляют 1,0 г (3,9 ммоль) RhAcac(CO)a (мольное отношение РРНз : Rh 4 : 1). Реакционную смесь перемешивают при 35°С в течение 1 час. При этом образуется желтая суспензия. Затем добавляют
раствор 0,74 г (19.5 ммоль) боргидрида натрия в 40 мл этанола (мольное отношение NaBH4 : Rh 15 : 1). Реакционную смесь перемешивают в течение 1 ч, отфильтровывают осадок. Осадок промывают этанолом и
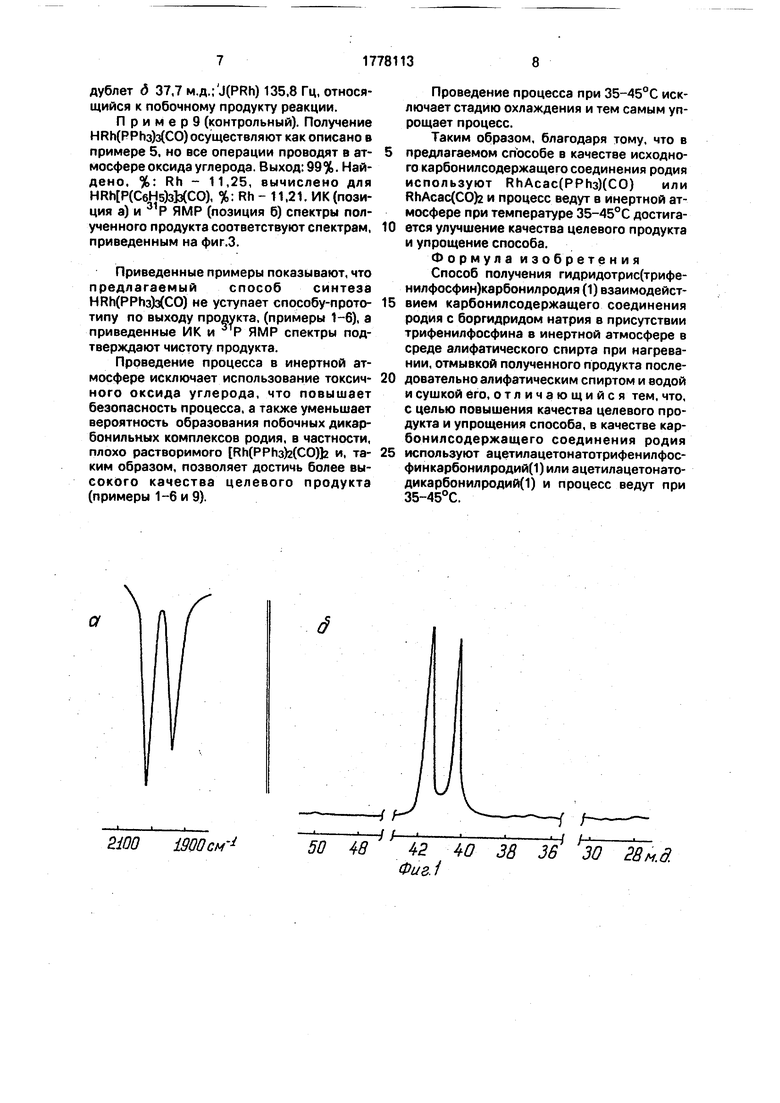
водой, затем высушивают в вакууме. Выход: 3.51 г (99%). Найдено, %: Rh - 11,18; вычислено для (C6H5bWCO), %: Rh- 11,21. На фиг.1 приведены спектры ИК (позиция а) и 31Р ЯМР (позиция б) полученного
продукта. В ИК спектре раствора HRh(PPh3MCO) в толуоле присутствуют две полосы поглощения: полоса валентных колебаний карбонильной группы v(CO) 1920 см и полоса, характеризующая валентные
колебания гидридного лиганда v( (RhH) 2003 .
В спектре 31Р ЯМР раствора HRh(PPh3)3(CO) в толуоле присутствует дублет с химическим сдвигом д 40,8 м.д.; кон- станта спин-спинового взаимодействия j(PRh) 154,2 Гц.
Пример2. Получение ННЬ(РРЬз)з(СО) осуществляют как описано в примере 1, но изменяют мольные отношения РРпз : Rh на 5 :1 и NaBhU: Rh на 6 : 1. Реакцию проводят в бутаноле при температуре 40°С. Выход: 99%. ИК и 31Р ЯМР спектры соответствуют спектрам, приведенным на фигуре 1.
ПримерЗ. Получение НРЬ(РРпз)з(СО) осуществляют как описано в примере 1, но изменяют мольные отношения РРЬз : Rh на 6:1 и NaBhU : Rh на б : 1. Взаимодействие проводят в этаноле при температуре 45°С. Выход: 99%. ИК и 31Р ЯМР спектры соответ- ствуют спектрам, приведенным на фиг. 1.
П р и м е р 4. Получение HRh(PPh3b(CO) осуществляют в атмосфере аргона. К раствору 1,5 г (6 ммоль) трифенилфосфина в 25 мл этанола добавляют 1 г (2 ммоль) RhAcac(PPh3)(CO) (мольное отношение PPhy : Rh 3 : 1). Реакционную смесь перемешивают при 35°С в течение 15 мин. Затем добавляют раствор 0,38 г (10 ммоль) боргидрида нтрия в 40 мл этанола (мольное отношение NaBH : Rh 5 : 1). Реакционную смесь перемешивают еще 30 мин. Осадок отфильтровывают, промывают этанолом, водой, высушивают в вакууме. Выход: 1,84 г (99%). Найдено, %: Rh - 11,20; вычислено для НРп РСбН5)(СО), %: Rh - 11,21. ИК и Р ЯМР спектры соответствуют спектрам, приведенным на фиг. 1.
П р и м е р 5. Получение HRh(PPh3)3(CO) осуществляют как описано в примере 4, но изменяют мольные отношения РРпз : Rh на 5 : 1 и NaBH4 : Rh на 6 : 1. Взаимодействие проводят в метаноле при температуре 40°С. Выход: 99% ИК и 31Р ЯМР спектры соответствуют спектрам, приведенным на фиг.1.
П р и м е р 6. Получение HRh(PPhs)3(CO) осуществляют как описано в примере 4, но изменяют мольные отношения PPhs : Rh на 4,5:1 и МаВЩ: Rh на 6 : 1. Взаимодействие проводят в бутаноле при температуре 45°С. Выход: 99%. ИК и 31Р ЯМР спектры соответствуют спектрам, приведенным на фиг.1.
Приме р7(контрольный по прототипу), Все операции проводят в атмосфере оксида углерода, растворитель и промывные жид- кости предварительно насыщают оксидом углерода.
К раствору 1,5 г (5,7 ммоль) трифенилфосфина в 75 мл этанола добавляют 1,0 г
(1,45 ммоль) Rh(PPrn)2(CO)CI. Смесь нагревают при перемешивании до температуры кипения (80°С). По каплям добавляют раствор 0,5 г (12 ммоль) боргидрида натрия в 55 мл этанола. Время реакции 8 ч. Реакционную смесь охлаждают до комнатной температуры в атмосфере оксида углерода. Осадок отделяют фильтрованием, промывают этанолом и водой, высушивают в вакууме. Выход: 1,3 г (98%). Найдено, %: Rh - 11,30; вычислено для HRhfPfCeHsbMCO), %: Rh - 11,21. Качественно определено (спекание с содой) наличие следов хлора в комплексе. ИК (позиция а) и Р ЯМР (позиция б) спектры полученного продукта приведены на фиг.2. ИК спектр: наряду с полосами поглощения V (СО) 1920 и v (RhH) 2003 , характерными для HRh(PPh3)s(CO) в спектре присутствует поглощение в области 1960- 1970см , присущее как исходному комплексу Ph(PPh3MCO)CI, так и побочному продукту Rh(PPhs)2(CO). 31P ЯМР спектр: наряду с дублетом д 40,8 м.д.; J(PRh) 154,2 Гц, характерным для HRh(PPh3b(CO), в спектре присутствуют дополнительные сигналы: дублет д 29,0 м.д.; j(PRh) 129,9 Гц, принадлежащий исходному комплексу Rh(PPh3)2(CO)CI и дублет 6 37,2 м.д.: J(PRh) 135.8 Гц. принадлежащий побочному продукту реакции.
Количество примесей согласно спектроскопическим данным составляет 5 - 10%.
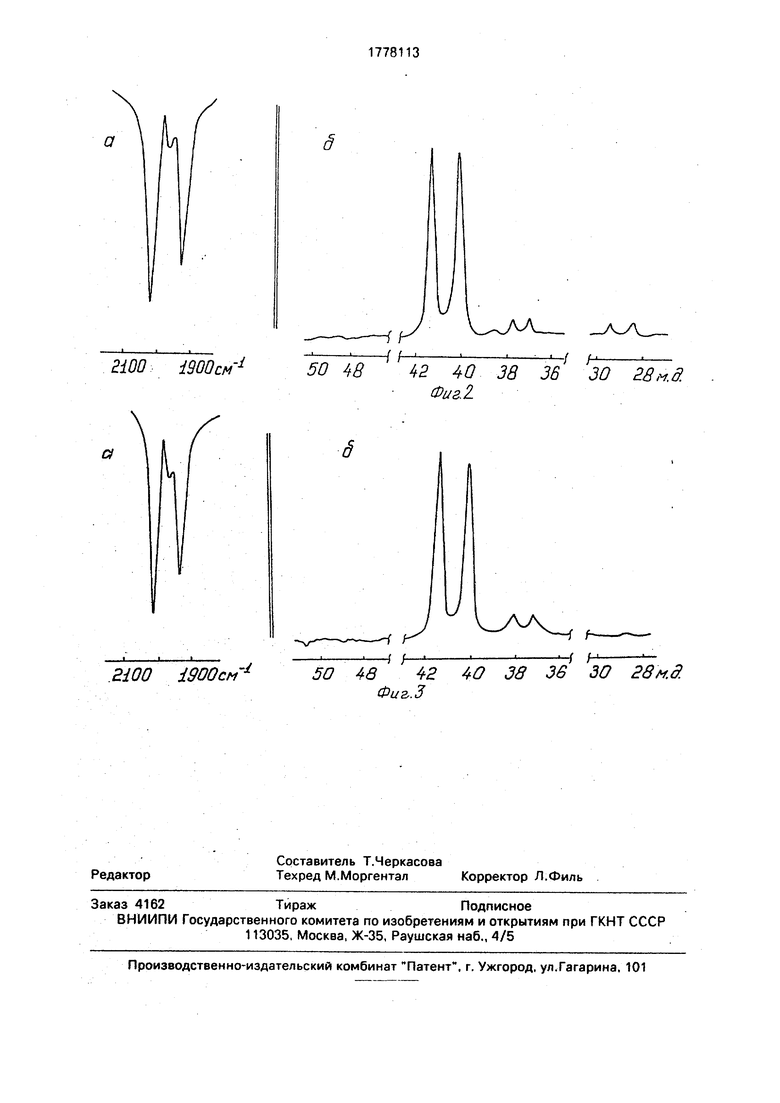
П р и м е р 8 (контрольный). Все операции проводят в атмосфере оксида углерода. К раствору 1,5 г (5,7 ммоль) трифенилфосфина в 75 мл этанола добавляют 6,7 г (1,4 ммоль) RhAcac(PPh3)(CO). Смесь нагревают при перемешивании до температуры кипения (80°С). По каплям добавляют 0,5 г (12 ммоль) боргидрида натрия в 55 мл этанола. Реакцию проводят в течение 8 ч. Реакционную смесь охлаждают до комнатной температуры в атмосфере оксида углерода. Осадок отделяют фильтрованием, промывают этанолом и водой, высушивают в вакууме. Выход: 0,91 г (98%). Найдено, %: Rh - 11,32, вычислено для (CfiH5)3b(CO), %: Rh- 11,21. ИК (позиция а)и31Р ЯМР (позиция б) спектры полученного продукта приведены на фигуре 3. И К спектр: наряду с полосами поглощения v (СО) 1920 и (RhH) 2003 , характерными для HRh(PPhs)3(CO), в спектре присутствует поглощение в области 1960-1965 , указывающее на наличие в продукте примесей, в частности, побочного продукта реакции Rh(PPh3b(CO)2. 31Р ЯМР спектр: наряду с дублетом д 40,8 м.д.; J(PRh) 154,2 Гц. характерным для HRh(PPh3b(CO). присутствует
дублет д 37,7 M.fl.; j(PRh) 135,8 Гц, относящийся к побочному продукту реакции.
П р и м е р 9 (контрольный). Получение НРИ(РРЬз)з(СО) осуществляют как описано в примере 5, но все операции проводят в ат- мосфере оксида углерода. Выход: 99%. Найдено, %: Rh - 11,25, вычислено для (C6H5)(CO), %: Rh - 11,21. ИК (позиция а) и 31Р ЯМР (позиция б) спектры полученного продукта соответствуют спектрам, приведенным на фиг.З.
Приведенные примеры показывают, что предлагаемый способ синтеза НВп(РРпз)з(СО) не уступает способу-прото- типу по выходу продукта, (примеры 1-6), а приведенные ИК и Р ЯМР спектры подтверждают чистоту продукта.
Проведение процесса в инертной атмосфере исключает использование токсич- ного оксида углерода, что повышает безопасность процесса, а также уменьшает вероятность образования побочных дикэр- бонильных комплексов родия, в частности, плохо растворимого Rh(PPti3)2(CO)2 и, та- ким образом, позволяет достичь более высокого качества целевого продукта (примеры 1-6 и 9).
Проведение процесса при 35-45°С исключает стадию охлаждения и тем самым упрощает процесс.
Таким образом, благодаря тому, что в предлагаемом способе в качестве исходного карбонилсодержащего соединения родия используют RhAcac(PPh3)(CO) или RhAcac(CO)2 и процесс ведут в инертной атмосфере при температуре 35-45°С достигается улучшение качества целевого продукта и упрощение способа.
Формула изобретения
Способ получения гидридотрис(трифе- нилфосфин)карбонилродия (1) взаимодействием карбонилсодержащего соединения родия с боргидридом натрия в присутствии трифенилфосфина в инертной атмосфере в среде алифатического спирта при нагревании, отмывкой полученного продукта последовательно алифатическим спиртом и водой и сушкой его, отличающийся тем, что, с целью повышения качества целевого продукта и упрощения способа, в качестве карбонилсодержащего соединения родия используют ацетилацетонатотрифенилфос- финкарбонилродий(1) или ацетилацетонато- дикарбонилродий(1) и процесс ведут при 35-45°С.


| название | год | авторы | номер документа |
|---|---|---|---|
| ГИДРИД-КАРБОНИЛЬНЫЙ ПОЛИФОСФИТНЫЙ КОМПЛЕКС РОДИЯ СО СМЕШАННЫМИ ФОСФОРОРГАНИЧЕСКИМИ ЛИГАНДАМИ ДЛЯ КАТАЛИЗА ПРОЦЕССА ГИДРОФОРМИЛИРОВАНИЯ ОЛЕФИНОВ | 2015 |
|
RU2584952C1 |
| Способ получения альдегидов | 1988 |
|
SU1801106A3 |
| Способ получения комплексного родиевого соединения | 1983 |
|
SU1709913A3 |
| СПОСОБ НЕПРЕРЫВНОГО ГИДРОФОРМИЛИРОВАНИЯ ОЛЕФИНОВ С-С В АЛЬДЕГИДЫ | 2014 |
|
RU2562971C1 |
| КАТАЛИЗАТОР ГИДРОФОРМИЛИРОВАНИЯ ОЛЕФИНОВ C-C, СПОСОБ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ) И СПОСОБ ПОЛУЧЕНИЯ АЛЬДЕГИДОВ C-C | 2007 |
|
RU2352552C1 |
| Способ получения комплексных родиевых катализаторов | 1982 |
|
SU1722230A3 |
| СПОСОБ ФУНКЦИОНАЛИЗАЦИИ ПОЛИОЛОВ ПУТЕМ ТАНДЕМНОЙ РЕАКЦИИ ГИДРОФОРМИЛИРОВАНИЯ-АЦЕТАЛИЗАЦИИ С ПРИМЕНЕНИЕМ ВОДОРАСТВОРИМОЙ КАТАЛИТИЧЕСКОЙ СИСТЕМЫ | 2018 |
|
RU2708256C1 |
| Родийсодержащие гетерогенные катализаторы для процессов получения пропаналя и диэтилкетона гидроформилированием этилена | 2018 |
|
RU2711579C1 |
| СПОСОБ НЕПРЕРЫВНОГО ГИДРОФОРМИЛИРОВАНИЯ ОЛЕФИНОВ C-C | 2015 |
|
RU2585285C1 |
| ФОСФИНСОДЕРЖАЩИЕ КАЛИКСАРЕНОВЫЕ ЛИГАНДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2016 |
|
RU2646763C1 |

Изобретение относится к металлооргани- ческим соединениям, в частности к новому способу получения гидридотриф-рифенил- фосфин)карбонилродия (1), который может быть использован в качестве катализатора гидроформилирования, гидрирования, гидро- силилирования и изомеризации олефинов. Цель - повышение качества целевого продукта и упрощение способа. Синтез ведут взаимодействием трифенилфосфина с солью родия-ацетилацетонато(трифенилфосфин) карбонил родием (1) или ацетилацетонатоди- карбонилродием (1) в алифатическом спирте при 3§-45°C с последующим добавлением NaBH4. Выход99%.Зил. i ( Ј
а
то то см 1
f- /
36 30 28м.д.
д
В100 1900см-1
50 48
а
.2100 1900см-1
ч h
50 48 42 Фиг.З
42 40 38
Фиг.2.
-( Р
36 30 28 пи
Ч
4О 38 36 30 28м.д.
| J.J.Levlson, S.D.Robinson, J.Chem | |||
| Soc (A), 1970, Nsl 1, p | |||
| Жатвенная машина | 1925 |
|
SU2947A1 |
| Руководство по неорганическому синтезу, Под ред | |||
| Г.Брауэра, т.6, стр | |||
| Сцепление с поворотной шпонкой | 1925 |
|
SU2086A1 |
| М.: Мир, 1986 | |||
| Патент США № 3644446 | |||
| кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Патент США № 4277414, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1992-11-30—Публикация
1990-06-29—Подача