Предлагаемое изобретение относится к химической отрасли и касается получения нитритов щелочных металлов путем поглощения горячих окислов азота раствором водного основания или солей этих металлов.
Известны способы получения неорганических нитритов 1 с низким содержанием соответствующих нитритов. Способ заключается в контактировании газообразной смеси, содержащей окислы азота, в состоянии окисления менее 70% с водным раствором основания с катионами аммония, щелочного или щелочноземельного металлов. Обычно способ проводят в две стадии. На первой - концентрированный раствор основания контактирует с концентрированной газообразной смесью Было установлено, что соотношение нитрита к нитрату на второй стадии увеличивается в том случае, когда концентрация окислов газообразной смеси значительно уменьшается по мере уменьшения концентрации основания. Это достигается добавлением к газовой смеси газа-разбавителя.
Недостатком указанного способа является большое содержание (9-13%) щелочного компонента в готовом продукте.
Известен также способ получения нитритов, включающий ступени образования смеси горячего газа, содержащей окислы азота, кислород и водяной пар; охлаждение смеси газа до температуры 300-500 С и мгновенное охлаждение Такой газовой смеси в водном растворе основания для избежания контакта горячей смеси газа с холодной поверхностью. Такая операция позволяет избежать конденсации водяного пара и соответственно образования нитратов.
Полученный товарный продукт содержит до 40 мае, % нитрита натрия, 0,1-3,0 мае. % нитрата натрия, 9-10 мае. % гидроокиси натрия, 0,5 мае. % карбоната натрия и 50-60 мае. % воды. Скорость подачи газа 90 кг/ч, а жидкости - 40-70 кг/г.
К недостаткам данного способа следует отнести:
-большое содержание в товарном продукте щелочного компонента (МО мае. %),
-невозможность получения готового продукта в кристаллическом виде с малым содержанием нитрата без многократной перекристаллизации.
(Л
С
vj
00
о
4
Целью способа является снижение содержания щелочного компонента в продукте.
Способ осуществляется следующим образом. Нитрозный газ, полученный окисле- нием аммиака состава, об. %: N0 - 5,9; МОа - 3,9; Oi - 3,6; N2 - 69,8; Н20 - 16,8, с температурой 385-415°С по трубопроводу 2 подают в нижнюю часть колонны 1 через распределитель 4.
Свежий раствор карбоната натрия концентрацией 260-340 г/л и температурой 90°С по трубопроводу 3 также подают в нижнюю часть колонны 1. В нижней части колонны под тарелкой 5 осуществляется ос- новной процесс взаимодействия горячих нитрозных газов с раствором соды по реакциям:
N0 + N02 + Ма2СОз 2NaN02 + C02 (1)
2N02 + МаСОз NaN02 + NaNOs + C02 (2)
В указанной секции проходит основной процесс взаимодействия на 86-90% всех реагирующих компонентов. Здесь же обра- зуется основное количество нитрита натрия 88-91%. Остальное количество карбоната натрия срабатывается на вышележащих тарелках.
Контактные устройства, принятые в данном предложении, работают при относительно высоких скоростях газа и жидкости в отверстиях тарелки - инжекционный режим.
Такой режим обеспечивает наиболее интенсивный процесс массообмена и исключает явление провала жидкости на нижележащие тарелки.
При инжекционном режиме осуществляется интенсивный захват и дробление жидкости, формируется динамический двухфазный слой, в котором сплошная фаза - газ, а дисперсная - жидкость.
В слое появляются сплошные газовые каналы, которые активно транспортируют жидкость в сепарационное пространство между тарелками.
В данном процессе, обеспечение исключения провала жидкости на нижележащие тарелки, играет важную роль, так как препятствует перемешиванию жидкой фазы по высоте колонны.
В секции между тарелками должен быть определенный состав раствора и срабаты- ваться определенное количество щелочи и окислов азота с нитрозных газов. Под первой тарелкой содержание щелочи 6-7% вес. на последней тарелке (продукционном растворе) 0,5% вес.
Отвод реакционного и физического тепла нитрозных газов осуществляется принудительной циркуляцией по схеме: линия 12, насос 13, линия 14, холодильник 15, линия 18. Охлаждение осуществляется водой, поступающей по линии 17 и отводящей линии 16.
Процесс прямотока жидкой и газовой фаз осуществляют в колонне 1 с затопленным слоем с сетчатыми тарелками (не менее 3), обеспечивающим движение жидкой фазы снизу вверх.
Смесь нитрозного газа и раствора соды проходит все тарелки, С восьмой тарелки непрореагировавший нитрозный газ по трубопроводу 10 поступает в колонну кислой абсорбции на получение азотной кислоты. Полученный раствор нитрит-нитрата натрия по трубопроводу 11 подают на дальнейшую переработку для получения кристаллического товарного продукта.
При соотношении скоростей газа в отверстиях тарелки и свободном сечении колонны ниже 15 может осуществляться переток жидкой фазы с верхнележащей на нижележащую тарелку, что приводит к нарушению содержания соды в растворе. В колонне начинается процесс инверсии, что не позволяет получить необходимое соотношение NaNOa/NaNOa в конечном продукте.
При соотношении скоростей газа в отверстиях тарелки и свободном сечении колонны выше 35 создается сопротивление в 8-10 раз выше, чем требуется для нормального прохождения газа через колонну.
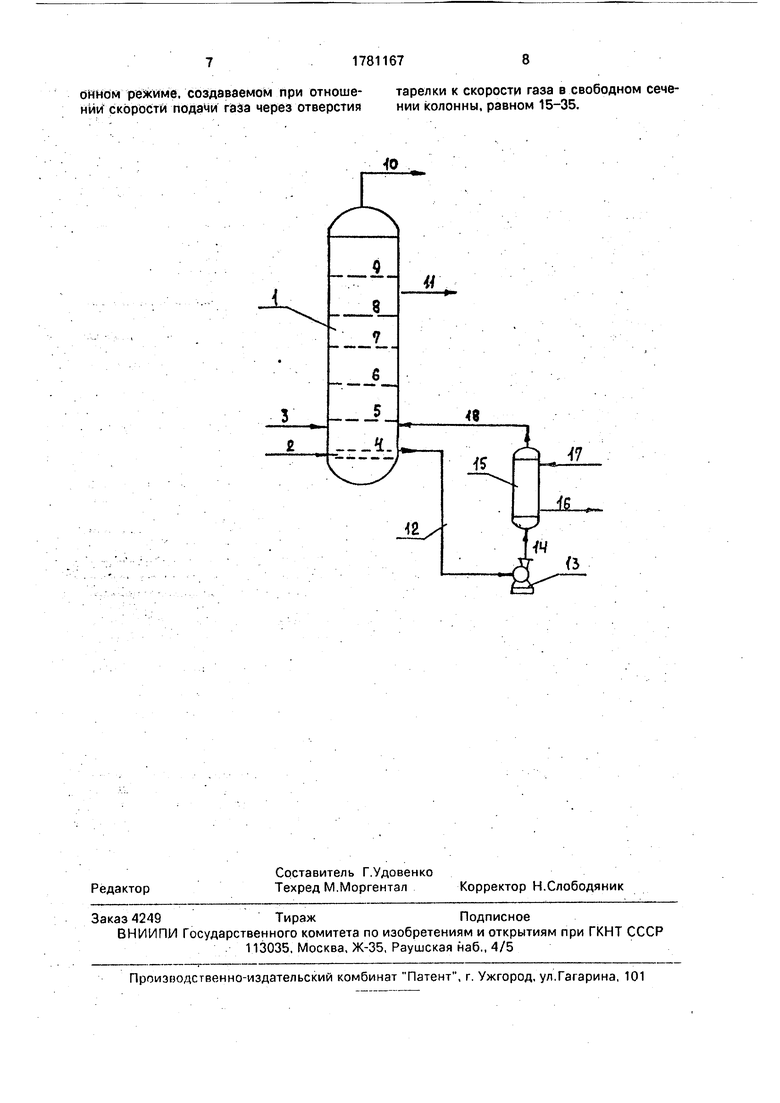
На чертеже представлена реакционная колонна (1), где
2-трубопроводдля подачи нитрозного газа,
3- трубопровод для подачи раствора Ыа2СОз,
4- распределитель,
5, б, 7, 8 - ситчатые тарелки, 910-трубопровод для вывода нитрозного газа,
11- трубопровод для вывода раствора нитрит-нитрата натрия,
12- линия, 13- насос,
14-линия,
15-холодильник,
16, 17 - линия ввода и отвода воды,
18 -линия.
Пример 1 (оптимальный вариант).
Полученные окислением аммиака нит- розные газы в количестве 50909,71 кг/час состава, мае, %: N0 - 7,48; N02 - 6,17; 02 - 2,85; N2 - 69,88; Н20 - 13,62 с температурой 400°С и давлением 0,6 МПа поступают по
трубопроводу 2 через распределитель 4 в нижнюю часть колонны 1, затопленную раствором соды. После распределителя 4 горячие нитрозные газы поступают под тарелку
5,куда по трубопроводу 3 подают раствор соды в количестве 40333,31 кг/час состава (% вес.): №2СОз - 25,75; Н20 - 74,25; с температурой 80°С и давлением 0,9 МПа, соотношение скоростей - 28. Линейная скорость газа в отверстиях тарелки 11,585 м/с, а линейная скорость в свободном сечении колонны 0,412 м/с.
Смесь нитрозного газа и раствора соды проходит все перфорированные тарелки 5,
6,7, 8, на которых осуществляется процесс их взаимодействия с получением нитрит- нитрату натрия.
С тарелки 8 непрореагировавший нит- розный газ в количестве 42731,65 кг/ч состава, мае. %: N0 - 0,19; МОа - 0,19; 02 - 1,83; N2 - 83,26; СОа - 9,81; Н20 - 4,72 направляют по трубопроводу 10 в колонну кислой абсорбции на получение азотной кислоты. По трубопроводу 11 выводят раствор нитрит-нитрата натрия в количестве 48511,38 кг/час состава, мае. %: NaN02 - 25,27; №МОз - 2,27; №2СОз - 0,58; Н20 - 71,88 и направляют на дальнейшую переработку для получения кристаллического продукта с соотношением NaNCWNaNOs 11. содержание щелочного компонента - 0,58% вес.
Пример 2. Нитрозные газы в количестве 49545,25 кг/час состава (% вес.): N0 - 7,26; N02 - 6,33; 02 - 2,86; N2 - 70,02; Н20 - 13,53 с температурой 400 °С и давлением 0,6 Мпа поступают по трубопроводу 2 через распределитель 4 в нижнюю часть колонны 1, затопленную раствором соды. После распределителя 4 горячие нитрозные газы поступают под тарелку 5, куда по трубопроводу 3 подают раствор соды в количестве 41922,78 состава (% вес.): Na2COs - 24,8; Н20 - 75,2 с температурой 80°С, соотношение скоростей 15 (6,18:0,412 15).
Смесь (жидкость и газ) проходит все перфорированные тарелки 5, 6, 7, 8, на которых проходит процесс их взаимодействия с получением нитрит-нитрата натрия.
С тарелки 8 непрореагировавший нит- розный газ в количестве 41127,77 кг/час состава (% вес.): N0 - 0,4; N02 - 0,6; 02 - 0,45; N2 - 91,35; С02 - 9,48, Н20 - 4,72 направляют по трубопроводу 10 в колонну кислой абсорбции на получение азотной кислоты.
По трубопроводу 11 выводят раствор нитрит-нитрата натрия в количестве 50337,47 кг/ч состава, мае. %: NaN02 - 17,27; NaNOa - 8,64; №2СОз - 2,00; Н20 - 72,09 и направляют на дальнейшую переработку для получения кристаллического продукта с соотношением NaN02/NaN03 2. Содержание щелочного компонента 2,00% вес.
5Пример 3. Нитрозные газы в количестве 48349,88 кг/час состава (% вес.): N0 - 7.29; N02 - 6,02; 04 - 3,31; N2 - 69,98; Н20 - 13,4 с температурой 400 С и давлением 0,6 МПа поступают по трубопроводу 2 через
0 распределитель 4 в нижнюю часть колонны 1, затопленную раствором соды. После распределителя 4 горячие нитрозные газы поступают под тарелку 5, куда по трубопроводу 3 подают раствор соды в ко5 личестве 41485,95 состава (% вес.): №2СОз
- 23,12; Н20 - 76,88; с температурой 80°С,
соотношение скоростей 20 (8,24/0,412 20).
Смесь (жидкость и газ) проходит все
перфорированные тарелки 5, 6, 7, 8, на ко0 торых проходит процесс их взаимодействия с получением нитрит-нитрата натрия,
С тарелки 8 непрореагировавший нит- розный газ в количестве 40640,48 кг/ч состава (мае. %): N0 - 0,37; N02 - 0,31; 0Ј 5 1,98; N2 - 83,26; С02 - 9,36; Н20 - 4,72 направляют по трубопроводу 10 в колонну кислой абсорбции на получение азотной кислоты.
По трубопроводу 11 выводят раствор
0 нитрит-нитрата натрия в количестве 49195,32 кг/час состава (% вес.): NaN02 - 20,92; NaNO.s -4,13; №2СОз - 0,85; Н20 - 74,10 и направляют на дальнейшую переработку для получения кристаллического про5 дукта с соотношением NaN02/NaN03 5. Содержание щелочного компонента 0,85.
Положительный эффект предложенного способа по сравнению с аналогами состоит
-в уменьшении щелочного компонента 0 в готовом продукте в 5-20 раз,
-в том, что способ дает возможность получать раствор, из которого можно получать кристаллический продукт.
Кроме указанных преимуществ необхо- 0 димо отметить то, что способ успешно можно использовать в промышленных условиях без значительных затрат, Способ можно рассматривать как узел (колонна), в технологической схеме получения азотной кислоты под повышенным давлением. 5 Формула изобретения
Способ получения нитрита щелочного металла, включающий взаимодействие оксидов азота с водным раствором оснований этих металлов в тарельчатой колонне, отличающийся тем, что, с целью снижения содержания в продукте щелочного компонента, взаимодействие проводят прямотоком в колонне с ситчатыми тарелками в инжекциокном режиме, создаваемом при отноше- тарелки к скорости газа в свободном сечений скорости подачи газа через отверстия нии колонны, равном 15-35.


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОИЗВОДСТВА НИТРИТА НАТРИЯ | 1993 |
|
RU2069173C1 |
| СПОСОБ ПРОИЗВОДСТВА НИТРИТА НАТРИЯ | 1993 |
|
RU2069174C1 |
| Способ получения нитрита кальция | 1983 |
|
SU1171417A1 |
| СПОСОБ ПОЛУЧЕНИЯ НИТРИТОВ | 1971 |
|
SU309903A1 |
| Способ снижения содержания оксидов азота в хвостовых газах производства слабой азотной кислоты | 1991 |
|
SU1809774A3 |
| Способ получения нитрита аммония | 1972 |
|
SU611879A1 |
| СПОСОБ ПОЛУЧЕНИЯ НИТРИТА НАТРИЯ И АБСОРБЦИОННЫЙ АППАРАТ ДЛЯ ПРОВЕДЕНИЯ ПРОЦЕССА | 2000 |
|
RU2174096C1 |
| СПОСОБ ПОЛУЧЕНИЯ НИТРАТА НАТРИЯ | 2002 |
|
RU2213696C1 |
| Способ электродиализа | 1991 |
|
SU1810088A1 |
| СПОСОБ ОЧИСТКИ ВЫХЛОПНЫХ ГАЗОВ ОТ окислов АЗОТА | 1973 |
|
SU392958A1 |
Сущность: в колонне с сетчатыми тарелками прямотоком осуществляют взаимодействие оксидов азота с водным раствором оснований требуемых металлов в инжекци- онном режиме при отношении скорости подачи газа через отверстие тарелки к скорости газа в свободном сечении колонны, равном 15-35. Содержание щелочного компонента в продукте. 1 ил.
fc±3

| Устройство для укладки подземного трубопровода из термопластического материала | 1985 |
|
SU1347909A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1992-12-15—Публикация
1990-04-26—Подача