Изобретение относится к области химии биологически активных веществ и касается нового соединения (2.2,3,3,4,4,4- гептафторбутил)-М-(диметилметоксисилил) азиридина, формулы 1
CHn CH CH2CjF.-. N1
Me-Si-Me u OMe
обладающего противосудорожным и транквилизирующим действием (анксиоли- тическим действием), что может найти применение в медицине. Известно, что соединения, содержащие азиридиновый фрагмент (азиридины, азиридиновые производные тиофосфорной кислоты и пр.), обладают противоопухолевой активностью. Кроме того, введение в молекулу как перф- торалкильных, так и триорганилсилильных заместителей приводит либо к усилению
имеющейся активности, либо к появлению новых ее видов.
Ведущее место в терапии разнообразных нарушений невротического уровня прочно заняли транквилизаторы бензазипи- нового ряда. Спектр психотропного действия препаратов этого ряда позволяет применять их помимо психиатрии и в других областях клинической медицине. Высокая эффективность при лечении неврозоподоб- ных состояний различного генеза, быстрое и надежное противотревожное(анксиолити- ческое) действие позволили расширить область применения транквилизаторов до использования их здоровыми людьми, находящимися в условиях длительного и интенсивного эмоционального напряжения. Основным специфическим действием психотропных препаратов при использовании редукции эмоциональных расстройств следует считать транквилизирующий эффект. Но при этом следует подчеркнуть, что параллельно с выраженным анксиолитическим
(Л
С
vj
00
кэ ю
действием регистрируются и побочные эффекты в виде сильной сонливости, атаксии, мышечной слабости и т.д.
Аналоги соединения I по структуре отсутствуют.
Цель изобретения - поиск препарата, обладающего противосудорожным и анкси- олитическим эффектом, менее токсичного, чем известные психотропные средства, лишенного миорелаксантного действия, раз- работка препаративного способа получения ранее неизвестного М-силилированного перфторалкилметилзамещенного азириди- на.
Поставленная цель достигается тем, что триорганил(аллиламино)-силан вводят в реакцию с триалкил(диэтиламино)станнаном и перфториодалканами:
R3SiNHCH2CH CHf RjSnNEtЈ RFI - RLCH jStfl+HHEt
N-SiRj
Реакцию осуществляют в отсутствие растворителей при инициировании УФ-об- лучением. Соединение представляет собой бесцветную подвижную жидкость со специфическим запахом, чувствительную к влаге и хорошо растворимую в инертных органических растворителях. Выход составляет 56- 78%.
Состав и строение соединения (I) однозначно доказаны данными элементного анализа, ИК- и ПМР-спектроскопии. LDso соединения I 328 мг/кг при внутрибрюшин- ном введении белым беспородным мышам.
Следующие примеры иллюстрируют изобретение.
Пример 1. Получение (2,2,3,3,4.4,4- гептафторбутил)-М-(диметилметоксисилил) азиридина.
В ампулу из стекла Пирекс помещают 9,4 г (0,065 мол) диметилметокси(аллилами- но)силана и 13,9 г (0,05 мол) триэтил(диэти- ламино)станнана,выделившийся
диэтиламин отгоняют при 54-60°С. Ампулу вакуумируют, добавляют в нее 16,3 г (0,055 мол) гептафториодпропана, продувают аргоном и освещают УФ-светом (лампа ДРТ- 400) в течение 6 часов при 30°С. Разгонкой в вакууме выделяют 11,7 г (75%) (2,2,3.3,4,4,4-гептафторбутил)-М-(диметил- метоксисилил)азиридина с Т.кип. 73- 75°С/25торр., ,3633, ,2289.
Спектр ПМР 1Н (,5 , м.д.): 3,42, с. ЗН(СНзО),2,19,м.,ЗН(СН2СН), 1.91,1,61, м„ 2Н(СН2), 0,07, с. 6Н (СНз51).
Масс-спектр, м/е: 313,194,129.
Пример 2, Фармакологическое исследование (2,2,3,3,4,4,4-гептафторбутил)-М- (диметилметоксисилил)азиридина.
Спектр психотропной активности включает 6 основных видов действия: транквили- зирующее,противосудорожиое,
седативное, снотворное, активирующее и миорелаксантное. Противосудорожную активность соединения I оценивали по его способности предупреждать тонико-клони- ческий компонент судорожного припадка. Эксперимент проводят на белых беспородных мышах весом 20-21 г. Коразол в дозе 130 мг/кг вводили п/кожно через 30 мин после введения препарата 1. Высокой активностью по предупреждению судорог обладает соединение в дозе 1 мг/кг: количество животных выживших в подопытной группе составляет 60% (6 из 10), в дозе 10 мг/кг-40% (4 из 10), в то время как в контроле наблюдается полная гибель животных (табл.1). Следует отметить, что противосудорожное действие соединения I в дозе 10 мг/кг сохраняется на протяжении 4 часов.
Влияние заявляемого соединения на пороги чувствительности к коразолу изучали по методике внутривенного титрования. Опыт проводили на белых беспородных мышах, весом 20-22 г. Соединение I вводили внутрибрюшинно за 30 мин до начала эксперимента. Затем в хвостовую вену мыши вводили 1%-ный растйор коразола с постоянной скоростью. В момент гибели животных регистрировали объем введенного раствора коразола с последующим пересчетом (мг/кг веса животного). Установлено, что с увеличением дозы от 0,1 до 10 мг/кг степень изменения порога чувствительности к коразолу возрастает. Максимальный защитный эффект соединения I проявляется в дозе 10 мг/кг. индекс составляет 6,38 (табл.1).
Наличие транквилизирующего эффекта заявляемого соединения определяли методом конфликтной ситуации.
Конфликтную ситуацию у крыс создавали путем столкновения питьевой и оборонительной мотивации при нанесении электроболевого раздражения в момент взятия воды в привычной обстановке осуществления питьевого рефлекса. Регистрацию числа взятий воды, подходов к поилке и двигательную активность проводили в течение 20 мин. Эксперимент начинали с тренировки создания у крыс чувства жажды и навыка взятия воды из поилки в камере. Животных содержали на сухом корме в течение 48 часов, затем в одно и то же время суток на протяжении 3-х дней крыс помещали в камеру, где они получали из поилки в течение 10 мин. В день опыта после начала питья (ч/з 10 сек.) крысе наносили электрическое раздражение пропусканием тока (80 в) через поилку, Таким образом, конфликтная ситуация создавалась столкновением 2-х рефлексов: питьевого и оборонительного. В дальнейшем в течение 20 мин. регистрировали следующие показатели поведения крыс: количество взятий воды, несмотря на получение при этом каждый раз нового злектроболевого раздражения, число подходов и величину общей двигательной активности. Регистрацию проводили автоматически, все показатели поведения фиксировали счетчиками в виде цифровых величин.
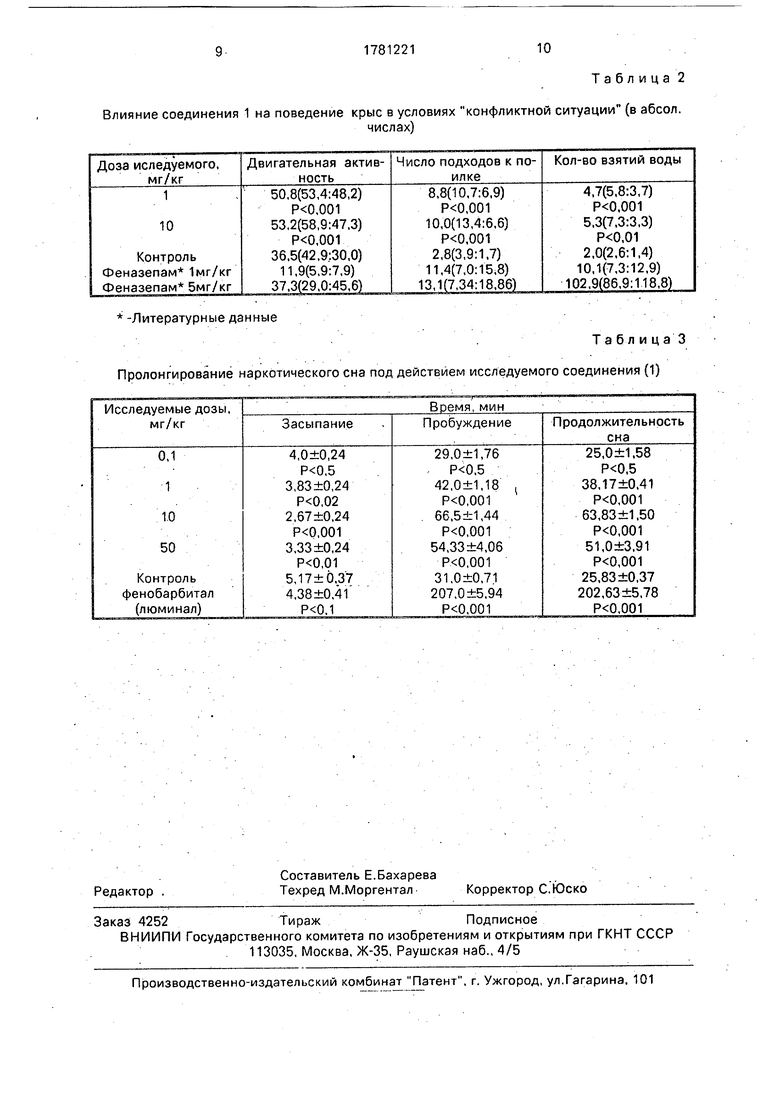
Исследования проводили на крысах- самцах весом 180-210 г. Введение вещества осуществляли внутрибрюшинно за 30 мин до начала эксперимента. Нами установлено, что после столкновения 2-х противоположных мотиваций, наибольшую биологическую значимость в контрольной группе приобретает внезапный болевой раздражитель, который и определяет поведение животных, характеризующееся незначительной двигательной активностью. В подопытной группе, несмотря на получение болевого раздражителя под действием заявляемого соединения в дозах 1 и 10 мг/кг питьевая мотивация приобретает большую биологическую значимость, становится доминирующей, в результате на фоне двигательной реакции, число подходов к поилке и взятие воды увеличивается по сравнению с контролем в 3,5 раза и в 2,6 раза соответственно (табл.2).
Сравнивая результаты заявляемого соединения с феназепамом, следует отметить, что хотя число взятий воды для феназепама возрастает в зависимости от дозы, значительно в большей степени, чем для исследуемого вещества, однако при этом для феназепама характерно снижение двигательной активности, что можно расценивать как развитие седативного эффекта на фоне проявления анксиолитического действия. Напротив, для соединения I в дозах, оказывающих анксиолитический эффект, наблюдается активация двигательной активности, что является несомненным преимуществом перед феназепамом
Изучено влияние соединения I также на поведение мышей в условиях эмоционального стресса, (открытое поле). Метод открытого поля основан на определении двигательного компонента ориентировочной реакции и эмоциональной реактивности животных. Наблюдение за животными проводили в затемненном помещении в одно и тоже время суток. Предварительно мышей размещали по одной в коробку и спустя 1 мин они поступали на 3 мин, на освещенный включением 4-х ламп мощностью по 60 Вт, манеж.
Регистрировали общую двигательную активность (ДА), это число пересечений сек- 5 торов по всей площади, число стоек, горизонтальную ДА - общее число пересечений секторов, периферическую ДА - число секторов, пересеченных по периферии, центральную ДА-число секторов, пересеченных
0 в центре. Каждое животное использовали в опыте однократно. Реакция мышей на эмоциональный стресс при введении соединения I в дозе 1 мг/кг и 10 мг/кг за 30 мин до начала опыта характеризовалась по всем
5 исследованным показателям незначительной активностью. Полученные результаты свидетельствуют, что хотя и не было выявлено статистически значимого эффекта препарата, все же наблюдается тенденция к
0 активации двигательной активности (прежде всего в дозе 10 мг/кг) Так в подопытных группах животных при введении соединения в дозе 1 мг/кг и 10 мг/кг изменения показателя исследовательской активности
5 составляет соответственно 59,0 ±50,9 и 67,0± 7,9 перемещений, в контрольной 52,0±4,6, что указывает на отсутствие седативного эффекта.
Наличие гипнотического, снотворного
0 эффекта у заявляемого соединения оценивали по изменению времени засыпания, пробуждения и продолжительности сна, вызванного гексеналом в дозе 60 мг/кг, гексе- нал вводили внутрибрюшинно через 15 мин
5 после инъекции исследуемого соединения с последующей регистрацией числа заснувших мышей по критерию утраты ими рефлексов переворачивания.Установлено,что соединение в диапазоне доз 1-50 мг/кг об0 ладает по сравнению с контролем, снотворным эффектом. Под влиянием вещества в дозе(1) 10 мг/кг наблюдается максимальное увеличение продолжительности сна у мышей от гексенала (в 2,5 раза) с укорочением
5 времени засыпания (в 1.9 раза). При этом следует отметить, что эффект соединения 1 менее выражен, чем снотворное действие фенобарбитала (табл.3).
0 Данные, характеризующие снотворное действие феназепама свидетельствуют, что в дозе 0,05 мг/кг (в/б) наблюдается увеличение продолжительности гексеналового Сна в 3,1 раза; в дозе 0,1 мг/кг - в 4,5 раза,
5 т.е. в дозах, при которых проявляется и его анксиолитическое действие. При повышении действующих доз снотворный эффект феназепама еще больше возрастает, в то время как снотворный эффект заявляемого
соединения с повышением дозы падает (табл.3).
Таким образом, и в данном случае выраженное преимущество заявляемого соединения отчетливо заметно и заключается в большей избирательности анксиолитиче- ского эффекта при меньшей выраженности снотворного действия.
Нарушение координации движений, походки и равновесия оценивали по тесту вра- щающегося стержня. На горизонтальный стержень диаметром 2 см и скоростью вращения 5 об/мин помещали мышей. Нами установлено, что животные удерживаются на стержне в течение 2 мин при введении вещества в дозах 1 и 10 мг/кг. Наличие глубоких нарушений, связанных с развитием выраженной миорелаксации определяли по тесту бокового положения. Показано, что при внутрибрюшинном введении заяв- ляемого соединения не утрачен рефлекс переворачивания животных на лапы из положения на спине на протяжении 2 мин в дозах 1-50 мг/кг.
Таким образом, проведенный сравни- тельный анализ психотропных эффектов заявляемого соединения, фенобарбитала и феназепама показал, что по силе противосу- дорбжного действия заявляемое соединение превосходит классический противосу- дорожный препарат фенобарбитал (люминал) в 3,79 раза, отличаясь от него менее выраженным снотворным эффектом (в 3,17 раза). В то же время, выявленная анксиоли- тическая активность заявляемого соединения, оцениваемая по величине действующих доз, находится на уровне аналогичной активности широко распространенногобенздиазепиновоготранквилизатора - диазепама, но уступает феназепаму. Однако, в отличие от последнего, анксиолитическое действие которого наблюдается на фоне быстроразвивающегося седативного и снотворного эффектов, гип- носедативное действие заявляемого соединения выражено слабо. Соединение I имеет мг/кг.
Формула изобретения (2,2.3,3,4,4,4Тептафторбутил)-1Ч-(диме тилметоксисилил)-азиридин формулы СН2-СН-СН2СзР7 ,
N СН3- Si-CH3
ОСН3
обладающий противосудорожным и транквилизирующим действием.
Таблица 1



| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ НЕВРОЗОПОДОБНЫХ И ПОГРАНИЧНЫХ РАССТРОЙСТВ | 1993 |
|
RU2102986C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНКСИОЛИТИЧЕСКОЙ, НООТРОПНОЙ, ПРОТИВОСУДОРОЖНОЙ, АНТИДЕПРЕССИВНОЙ, ЦЕРЕБРОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ И СПОСОБНОСТЬЮ НОРМАЛИЗОВАТЬ ПРОЦЕССЫ ПЕРЕДАЧИ В СИНАПСАХ МОЗГА | 2007 |
|
RU2335293C1 |
| 5-П-ИЗОПРОПОКСИФЕНИЛ-N-КАРБАМОИЛ-2-ПИРРОЛИДОН, ОБЛАДАЮЩИЙ ТРАНКВИЛИЗИРУЮЩЕЙ АКТИВНОСТЬЮ | 1987 |
|
SU1499877A1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНКСИОЛИТИЧЕСКОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2571286C1 |
| N-( γ -АМИНОБУТИРИЛ)-1-АЗА-4,7,10,13-ТЕТРАОКСАЦИКЛОПЕНТАДЕКАН-ГИДРОХЛОРИД, ОБЛАДАЮЩИЙ АНТИАМНЕСТИЧЕСКОЙ, АНТИГИПОКСИЧЕСКОЙ И ПРОТИВОСУДОРОЖНОЙ АКТИВНОСТЬЮ | 1984 |
|
SU1197407A1 |
| 8-МЕТИЛ-8-ФЕНИЛ-3-ОКСОТИАЗОЛИДИНО-[3,2-A]ПИРЕРАЗИН ИЛИ ЕГО ГИДРОХЛОРИД, ОБЛАДАЮЩИЕ ТРАНКВИЛИЗИРУЮЩИМ ДЕЙСТВИЕМ | 1991 |
|
SU1829361A1 |
| 2-АМИНО-5,5-ДИМЕТИЛ-4,5-ДИГИДРО-7Н-ПИРАНО [4,3-d] ТИАЗОЛ, ОБЛАДАЮЩИЙ ТРАНКВИЛИЗИРУЮЩЕЙ АКТИВНОСТЬЮ | 1987 |
|
SU1441749A1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИДЕПРЕССАНТНЫМ, АНКСИОЛИТИЧЕСКИМ, НЕЙРОПРОТЕКТОРНЫМ И ИММУНОСТИМУЛИРУЮЩИМ ДЕЙСТВИЕМ | 2010 |
|
RU2429834C1 |
| АНКСИОЛИТИЧЕСКОЕ СРЕДСТВО | 1999 |
|
RU2175229C2 |
| ПРОТИВОСУДОРОЖНОЕ И ТРАНКВИЛИЗИРУЮЩЕЕ СРЕДСТВО | 2015 |
|
RU2593885C1 |
Сущность изобретения: продукт - 
Влияние (2,2,3,3,4,4,4-гептафторбутил)-М-(диметилметоксисилил) азиридина на противосу- дорожную активность при подкожном введении коразола (130 мг/мл) и при титровании 1%
раствором коразола
Таблица 2
Влияние соединения 1 на поведение крыс в условиях конфликтной ситуации (в абсол.
числах)
-Литературные данные
Таблица 3
Пролонгирование наркотического сна под действием исследуемого соединения (1)
| Машковский М.Д | |||
| Лекарственные средства М.: Медицина, 1972, с | |||
| Катодная лампа с внешним подогревом | 1923 |
|
SU493A1 |
| Воронков М.Г | |||
| и др | |||
| - Кремний и жизнь, Рига: Зинатне, 1971, с | |||
| Вагонетка для кабельной висячей дороги, переносной радиально вокруг центральной опоры | 1920 |
|
SU243A1 |
Авторы
Даты
1992-12-15—Публикация
1991-03-25—Подача