ел
С

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования развития рецидива диффузной В-крупноклеточной лимфомы | 2021 |
|
RU2758126C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ЛЕЙКОЗОВ | 1992 |
|
RU2049997C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ЛЕЙКОЗА | 1991 |
|
RU2069858C1 |
| Способ диагностики поражения нервной системы при лейкозе | 1991 |
|
SU1765767A1 |
| СПОСОБ ЛЕЧЕНИЯ ЛЕЙКОЗА С АУТОИММУННЫМИ ПРОЯВЛЕНИЯМИ, ИНДУЦИРОВАННОГО В ЭКСПЕРИМЕНТЕ | 1993 |
|
RU2085215C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РЕЦИДИВОВ У БОЛЬНЫХ ОСТРЫМ ЛЕЙКОЗОМ | 2006 |
|
RU2319151C1 |
| Способ лечения аллергических заболеваний | 2020 |
|
RU2742976C1 |
| СПОСОБ ЛЕЧЕНИЯ ОНКОЗАБОЛЕВАНИЙ В ЭКСПЕРИМЕНТЕ | 2007 |
|
RU2396967C2 |
| СПОСОБ РАННЕЙ ДИАГНОСТИКИ РЕЦИДИВОВ ОСТРОГО ЛИМФОБЛАСТНОГО ЛЕЙКОЗА У ДЕТЕЙ | 1992 |
|
RU2085943C1 |
| ГЕМОСТИМУЛИРУЮЩЕЕ СРЕДСТВО, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ СТИМУЛИРОВАНИЯ ГЕМОПОЭЗА | 2011 |
|
RU2482869C1 |
Изобретение относится к области медицины, в частности к гематологии, и может быть использовано для лечения лейкозов. Цель способа - повышение терапевтической эффективности. Для этого циклофосфай в дозе 100 мг/кг вводят внутрибрюшинно до достижения ремиссии, после чего осуществляют многократную подкожную иммунизацию идентичными заболеванию живыми лейкозными клетками, модифицированными конкановалином А при 37°С в течение 30-90 мин из расчета 50-150 мкг на 5 106 клеток. 1 з. п. ф-лы, 1 табл. .
Изобретение относится к области медицины, в частности к гематологии, и может быть использовано для лечения лейкозов.
Известен способ усиления противолей- козной активности циклофосфана, включающий его внутрибрюшинное введение с последующей иммунизацией вакциной из обработанных глютаровым альдегидом лей- козных клеток того же штамма.
Однако известный способ обладает низким терапевтическим эффектом, связанным с использованием для иммунизации инакти- вированных лейкозных клеток после их обработки глютаровым альдегидом, а также со схемой лечения.
Целью изобретения является повышение терапевтической эффективности.
Цель достигается тем, что циклофосфан вводят до достижения ремиссии, после чего осуществляют многократную подкожную иммунизацию идентичными заболеванию
живыми лейкозными клетками, модифицированными конкановалином А.
Модификацию лейкозных клеток осуществляли, путем обработки 5 10 нативных клеток асцитической жидкости животных с .лейкозом в среде 199 с 50-150 мкг/мл конкановалином А при температуре 37°С в течение 30-90 мин.
Реализация способа поясняется следующими примерами.
П ри мер 1. Мышь беспородная, самка, масса 19,7г, исходные показатели периферической крови: гемоглобин - 170 мг/л, эритроциты - 9,9 10 /л, лейкоциты - 11,3 109/л, Тобщ.-96%, В-42%.
Лейкоз МК/1у перевит 1 105 лейкозных клеток внутрибрюшинно в объеме 0,2 мл. Циклофосфан в дозе 100 мг/кг вводили внутрибрюшинно на 1 и 6 сутки после перевивки лейкоза. После завершения курса асцит пальпаторно не определялся. Показа 4 О О Ю
N
4
толи крови:гемоглобин - 152 г/л, эритроциты - 7,6 1012/л, лейкоциты - 6,45 Ю9/л, Тобщ.-35%, В- 11%.
Иммунизацию осуществляли на 12,15 и 18 сутки после перевивки лейкоза живыми лейкозными клетками того же штамма, обработанными конкановалином А при 37°С в течение 30-90 мин из расчета 120 мкг/мл на 5 106 клеток. На 21 сутки после перевивки лейкоза показатели периферической крови составили: гемоглобин - 158 г/л,-эритроциты - 7 10 /л, лейкоциты - 12,1 10 /л, Тобщ. -68%, В -12%.
Мышь наблюдалась до 120 суток, рецидива лё йкоза-не выявлеШ.
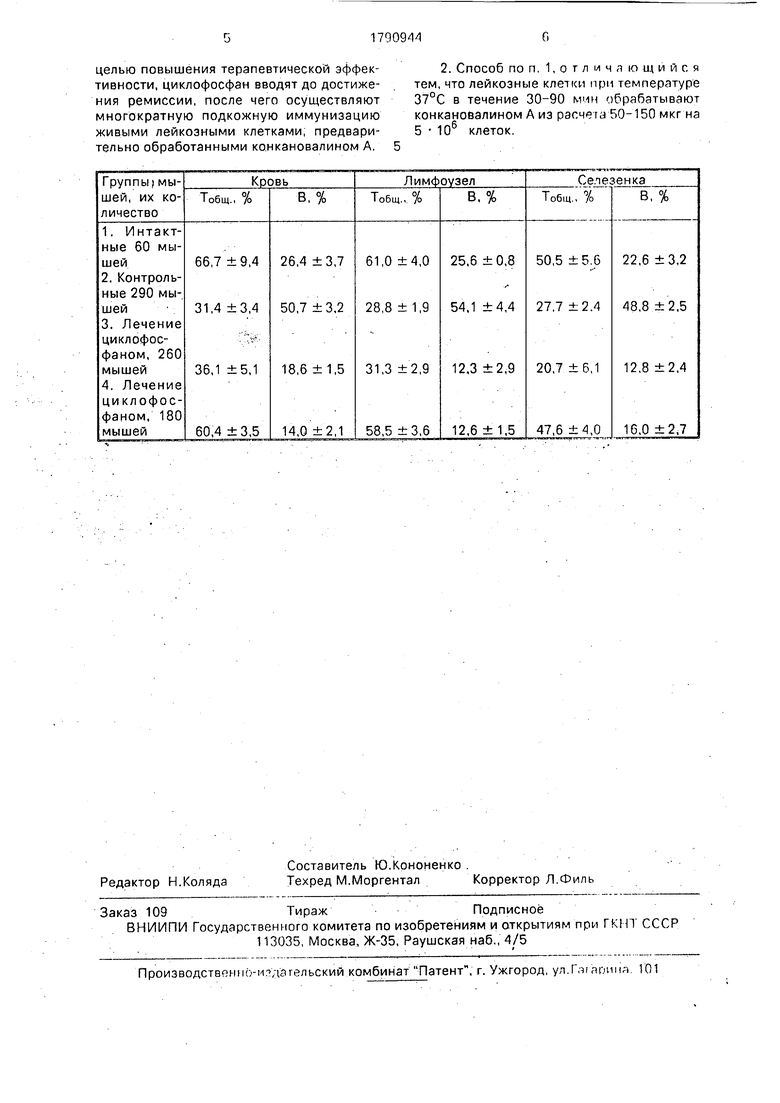
Пример 2, ВЗ сериях опытов использовали 790 мышей, из которых 60 являлись интзктны ми, 290 - контрольными, которых после перевивки лейкоза не подве ргали лечению, 290 мыгией лечили циклофосфаном и 180 мышей лечили циклофосфаном с последующей иммунотерапией, как в примере 1, Модификацию лейкозныхклеток осуществляли конканЪвалином А, как описано в примере 1. - -.- ;-. ..-...;..... .,..;..
Результаты опыта на 20 сутки после перевивки лейкоза приведены в таблице.
ПримерЗ. Больная НЫВ, 1958 года рождения , история болезни № 5985.
После перенесенной острой респираторной инфекции начала ощущать общую слабость, кашель и периодическое повышение температуры до 39,0°С.
При поступлении: жалобы на боли в гор- ле при глотании, кашель, общую слабость, Температура - 39,0°С, кожные покровы бледные, в легких ослабленное дыхание и очаговыехрипы в нижних отделах, тоны сер- дца п рйглушёны, границы сердца расширены влево, печень выступает из-под края реберной дуги на 3,5-4,5 см, безболезненная,лймфатическйёузлы и селезенка в норме. Анализ крови: гемоглобин - 94 г/л, эритроциты - 2,5 Т012/л, лейкоциты - 1,6 1011/л, тромбоциты - 2,37 1021/л, бластные клетки -. 68%, палочкоядерные нейтрофилы - 1%, сегментоядерные нейтрофилы - 13%, эозинофилы -4%, лимфоциты- 1. : - ::- : :: -. .
На основа н |/1Й КЛини кр-гематологиче- ского обследования и данных цитохимиче- ских реакций поставлен диагноз, острый миелрбластный лейкоз, первый острый период. Сопутствующие заболевания: двух- сторон няя н ижнедолевая пневмония, тромбофлебит нижних конечностей.
Специфическое лечение проводилось по схеме 7+3 и сопровождалось гемотранс- фузиями. Для лечения сопутствующих заболеваний использовались антибиотики,вита- минные препараты, симптоматические средства.
После специфического лечения наступала полная клинико-гематологическая ремиссия, что подтверждено данными стернальнбй пункции. Иммунологические показатели резко снижены: Т0бщ-7%, Такт- 30%, Тх-13%,Тс-0, В-2%, ЕК-0, ЕКА-7%.
0 Под контролем иммунологических показателей проведена 5-кратная подкожная иммунизация в 4 точки живыми аллогенны- ми криоконсервированными клетками, обработанными конкановалином А по схеме,5 описанной в примере 1. Интервалы между иммунизациями составили от 16 суток до 36 суток.
.После 3-й иммунизации показатели периферической крови составили: палочкоя0 дерные лимфоциты - 3%, сегментоядерные лимфоциты - 46%, эозинофилы - 8%, лимфоциты - 36%, моноциты - 6%, Иммуноло- гический статус: Тобщ. - 41 %, Такт. - 26%, Тх - 42% , Те- - О, В - 20%, ЕК - 39%, Общее
5 состояние удовлетворительное, жалоб нет. Через 3,5 месяца от начала иммунизации миелограмма: бластные клетки - 3,5, промиелодные клетки - 2 %, миелоидные нейтрофилы - 14,5 %, миелоидные эозйно0 филы - 2%, метамиелоидные клетки - 8%, палочкоядерные нейтрофилы - 14,5%, сегментоядерные нейтрофилы - 15,5%, лимфоциты - 6,5%, плазмоциты - 0,5%, эритробласты - 0,5%, пронормбциты -.
5 1,5%, нормоциты базофильные - 3%, нормальные полихромные клетки - 27,7%. Ге- мограмма: палочкоядерные нейтрофилы - 3%, сегментоядерные нейтрофилы - 52%, лимфоциты - 37%, моноциты - 8%. Состоя0 ние больной удовлетворительное.
В связи с полной клинико-гематологиче: ской и иммунологической ремиссией нет показаний к проведению повторного курса цитостатическими препаратами.
5 Использование циклофосфана в сочета- нии с активной специфической иммунотерапией идентичными заболеванию живыми лейкозными клетками, модифицированными конкановалином А, обеспечивает высокий
0 терапевтический эффект. Такой результат достигнут благодаря значительной активации отдельных звеньев иммунитета, обусловленной влиянием иммунотерапии модифицированными клетками..
v 1. Способ усиления противолейкозной активности циклофосфана, включающий введение циклофосфана и иммунизацию идентичными заболеванию, лейкозными клетками, о тличающийся тем, что, с
целью повышения терапевтической эффек-2. Способ по п, 1, о т л и ч я ю щ и и с я
тивности, циклофосфан вводят до достиже-тем, что лейкозные клетки при температуре
ния ремиссии, после чего осуществляют37°С в течение 30-90 мин обрабатывают
многократную подкожную иммунизациюконкановалином А из расчета 50-150 мкг на
живыми лейкозными клетками, предвари-5 10 клеток,
тельно обработанными конкановалином А.5
| Kataoka Т | |||
| et al | |||
| Jmmunoprophylactic and immunotherapeutic response by concanavatis A - hound tumor vaccine enhanced by chemotherapeutic adents eliminating possible supressors | |||
| Cancer Reseach, 1980, 40, 10, 3839-3845. |
Авторы
Даты
1993-01-30—Публикация
1987-01-28—Подача