Изобретение относится к обработке осадков сточных вод гальванических производств с высоким содержанием ионов железа и меди и может быть использовано на предприятиях приборостроительной промышленности,
Цель изобретения - обеспечение возможности разделения компонентов осадка - железа и меди, а также повышение степени извлечения меди.
Пример/. Железо-медные осадки, полученные при очистке сточных вод приборостроительных предприятий от ионов тяжелых металлов, подают в подогреваемый реактор, перемешивают с водой, в полученную суспензию, содержащую 2 г/л Си(И)и2г/л Fe(lll), добавляют раствор, содержащий роданид-ионы в количестве, эквивалентном содержанию меди в осадке (2 г/л CN$), и при 40-50°С дозируют сернистый ангидрид в количестве (4,5-7,6): 1. Количество $02 регулируют скоростью подачи газа (по используемому ротаметру) в течение 3 мин и выдерживают- суспензию в течение 40 мин для созревания и оседания нерастворимого в воде - и кислотах осадка роданида меди (I). Полное отделение осадка достигается фильтрацией. Содержание меди в фильтрате составляет 2,1-2,3% от исходного количества.
Исходный железо-медный осадок представляет собой смесь гидроксидов металлов, основными компонентами которого являются гидроксид железа и гидроксид ме ди:
мае. %
46-47,24
43,8-46,6
1,2-1,7
0,86-0,94
0,28-0,46
0,64-0,85
0,94-1,25
0,02-0,0а
0,15-0,25
ел
Ингредиенты
Ре(ОН)з
Си(
Мд(ОН)2 . - Са(ОН)2
ZnfOHfe
Сг(ОН)з
Ni(OH)2
КОН
NaOH
При этом в реакторе протекают следующие основные реакции:
S02-t-H2O H2S03(1)
2Ре(ОН)з + 2Н250з + О
2FeS04 + 5Н2О(2)
О 00
W
ho
2Cu(OH)2 + Н250з Cu2S04 + 3H20 (3) Cu2S04 + 2KCNS - 2CuCNS,+ K2S04 (4)
При дозировании сернистого ангидрида в водную суспензию железо-медного осадка происходит образование сернистой кислоты, которая способствует не только растворению осадка, но одновременно и восстановлению его компонентов - гидро- ксида железа и гидроксида меди, до ионов с более низкой валентностью - Fe(ll) и Cu(t).
Растворившаяся и химически восстановленная часть осадка, основу которой составляет Cu(l), взаимодействует с присутствующими в среде ионами CNS, образуя при этом нерастворимый в воде и кислой среде кристаллический осадок CuCNS, который оседает на дно отстойника.
Роданид меди обладает высокой гидравлической крупностью, легко оседает, обезвоживается и утилизируется. Благодаря низкой растворимости роданида меди (I) достигается высокая степень (97.5-98,4%) извлечения меди из железо-медных осадков.
Повышение температуры до 40-50°С приводит к ускорению восстановительного действия газообразного сернистого ангидрида на Си(ОН)2 и Ре(ОН)з. В найденном оптимальном интервале температур 40- 50°С продолжительность обработки железо-медного осадка составляет 30-60 минут.
Нагревание способствует также повышению укрупненности и оседаемости частиц осадка CuCNS, что ускоряет процесс извлечения меди из осадка.
Результаты обработки осадков сточных вод гальванических производств приведены а табл. 1-4.
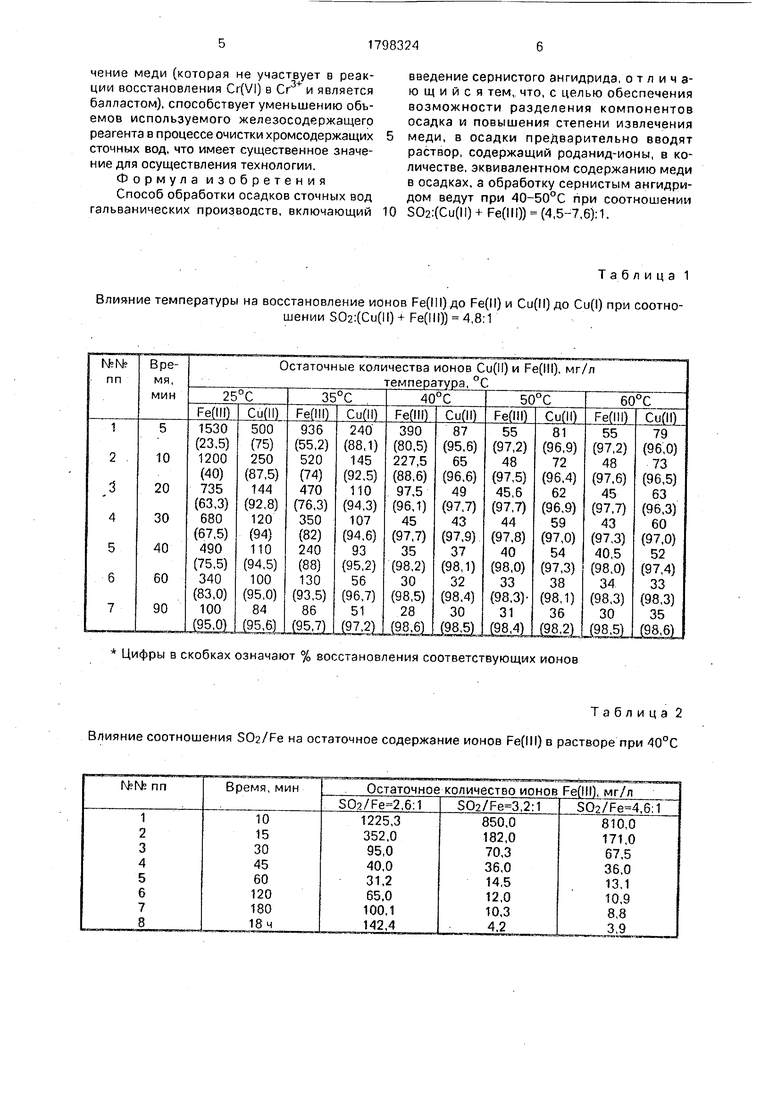
Как видно из данных табл. повышение температуры более 50°С нецелесообразно, так как это, хотя и способствует значительному ускорению реакции восстановления Fe(lll) до Fe(ll)только в первые 10-20 минут, в дальнейшем не влияет на скорость процесса, и уже через 30 минут остаточные концентрации ионов Си(П) и Fe(ll) при этих температурах практически не отличаются. Помимо этого, повышенная температура в дальнейшем приводит к частичному растворению образовавшегося осадка CuCNS, чем и объясняется некоторое повышение содержания ионов Си в растворе в этих условиях.
Понижение температуры менее 40°С приводит к резкому уменьшению скорости восстановления ионов Fe(lll),
Увеличение соотношения S02/Fe с 2,6 до 3,2 способствует уменьшению концентрации ионов Fe(MI) в растворе (табл. 2). Однако дальнейшее увеличение этой величины до 4,6 не приводит к улучшению параметров процесса.
Следовательно, оптимальным значением соотношения SOa/Fe в данном случае следует считать 3,2:1.
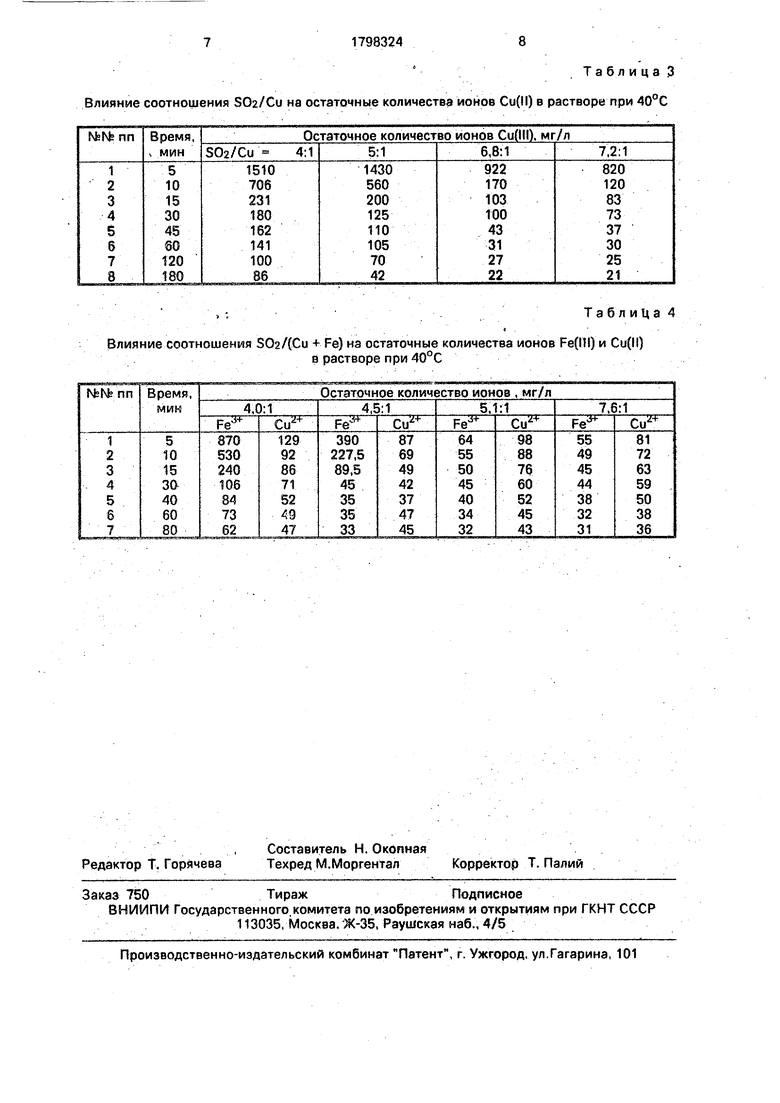
Из данных табл. 3 видно, что уменьшение соотношения S02/Cu менее 6,8:1 приводит к замедлению скорости восстановления ионов Cu(ll) до Cu(l) и увеличению времени процесса, в то время как увеличение соотношения выше этой величины не способствует ускорению процесса.
5 Опыты показали, что в оптимальном интервале температур количество S02, пошедшее на восстановление железа и меди в смеси, меньше, чем при восстановлении каждого из этих элементов в отдельных рас0 творах. Причем как реакция их восстановления, так и осаждение и отделение осадка CuCNS протекают намного быстрее.
Таким образом, исходя из оптимальных величин соотношений для Си и Fe3+, отно5 шение количества S02 к сумме (Си + Fe ) должно составить (6,8+3,2) 10:1. В то же время, как следует из данных табл. 4, для восстановления ионов Cu2+ + Fe3+ достаточно соотношения 5:1 для того, чтобы скорость
0 процесса совместного восстановления ионов Си + и Fe была такой же, как и восстановления этих ионов по отдельности. Увеличение этого соотношения вплоть до 7,6:1 практически не влияет на скорость вос5 становления ионов Fe(l11) и Си(Н), а уменьшение ниже 4,5:1 приводит к существенному замедлению восстановления Си , практически не влияя на восстановление FefHI). Таким образом, соотношение S02/(Fe +
0 +Сг) (4,5-7,6): 1, можно считать.оптимальным.
При. таких соотношениях S02/(Fe +Cu) в растворе сохраняется определенное количество сернистого ангидрида, что препятст5 вует окислению ионов Fe(ll) растворенным кислородом, а также кислородом воздуха до ионов Fe(lll); Дальнейшее повышение соотношения более 7,6:1 приобретает смысл лишь только при очень длительном хране0 нии реагента Fe(It) перед его использованием в качестве восстановителя для очистки хромсодержащих сточных вод.
Предложенный способ позволяет разделить основные компоненты железо-мед5 кого осадка, извлечь из него и вернуть в производство ценный металл - медь, а железо в виде раствора соли FeS04, содержащего остаточные количества SOa использовать в процессе очистки хромсодержащих сточных вод для восстановления CrfVI) в Сг34 Извлечение меди (которая не участвует в реакции восстановления Cr(VI) в Сг34 и является балластом), способствует уменьшению объемов используемого железосодержащего реагента в процессе очистки хромсодержащих сточных вод, что имеет существенное значение для осуществления технологии. Формула изобретения Способ обработки осадков сточных вод гальванических производств, включающий
введение сернистого ангидрида, отличающийся тем,, что, с целью обеспечения возможности разделения компонентов осадка и повышения степени извлечения
меди, в осадки предварительно вводят раствор, содержащий роданид-ионы, в количестве, эквивалентном содержанию меди в осадках, з обработку сернистым ангидридом ведут при 40-50°С при соотношении
S02:(Cu(ll) + Fe(lll)) (4,,6):1.

| название | год | авторы | номер документа |
|---|---|---|---|
| "Способ получения железосодержащего реагента "Ковиол" для очистки сточных вод от ионов тяжелых металлов и устройство "Элеферр" для его осуществления" | 1990 |
|
SU1756282A1 |
| Способ очистки цинковых растворов от хлора | 1989 |
|
SU1677076A1 |
| СПОСОБ ОЧИСТКИ СТОЧНЫХ ВОД ОТ ИОНОВ ТЯЖЕЛЫХ МЕТАЛЛОВ | 1992 |
|
RU2061660C1 |
| Способ комплексной переработки сточных вод гальванических производств | 2018 |
|
RU2674206C1 |
| СПОСОБ ПЕРЕРАБОТКИ ОТРАБОТАННЫХ РАСТВОРОВ, СОДЕРЖАЩИХ СОЕДИНЕНИЯ ШЕСТИВАЛЕНТНОГО ХРОМА | 1996 |
|
RU2110486C1 |
| Аппарат для обработки осадка сточных вод | 1987 |
|
SU1474098A1 |
| Способ обезвреживания сточных вод от хрома | 1979 |
|
SU881004A1 |
| СПОСОБ ОЧИСТКИ СТОЧНЫХ ВОД ОТ ТИОЦИАНАТОВ | 2008 |
|
RU2366617C1 |
| СПОСОБ ОЧИСТКИ СТОЧНЫХ ВОД ОТ ИОНОВ ТЯЖЕЛЫХ МЕТАЛЛОВ | 1994 |
|
RU2054387C1 |
| СПОСОБ КОМПЛЕКСНОЙ ПЕРЕРАБОТКИ ОТРАБОТАННЫХ РАСТВОРОВ ГАЛЬВАНИЧЕСКОГО ПРОИЗВОДСТВА | 1999 |
|
RU2179534C2 |
Использование: выделение меди и железа из осадков сточных вод гальванических производств. Сущность изобретения: осадки обрабатывают сернистым ангидридом при температуре 40-50°С в присутствии роданид-ионов. Соотношение S02:(Cu + Fe) (4,5-7,6):1, Количество роданид-ионов эквивалентно содержанию меди в осадке. Степень извлечения . 4 табл.
Т а. блица 1
Влияние температуры на восстановление ионов Ре(Ш)до Fe(ll) и Cu(ll) до Cu(l) при соотношении S02:(Cu(ll) + Fe(lll)) 4,8:1
Цифры в скобках означают % восстановления соответствующих ионов
Таблица 2 Влияние соотношения S02/Fe на остаточное содержание ионов Fe(lll) в растворе при 40°С
;Т а б л и ц а 3 Влияние соотношения SOa/Cu на остаточные количества ионов Си(И) в растворе при 40°С
, ;Та б л и Ц а А
Влияние соотношения S02/(Cu + Fe) на остаточные количества ионов Fe(lll) и Cu(ll)
в растворе при 40°С
| Аппарат для обработки осадка сточных вод | 1987 |
|
SU1474098A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
1993-02-28—Публикация
1990-07-27—Подача