Изобретение относится к новым химическим соединениям, конкретно к производным арилсульфокислот, которые проявляют гипогликемическую активность и могут использоваться в медицинской практике в качестве антидиабетических средств.
Целью изобретения являются новые соединения, проявляющие гипогликемическую активность и обладающие низкой токсичностью.
Поставленная цель достигается не описанными ранее производными арилсульфокислот общей формулы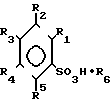 , где R1 H, CH3, Cl, NO2;
, где R1 H, CH3, Cl, NO2;
R2 H, COOH, OH;
R3 H, CH3, Cl, NH2, OH, NHCOOCH3;
R4 H, COOH, NO2,
R4R5 (CH)4;
R5 H;
R6= NH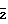 CH
CH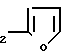
NH(CnH2n+1)2 N(CnH2n+1)3. где n 2-4;
NH2-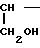
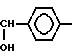 NO2
NO2
NH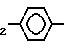 SO2-NH-
SO2-NH-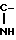 NH2;
NH2;
HN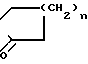 где n 1-3, NH2(CH2)nCOOH, где n 3-5, а также гуанидин, мочевина, тиомочевина.
где n 1-3, NH2(CH2)nCOOH, где n 3-5, а также гуанидин, мочевина, тиомочевина.
При этом следует отметить, что главным компонентом соединений, обеспечивающим гипогликемическую активность, является группировка SO3H˙R6, где R6 аминокомпоненты из группы самых различных аминопроизводных; алифатических, ароматических, гетероциклических аминов, аминокислот и др.
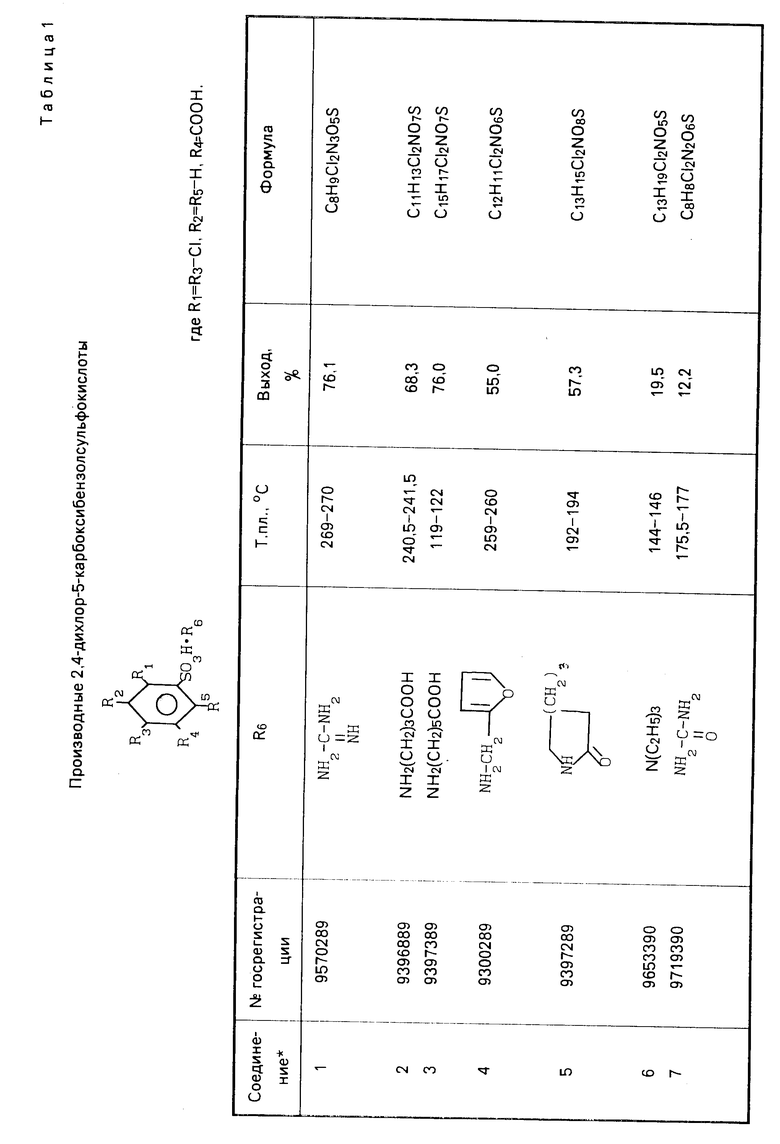
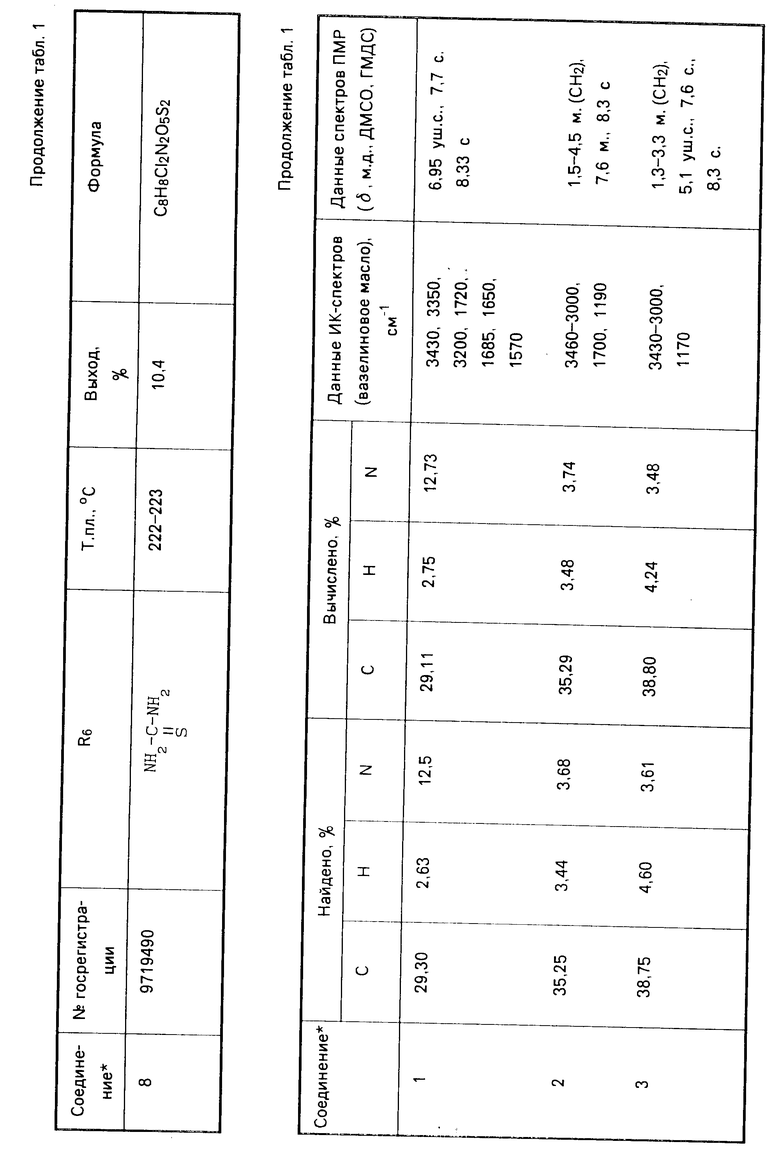
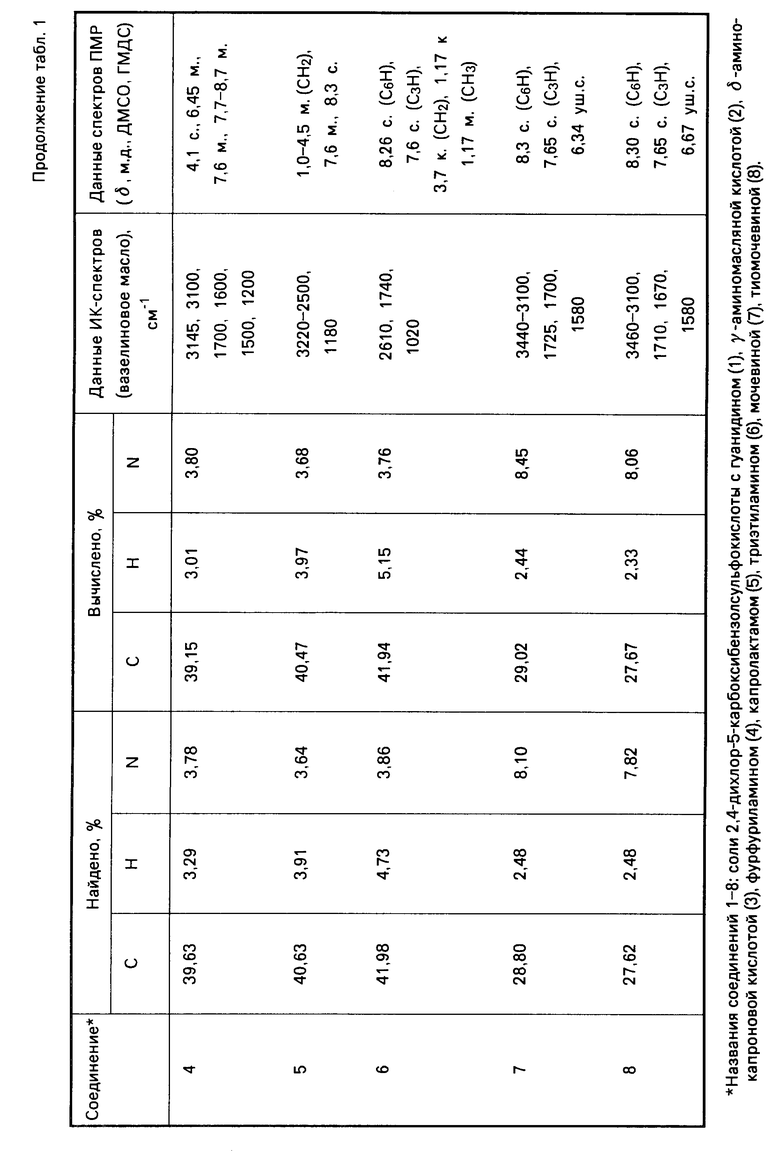
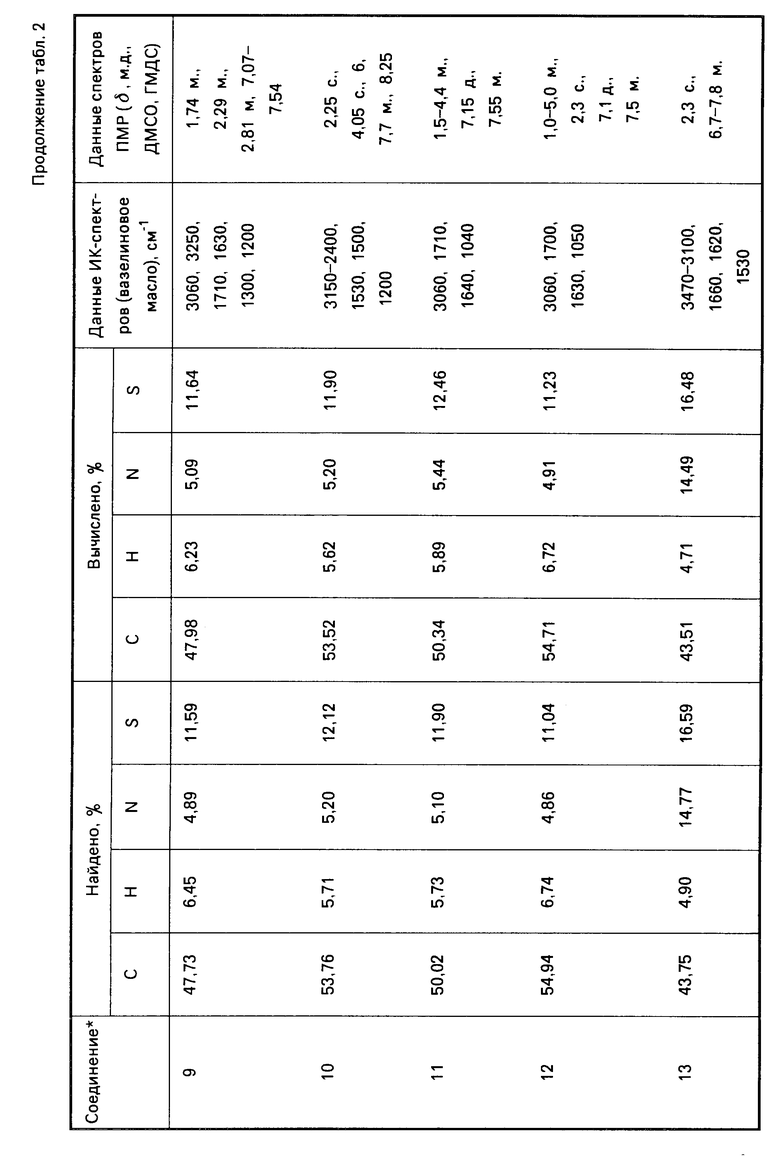
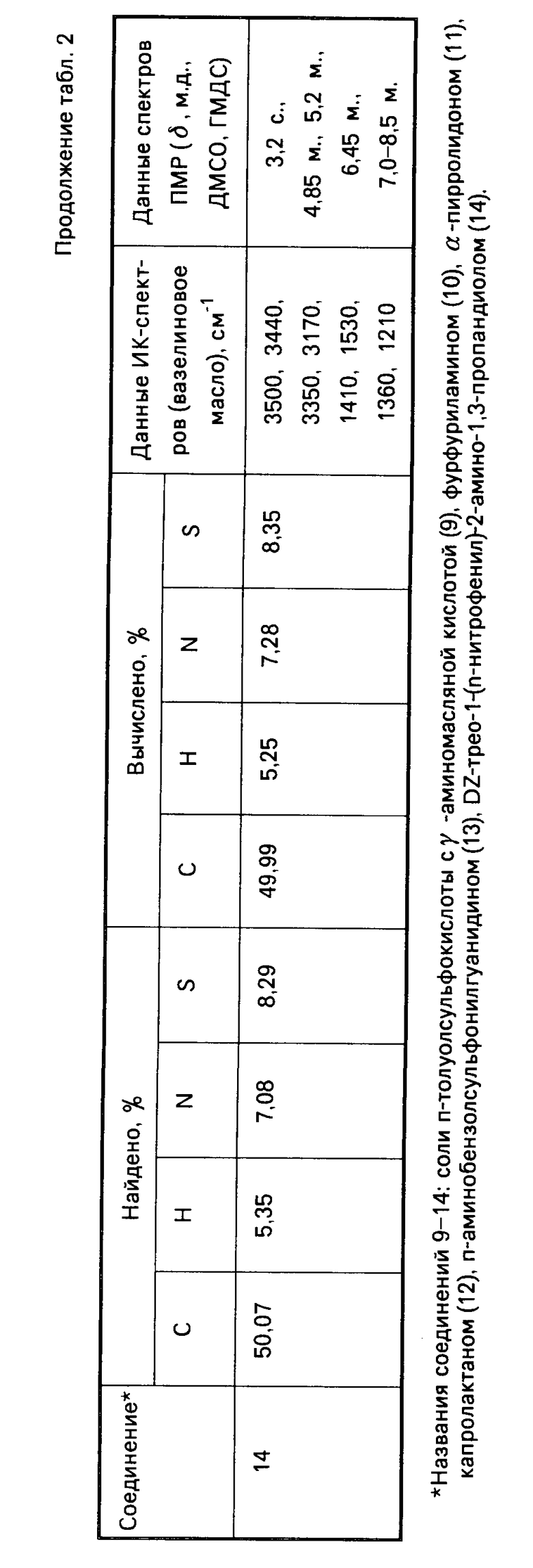
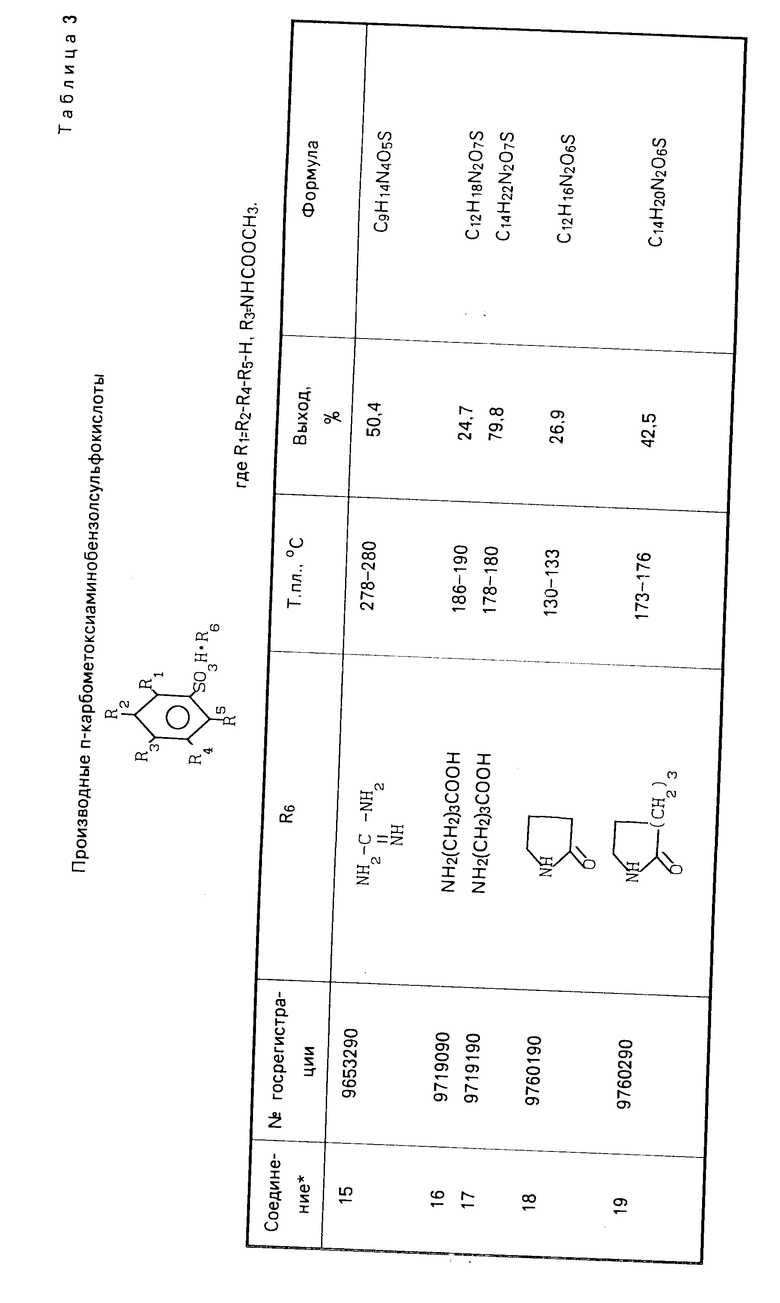
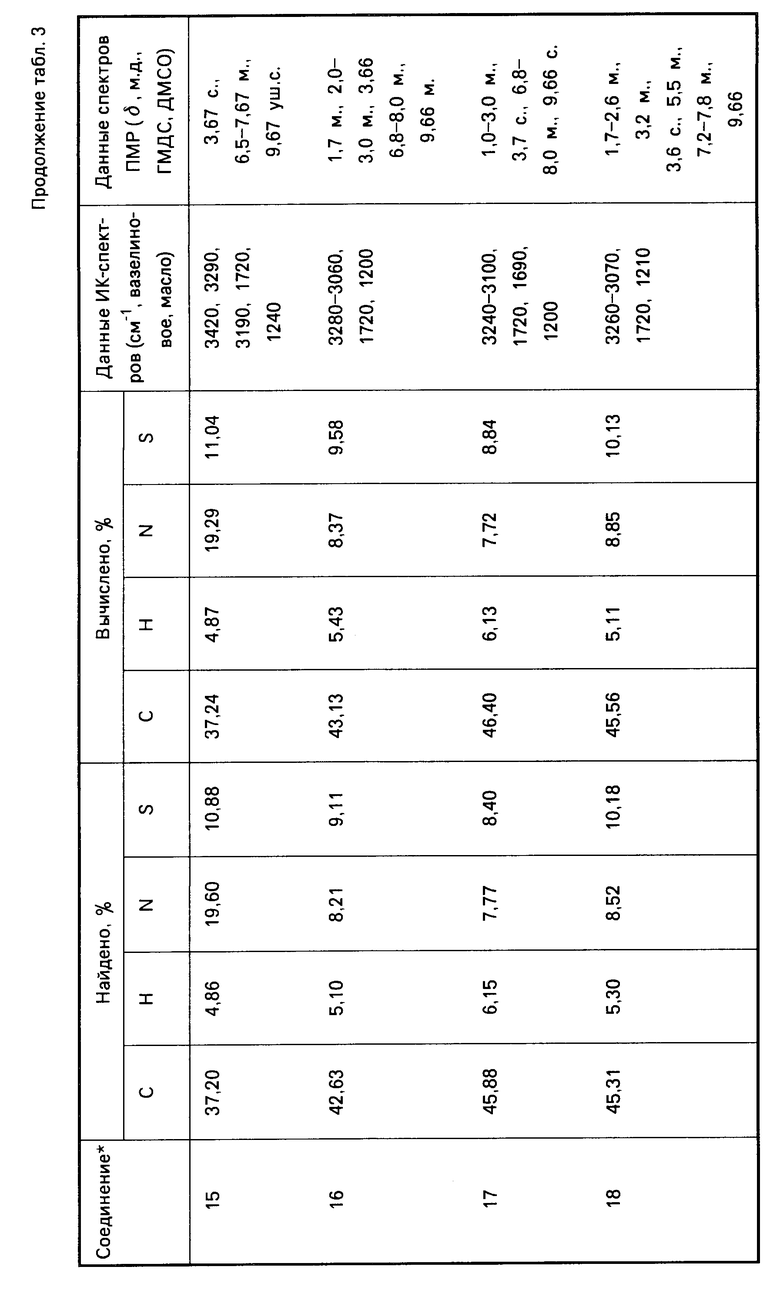
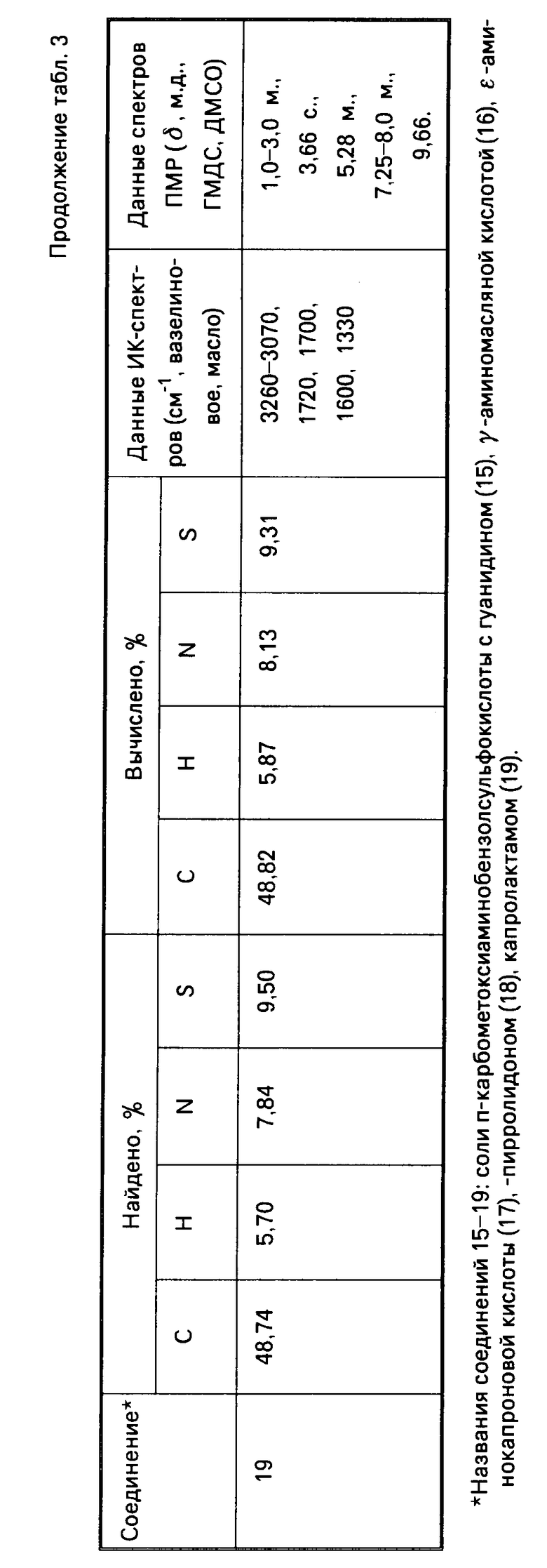
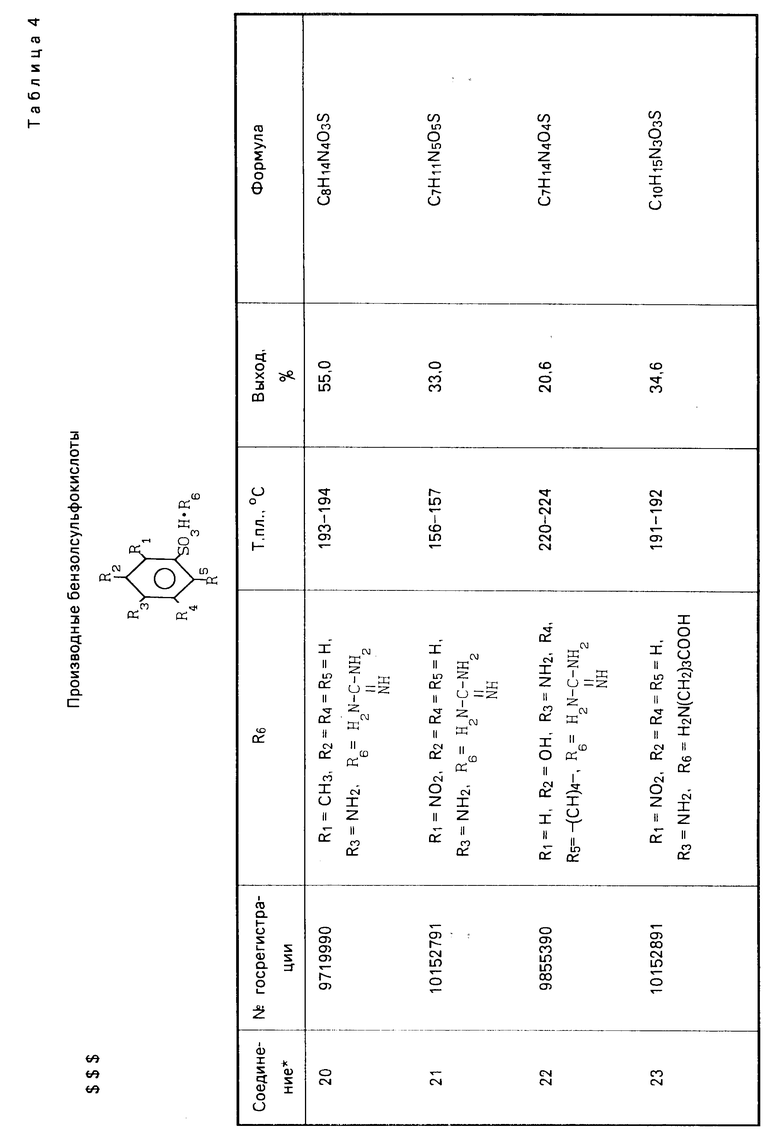
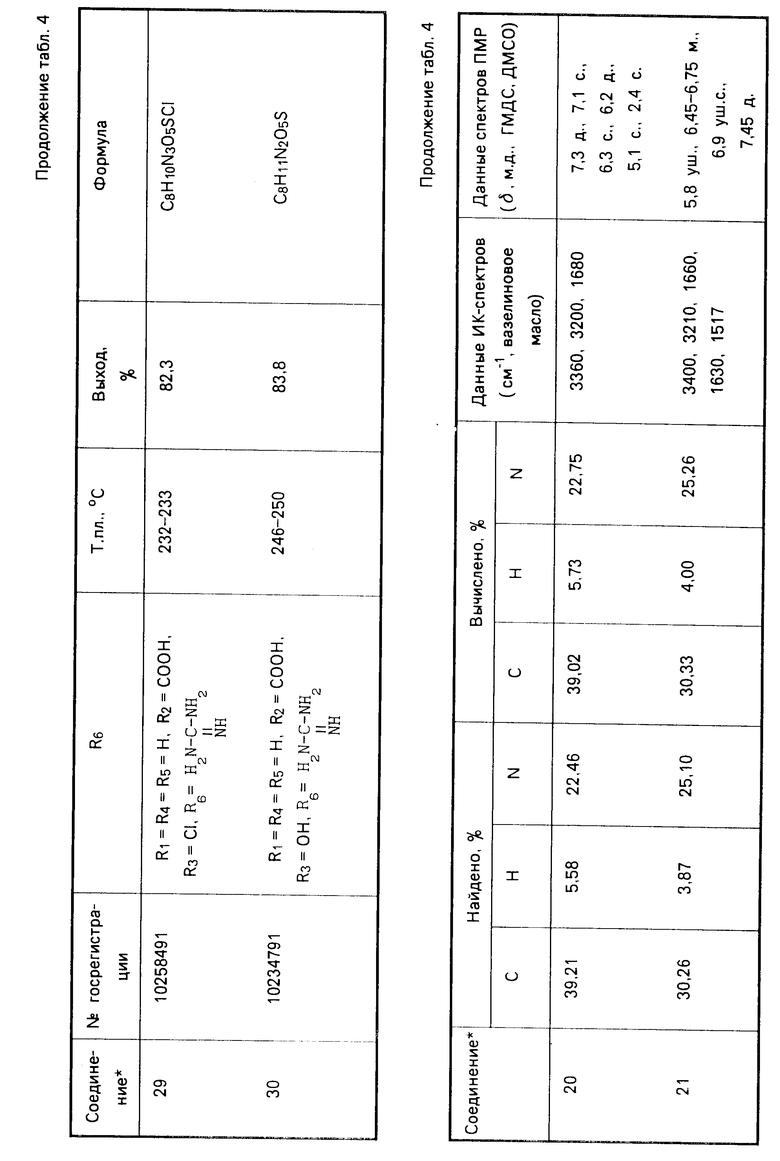
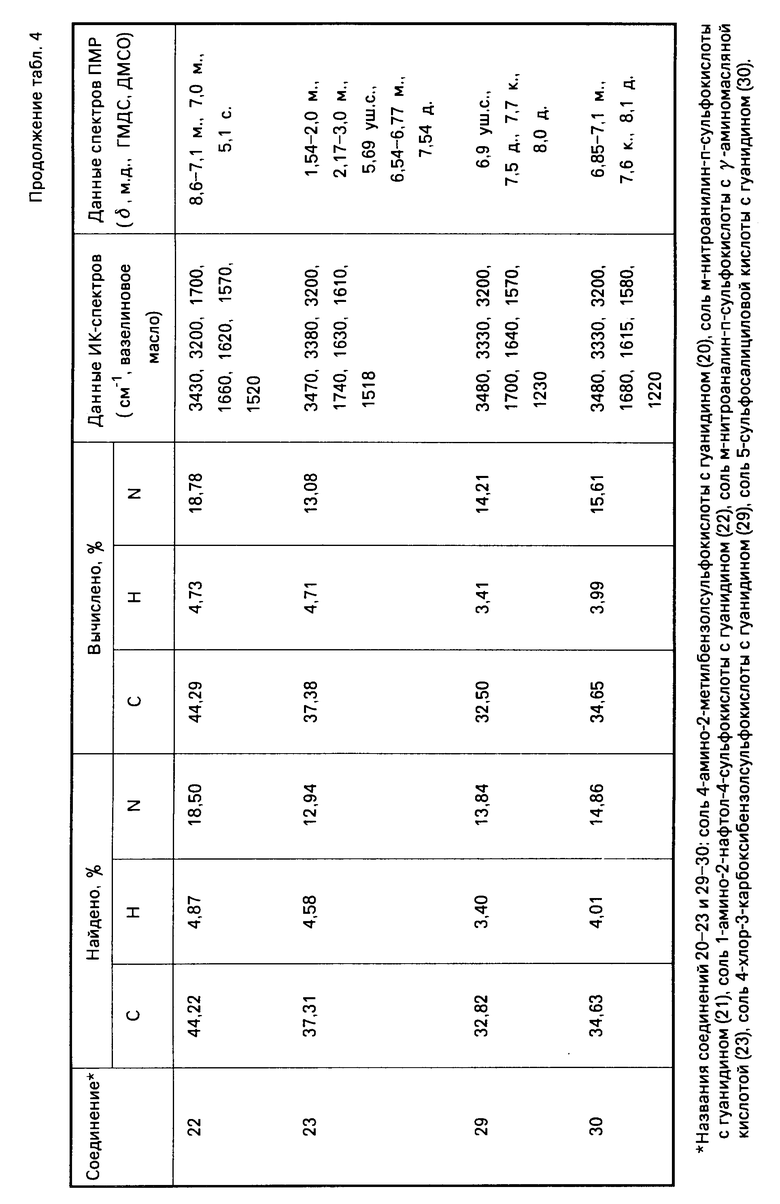
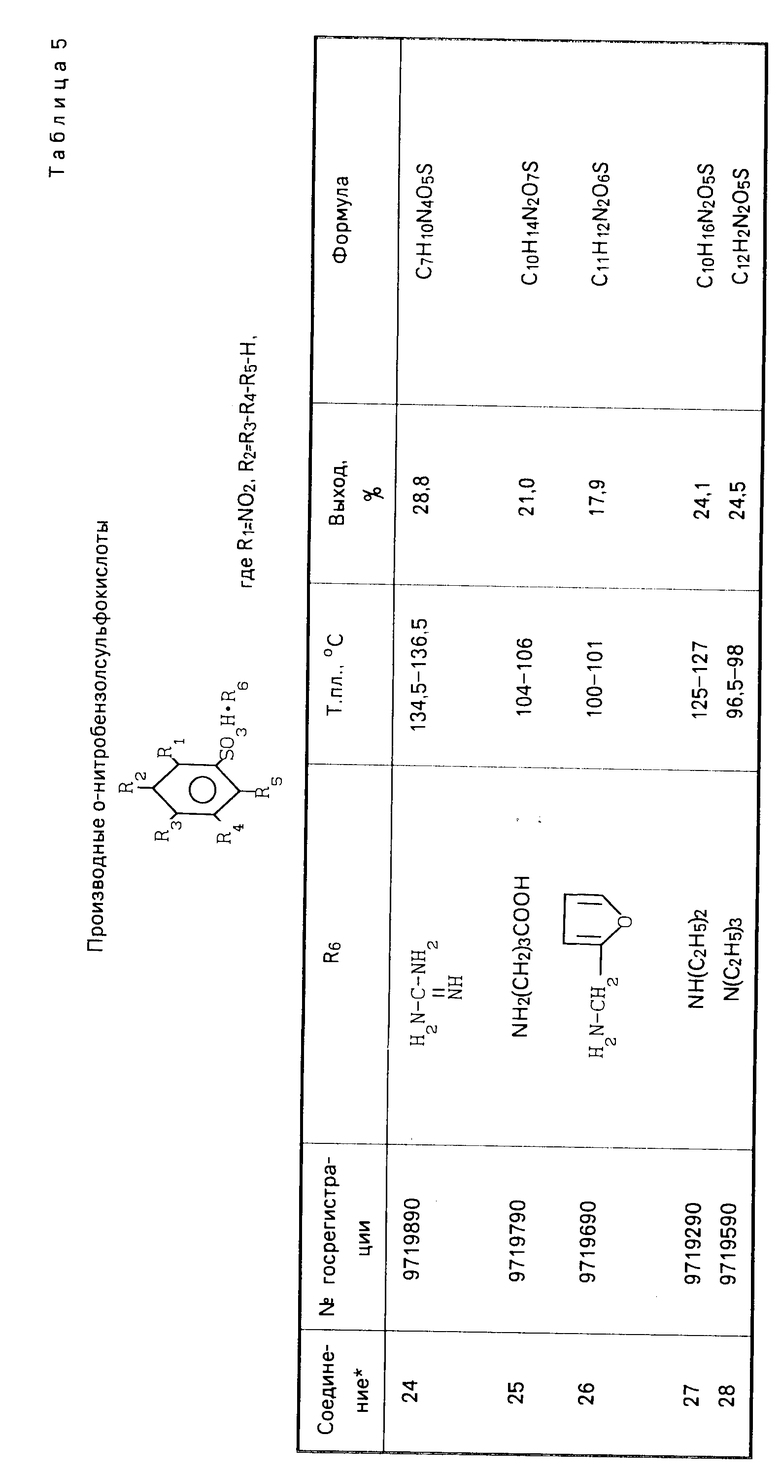
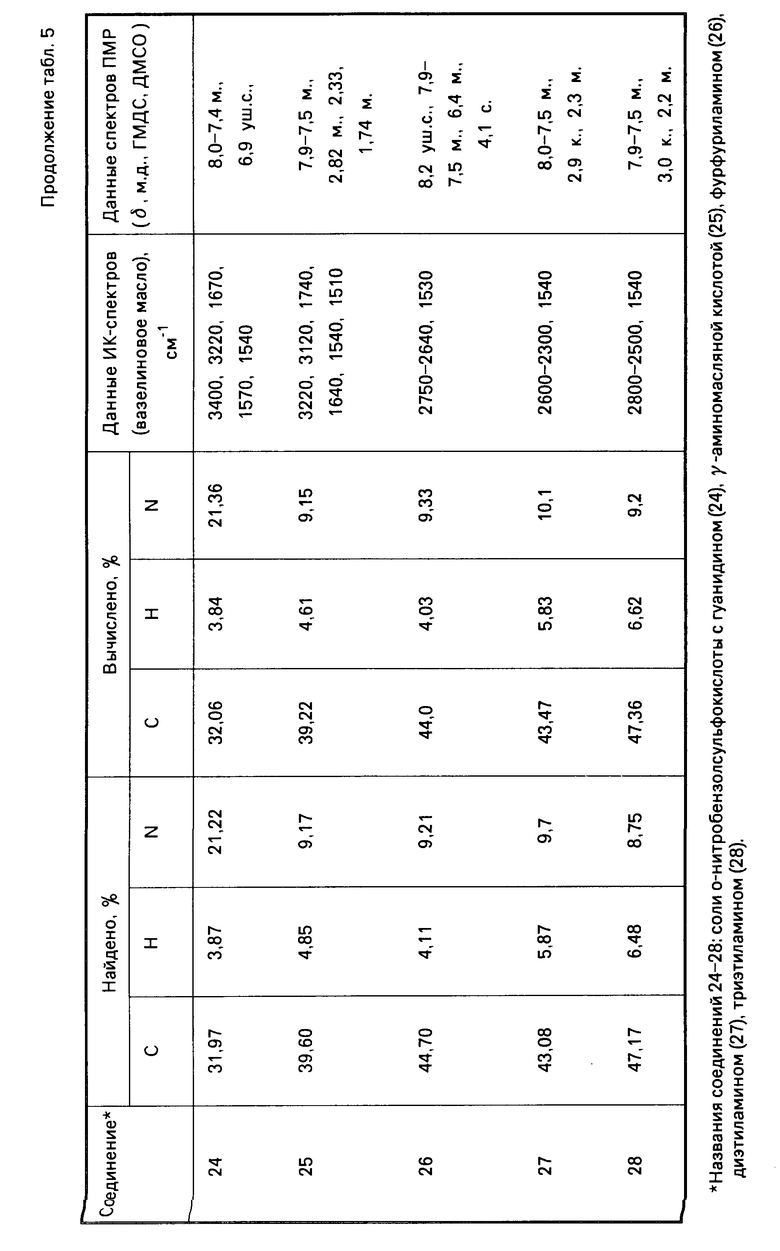
Указанные соединения получают известным способом взаимодействием эквимолекулярных количеств арилсульфокислоты с соответствующим аминокомпонентом. Данные элементного анализа, температуры плавления, выходы синтезированных соединений, параметры ИК- и ПМР-спектров представлены в табл.1-5.
П р и м е р 1. Получение гуанидиновой соли 2,4-дихлор-5-карбоксибензолсульфокислоты (соединение).
В трехгорлую колбу, снабженную мешалкой, термометром и холодильником с газоотводной трубкой, загружают 28,9 г (0,1 моль) 2,4-дихлор-5-хлорсульфонилбензойной кислоты, 80 мл дистиллированной воды и нагревают в бане до кипения. После полного растворения добавляют 0,5 г активированного угля и через 20 мин горячий раствор фильтруют и охлаждают до комнатной температуры. К полученному раствору сульфокислоты прибавляют свежеприготовленный раствор гуанидина основания. Для этого берут 11,93 г 80%-ного (9,55 г 100%-ного, 0,1 моль) гуанидина гидрохлорида, растворяют в 20 мг воды и отфильтровывают от нерастворимых в воде примесей, добавляют 4,0 г (0,1 моль) едкого натра, перемешивают до полного растворения.
После сливания двух растворов реакционную массу охлаждают до 0-5оС и выдерживают при перемешивании несколько часов, затем отфильтровывают выпавший осадок, перекристаллизовывают его из воды. Получают 25,1 г гуанидиновой соли 2,4-дихлор-5- карбоксибензолсульфокислоты (1), выход 76,1%
Аналогично получают соединения 2-8, 15-19, 24-28. Константы и выходы указанных соединений приведены в табл.1, 3 и 5.
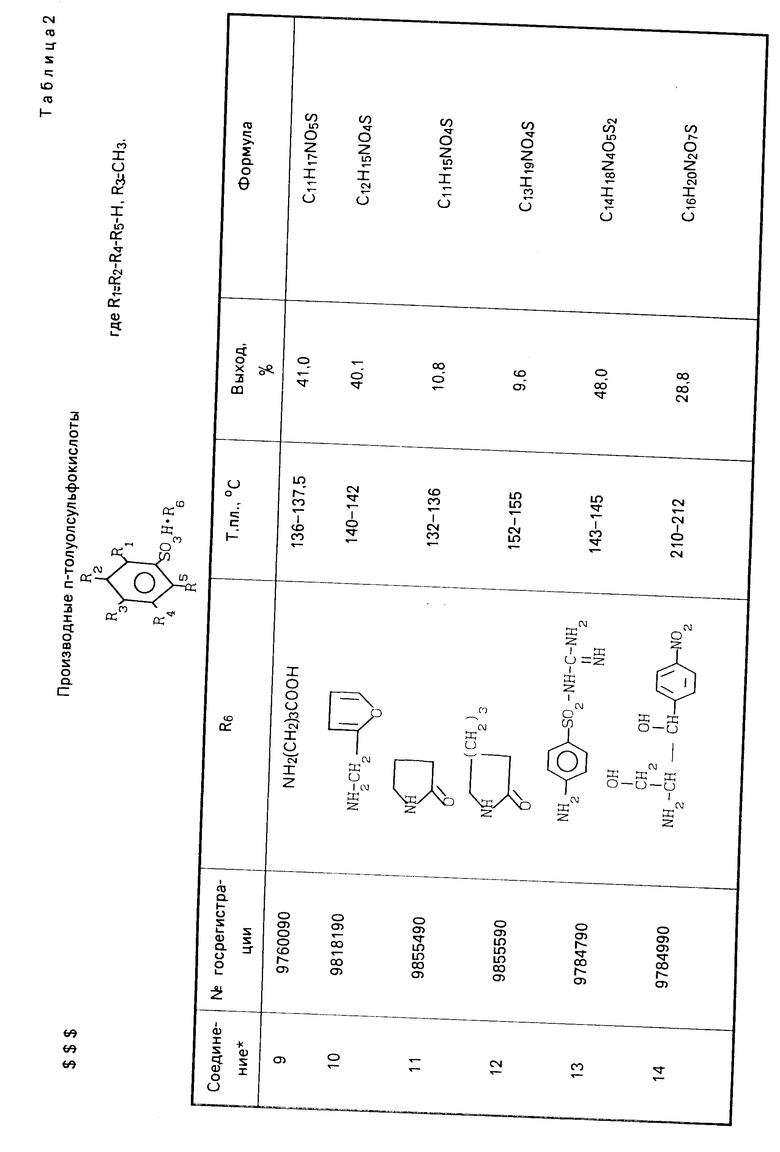
П р и м е р 2. Получение соли п-толуолсульфокислоты с γ-аминомасляной кислотой (соединение 9).
В стеклянном стакане растворяют 9,5 г (0,05 моль) п-толуолсульфокислоты в 10 мл воды, к полученному раствору прибавляют 5,2 г (0,05 моль) γ-аминомасляной кислоты, перемешивают и выдерживают при температуре 0-5оС несколько часов. Отфильтровывают выпавший осадок и перекристаллизовывают из воды. Получают 5,6 г соли п-толуолсульфокислоты с γ-аминомасляной кислотой (9), выход 41%
Аналогично получают соединения 10-14, 20-23, 29, 30. Константы и выходы указанных соединений приведены в табл.2 и 4.
Острая токсичность заявляемых соединений изучена на белых мышах весом 18-20 г с определением величины ЛД50 по Литчфилду и Уилкоксону при внутрибрюшинном введении соединений в водном растворе.
Гипогликемизирующая активность изучена на белых крысах с экспериментальным аллоксановым диабетом, вызванным однократным внутримышечным введением аллоксангидрата в дозе 165 мг/кг. Апробацию соединений начинали после развития устойчивой модели, о чем свидетельствовало появление полифагии, полидипсии, полиурии и стабильное повышение сахара в крови, содержание которого определяли ортотолуидиновым методом непосредственно до, а также через 5 ч после применения через рот в эквитоксической дозе, равной 0,1 ЛД50, изучаемых веществ, а в контроле эквиобъемного количества воды.
Животных лишали пищи за 14 ч до опыта и на время его проведения, не ограничивая водный режим.
Поскольку заявляемые соединения не имеют аналогов в ряду пероральных антидиабетических средств, то в качестве эталонов сравнения были использованы пероральные противодиабетические средства всех известных классов, букарбан (производное сульфонилмочевины), тиформин (производное γ-аминомасляной кислоты и гуанидина) и глюкофаг (производное бигуанида).
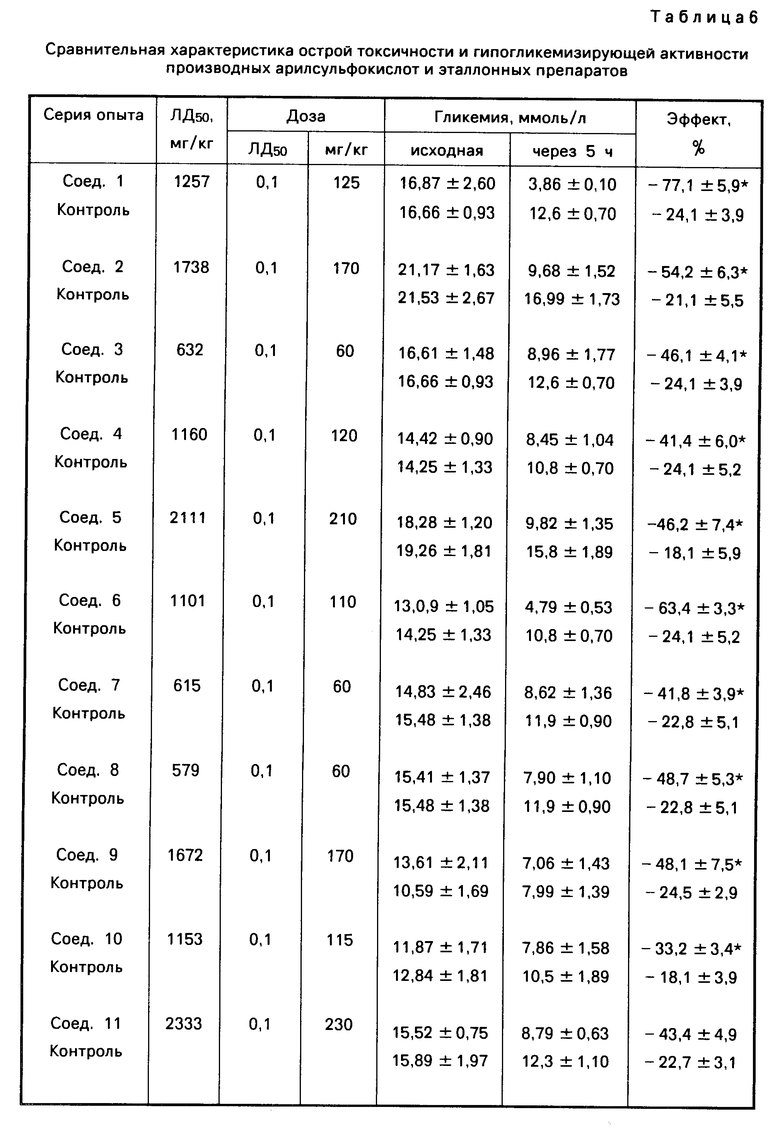
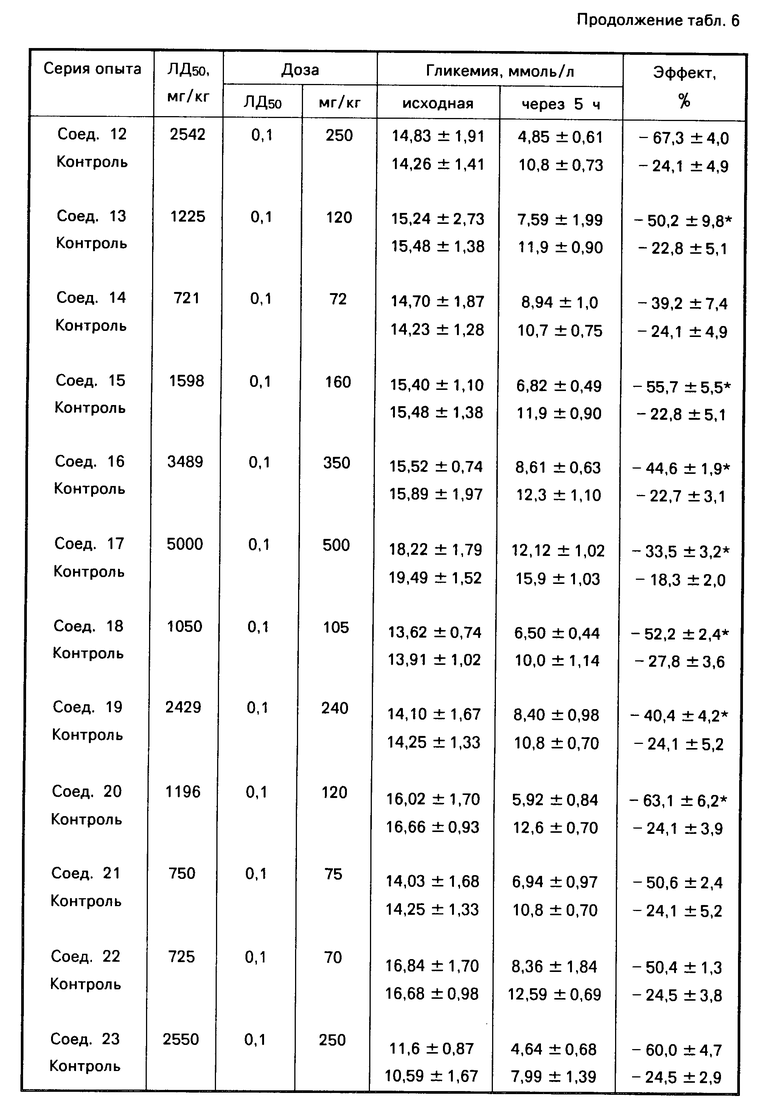
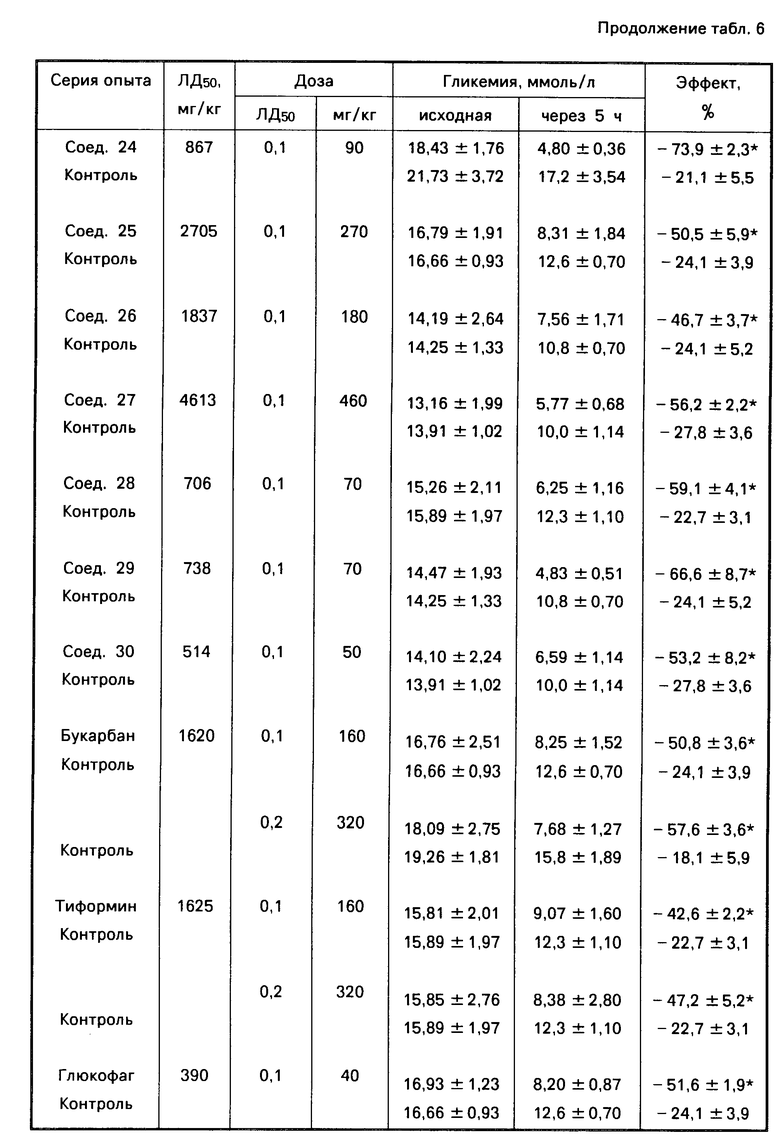
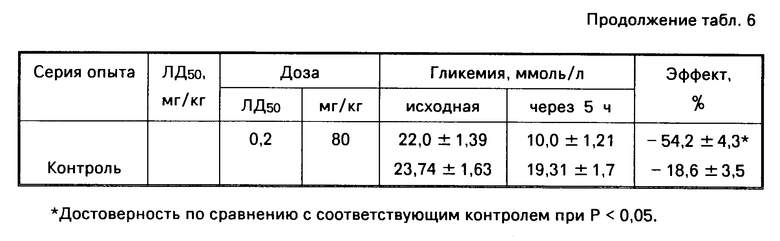
Сравнительная характеристика острой токсичности и гипогликемической активности производных арилсульфокислот и эталонных препаратов приведены в табл.6.
В результате проведенных исследований показано, что все изученные производные сульфокислот обладают низкой токсичностью: соединения 3, 7, 8, 14, 21, 22, 24, 28-30 относятся к IV классу токсичности (малотоксичны), соединения 1, 2, 4-6, 9, 10-13, 15, 18-20, 23, 25 и 26 к V классу (практически нетоксичны), а вещества 16, 17, 27 к VI классу (относительно безвредны).
Все характеризуемые вещества менее токсичны, чем эталонный бигуанид глюкофаг (в 1,3-13 раз), а соединения 9, 11, 12, 16, 17, 23, 25-27 сравнимы или превосходят по данному показателю также букарбан и тиформин (в 1,1-3,1 раза).
Все изученные соединения обладают гипогликемической активностью различной степени выраженности. Умеренный противодиабетический эффект, сравнимый с таковым эталонных препаратов, присущ соединениям 2-5, 7-11, 13-19, 22, 25-27, 30, тогда как специфическое действие веществ 1, 6, 12, 20, 24, 28 и 29 превосходит их.
Дополнительным ценным свойством заявляемых соединений является простой (фактически одностадийный) способ их получения.
Таким образом, изученные производные арилсульфокислот перспективны в качестве потенциальных сахароснижающих средств и могут служить основой создания нового направления синтеза пероральных антидиабетиков.
| название | год | авторы | номер документа |
|---|---|---|---|
| АДДУКТЫ ОРОТОВОЙ КИСЛОТЫ С АМИНОКИСЛОТАМИ ИЛИ АМИНАМИ, ПРОЯВЛЯЮЩИЕ ГЕПАТОЗАЩИТНЫЙ ЭФФЕКТ | 1993 |
|
RU2047606C1 |
| ПРОИЗВОДНЫЕ 2-(3,4-ДИГИДРОКСИФЕНИЛ)-ЭТИЛАМИНА, ПРОЯВЛЯЮЩИЕ ИММУНОТРОПНУЮ АКТИВНОСТЬ И ОБЛАДАЮЩИЕ СПОСОБНОСТЬЮ ТОРМОЗИТЬ РЕПЛИКАЦИЮ ВИРУСА | 1992 |
|
RU2039733C1 |
| 5-ГИДРОКСИНИКОТИНАТ МАГНИЯ, ОБЛАДАЮЩИЙ КОМПЛЕКСНЫМ АНТИДИАБЕТИЧЕСКИМ ДЕЙСТВИЕМ | 1998 |
|
RU2136663C1 |
| 1-БЕНЗИЛ-2-ОКСОТРИПТАМИН ГИДРОХЛОРИД И ЕГО ПРОИЗВОДНЫЕ, ОБЛАДАЮЩИЕ ГЕПАТОЗАЩИТНОЙ АКТИВНОСТЬЮ | 1994 |
|
RU2084449C1 |
| ЩЕЛОЧНЫЕ СОЛИ АМИДОВ ОРОТОВОЙ КИСЛОТЫ И АМИНОКИСЛОТ, ОБЛАДАЮЩИЕ ГИПЕРТЕНЗИВНЫМ ЭФФЕКТОМ | 1995 |
|
RU2086543C1 |
| ПРОИЗВОДНЫЕ 3,4-ДИГИДРО- ИЛИ 1,2,3,4-ТЕТРАГИДРО- β -КАРБОЛИНОВ ИЛИ ИХ СОЛИ С ОРГАНИЧЕСКИМИ ИЛИ НЕОРГАНИЧЕСКИМИ КИСЛОТАМИ, ПРОЯВЛЯЮЩИЕ АНТИМИКРОБНУЮ АКТИВНОСТЬ | 1994 |
|
RU2068847C1 |
| СПОСОБ ВЫДЕЛЕНИЯ 3-ХЛОР-4,6-ДИХЛОРСУЛЬФОНИЛАНИЛИНА | 1990 |
|
RU1736145C |
| АНТИАЛЛЕРГИЧЕСКОЕ И ПРОТИВОВОСПАЛИТЕЛЬНОЕ СРЕДСТВО | 1999 |
|
RU2170091C2 |
| ПРОИЗВОДНЫЕ 2-АМИНО-1,3,4-ТИАДИАЗОЛА, ПРОЯВЛЯЮЩИЕ АНТИМЕТАСТАТИЧЕСКУЮ АКТИВНОСТЬ | 1995 |
|
RU2114109C1 |
| ЦИНКОВЫЕ СОЛИ МОНО-ИЛИ ДИКАРБОНОВЫХ КИСЛОТ, ПРОЯВЛЯЮЩИЕ ПРОТИВОЯЗВЕННУЮ АКТИВНОСТЬ ГАСТРОЗАЩИТНОГО ТИПА | 1995 |
|
RU2116292C1 |
Использование: в качестве гипогликемического средства. Сущность изобретения: продукт (R1)(R2)(R3)(R4)(R5)C6-SO3H·R6 где R1-H, CH3, Cl, NO; R2-H, OH, COOH; R3-H CH3, Cl, OH, NH2 NHCOOH3; R4-H COOH, NO2, R5-H или R4R5-(CH)4; R6 алифатические, ароматические, циклические и гетероциклические амины, аминокислоты, гуанидин, мочевина, тиомочевина. Реагент 1: арилсульфокислоты. Реагент 2: аминокомпонент. 6 табл.
Производные арилсульфокислот общей формулы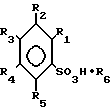
где R1 H, CH3, Cl, NO2;
R2 H, OH, COOH;
R3 H, CH3, Cl, OH, NH2, NHCOOCH3;
R4 H, COOH, NO2;
R4,R5 -(CH)4-;
R5H;
R6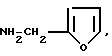 NH(CnH2n+1) 2,N(CnH2n+1)3,
NH(CnH2n+1) 2,N(CnH2n+1)3,
где n 2-4,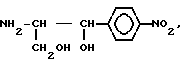
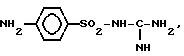
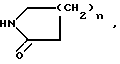
где n= 1-3, NH2(CH2)nCOOH, где n=3-5,
а также гуанидин, мочевина, тиомочевина, проявляющие гипогликемическую активность.
| Машковский М.Д | |||
| Лекарственные средства, т.1 | |||
| М.: Медицина, с.556-564, 1984. |
Авторы
Даты
1995-12-20—Публикация
1991-11-27—Подача