Изобретение относится к новым биологически активным соединениям - производным 2-амино-1,3,4-тиадиазола, обладающим антиметастатической активностью, в результате чего они могут найти применение как лекарственные препараты в медицинской практике.
Известны структурные аналоги заявляемых соединений, обладающие психотропной активностью (M.Pradcep и др. J.Indian Chem. Soc, 1990, 67 (6), 520), антимикробной активностью (B. T. Veere им др. Indian Drugs, 1986, 24 (3), 136), противоопухолевой активностью (M.Michiko Chem. Pharm. Bull, 1982, 30 (12), 4402), но не оказывающие антиметастатического действия.
Целью предлагаемого изобретения являются новые химические соединения, проявляющие антиметастатическую активность.
Поставленная цель достигается неописанными ранее производными 2-амино-1,3,4-тиадиазола общей формулы I: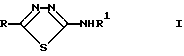 ,
,
где
R - водород или группа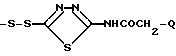 ,
,
в которой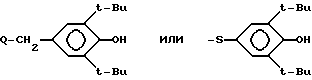
R1 группа формулы CO(CH2)nQ, где Q - хлор, если n = 3 или 4,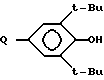 ,
,
если
n = 2 и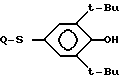 ,
,
если
n = 1
Q-CONH-N(C6H5)CH2C6H5,
когда
n = 2 или 3, проявляющие антиметастатическую активность.
Соединения I получают известными методами. Изобретение иллюстрируется следующими примерами.
Пример 1. Получение 2 - ( ω -хлоралканоиламино)-1,3,4-тиадиазолов 1 (1-2) (общая методика).
К суспензии 10 ммоль 2-аминотиадиазола в 50 мл хлороформа при перемешивании прибавляют 12 ммоль триэтиламина, охлаждают смесь до температуры 5-10oC и прикапывают раствор 12 ммоль хлорангидрида соответствующей ω-хлоркарбоновой кислоты в 30 мл хлороформа так, чтобы температура реакционной массы не превышала 10oC. Затем реакционную смесь перемешивают при комнатной температуре до исчезновения исходного 2-аминотиадиазола (ТСХ, силуфол, УФ 254, бензол-этанол-аммик, 40: 9:1), pH среды 7,5-8. По окончании реакции реакционную массу промывают водой, отделяют органический слой, сушат, упаривают. Остаток растирают в гексане, отфильтровывают осадок, промывают на фильтре гексаном. Перекристаллизовывают из этилацетата.
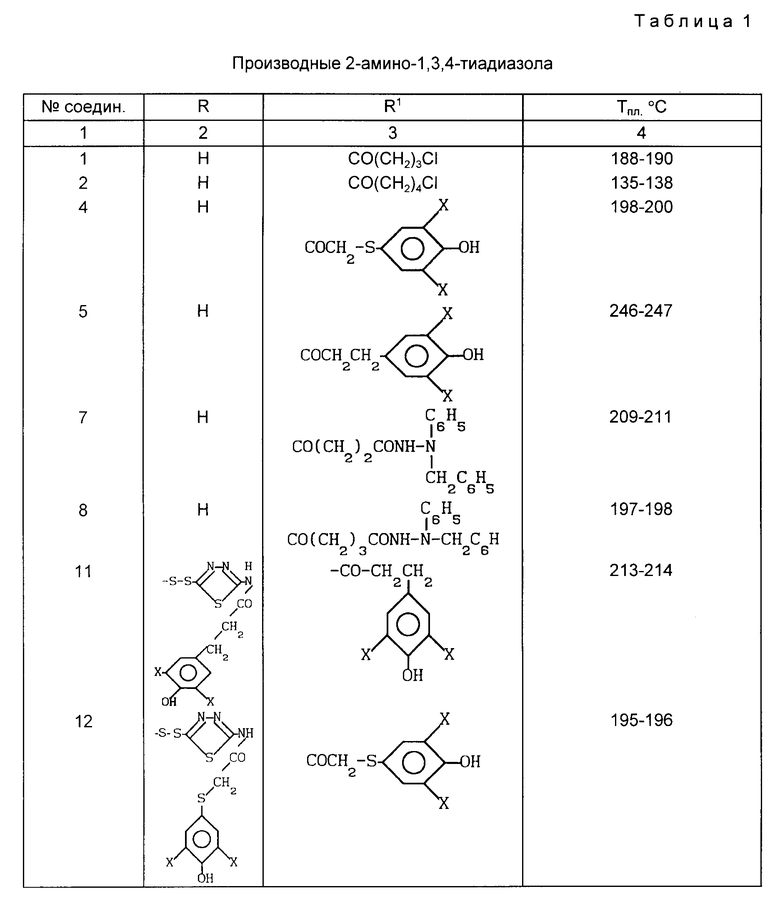
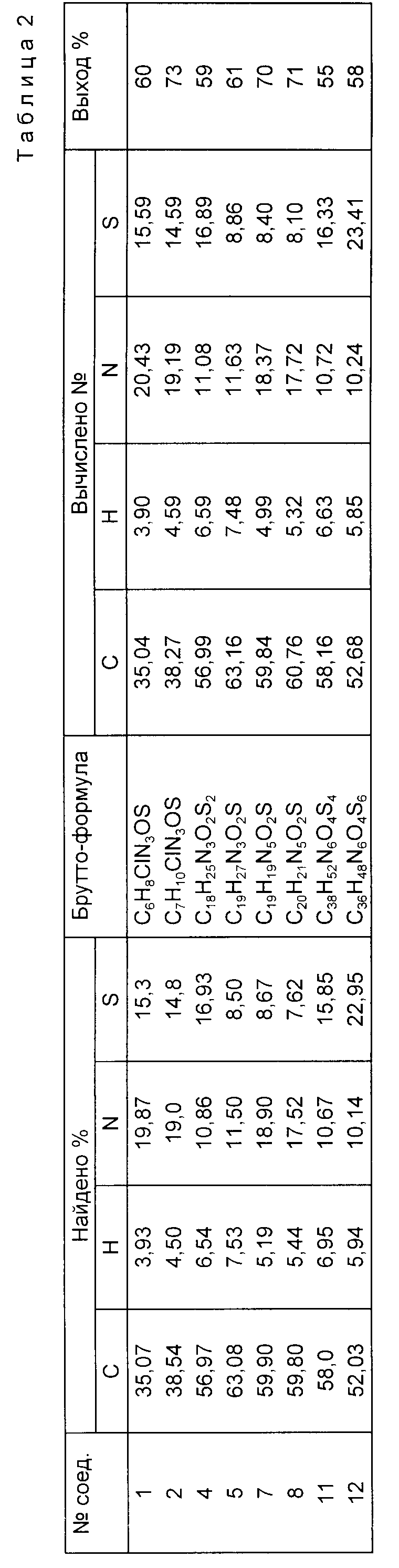
Константы и выходы полученных соединений 1 (1-2) приведены в табл. 1,2.
Пример 2. Получение 4-[(1,3,4-тиадиазол-2-ил)-аминокарбонил]бутановой кислоты 1(3).
Смесь 2 г (0,02 моль) 2 - амино-1,3,4-тиадиазола и 2,6 г (0,023 моль) глутарового ангидрида в 40 мл диоксана кипятят 12 ч. После охлаждения отфильтровывают выпавший осадок, промывают диоксаном, сушат. Кристаллизуют из спирта. Получают 3,1 г (72%) соединения 1 (3). Белые кристаллы, т.пл. 257oC. Найдено, % C 38,64; H 3,91; N 19,18; C7H9N3O3. Вычислено,%: C 39,06; H 4,22; N 19,52. ИК-спектр: 3160, 1890, 1670 см.
Пример 3. Получение 2[(4-гидрокси-3,5-ди-третбутилфенил)-ациламино] 1,3,4-тиадиазолов 1 (4-5) (общая методика).
5 ммоль 2-амино-1,3,4-тиадиазола растворяют при перемешивании в смеси ацетонитрила и воды, затем прибавляют 5 ммоль соответствующей карбоновой кислоты и 5 ммоль дициклогексилкарбодиимида. Перемешивают при комнатной температуре 6 ч, оставляют на ночь. Отфильтровывают осадок, промывают небольшим количеством хлористого метилена. Фильтрат упаривают, остаток перекристаллизовывают из этанола. Выход и характеристики соединений 4-5 приведены в табл. 1 и 2.
Пример 4. Получение 2[(бис(этоксикарбонил)метиламино] ацетиламино-1,3,4-тиадиазол 1(6).
К 0,7 г (4,1 ммоль) 2-хлорацетамидо-1,3,4-тиадиазола в 20 мл этанола прибавляют 1,0 г (4,1 ммоль) гидрохлорида диэтилового эфира иминодиуксусной кислоты 0,7 г (8,2 ммоль) бикарбоната натрия и 0,7 г (4,1 ммоль) иодистого калия, кипятят 16 ч, охлаждают, отфильтровывают осадок. Фильтрат упаривают досуха, остаток растворяют в хлороформе, переносят на колонку с окисью алюминия, элюируют хлороформом. Получают 0,88 г (65%) маслообразного вещества, которое при хранении самопроизвольно кристаллизуется. Т.пл. 73 - 74oC.
Найдено: М 330 (масс-спектрально); С 43,24; Н 5,39; N 16,52; S 9,48; С12H18N4O5S.
Вычислено: М: 330; С 43,64; Н 5,45; N 16,97; S 9,69. ИК-спектр: 3120,3070,1720,1680 см-1.
Пример 5. Получение 2-{3-[21-бензил-21-фенилгидразинокарбонил]ацил-амино{-1,3,4-тиадиазолов 1 (7-8) (общая методика).
Смесь 2 ммоль соответствующей 2-бензил-2-фенилгидразинокарбонилалканкарбоновой кислоты и 2 ммоль триэтиламина в 15 мл хлороформа охлаждают до -5oC, прибавляют 2 ммоль изобутилхлоркарбоната, перемешивают 30 мин при -5oC, затем добавляют 2 ммоль 2-амино-1,3,4-тиадиазола и осталяют при перемешивании на 3 ч. Отфильтровывают осадок, промывают водой, сушат, перекристаллизовывают из этанола.
Выход характеристики соединений 1 (7-8) приведены в таб.1 и 2.
Пример 6. Получение 1,3-диметил 2-[N(1,3,4-тиадиазолил)-амино]ацетамидоиндола I (9).
0,9 г (3,8 ммоль) 1,3-диметил-3-хлорацетамидоиндола 1(3) и 0,76 г (7,6 ммоль) 2-амино-1,3,4-тиадиазола в 20 мл ацетонитрила кипятят 14 ч, затем упаривают ацетонитрил, к остатку приливают 10 мл хлороформа, отфильтровывают образующиеся кристаллы, промывают водой, затем спиртом, сушат. Получают 0,65 (58%) соединения I(9), т. пл. 218oC. Найдено: М 301 (масс-спектрально), S 10,51%; C14H15N5SO. Вычислено: М 301; S 10,63%.
Пример 7. Получение 1-(3,4-дихлорфенил)-3-(1,3,4-тиадиазол-2-ил)триазена I(10).
К суспензии 1,0 г (0,01 моль) 2-амино-1,3,4-тиадиазола и 2 г ацетата натрия в 10 мл ледяной уксусной кислоты при охлаждении (+5oC) и при перемешивании прибавляют порциями раствор соли диазония, полученной обычным методом из 1,62 (0,01 моль) 3,4-дихлоранилина. Реакционную смесь перемешивают 2 ч при 0oC, отфильтровывают осадок, промывают водой, сушат в темноте. Получают 1,79 г (65%) соединения I(10) т.пл. 186 - 187oC (разл.). Найдено: М 274 (масс-спектрально), С 34,90%, H 2,08%.
C8H5Cl2N5S, вычислено: М 274; C 35,04%; H 1,82%. ИК-спектр: 3420,1635 см-1.
Пример 8. Получение 5,5-дитио-бис{ 2(4-гидрокси-3,5-ди-третбутилфенил)ацил]амино}-1.3,4-тиадиазолы 1 (11-12).
Растворяют при перемешивании 4 ммоль 5,5-дитио-бис-(2-амино-1,3,4-тиадиазола), полученного по известной методике (Рубцов М.В. и Байчиков А.Г. Синтетические химико-фармацевтические препараты. М., 1971, с. 176) в смеси ацетонитрила и воды 10:1. Прибавляют 8 ммоль 4-гидрокси-2,3-ди-трет-бутилфенилтиоуксусной (для получения соединения 12) или 8 ммоль 4-гидрокси-2,3-ди-трет-бутилфенилпропионовой (для получения соединения 11) кислоты и 8 ммоль дициклогексилкарбодиимида, перемешивают 7 ч. при комнатной температуре, отфильтровывают осадок, фильтрат упаривают досуха, к остатку приливают эфир, охлаждают, отфильтровывают образующийся осадок. Выход и характеристика соединения 1 (11-12) в табл. 1 и 2.
Оценку антиметастатической активности предлагаемых соединений проводили, используя в качестве тест-объекта сигненную опухолевую систему карциному легкого Льюис. Экспериментальным животным-мышам линии ВДГ1, самками массой 20-23 г внутримышечно перевивали опухолевую взвесь. Начиная с 7 сут после трансплантации, 3-4-кратно через день внутримышечно вводили испытуемые вещества в крахмальном геле. На 21 сутки животных забивали, взвешивали первичную опухоль и после фиксации в растворе Боуэна подсчитывали под микроскопом количество микроскопических колоний в легких.
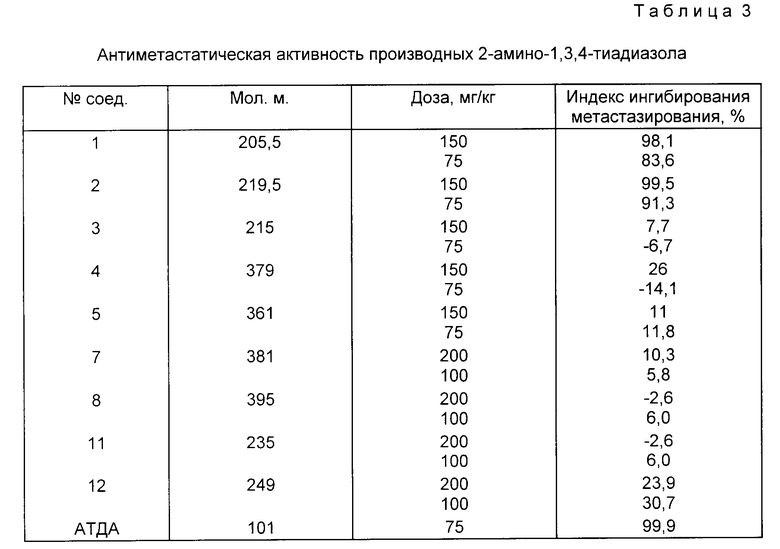
Результаты испытаний синтезированных соединений, включая 2-амино-1,3,4-тиадиазол (АТДА), представлены в табл. 3.
Из представленных в табл. 3 данных следует, что производные АТДА обладают достаточно высоким антиметастатическим действием. Так, например, соединения 1,2,11 на 97-99% подавляют образование метастазов в легких экспериментальных животных, что соответствует степени ингибирования метастазов исходным соединением АТДА. Однако следует отметить, что по показаниям токсичности новые соединения отличаются от исходного. При изучении ЛД50 для некоторых наиболее активных соединений методом Литчфилда и Уилкоксона установлено, что ЛД50 для соединения 1 при внутрижелудочном введении равняется 2860 мг/кг, а при внутрибрюшинном введении 1450 мг/кг. При этом известно, что у АТДА ЛД50 при пероральном введении равняется 1910 мг/кг, а при внутрибрюшинном 235 мг/кг (Hill Donald L., Aminothiadiazoles Cancer Chemother Phormacol, 1980, 4(4), 215-220).
По химической структуре среди противоопухолевых препаратов аналогов представляемым химическим соединениям нет. По механизму действия наиболее близок антиметаболит фторафур - один из известных и высокоэффективных лекарственных препаратов. При изучении антиметастатического действия фторафура на модели опухоли Льюс (Shiio Tsuyoshi Jagari Jasumi "Huxonnaraky pexoreckoi gzaccu, Chemotherary, 1987, 35, N 7, 551-556) установлено, что 5-кратное пероральное введение препарата в дозах 75-100 мг/кг снижает число метастатических колоний в легких на 61-82%. Кроме того, токсичность фторафура выше, ЛД50 при внутрибрюшинном введении мышам равна 600 мг/кг (ред. H.H. Блохин. Химиотерапия злокачественных опухолей. М.: Медицина, 1977).
Таким образом, проведенные исследования показали, что данный класс соединений обладает антиметастатической активностью, а отдельные его представители могут составить основу для разработки принципиально новых противоопухолевых средств - антиметастатиков.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ 3,4-ДИГИДРО- ИЛИ 1,2,3,4-ТЕТРАГИДРО- β -КАРБОЛИНОВ ИЛИ ИХ СОЛИ С ОРГАНИЧЕСКИМИ ИЛИ НЕОРГАНИЧЕСКИМИ КИСЛОТАМИ, ПРОЯВЛЯЮЩИЕ АНТИМИКРОБНУЮ АКТИВНОСТЬ | 1994 |
|
RU2068847C1 |
| СПОСОБ ПОЛУЧЕНИЯ КИСЛОТНО-АДДИТИВНЫХ СОЛЕЙ ТРУДНОРАСТВОРИМЫХ КАРБОНОВЫХ КИСЛОТ И АМИНОВ ИЛИ АМИНОКИСЛОТ | 1993 |
|
RU2084441C1 |
| ЩЕЛОЧНЫЕ СОЛИ АМИДОВ ОРОТОВОЙ КИСЛОТЫ И АМИНОКИСЛОТ, ОБЛАДАЮЩИЕ ГИПЕРТЕНЗИВНЫМ ЭФФЕКТОМ | 1995 |
|
RU2086543C1 |
| ПРОИЗВОДНЫЕ 2-(3,4-ДИГИДРОКСИФЕНИЛ)-ЭТИЛАМИНА, ПРОЯВЛЯЮЩИЕ ИММУНОТРОПНУЮ АКТИВНОСТЬ И ОБЛАДАЮЩИЕ СПОСОБНОСТЬЮ ТОРМОЗИТЬ РЕПЛИКАЦИЮ ВИРУСА | 1992 |
|
RU2039733C1 |
| АДДУКТЫ ОРОТОВОЙ КИСЛОТЫ С АМИНОКИСЛОТАМИ ИЛИ АМИНАМИ, ПРОЯВЛЯЮЩИЕ ГЕПАТОЗАЩИТНЫЙ ЭФФЕКТ | 1993 |
|
RU2047606C1 |
| 1-БЕНЗИЛ-2-ОКСОТРИПТАМИН ГИДРОХЛОРИД И ЕГО ПРОИЗВОДНЫЕ, ОБЛАДАЮЩИЕ ГЕПАТОЗАЩИТНОЙ АКТИВНОСТЬЮ | 1994 |
|
RU2084449C1 |
| ЦИНКОВЫЕ СОЛИ МОНО-ИЛИ ДИКАРБОНОВЫХ КИСЛОТ, ПРОЯВЛЯЮЩИЕ ПРОТИВОЯЗВЕННУЮ АКТИВНОСТЬ ГАСТРОЗАЩИТНОГО ТИПА | 1995 |
|
RU2116292C1 |
| СОЛИ АЗОТСОДЕРЖАЩИХ ГЕТЕРОЦИКЛИЧЕСКИХ ПРОИЗВОДНЫХ И 5-ГИДРОКСИНИКОТИНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩИЕ АНТИАНГИНАЛЬНЫМИ И ПРОТИВОАРИТМИЧЕСКИМИ СВОЙСТВАМИ | 1993 |
|
RU2067577C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОЛЕЙ ГИДРОХИНОНСУЛЬФОКИСЛОТЫ | 1992 |
|
RU2041872C1 |
| ОСНОВАНИЯ ШИФФА 2-АМИНОИНДОЛА, ПРОЯВЛЯЮЩИЕ ГЕПАТОПРОТЕКТОРНУЮ АКТИВНОСТЬ | 1994 |
|
RU2084450C1 |
Изобретение относится к новым биологически активным соединениям. Производные 2-амино-1,3,4-тиадиазола, полученные действием аминотиадиазола с соответствующей карбоновой кислотой или ее галоидангидридом, могут быть использованы в качестве лекарственного препарата, обладающего антиметастатической активностью. 3 табл.
Производные 2-амино-1,3,4-тиадиазола общей формулы I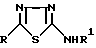
где
R - водород или группа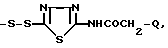 ,
,
где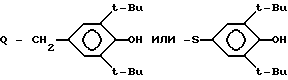 ,
,
R1 - группа формулы CO(CH2)n Q, где Q - хлор, если n = 3 или 4,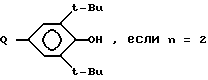
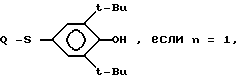
Q -CONH-N(C6H5)CH2C6H5, когда n = 2 или 3,
проявляющие антиметастатическую активность.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| J | |||
| Indian Chem | |||
| Soc., 67 (6), 520, 1990 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Indian Dmugs, 24(3), 136, 1986 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Chem | |||
| Pharm | |||
| Bull., 30(12), 4402, 1982 | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Cancer | |||
| Chemother Phar macol, 4(4), 215-220, 1980 | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Chemotherary, 35, N 7, 1987, 551-556 | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Бл охин Н.Н | |||
| Химиотерапия злокачественных опухолей, - M.: Медицина, 1977. | |||
Авторы
Даты
1998-06-27—Публикация
1995-09-19—Подача