Изобретение касается способа электролитического совместного осаждения кадмия и железа в губчатой форме для приготовления активной массы отрицательных электродов щелочных аккумуляторов с применением электролита из сернокислых солей и отдельных анодов из растворяемых металлов.
В предлагаемом способе для автоматической регулировки кислотности электролита и получения однородного по составу осадка предназначен дополнительный нерастворимый диафрагмированный анод.
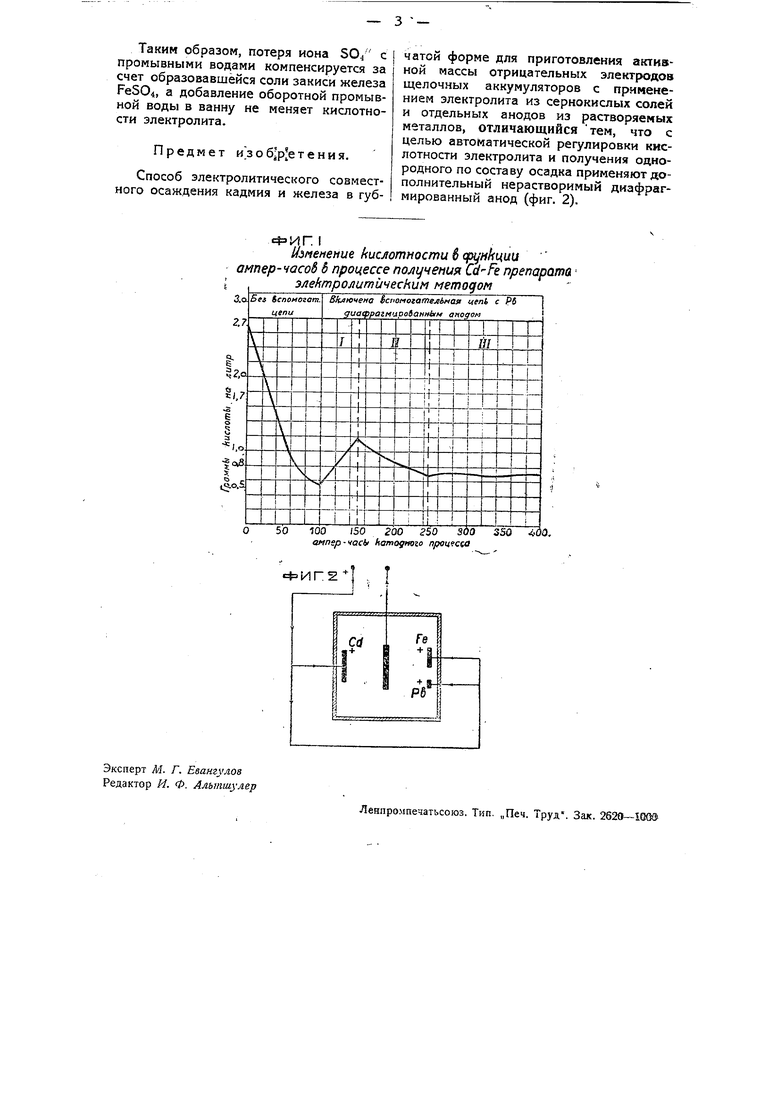
На чертеже фиг. 1 изображает диаграмму изменения кислотности электролита в функции ампер-часов процесса и фиг. 2 - схему включения ваннь с применением дополнительной цепи с нерастворимым анодом.
Электролитический метод получения Cd - Fe губчатого осадка, в общих чертах описанный в патенте Юнгера, сводится к тому, что из растворов сернокислых солей кадмия и железа при растворимых анодах Cd и Fe и катодной плотности тока около 10 ампер на квадратный дециметр осаждают на катоде Cd - Fe сплав или смесь в губчатой форме.
Для правильного ведения процесса необходимо электролит поддерживать слабо кислым. В данном случае одновременного осаждения двух металлов при необходимости длительного сохранения постоянства состава катодного
/Cd,
осадка (отношение -р) ведение процесса без частой корректуры электролита встречает значительные трудности. Одно из существенных затруднений вызывается неодинаковым реагированием Cd и Ре на степень кислотности электролита:
1)Катодный вуход Cd значительно менее чувствителен к кислотности, нежели Fe.
2)В момент, близкий к нейтрализации, происходит побочная реакция, а именно образуется Fe(OH)2, легко переходящий в Fe(OH)3 по уравнению 4Fe(OH)o + ЗНзО + O. - 4Ре(ОН)з.
С другой стороны нетрудно видеть, что самый процесс по cyifi дела связан с постоянным уменьшением содержания свободной кислоты электролита, так как нормальные электрохимические реакции выражаются уравнениями:
На катоде
+ 2(-) металл
(-) металл
2Н-- + 2(-) газ
На аноде Qd - 2(-) Fe -2(-)
то-есть, нормальному растворению металлов на аноде противостоит дополнительный процесс выделения водорода на катоде, на который расходуется часть суммарного тока. Кроме того, мелко раздробленные металлы, а также анодный шлам легко поддаются действию электролита даже той слабой кислотности, которая требуется данным процессом, т. е. происходят химические реакции
Cd- CdS04
,,+2H2SO4 +2Н,
Fe FeSOj
Следовательно, если не будет обеспечено постоянство кислотности, состав электролита быстро изменяется, а вместе с ним и состав катодного осадка. Это вызывает необходимость постоянного контроля ванны и корректуры электролита добавлением серной кислоты.
Для автоматического регулирования кислотности электролита предлагается к двум цепям с растворимыми анодами Cd и Fe ввести дополнительную цепь с нерастворимым анодом, то-есть побочным процессам электрохимического и химического выделения водорода противопоставить в эквивалентном количестве выделение кислорода на аноде, чтобы кислотность в течение процесса сохранялась неизменной.
Практическое оформление нерастворимого анода для данного процесса сох:тоит в применении свинцового или другого нерастворимого в сернокислом электролите электрода, диафрагмированного тем или иным из известных способов, например, асбестовой тканью. Необходимость диафрагмирования вызывается тем обстоятельством, что в противном случае анодно выделяющийся кислород по реакции
SO4 - 2(-f) + НзО - HsSOj + VaOa
будет переводить в Fe+H-l- по уравнению
2FeSO4H-H2SO4-b 2Oo- Fes (80)3+НгО.
Силу тока в цепи с нерастворимым анодом легко установить подбором в зависимости от общего расхода кислоты в процессе.
На фиг. 1 представлен график изменения кислотности электролита в функ.ции ампер-часов процесса.
Кривая участка без вспомогательной цепи показывает скорость снижения кислотности для данной ванны.
На участках I, И и III показано изменение кислотности с введением вспомогательной цепи, причем на участке 1 сила тока нерастворимого анода составляла 10% от суммы анодных токов кадмия и железа, что вызвало нарастание кислотности. На участке II сила тока была снижена до 5%, что вызвало более медленное снижение кислотности, а на участке сила тока окончательно установлена в , при которой кислотность практически уже не изменялась, то-есть при этом режиме достигается равновесие между расходуемой и образующейся кислотой по указанным выше реакциям.
Схема включения ванны с применением дополнительной цепи -С нерастворимым анодом показана на фиг. 2.
Подобное автоматическое регулирование кислотности электролита, кроме приведенного случая, с успехом может быть использовано и во всех случаях, когда в процессе электролиза при совместном осаждении двух или нескольких металлов существенно поддержйние постоянной кислотности в силу различного влияния этого фактора на катодный выход отдельных металлов, например, Cd и Ni.
Соотношение в электролите между ионами кадмия и железа устанавливается в зависимости от выбранного ICd
режима -jpT- и держится при неизменности электролитического режима достаточно постоянным для практики. В виду того, что в процессе удаления осадка из ванны захватывается электролит, то, таким образом, постепенно, хотя медленно, ванна должна разбавляться. Чтобы компенсировать эти потери, предлагается следующий способ периодического корректирования электролита. Первые порции промывных вод, содержащие заметное количество электролита, которое может слун{ить возвратом для пополнения электролита по мере его испарения, должны храниться, чтобы не вводить в ванну окисное железо, под слабым током водорода, для чего в сосуд кладутся железньге стружки (мелко раздробленное железо), и промывная вода подкисляется крепкой серной кислотой.
Таким образом, потеря иона SO с j промывными водами компенсируется за счет образовавшейся соли закиси железа FeSOi, а добавление оборотной промывной воды в ванну не меняет кислотности электролита.
Предмет и о т е н и я.
Способ электролитического совместного осаждения кадмия и железа в губсфэИП..
изменение кислотности о срунИции ампер-часоб 6 процессе пол1 чепия препарата эле тролитйчесНим методом
чатой форме для приготовления активной массы отрицательных электродов щелочных аккумуляторов с применением электролита из сернокислых солей и отдельных анодов из растворяемых металлов, отличающийся тем, что с целью автоматической регулировки кислотности электролита и получения однородного по составу осадка применяют дополнительный нерастворимый диафрагмированный анод (фиг. 2).



4 ИГ2
Ге
Авторы
Даты
1933-12-31—Публикация
1931-09-05—Подача