1
Изобретение относится к способу получения 3,4-аигидро- об -карболинов, которые могут быть использованы как промежуточны соединения при получении лекарственных веществ, как флуоресцентные индикаторы в окислительно-восстановительных реакциях, а также являясь производными 2- миноиндолов, могут проявлять присущие им физиологические свойства.
Гидрированные в пиридиновом кольце
о -карболины в литературе не известны.
Известно лищь получение тетрагидро- вС -карболинов, гидрированных в бензольном кольце.
Известен также способ получения полно- стью ароматизованных «6 -карболинов взаимодействием 1-алкил-2-аминоиндола с «6 , R - непредельными кетонами в спиртовой среде в присутствии триэтиламина, однако для этого аминоиндол берут в алкилированной форме, а условия реакции ( при доступе кислорода воздуха) выбраны для получения не дигидроструктуры, а полностью ароматизованных веществ.
Проведение реакции в токе инертного газа, например азота, позволяет выделять неизвестные промежуточные соединения -3,4-цигидро- вС -карболины.
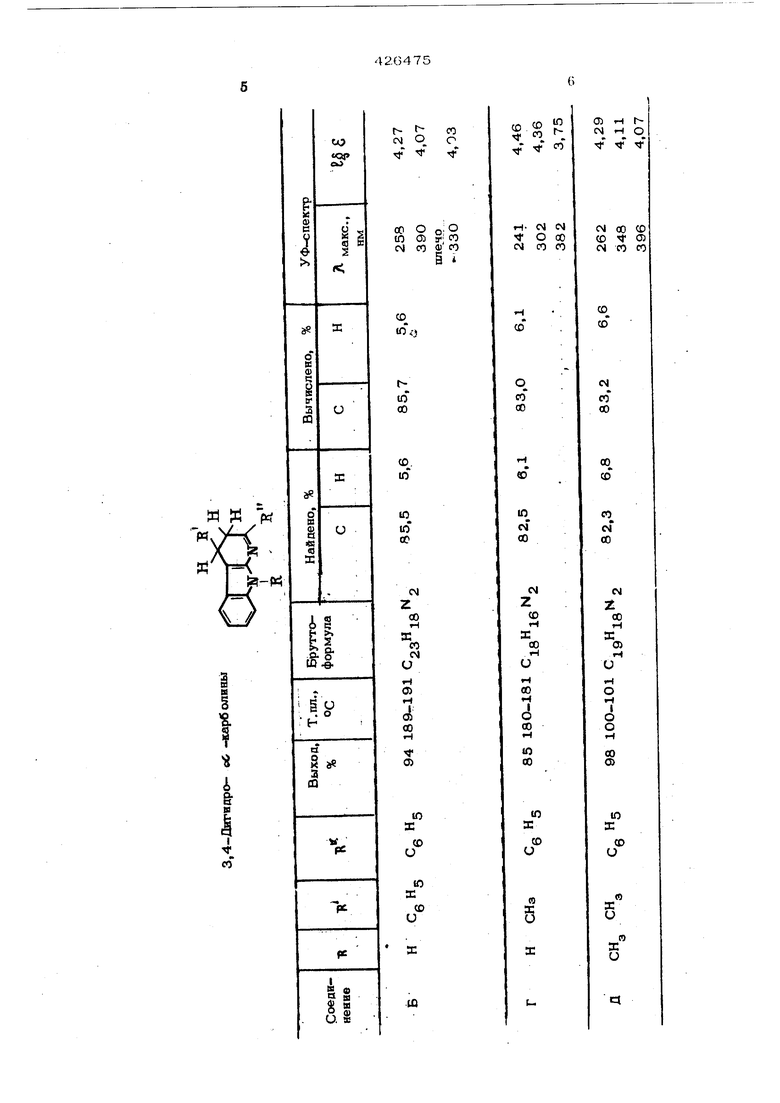
Предложен способ получения 3,4-дигидро- д -карболинов как нового класса соединений, заключающийся во взаимодействии 2-аминоиндолов с оС , J5 -непредельными кетонами, в присутствии неорганического ил органического основания, например едкого кали или триэтиламина, в подходящем органическом растворителе, например этиловом или изопропиловом спирте, при температуре кипения растворителя в токе инертного газа с последующим выделением целевого продукта известным способом. P Й или a лкил; 1г и1Ь-Н| алкил или арил. По аналогии с реакциями ароматических ароминов с «С , fii - непредельными оксосоеаи нениями, где в ряде случаев выделены промежуточные 1,2-дигидрохиноливы, предпо- i ложено образование 1,2-дигидро- «Л-карболинов. Однако оказалось, что реакция j привр дит не к 1,2 -, а к 3,4-днгидро-)в6 карболинам. Кроме того, направление циклизаци при взаимодействии с «С , ft - непредельными оксосоединениями при переходе от обычных ароматических аминов к 2-«моноиндола изменяется на обратное, то есть р -углерод ный атом непредельного соединения в данно случае атакует не аминогрз лпу, а углеродный атом. Строение полученных соединений доказано совокупностью методов физико-химическо го анализа ( УФ-, ЯК.-1ПМР - и массспектрами) и аутокислением до «С-карболинов известного строения. Так, УФ-спектры, 3,4-дигидро-оС-карболинов почти полностью идентичны со спект ром основания Шиффа заведомого строения {1,3-диметил-.2-бензилидениминоиндола), циклическими аналогами которых они являются. В ИК-спектрах имеются характеристические полосы валентных колебаний NH {348О см ), которые не наблюдаются, когда Т - CHj . В спектрах ПМР 3,4-дигидро- оС -карболинов { в пиридине) в случае, если имеется дублет протонов метильной группы в области 1,32 М.Д., а сигналы трех протонов при Cj и С видны в виде мультиплета В случае Т наблюдается группа пиков системы АВХ. Протон при С проявляется в виде триплета в более сильном поле по рядка 4,0-4,5 м.д., а два протона при С, в виде октета в более сильном поле порядка 2,0-3,5 м.д, ;. В масс-спектрах полученных соединений помимо молекулярного иона имелись пики, соответствующие выбросу заместителя (при Сц ) и бензо- или ацетонитрила из мо-(лёкулярного иона. Б 0 OCHo6oHi/e Пример 1. 2-Метил-4-фенил-3,4-дигидро-о6-карболин (А). Смесь 0,084 г {0,5 ммоль) хлоргидра та 2-аминоиндола, 0.08 г (0,О73 ммольГ бензальацетона, 1,5 мл изоАррпилового спирта и 0,14 мл ( 1 ммоль) триэтилами на кипятят в течение 30 мин в токе азота Выпавший осадок быстро отсасывают в атн мосфере азота и промывают изопропиловыц спиртом. Выделяют 0,1 г {76%)| 2-метил-4-фенил-3,4-дигидро-(С-карболина; т.пл, 210-212°С. УФ-спектр ( в метаноле): А ц,ке 2О5, 240, 319 нм а 4,50, 4,38, 3,97), ИК-спектр ( в ССе ): 3480 см ( NH), Спектр ПМР (в пиридине) : 2,0 м.д. (синглет, СНд ), 4,28 м.д. (триплет, 1Н) 2,15-2,96 м.в, (октет, 2Н). Молекулярный вес 260 (масс-спектроскопия). При стоянии в метанольном растворе на воздухе медленно окисляется, образуя известный 2-метил-4-фенил- сС -карболин. Аналогично получают и другие соединения,, данные которых приведены в таблице (см. соединение Б). П р и м е р 2. 2-Фенил-3,4-ДИГИ1ФО-вС-карболин (В). Смесь 0,084 г (0,5 ммоль) хлоргидрэ-т та 2-лминоиндола, 0,079 г (0,06 ммоль) свежеперегнанного ;фенилвинилкетона, 1,5 гЛп иаопропилового спирта и 0,14 мл (1 ммол|з) трйэтиламина |кипятят в течение ЗО мин в токе азота. Быстро упаривают pacтвopнтeлli, а остаток растворяют в бензоле, фильтруют и снова упаривают растворитель. Выделяют: 0,066 г (53%) 2-4енил-3,4-дигидро-вС-карболина - желтые кристаллы при рартирании с петролейным эфиром, т.пл. 218-22ofc, УФ-спектр (в метаноле) Д-иаке 218, 258, 322-327 нм ( fe 6 4,31; 4,19i 4,02). ИК-спектр (в ССг ) : 3480 смЧ NHl). Найдено, % С 82,7; Н 5,6. л1 Вычислено, %: С 82,9; Н 5,7, Аналогично получают соединения Г и Д ( см. таблицу).
to
f i:;
CM о
rf t

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения -карболинов | 1973 |
|
SU487071A1 |
| Соли индоло(3,2- @ )тиазоло(3,4- @ )пиримидиния и способы их получения | 1983 |
|
SU1139735A1 |
| Способ получения производных 3,4-дигидро-2H-тиопирана | 2018 |
|
RU2670977C1 |
| ОЖЙТНО-ИХКЙЧЕСИБИБЛИОТЕКА | 1971 |
|
SU309933A1 |
| СПОСОБ ПОЛУЧЕНИЯ 9-АЛКИЛ-а-КАРБОЛИНОВ | 1970 |
|
SU287945A1 |
| Применение 9-ароил-8-гидрокси-6-(2-гидроксиалкил)-2-имино-1-тиа-3,6-диазаспиро[4,4]нон-8-ен-4,7-дионов в качестве средств, обладающих высокой противомикробной активностью | 2024 |
|
RU2829454C1 |
| 1H-ПИРРОЛО[3,4-b]ХИНОЛИН-3,9(2H,4H)-ДИОНЫ, ОБЛАДАЮЩИЕ ПРОТИВОТУБЕРКУЛЕЗНОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2009 |
|
RU2457208C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭТИЛ 2-АМИНО-2',5-ДИОКСО-5'-ФЕНИЛ-3-ЦИАНО-1',2'-ДИГИДРО-5H-СПИРО{ИНДЕНО[1,2-B]ПИРАН-4,3'-ПИРРОЛ}-4'-КАРБОКСИЛАТОВ | 2014 |
|
RU2569898C1 |
| Способ получения -карболинов | 1974 |
|
SU491630A1 |
| 2-АРОИЛМЕТИЛЕН-3,4-ДИГИДРО-2Н-1,3-БЕНЗОКСАЗИН-4-ОНЫ, ПРОЯВЛЯЮЩИЕ ФЛУОРЕСЦЕНТНЫЕ СВОЙСТВА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2003 |
|
RU2240323C1 |

0)
se d
Ш 0)
tr
и
ae
W
§ g §
и
.
H
S a c§
V
в ф
lg Ss
CO о o Ю 03 tr CO
CM CO a; CO
a 1
CO
rtn
CD
Ю
ю
ОС
CNJ
CO
и
a:
CO CM
о
t-i 0) -(
ci
00
t
0)
CO
и
ю
ж
(О
и
ш
78
Фоомула изобретенияганического растворителя при нагревании
токе инертного газа, с последующим вы1. Способ получения 3.4-цигицро- -делением целевого продукта известными
карболинов, отличающийся тем,приемами.
что соль 2-аминоинцола подвергают взаимо- 5
действию с оС , & - непредельными оксосое-2. Способ по п. 1, о т л и ч а ю ш и йдинениями в присутствии органического ос-с я тем, что процесс ведут при температунования, например триэтиламина, в среде ор-ре кипения растворителя.
Авторы
Даты
1977-02-25—Публикация
1972-11-28—Подача