СПОСОБ ПОЛУЧЕНИЯ 1- (П - АМИНОФЕНИЛ)(54) «3-(М- АМИНОФЕНИЛ) - 7Н-ПИРИДО(2,3-с)КАРБАЗОЛА
| название | год | авторы | номер документа |
|---|---|---|---|
| 1,3-Дизамещенные 7н-пиридо-/2,3-с/карбазолы,обладающие свойствами флюорохромов | 1977 |
|
SU658131A1 |
| ПРОИЗВОДНЫЕ 2,3-БЕНЗОДИАЗЕПИНА, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ДЛЯ ИХ ПОЛУЧЕНИЯ И СРЕДСТВО, ОБЛАДАЮЩЕЕ ИНГИБИРУЮЩЕЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ АМРА-РЕЦЕПТОРОВ | 1997 |
|
RU2179557C2 |
| Способ получения 4-теноил-0-фенилендиамина | 1981 |
|
SU1004383A1 |
| ФИЗИЧЕСКАЯ ФОРМА (R)-7-АЦЕТИЛ-5-(4-АМИНОФЕНИЛ)-8,9-ДИГИДРО-8-МЕТИЛ-7Н-1,3- ДИОКСОЛО[4,5-H] - [2,3]-БЕНЗОДИАЗЕПИНА, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2142465C1 |
| Способ получения нитроцинхофенов | 1977 |
|
SU642307A1 |
| СПОСОБ ПОЛУЧЕНИЯ 5- | 1972 |
|
SU427013A1 |
| ПРОИЗВОДНОЕ БЕНЗИМИДАЗОЛА, ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ И СПОСОБ МОДУЛЯЦИИ ГАМК-РЕЦЕПТОРНОГО КОМПЛЕКСА | 1996 |
|
RU2135493C1 |
| ФИЗИЧЕСКАЯ ФОРМА (R)-7-АЦЕТИЛ-5-(4-АМИНОФЕНИЛ)-8,9-ДИГИДРО-8-МЕТИЛ-7Н-1,3- ДИОКСОЛО[4,5-H]-[2,3]-БЕНЗОДИАЗЕПИНА, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2146677C1 |
| СПОСОБ ПОЛУЧЕНИЯ АКТИВНЫХ СУЛЬФАМИДОВ | 1969 |
|
SU258170A1 |
| Способ получения производных пиридо (3,4- )-асимм-триазина или их солей | 1977 |
|
SU888823A3 |

Изобретение касается способа получения нового соединения - 1 - (п-аминофено -3-(м-аминофенол)-7Н-пиридо(2,3-с)карбазола формулы которое обладает физиологической активностью. Способ получения соединения фсфмулы 1 основан на известной реакции конденсации ароматических оснсшаний Шиффа с ацет фенонами, сопрсшождающейся циклизацией прсш1ежуточного продукта с образованием . азотсодержащего гетероциклического сое- аинения. Согласно идобретенюс способ получения соединения форму;&1 1 заключается в гом, что м- нитробензаль-3-аминокарбазол поо врргают взаимодействию с п-нитроапетофеноном в присутствии кскицентрированной соляной кислоты в спиртсео-диметилформамидной среде при нагревании до 80 С, образовавшийся 1-(п-нитрофенил)-З-(м-нитрофенил)-7Н-пиридо(2,3-с)-карбазоп восстанавливают двухлс эистым оловом в смеси спирта и концентрированной соляной кислоты. Исходный продукт -м-нитробензаль-3- i аминокарбазол - может быть получен известным способом. П р и м е р 1. 1О г/0,0318 моль/мнитробензаль-3-аминокарбазола, 20 мл спирта, 2О мл диметилформамида в колбе с обратным холодильником нагревают на водяной бане до раствс ения оснсквания Шиффа, после чего добавляли 5,3 г/О,О322 моль/п-нитроацетофенона и 1,5 мл концентрированной соляной кислоты и нагревают при 80 С еще 6 час. Образовавшиеся красные кристаллы отфильтровьтают, промьгеа- ют на фильтре спиртом. Вновь помешают в колбу с обратным холодильником, приливают 1О мл спирта и кипятят ЗО мин.
Получают 8,2 кристаллическрго вещества красного цвета, разлагающегося при температуре выше 300°С. Перекристаллизованное из толуола, оно также не имеет характерной точки плавления. Выход 58%.
Элементарный анализ:
Найдено,%: С 70,5, 70,2; Н 3.3, 3,4; N12,1
Вычислено, %: С 70,5; Н 3,48;
N 12,19
П р и м е р 2. 10 г(0,0218 моль) полученного в предыдущем опыте 1-/п-нитрофенил/-3-/м-нитрофенил/-7Н-пиридо(2,3-с)-карбазола помещают в стакан емкостью 0,2 л, приливают 20 мл спирта и 25 мл концентрированной соляной кислоты, нагревают на водяной бане и к горячей смеси в течение 10 мин небольшими порциями при постоянном перемешивании добавляют ЗОг/ОДЗб моль/ двухлористого олова. Затем нагревают еще полчаса и смесь охлаждают льдом с солью. Твердую часть отфильтровывают и не проьлывая, „. тщательно отсасывают растворитель. Твердый продукт красного цвета обрабатывают 60 мл ЗО%-пого охлажденного раствора едкого натра. Твердую часть отфильтровывают, промывают на фильтре водой и высушивают. Получено 7,3 г коричневого вещества. Выход 84%. Перекристаллизация и толуола давала мелкокристаллическое ве-
щество желто-коричневого цвета, плавящегося при 208-209°.
Элементарный состав:
Найдено,%: С 80,85; 80,97; Н 4,9 4,85; 13,9, 13,97
Вычислено, %:С 81,0; Н 5,0;N4,0
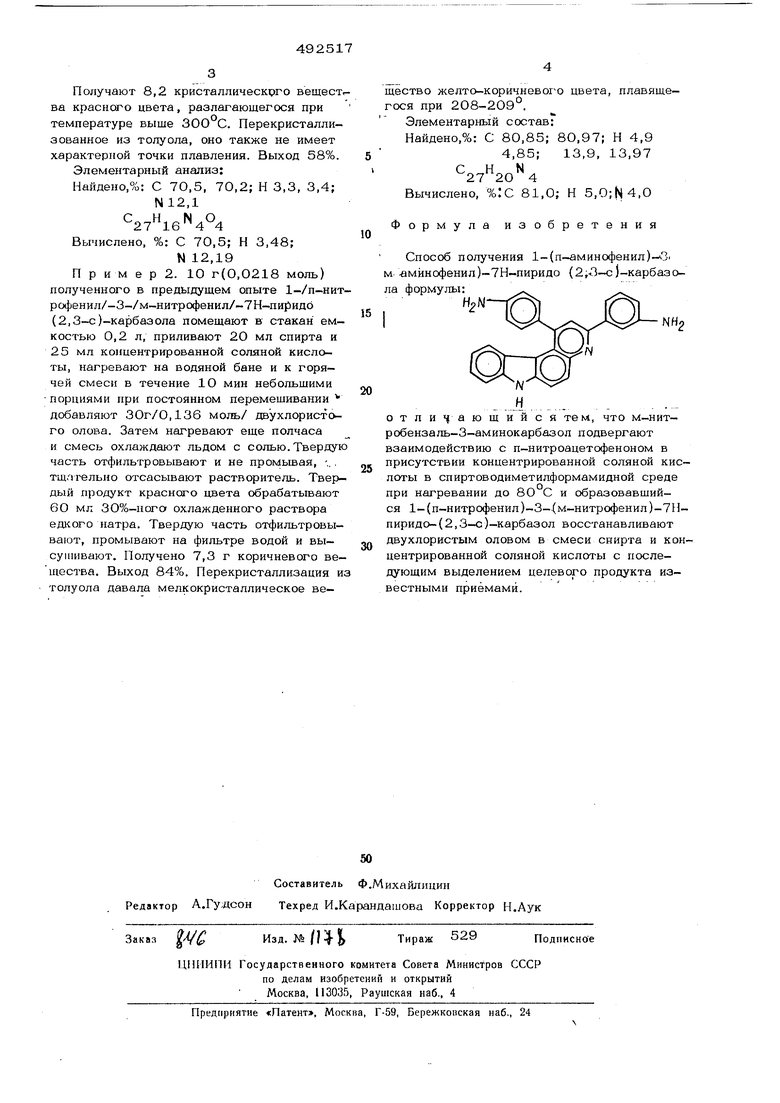
Формула изобретения
Способ получения 1-(п-аминофенил)--С. м аминофенил)-7Н-пиридо (2,-3-с)-карбазола формулы:
о jD
О
исо
/V
Н., . ....
отли дающийся тем, что м-нит- робензаль-3-аминокарбазол подвергают взаимодействию с п-нитроацетофеноном в присутствии концентрированной соляной кислоты в спиртоводиметилформамидной среде при нагревании до 8О С и образовавшийся 1-(п-нитрофенил)-3- м-нитpoфeнил)-7Ппиpидo-(2,3-с)-карбазол восстанавливают двухлористым оловом в смеси снирта и концентрированной соляной кислоты с последующим выделением целевого продукта известными приёмами.
Авторы
Даты
1975-11-25—Публикация
1974-04-12—Подача