Изобретение относится к новым производным 2-арилзамещенных 4,5,6,7-тетрагидроизо(или метаноизо)индолов, обладаю- щих выраженным седативным действием на центральную нервную систему.
Целью изобретения является синтез биологически активных соединений для расширения аpсенала фармакологических средств, что достигается получением оксипроизводных 2-арилзамещенных 4,5,6,7-тетрагидроизо(или метаноизо)индолов общей формулы
A 
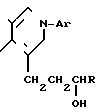 где
где 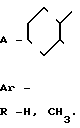
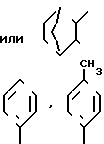 ;
;
Производные изоиндолов с оксиалкильной группой в пиррольном ядре неизвестны, поэтому предлагаемые соединения не имеют ближайших аналогов.
Известен способ получения 2-арилзамещенных 4,7-дигидро и 4,5,6,7-тетрагидроизоиндолов взаимодействием ароматичес- кого амина и продукта диеновой конденсации 2,5-диметокси-2,5-дигидрофурана с алифатическим или циклическим диеном в кислой среде.
Предлагаемый способ получения оксипроизводных 2-арилзамещенных 4,5,6,7-тетрагидроизо(или метаноизо)индолов аналогичен известному способу и заключается в том, что ароматический амин подвергают взаимодействию с насыщенным аддуктом диеновой конденсации, содержащим спироацетальную структуру, в кислой среде при 100оС в инертной атмосфере. Синтез лучше проводить при эквимолярном соотношении исходных компонентов.
П р и м е р 1. 1-(3'-Оксипропил)-2-п-толил-4,5,6,7-тетрагидро-4,7-метаноизоиндол.
В трехгорлую колбу, снабженную механической мешалкой и обратным холодильником, помещают 1,2 г (0,005 моль) 1-метокси-3-спиро-(1'-тетрагидрофуран)ок- тагидрометаноизобензофурана, 0,52 г (0,005 моль) п-толуидина и 3 мл ледяной уксусной кислоты. Реакцию проводят в атмосфере инертного газа (азота или аргона).
Содержимое колбы нагревают 1,5 ч на кипящей водяной бане. После охлаждения реакционную смесь выливают в толченый лед и нейтрализуют поташом. Выпавшее масло экстрагируют эфиром. Эфирные вытяжки несколько раз промывают водой (по 25 мл). После удаления растворителя оставшееся масло растворяют в 2 мл горячего спирта и раствор выливают в толченый лед. Выпавшие кристаллы отфильтровывают и промывают несколько раз 50%-ным спиртом. Выход 1 г (73%), т.пл. 90-91оС.
Найдено, C 81,18; 81,33; H 8,11; 8,25; N 4,49; 4,92.
C19H23NO
Вычислено, C 81,08; H 8,24; N 4,99.
ИК-спектр, см-1: νOH 3420; ν  - 1050; γ С-Н 830.
- 1050; γ С-Н 830.
П р и м е р 2. 1-(3'-Оксибутил)-2-п-толил-4,5,6,7-тетрагидро-4,7-метаноизоиндол.
Продукт получают и обрабатывают, как в примере 1, исходя из 1,2 г (0,005 моль) 1-метокси-3-спиро-(1'3'-метилтетрагидро-фуран)октагидрометаноизобензофурана, 0,52 г (0,005 моль) п-толуидина и 3 мл ледяной уксусной кислоты. Выход 1,1 г (81%), т.пл. 81-83оС.
Найдено, C 81,28; 81,11; H 8,97; 8,67; N 4,64; 4,68.
C20H25NO.
Вычислено, С 81,31; H 8,53; N 4,75.
ИК-спектр, см-1: ν ОН3400 ν 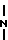 - 1080; γС-Н 830.
- 1080; γС-Н 830.
П р и м е р 3. 1-(3'-Оксипропил)-2-п-толил-4,5,6,7-тетрагидроизоиндол.
Продукт получают аналогично исходя из 0,66 г (0,033 моль) 1-метокси-3-спиро-(1'-тетрагидрофуран)октагидроизобензофурана, 0,32 г (0,003 моль) п-толуидина и 2 мл пропионовой кислоты. Эфирный экстракт сушат прокаленным сульфатом магния. После удаления растворителя остаток перегоняют в вакууме. Выход 0,32 г (42%), т. кип. 185-190оС/2 мм рт.ст.
Найдено, C 79,92; 80,46; H 8,93; 8,72; N 5,40; 5,65.
C18H23NO.
Вычислено, C 80,25; H 8,60; N 5,20.
ИК-спектр, см-1: ν ОН3430; ν 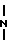 - -1075; γС-Н 830.
- -1075; γС-Н 830.
П р и м е р 4. 1-(3'-Оксибутил)-2-п-толил-4,5,6,7-тетрагидроизоиндол.
Продукт получают, как в примере 1, исходя из 0,7 г (0,003 моль) 1-метокси-3-спиро-[1'-(3'-метилтетрагидрофуран)] -октагидро-изобензофурана, 0,32 г (0,003 моль) п-толуидина и 2,5 мл ледяной уксусной кислоты. Остаток после удаления эфира представляет собой стекловидную массу, которая разлагается при перегонке в вакууме. Поэтому вещество очищают пятикратным промыванием 50%-ным спиртом и сушат в вакууме. Выход 0,36 г (45%).
Найдено, C 80,75; 80,98; H 8,82; 8,63; N 4,82; 4,59.
C19H25NO.
Вычислено, C 80,64; H 8,90; N 9,94.
ИК-спектр, см-1: ν OH4310; ν 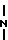 - 1045; γC-H 830.
- 1045; γC-H 830.
П р и м е р 5. 1-(3'-Оксипропил)-2-фенил-4,5,6,7-тетрагидрометаноизоиндол.
Продукт получают аналогично исходя из 0,7 г (0,003 моль) 1-метокси-3-спиро-(1'-тетрагидрофуран)октагидрометаноизобензо-фурана, 0,28 г (0,003 моль) анилина и 2 мл ледяной уксусной кислоты. Остаток после удаления эфира обрабатывают, как в примере 3. Выход 0,32 г (40%), т.кип. 120-121оС/3 мм рт. ст.
Найдено, C 80,52; 80,64; H 7,55; 7,43; N 5,59; 5,62.
C18H21NO
Вычислено, C 80,85; H 7,92; N 5,23. ИК-спектр, см-1: ν OH 3420; ν 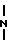 - 1050; γC-H 750.
- 1050; γC-H 750.
Проведенные фармакологические исследования показали, что синтезированные оксипроизводные 2-арилзамещенных 4,5,6,7-тетрагидроизо(или метаноизо)индолов при малой токсичности обладают действием на функции центральной нервной системы.
Биологическая активность проявляется при внутрибрюшинном введении белым мышам масляных растворов веществ в дозе 0,1 LD50.
Так, 1-(3'-оксибутил)-2-п-толил-4,5,6,7-тетрагидрометаноизоиндол вызывает снижение ориентировочной реакции в два раза. В той же дозе препарат способствует снижению температуры тела мышей через 3 ч после введения на 1,5оС. LD50 для белых мышей при внутрибрюшинном введении составляет для 1-(3'-оксипропил)-2-п-толил-4,5,6,7-тетрагидрометаноизоиндола 500 мг/кг.
| название | год | авторы | номер документа |
|---|---|---|---|
| 2-(1-Оксиэтил) /октагидроизоло/ или метаноизо/ индолы, обладающие седативным действием на центральную нервную систему и спосоь их получения | 1975 |
|
SU550384A1 |
| ГИДРОХЛОРИД 6,7- ДИМЕТОКСИ- 4,4 -СПИРОТЕТРАГИДРОПИРАН-N- (3-ФЕНИЛ-2-ПРОПЕНИЛ) -1,2,3,4-ТЕТРАГИДРОИЗОХИНОЛИНА, ОБЛАДАЮЩИЙ ЦЕНТРАЛЬНЫМ М-ХОЛИНОЛИТИЧЕСКИМ ДЕЙСТВИЕМ | 1983 |
|
SU1127271A1 |
| 2-ЗАМЕЩЕННЫЕ-6-МЕТОКСИ-1,3-ОКСАЗИН-4-ОНЫ, ОБЛАДАЮЩИЕ ПРОТИВОГРИБКОВОЙ АКТИВНОСТЬЮ | 1990 |
|
SU1769519A1 |
| СПОСОБ ПОЛУЧЕНИЯ 3-АМИНО-8-ГИДРОКСИ-1,6-ДИОКСО-2,7-ДИАЗАСПИРО[4.4]НОН-3-ЕН-4-КАРБОНИТРИЛОВ | 2012 |
|
RU2495040C1 |
| 4-АМИНО-6,6-ДИМЕТИЛ-5,6-ДИГИДРО-8Н-ПИРАНО /4′,3′:4,5/ ПИРРОЛО [2,3-D]ПИРИМИДИН | 1982 |
|
SU1088331A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 3-ФОРМИЛИНДОЛ-5,6-ДИКАРБОНИТРИЛОВ | 2014 |
|
RU2570202C1 |
| Способ получения 2,3-дизамещенных 1-гидрокси-1H-индол-5,6-дикарбонитрилов | 2017 |
|
RU2641006C1 |
| КОМПОЗИЦИЯ ДЛЯ КРАШЕНИЯ КЕРАТИНОВЫХ ВОЛОКОН, СОДЕРЖАЩАЯ N-ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ 4-ОКСИИНДОЛА, НОВЫЕ ПРОИЗВОДНЫЕ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ПРИМЕНЕНИЕ ИХ ДЛЯ КРАШЕНИЯ И СПОСОБ ОКРАШИВАНИЯ | 1996 |
|
RU2166929C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-АРИЛЗАМЕЩЕННЫХ 4,7-ДИГИДРО- ИЛИ 4,5,6,7-ТЕТРАГИДРОИЗОИИДОЛОВ | 1969 |
|
SU253806A1 |
| АМИДСОДЕРЖАЩИЕ ПРОИЗВОДНЫЕ 2-ОКСИНДОЛА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2017 |
|
RU2685501C1 |
Оксипроизводные 2-арилзамещенных 4,5,6,7-тетрагидроизо(или метаноизо)индолов общей формулы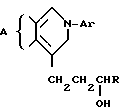
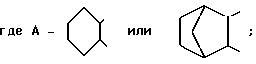
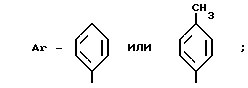
R - H, CH3,
обладающие седативным действием на центральную нервную систему.
Оксипроизводные 2-арилзамещенных 4,5,6,7-тетрагидроизо(или метаноизо)индолов общей формулы
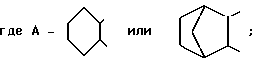
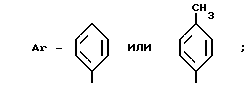
R - H, CH3,
обладающие седативным действием на центральную нервную систему.
| СПОСОБ ПОЛУЧЕНИЯ N-АРИЛЗАМЕЩЕННЫХ 4,7-ДИГИДРО- ИЛИ 4,5,6,7-ТЕТРАГИДРОИЗОИИДОЛОВ | 0 |
|
SU253806A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1996-03-10—Публикация
1975-09-08—Подача