(54) СПОСОБ ПОЛУЧЕ}1ИЯ ПРОИЗВОДНЫХ ТЕТРАЗОЛО а ХИНАЗОЛОИА 5



Изобретение относится к способу nt лучения новых производных тетразоло |а хиназсв1она 5 формулы 1
-Н
где R или Т1;г - каждый означает С -С. т алкил, С- Сд-алкоксигруппу, С.-С алканоилоксигруппу, бензилокси-или оксигруппу, трифторметил, сулы})онамидогруппу или галоид, или R означает водород и Т, взятые вместе, означают -O-CHg О - или -O-CH g .QH-- О-группу, которые могут найти применение в качестве биологически активных соединений.
В Литературе описан тетразоло а хиназолон-5 l . Однако, в литературе нет указаний о биологической активности описанного соединения.
Целью изобретения является способ получения новых производных тетразоло а хиназолона-5 формулы 1 , которые обладают биологической активностью.
Предлагаемый способ получения соединений формулы I, заключается в том, Что соединение формулы Т|
где К и 2 имеют указанные значения, подвергают взаимодействию с щелочного металла при 50-1ОО С среде растворителя.
Процесс проводят преимущественно с 5-2О%-ным молярным избытком азида щелочного металла и в водном этаноле или водном N, N-диметилформамиде,
Пример. 7-Метокси-8-пропокситетразоло а хиназолон-5. Готовят суспензию 30 г (11 ммоль) 311-в-метокси-8-пр опоке и-2-хлорхиназо- линэна-4 всмеси бОмл N, N -диметилформамида и 40 мл воды, вносят 0,8 г (12 ммоль) азида натрия и смесьнагревают в течение 2 ч при дефлегмации. После охлаждения приливают 20 мл воды отфильтровьшают, выкристадлиз овавшийся продукт, промывают водой, сушат. При перекристаллизации из смесей N, N-диметилформамида и воды получают 1 г целевого продукта (33%), т. пл. 2-М-245°С. Вычислено,%: С 52,36; Н 4,76; N 25,44. .
(с разложением)
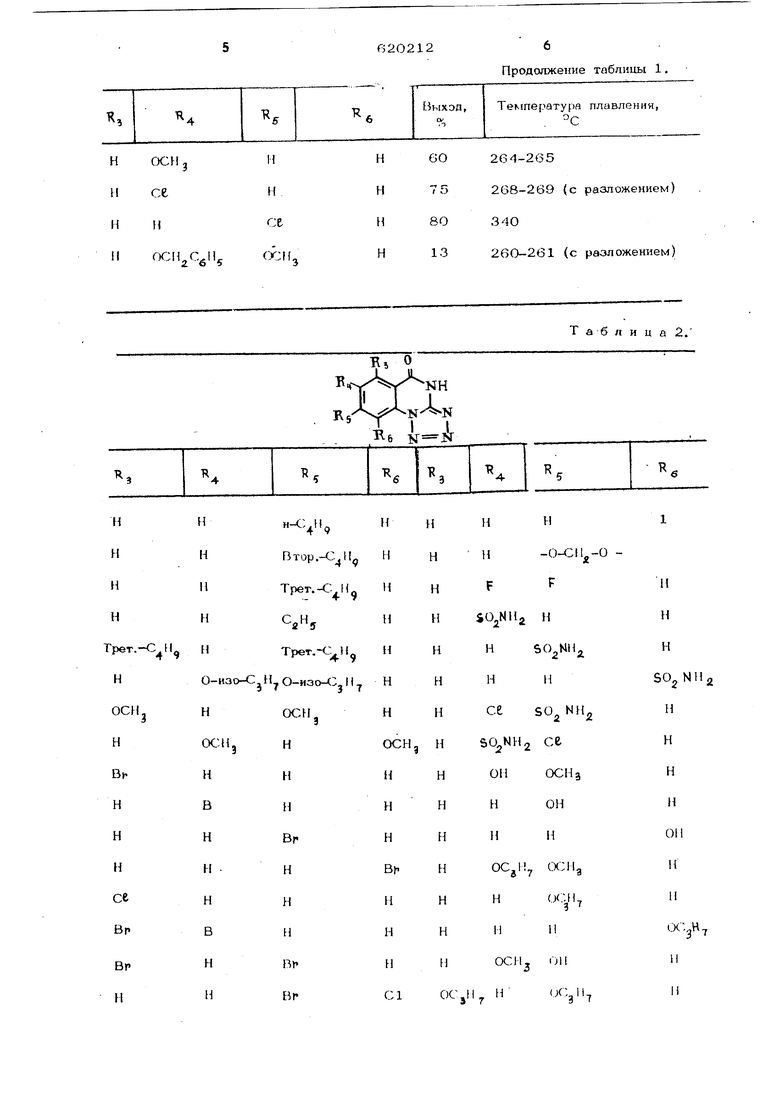
(с разложением) C,,,H,0,. Найдено,%: С 52,66; Н 4,96; N.25,60. П р и м е р 2. Описа}шым в примеое 1 способом получают приведенные в табл. 1 тетраэоло а хиназолоны-5 из соответствующих 3|1-2-хлорхиназолинонов-4. П р и м е р 3. Следующие соединения, приведённые в табл. 2, получают из соответственно замещенных производных бензойной кислоты методом, описанным в примере 1. Таблица 1.
и и
ОСИ
се и
СЕ.
ГЮИ.,,
cx:if.
Продолжение таблицы 1,
НGO26 -265
Н75268-269 (с разложением)
И8О34О
Н13260-261 (с разложением) , Вгор. Tper.-C.fi Трет., О-изо-С Н О-изо-С Н Н
F SO,jNH2 50,jNH он Н Н ocj OCjH Н -0-С11 -0 FН , SOjNHg Н 0„ NH, Н Н Н Н 2 се ОСНз он Н сх:н, Формула Изобретен и я 1, Способ попучеция производных тетразопо aj хиназопона-б формулы 1 да Т или - каждый означает Cf -Сд «алднл, С jfr nKOKcarpyaay C влкаяоилоксигрунпу, бензилоксн-или окси f Рупиу, трифторметал, сульфонамидогруп пу клв галоид или означает водород, шщ 1f и 2 взятые вместе, озна- ч«ог -O-CH.gO - или -О-СН,2-СН,-О Tf/snaay, отличающейся тем, что соединеняе формулы |
8
Продолжение табл. 2 где R, и Кд имеют указанные значения, подвергают взанмодейсгашо с азидом щелочного металла, при в среде растворителя, 2. по п. 1/ о т л и ч а JBJщ и и с я тем, что азид щелочного металла берут с 5-20%-ным мсглярным избытком, 3.Способ по п. 1, отличающий с я тем, что процесс проводят в водном этаноле или водном N,H -димегапформамиде. Источники информаыии, принятые во внимание при экспертизе: 1. Журнал общей химии, 33, 2334 2341,. 1963.
Авторы
Даты
1978-08-15—Публикация
1976-07-09—Подача