(54) ИНСЕКТИЦИДНЫЙ СОСТАВ радикалов Rj, 2 , У и R должны представлять собой радр.кйл, огличный от 4. -фторзамещенного радикала; 3 ) X - галоген, го не менее чем один из радикалов R, R2 К,, О. , У и- Т отличен от водорода или его натриевых и калиевых солей. Лиазотиробание Аг1Н2 ЛГ1{2 .5-ArFHM dC где Т ОН, OR, NHR и F - Н или алкил с 1-4 атомами углерода; S С6, HSOx, H2PQi или другие ионы в COOTветствии с кислотой. Применяемой для получения соли амина. Согласно приведенной схеме можно получить замещенные 1,5 дифениЛ«3 формазанкарбонитрилы (AV Ar ). Несимметричные формазаны (At - Аг ) получают из 1 моль активного метиленового соединения и 2 моль соли диазония, иАгМ2- 3 ,причемАг Аг Таким образом получают следующие соединения. Пример 1. 1,5-Бис(4«.трифторме тилфенил )-3-4)ормазанкарбонитрил. Раствор, приготовленный из 16,1 г (0,1 моль) П-аминобензтрифторида и 30 мл 12 н. хлористоводородной кислоты, разбавленный 300 мл воды, охлаждают до , добавляя дробленный лед до досгижв ния объема 5ОО мл. К полученному раствору при перемешивании приливают раство пригоговленный из 7,0 г (0,1 моль) азо тистокислого натрия и 70 мл воды, после чего {ВНОСЯТ раствор, приготовленный из 4,2 г (0,05 моль) цианацетамида и 50м воды. Гголученную смесь выливают в 450 мл буферного растюра из 1 моль NaH-РОд с рН 7,5, в результате чего . получают оранжевый осадок в растворе. Значение рН раствора доводят до 7,5, при ливая 100 мл. 10% нного раствора гидро окиси натрия. Выделяется двуокись угле рода. Полученный оранжевый осадок отфильтровывают, выход сырого продукта ко личе(;твенный. После рекристаллизации из ацетона оранжево красное вещество плавится при 232-234С, оно представляет собой 1,5-бис(4-трифторметилфенил)3 -формазанкарбонитрил. Содержание активного вещества в составе от 0,025 до 99 вес.%, остальное добавка. Соединения согласно изобретению получают по следующей схеме: -- С Пример 2. 1,5-Бис{4-.трифгор мегилфенил)3-форма занкарбонитрил. Раствор, приготовленный из бензтрифторида (120,8 г; 0,75 моль; точка кипения 117,5°/6О мм, ,4815) в 12 н. хлористоводороднЬй кислоте, разбавленный водой (1167 мл) и метанолом (335 мл ) фильтруют для удаления небольи того количества нерастворимых веществ. К полученному фильтрату добавляют дроб- , пенный лед с целью охлаждения раствора до С. Быстро добавляют азотистокис- лый натрий (52,5 г; 0,76 моль) в воде (ЮО мл).с последующим перемешиванием раствора при 0-5°С в течение 10 мин. Полученный раствор соли диазония медленно, перемешивая, приливают к раствору, приготовленному из цианацегамида {31,5г; 0,37 .моль) и буфера кислого фосфорнокислого калия-Гидроокиси натрия (рН 8,65; 666 мл), при одновременном добавлении 10%-4joro водного раствора гидроокиси нат ркя в количестве, необходимом для получения рН 8,. Оранжево-красную суспензию перемешивают 10-20 мин с последующим фильтрованием. Остаток на фильтре промывают водой до тех пор, пока он не будет свободным от солей, затем его подсушивают. Получают 1,(4-.трифторме тйлфенил)«-3-формазанкарбонитрил (144 г; точкаплавления 227 230С) в виде оранжево-красного твердого вещества. Полученный продукт и без дальнейшей очистки отличается превосходными инсектицидными свойствами. Применяя замещенные анилины вместо П «минобензтрифгорида, получают симметрично замещенные соединения общей формулы I . Формы применения средств обычные порошки, суспензии, эмульсии, дусты гра- нулы. Их приготавливают методами, общими при изготовлении препаративных форм пестицидов. Изобретение иллюстрируется следующим примерами.. Пример. Группы по 25 только что выращенных личинок комара, переносящего вирус желтой лихорадки, помещают в 25 мл воды. Взвешенные количества каждого соедине ВИЯ, приведенного в табл. 1, растворяют в ацетоне. Полученные растворы вносят в чащки с личинками. Корм для личинок добавляют периодически. Ежедневно подсчитьгеают количество умерщвленных личинок и куколок. Результаты .воздействия инсектицидного состава опредеяян т после развития взрослых насекомых и умерщвления остающихся личинок и куколок. Таким образом устанавливают летальную дозу ЕС (концентрация, необходимая для умерщвления 50% личинок и куколок комара), выраженную в частях на милпон, Полученные данные приведены в табл. 1. :Таблица1 Соединения общей формулы flfClЛ . S, ) С -Ъ-й ннСоединения обтай формулы
полученные результаты приведены в табл. 2.
2
Таблица
Н CF н.
:V Продолжение табл. 1. Пример 2. Бобовые растения в стадии развития двух листьев опрыскивают до каплеобразования препаратом, содержащим указанные в табл. 2 соединения. Эти препараты изготовляют растворением 50 мг соединения в 1О мл ацетона, добавлением 1 мл Метоцела 15 и разбавлением смесью Дупонола и воды в соотно- щении 1:3000. Через 1 ч после опрыскивания листья отделяют, помещают в чаш- ки Пегри с 10 личинкам и Prodema eridania и чашки закрывают. По истечении 1 и 2 суток определяют проценть умерщвленных личинок и разъеденных листьев.









4-SCF - 4-SCF - 0,05
lOO
6564608
24
Необработанный контроль
Пример 3. Бобовые растения в стадии развития двух листьев опрыскивают до каплеобразования суспензией, пригоговленной растворением 50 мг 1,5-бис(4-трифтормегилфенил-3-форма занкар бонитрила в 1О мл ацетона с добавлением 1 мл 1%-ного Метоцела 15 и разбавлением смесью Дупонола и воды в соот0,0510О3
Необработанный контрольО1ОО
Пример 4. Растения красных французских бобов в стадии развития двух листьев опрыскивают до каплеобразования суспензией 1,5-бис(4-трифторметоксифенил)3 «формазанкарбонитрила, изготовлен ной растворением его в 15 мл ацетона с добавлением 1 мл 1%-ного раствора, со держа| 1его Метоцел 15, и разбавлением смесью Дупонола и воды в соотношении
Продолжение табл. 2
10О
О
100
ношении 1:3000. По истечении 2 сут. листья отделяют, помешают в чашки Петри с 10 личинками Prodenia eHdania и чашки закрывают. По истечении суток определяют количество умерщвленных личинок и разъеденных листьев.
Полученные результаты приведены в габл. 3 Таблиц
1:ЗООО. После сушки листья отделяют, помещают в чашки Петри с 10 личинками Pi-odemci eridaniaiH чашки закрьшают.
Ежедневно в течение 3 сут. определяют процент умерщвленных личинок и разъе.денных листьев.
Полученные результаты приведены в табл. 4.
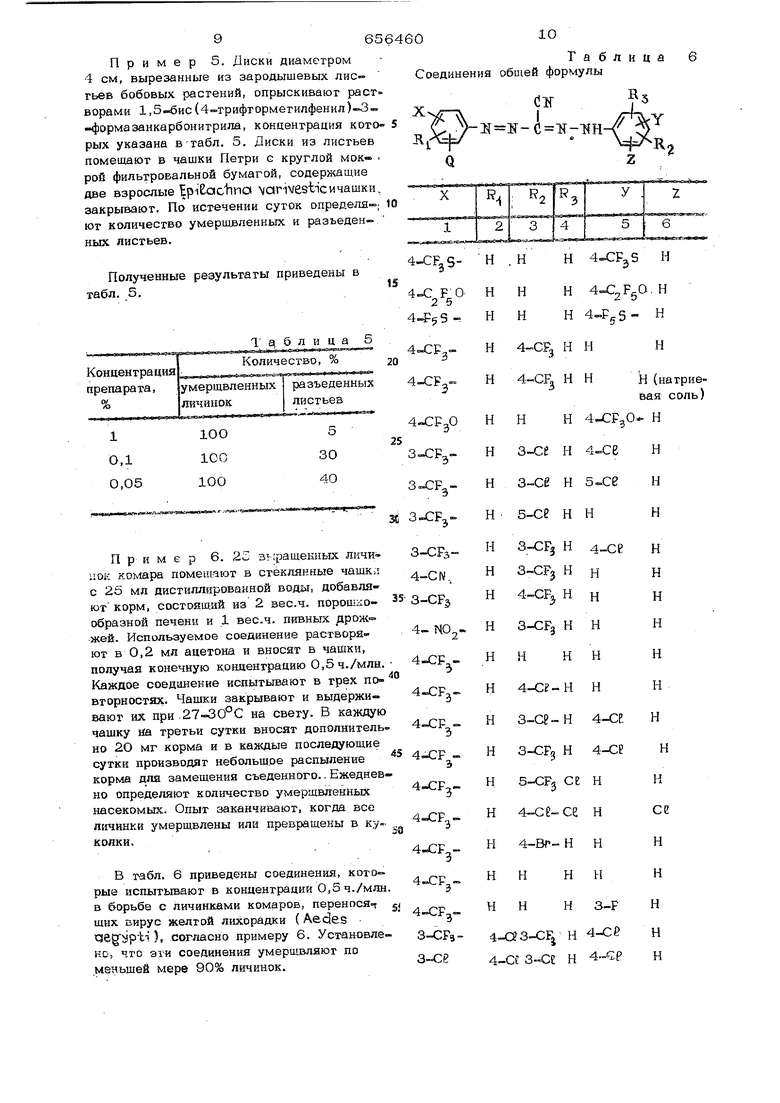
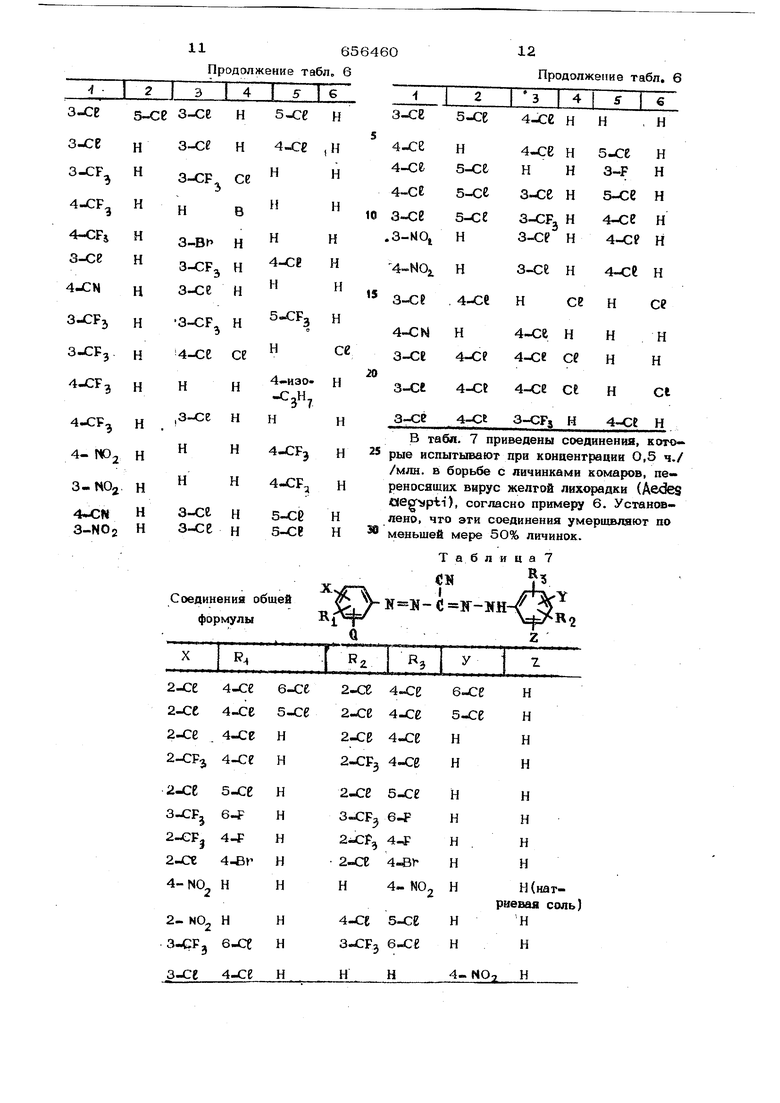
Таблица 4 Пример 5. Диски диаметром 4 см, вырезанные из зародышевых лис гьев бобовых растений, опрыскивают раст ворами 1, (4 трифгорметилфенил) -формазанкарбонитрила, концентрация кото рых указана в табл. 5. Диски из листьев помещают JB чашки Петри с круглой мок рой фильтровальной бумагой, содержащие две взрослые Bpi&aclina Vaг1vest1cv чaшки закрывают. По истечении суток опредеяяют количество умерщвленных и разъеденных листьев. Полученные результаты приведены в табл. 5. Т ( б л и ц а 5 Пример 6. 2S з фащекных личицок комара помещают в стеклянные чашкл с 25 мл дистиллированной воды, добавляют корм, состоящий из 2 вес.ч. порошкообразной печени и 1 вес.ч. пивных дрожжей. Используемое соединение растворяют в 0,2 мл ацетона и вносят в чашки, получая конечную концентрацию 0,5ч./млн Каждое соединение испытывают в трех повторностях. Чашки закрывают и выдерживают их при .27-30°С на свету. В каждую чашку на третьи сутки вносят дополнитель но 2О мг корма и в каждые последующие сутки производят небольшое распыление корма для замещения съеденного.. Ежеднев но определяют количество умерщвленных насекомых. Опыт заканчивают, когда все личинки умерщвлены или превращены в куколки. в табл. 6 приведены соединения, кото рые испытьгоают в концентрации О,S ч./млн в борьбе с личинками комаров, перенося щих вирус желтой лихорадки (Aedes ), согласно примеру 6. Установлено, что эги соединения умерщвляют по меньшей мере 90% личинок. Таблица Соединения обшей формулы v-ТТггК-( ,S 4 Рз54 2 б . 4 534-СРз Н Н 4-CF.-34-CF Н Н н (натриевая соль) НН Н 3-се н 4д:е З СР з-се н ,.э5-се н н . a-cFj н 4-се 3-СРз3 CFj Н н н 4-CF Н З-СР З-СРд Нн 4. КО,н н н 4-CF 4-сг-н4-CF з-се-н З-СРл н S-CPj СЕ 4.CF 4-се-сеU:F. 4-Bf-HJ:F н н -CFjн н CF.,э4-a3-cFj н 4-се 3-CF34-се З-С;Е н 4--€р
11656460
Продолжение табл. 6
12
Продолжение табл. 6
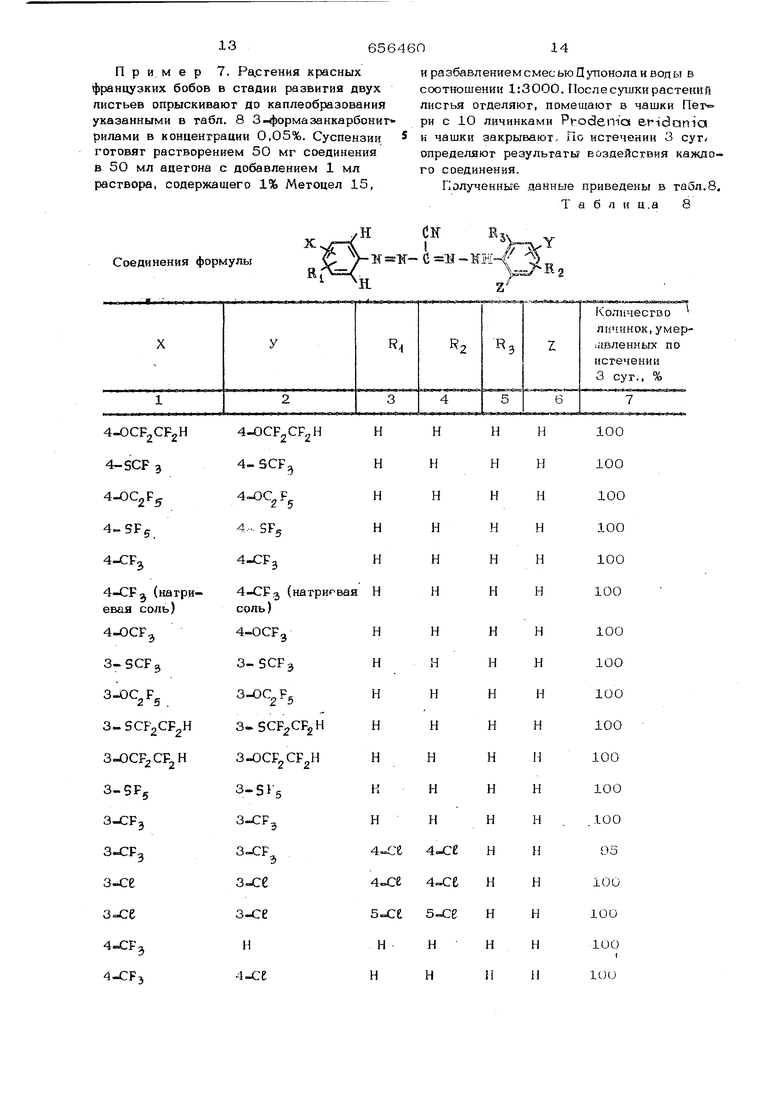
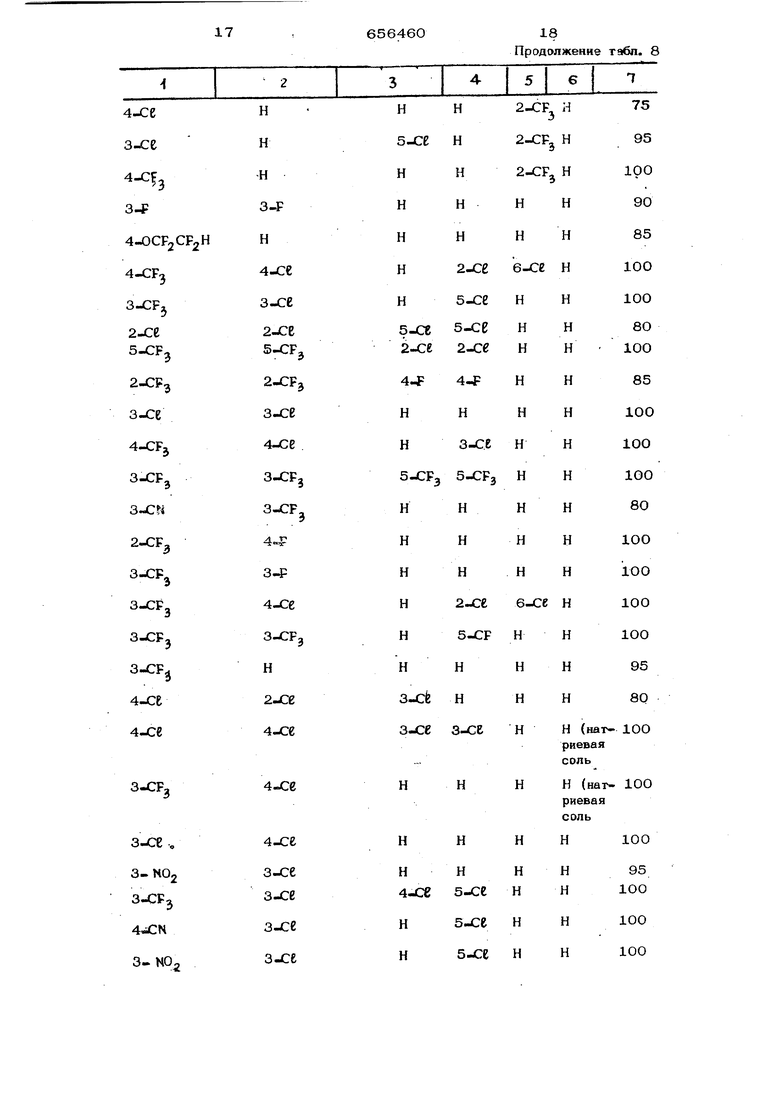
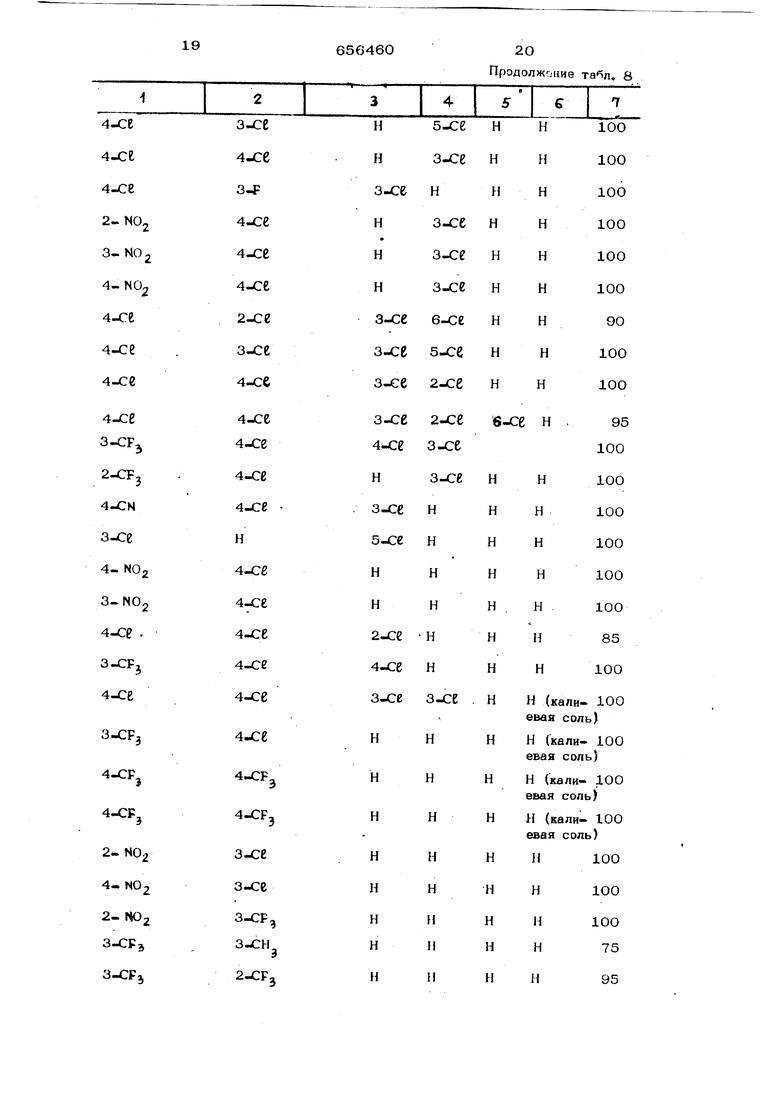
Пример 7. Ра.сгения красных французких бобов в стадии развития двух листьев опрыскивают до каплеобразования указанными в табл. 8 3-формазаикарбонит рилами в концентрации 0,05%. Суспензии готовят растворением 50 мг соединения в 50 мл ацетона с добавлением 1 мл раствора, содержащего 1% Метоцел 15,
формулы
йЛ 4-OCF2CF2H 4-OCF2C 4-SCF 4-SCF 3 4-SF5 4.-. SF« , 4-CF,3 ( 4-CF (натриевая соль) соль) 4-OCf 4-OCF3 3-SCF3 з-дср 3-OC2Fg 3- SCF2CF2H 3-SCF2C 3-OCF2C 3-OCF2CF2H S-SFg 3-515 3-CF3 3-CF3 4-СРз 4-CF3
и ра збавл ение м смесью Ц упоно лай ВОДЬ в соотношении 1:3000. После сушки растений листья отделяют, помещают в чашки Пет ри с 10 личинками Pt-odema &ridania и чашки закрывают.. По истечении 3 сут/ определяют результаты воздействия каждого соединения.
Полученные данные приведены в табл.8. Т а б л и ц. а 8
НСКЕ
Y R2
-§ ft2 100 100 100 100 00 100 100 95 OO OO
Продолжение табл. 8
17
65646О
18 Продолжение табл. 8
19
656460
20
Продолжо 1ие . 8
21
22
656460
Процолжение табл. 8
Пример 9. Диски диамегром4 см вырезают из лисгьев липы, их слегка оп- рыскиваюг растворами 1,5-бис(4- трифгорметилфенил)-3-формаэанкарбонитрила (А), 1-(3,5-дихлорфенил)-5-(3-.трифторметил
фенил)-3-формазанкарбонитрила (Б) и 1,5-бис-(3,4-дихлорфенил )-3-формазан-.
Пример 1О. Растворы 1,5-бис-к6,5 см) с целью получения тонкого покры
(4-трифторметилфенил)-3-формазанкарбо- тия из них. После сушки помешают 5 нанитрила (А) и 1,5-6ис(3,4-дихлорфенил)-25 секомых Dermacentor vqriaWtls в каж-ЗН|юрмазанкарбонитрила (Б) в ацетоне,дую чашку и закрывают ее.
каждый в концентрации 1ОО ч./млн., раз- Полученные по истечении 2 сут. резуль.
брызгивают в чашки и крышки (6,5 смхтаты приведены в табл. 11.
А Б
Необрабср-анный контроль
Пример 11. Проводят опыты с растениями капусты, применяя 1,5-(бис(4-тр фтормвтилфенил)-3-форма занкарбонйт рил (А) и 1-{4-хлорфенил)-5-{3-трифтор- 5 метилфенил)- 3 формаэанкарбонитр({л (Б) в концентрации 320 ч./млн. в полевых усло« ВИЯХ. Длина участка 7 м. Растения высаживают поздней весной. После появления
карбонигрила (В) в ацетоне. Диски листьев помещают на мокрую фильтровальную бумагу в чашки Петри вместе с двумя йпонскими жуками. 5
Результаты наблюдений по истечении 2 сут. приведены в табл. 10.
Таблица 10
Т а б л и ц а 11
10О
100
о
насекомых начинают опрыскивание по еженедельному плану. На необработанных участках быстро образуются обширные популяции введенных репниц и Epitrix CUCUfheHs,
Полученные результаты приведены в
табл. 12, из которой видна эффективность соединений в борьбе с насекомыми. аб|лица 12
Необработанный контрольО
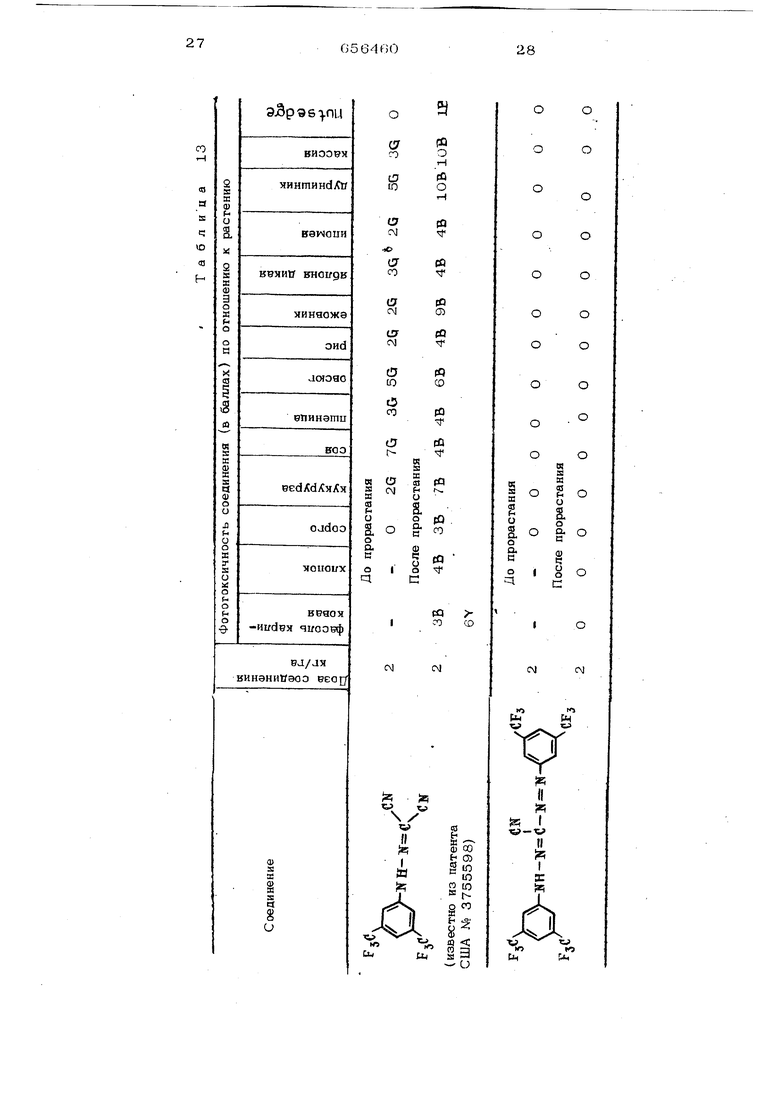
(93% листьев разьеденр.) Ниже описан опыт по определению фитотоксичности предлагаемого инсектицидно го состава. Семена дикой яблони (DigrHotria), ежовника (EchinocliEooi orusgroieei), овсюга (Avena fatura), Cassia toroi, ип меи ( Зротеазрр), дypнишникa(Xant1 1un1 сорго кукурузы, сои, риса, пшеницы и клубни nutsedge высаживают в растительной среде и обрабатьшают перед прорастанием химикалиями, растворенными в нефитотоксичном расгворителе. Одновременно опрыскивают хлопок с пятью листьями (включая семядольные листья), фасоль карликовую третьей стадией распускания трехлистника, дикую яблоню с двумя листьями, ежовник с двумя листьями, овсюг с одним листом, сс(531СЯ с тремя листьями (включая семядольные листья), ипомею с четырьмя листьями (включая семядольные листья), дурнишки с четырьО
(30-)& внешней и 50.% внутренней поверхности листьев разъедено) мя листьями (включая семядольные листья), сорго с тремя листьями, пшеницу с тремя листьями, сою с двумя семядольными листьями, рис с двумя листьями, пшено с одним листом и tiutsedge с тремя-пятью листьями. в течение 16 дней обработанные и контрольные растения выдерживают в теплице, после чего все разновидности сравнивают с контрольными растениями и визуально оценивают результаты обработки. Количественную оценку проводят по шкале 0-10; при этом Ю баллов означают полное уничтожение, О - отсутствие повреждения. Была проведена также качественная оценка типа повреждения, буква В оз11ачает ожог листвы; G указыьает на замедление роста, а Y-опадание почек или цветка. Полученные результаты приведены в табл. 13. 656 Таким образом, предложенные соединения не обладают фитогоксичностью. Формула изобрегения Инсектицидный состав, содержащий про изводные фенилгидразона как активное вещество, а также добавку, выбранную из группы наполнитель, инертный разбавитель, поверхностно-активный агент, о т л и ч а- ю щ и и с я тем, что, с целью снижения фитотоксичносги состава, он содержит в качестве производного фенилгидразона со единение общей формулы СМНу (Ж-1ГН н.Z где X грифторметокси, трифторметилтио, 1,1,2,2-.тетрафторэтокси, 1,1,2,2-тетрафторэтилтио, пентафторэтокси, пентафтортио, цианогруппа, трифторметил, хлор, фтор или нигрогругша; У - водород, грифгормегокси, грифтор метилгйо, 1,1,2,2-.-теграфторэтокси, 1,1, 2,2- етрафторэтклтио5 пентафторэтокси, пентафтортйо, хлор, бром, фтор, трифтор« метил, метил или изопропил; 030 Rj - водород, бром, фгор или грифгорметил;Г водород, хлор, бром, фтор или трифторметил, водород, хлор, бром, фтор, трифторметил, нитрогруппй, 2 - водород, хлор, фтор; QV - водород, хлор, фгор; однако в случае, если 1)У - метил, изопропил, то X три фторметил; 2)X - 4-фторзамещенный радикал и R, Q и гри из радикалов R, Z , У и Ra обозначают водород, то оставшиеся из радикалов Р2 Z , У и Rj, должны представлять собой радикал, отличный от 4 -фторзамещенного радикала; 3) X - галоген, то не менее чем один из радикалов R, F(2 3 О, У к Z отпичен от водорода его натриевых и калиевых солей, причем содержание активного вещества в составе от 0,О25 до 99 вес./ь, остальное добавка, Источники информации, принятые во внимание при экспертизе 1. Патент СССР № 578821, кл. А О1 N 9/20, 1972. 2. Патент США № 3755598, кл, , 28.08.73.
Авторы
Даты
1979-04-05—Публикация
1974-12-17—Подача